Гидролиз крахмала термои РН-стабильной глюкоамилазой при изменении физико-химических факторов
Автор: Григоров В.С., Яковлев А.Н., Яковлева С.Ф.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Биотехнология, бионанотехнология и технология сахаристых продуктов
Статья в выпуске: 4 (58), 2013 года.
Бесплатный доступ
Изучена закономерность изменения скоростей ферментативных реакций в зависимости от различных температур, величин рН среды при образовании и распаде фермент-субстратного комплекса. Установлено, что кинетика гидролиза крахмала под действием термо- и рН-стабильных глюкоамилаз носит сложный характер, о чем свидетельствует изменение величины K m, которая служит мерой сродства фермента к субстрату, активные центры исследуемых глюкоамилаз и крахмал претерпевают конформационные изменения при рН 4,0-5,0; 4,5-5,5 и температуре 60-65 оС.
Гидролиз крахмала, концентрация субстрата, фермент, температура, рн-среды
Короткий адрес: https://sciup.org/14040126
IDR: 14040126 | УДК: 577.154.31
Hydrolysis of starch by thermo-and ph-stable glucoamylase at change physico-chemical factors
Regularity of the change rate of the enzymatic reactions depending on different temperatures, pH values in the formation and decay of the enzyme-substrate complex was investigated. Found that the kinetics of hydrolysis of starch by the action of heat and pH stable glucoamylases is complex as evidenced by the change in the value Km, which is a measure of the affinity of the enzyme to the substrate, active centers studied glucoamylases and starch undergo conformational changes at pH 4,0-5,0; 4,5-5,5 and a temperature of 60-65 °C.
Текст научной статьи Гидролиз крахмала термои РН-стабильной глюкоамилазой при изменении физико-химических факторов
Важными факторами, влияющими на скорость ферментативной реакции, являются концентрация субстрата и фермента, температура и рН-среды.
Особенности протекания реакции гидролиза при использовании мезофильных ферментов для гидролиза крахмала отражены в литературных источниках [1].
Однако отсутствуют данные о гидролизе крахмала термо- и рН-стабильными глюкоамилазами, полученными из термотолератных штаммов рода Rhizopus и Aspergillus .
Целью настоящей работы явилось изучение закономерностей изменения скоростей ферментативных реакций в зависимости от различных температур, величин рН среды при образовании и распаде фермент-субстратного комплекса.
Объектами исследования были термостабильные глюкоамилазы (ГлА), полученные из термотолерантных штаммов: R. Pygmaues P1 [2] и Asp. Avamori ВУДТ-2 [4], очищенные по методу [3] с удельной активностью 280 ед./мг белка. Скорость гидролиза крахмала в зависимости от его концентрации определялась при значениях рН 2,5-6,5 и температуре 30-65 оС. Концентрация крахмала изменялась в возрастающем порядке от 2 до 4 %. Высокоочищенные глюкоамилазы вносились в субстрат из расчета 0,4-2,0 ед./100 мг крахмала.
Установлено, что изменение концентрации субстрата в указанных пределах при температуре 30-40 оС и рН 5,0 мало влияют на скорость ферментативной реакции. С повышением температуры скорость реакции, как функция концентрации субстрата, выражается гиперболическими кривыми (рисунок 1) в соответствии с уравнением Михаэлиса-Ментен:\
V =
V max
Km
1 +[^ ] где V – скорость реакции при [S];
V max – достигаемая полным насыщением фермента субстратом;
K m – константа Михаэлиса.
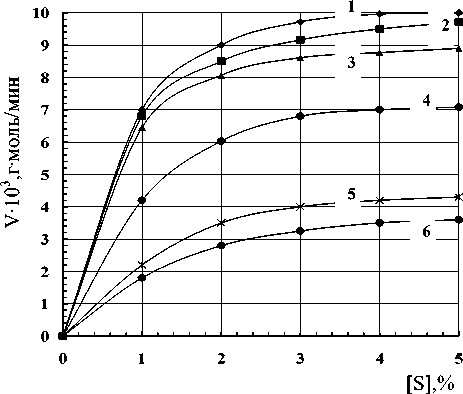
Рисунок 1 - Зависимость скорости ферментативной реакции от концентрации крахмала при рН 4,5 и температуре 0С: 1 – 65; 2 – 60; 3 – 55; 4 – 50; 5 – 40; 6 – 30.
K m определяет меру средства ферментов с субстратом: чем больше возможность образования фермент-субстратного комплекса, тем меньше величина K m , которая численно равна концентрации субстрата, при которой V = 0,5 ∙V max [1]. Определение V = f([S]) позволило вычислить K m для ГлА R. Pygmaues P 1 и Asp. Avamori ВУДТ-2 при температуре 60 и 65 оС.
Различными авторами предлагаются разные методы определения K m [1]. Если построить график зависимости начальной скорости реакции от концентрации крахмала, то можно определить V max . По этому же графику находится [S] при скорости равной 0,5∙ V max . Однако наибольшая трудоемкость в этом методе связана с определением V max , так как нельзя точно установить предельное значение скорости реакции.
Для определения K m применялся графический метод [1], так как в нем используется линейная форма уравнения для равнобочной гиперболы.
График зависимости обратных величин скорости реакции и концентрации субстрата представляет из себя прямую, и в обратной форме уравнения имеет вид:
-
— = — + Km г 1 (2) V V max V max • [ 5 ]
Данное уравнение прямой с наклоном K m / V max дает возможность на оси ординат отсечь отрезок 1/ V max . По этому графику определена величина K m для ГлА (1, 2) микромицетов. Изменение величины K m в зависимости от рН среды и температуры представлено в таблице 1.
Таблица 1
Изменение величины K m в зависимости от рН и температуры
|
t 0C |
pH |
|||||||
|
2,5 |
3,0 |
3,5 |
4,0 |
4,5 |
5,0 |
5,5 |
6,0 |
|
|
60 |
0,55 |
0,39 |
0,30 |
0,13 |
0,14 |
0,17 |
0,20 |
0,28 |
|
0,76 |
0,58 |
0,41 |
0,22 |
0,17 |
0,18 |
0,22 |
0,29 |
|
|
65 |
2,81 |
0,88 |
0,67 |
0,19 |
0,20 |
0,31 |
0,47 |
0,92 |
|
3,25 |
1,05 |
0,80 |
0,59 |
0,48 |
0,50 |
0,52 |
1,10 |
|
Числитель – K m ГлА R. Pygmaues P 1
Знаменатель – K m ГлА Asp. Avamori ВУДТ-2.
Из данных таблицы 1 видно, что K m пpи 60 и 65 оС для ГлА микромицетов имеет наименьшее значение при рН 4,0-5,0, а для ГлА (2) при рН 4,5-5,5, что указывает на оптимальные условия образования фермент-субстратного комплекса.
Повышение температуры до 67 оС приводит к частичной термической инактивации ГлА (1), особенно при низком значении рН, на что указывает величина K m . Изменение K m в зависимости от температуры (Х 1 ) и рН (Х 2 ) для ГлА R. Pygmaues P 1 (у 1 ) и Asp. Avamori ВУДТ-2 (у 2 ) можно описать уравнениями регрессии следующего вида:
у 1 = -15,13 + 0,35Х 1 + 0,56Х 2 -0,055Х 1 Х 2 + 0,32Х 2 2 (3); у 2 + -15,37 + 0,36Х 1 + 0,11Х 2 –
0,0051Х 1 Х 2 + 0,33Х 2 2 (4).
Увеличение концентрации крахмала до 3,5-4,0 % сдвигает температурный оптимум действия ферментов в область более высоких температур (60-65 оС). Особенно это проявляется при рН 4,0-4,5.
Из элементарных математических функций наиболее удобной и близкой к экспериментальным кривым (рисунок 1) является экспонента с соответствующим показателем степени. Поэтому кривые зависимости скорости ферментативной реакции от концентрации крахмала можно представить в виде:
V = Vmax - ( t ) [1 - e - Km ( p H, t ) [ S ]] (5)
Как видно из рисунка 1 максимальная скорость (Vmax), достигаемая полным насыще- нием ф ермента субстратом, является функцией Vmax = f(to), график которой можно аппроксимировать прямой линией:
V max = a + ʙto (6)
Коэффициенты уравнения данной закономерности были найдены по методу наименьших квадратов для ГлА R. Pygmaues P 1 :
V max = -7,09t + 0,29
Величина K m , согласно данным таблицы 1 и уравнений (5), (6), определяется в основном природой глюкоамилазы и является функцией рН и температуры. Анализ этих уравнений показал, что математически они описываются одинаково, где имеет место совпадения знаков перед коэффициентами уравнений. Поэтому структуру данных уравнений можно записать в виде:
K m ( pH ,t0 ) =- a o + a1 t o + a 2 (PH)-
-
- a i,2 (t0 • pH ) + an(pH)2 [ s ]
В общем виде уравнение зависимости скорости ферментативной реакции глюкоамилаз исследуемых микромицетов можно представить как:
V = (a + bt) . (1-
-
- (-a o + a l to + a 2 ( PH )- a 1,2 (t ° pH) + a 11 ( PH ) 2 [ ^ ] . (9)
-e , )
Для R. Pygmaues P 1 такое уравнение имеет вид:
V = ( 7,09 + 0,29to ) .
. (1 - exp(-(15,13 + 0,35to + 0,56(pH)- (10)
-
- 0,055(to . pH ) + 0,32(pH)2 [ S ] ))
Таким образом, кинетика гидролиза крахмала под действием термо- и рН-стабильных глюкоамилаз носит сложный характер, о чем свидетельствует изменение величины K m , которая служит мерой сродства фермента к субстрату.
Можно предположить, что активные центры исследуемых глюкоамилаз и крахмал претерпевают конформационные изменения при рН 4,0-5,0; 4,5-5,5 и температуре 60-65 оС.


