Подбор затравочных молекул при создании ПЦР-тест-системы для идентификации растительного сырья в продуктах питания
Автор: Голубцова Ю.В.
Журнал: Вестник Красноярского государственного аграрного университета @vestnik-kgau
Рубрика: Технология переработки
Статья в выпуске: 10, 2014 года.
Бесплатный доступ
Подбор затравочных молекул (праймеров) - ключевое звено ПЦР (полимеразной цепной реакции), поскольку именно ими определяется возможность амплификации и выявления нужной последовательности, а также чрезвычайная гибкость метода. В связи с этим произведен выбор нуклеотидных последовательностей, которые будут многократно воспроизводиться в процессе ПЦР. Осуществлен поиск гомологичных последовательностей и их анализ. Подобраны универсальные праймеры для тест-системы.
Праймеры, тест-система, полимеразная цепная реакция, идентификация, пищевые продукты
Короткий адрес: https://sciup.org/14083365
IDR: 14083365 | УДК: 579.67:[641:613.26]
Selection of seeding molecules in the process of PCR-test-system creation for identification of vegetable raw materials in foodstuffs
The selection of seeding molecules (primers) is one of the key factors in the (PCR) as these primers determine the possibility of amplification, detection of the needed sequence and extreme flexibility of the method. Thereby the selection of the nucleotide sequences that will be reproduced repeatedly in the PCR process are made. The search of homologous sequences and their analysis are performed. The universal primers for test-system are selected.
Текст научной статьи Подбор затравочных молекул при создании ПЦР-тест-системы для идентификации растительного сырья в продуктах питания
В эпоху научно-технического прогресса, в связи с изменившимися условиями труда и быта, возникла проблема роста числа заболеваний у людей, обусловленных нехваткой биологически активных нутриентов в рационе питания [1].
Одним из наиболее эффективных путей ликвидации дефицита эссенциальных нутриентов в питании человека является обогащение продуктов питания массового потребления биологически активными компонентами природного происхождения. Вследствие чего сегодня все большее внимание уделяется применению растительного сырья (плодов и ягод) в производстве продуктов питания, о чем свидетельствует рост объемов российского рынка продуктов с использованием данного вида сырья.
Интерес к съедобным растениям оправдан. Пищевые растения представляют большую ценность, прежде всего благодаря специфичным сочетаниям биологически и фармакологически активных компонентов. Такие вещества трудно создать искусственно, они хорошо усваиваются человеческим организмом, обладают лечебным и/или профилактическим действием. Благодаря природной гармонии и многообразию входящих в их состав макро- и микронутриентов (углеводы, витамины, минеральные вещества и др.), использование данного вида сырья позволит повысить пищевую и биологическую ценность пищевых продуктов [7].
При производстве пищевой продукции, обогащенной растительным сырьем, необходимо осуществлять жесткий контроль качества и достоверности видовой принадлежности вводимых природных компонентов вследствие распространяющейся фальсификации продуктов питания. По экономическим соображениям наиболее распространенный метод фальсификации – использование более дешевых заменителей ингреди- ентов, входящих в рецептуру продукта питания, имеющих, как правило, пониженную пищевую ценность. Так, например, вместо земляники садовой предлагают клубнику, а вместо персиков – абрикосы.
Решение проблемы обнаружения фальсификаций растительного сырья в продуктах требует соответствующих методов идентификации и имеет первоочередное значение в списке мероприятий, направленных на достижение безопасности и качества реализуемой пищевой продукции. В целях установления фальсификации пищевой продукции идентификация осуществляется путем совокупной оценки физико-химических, органолептических и других показателей [8]. Для этого на практике наиболее широко применяются следующие методы исследования.
Спектральные методы исследования – совокупность методов качественного и количественного определения состава объекта, основанная на изучении спектров взаимодействия материи с излучением. Спектральный анализ используется для определения пектиновых веществ, фенольных соединений, макро- и микроэлементов, содержания тяжелых металлов, степени окисления жиров и др.
Хроматографические методы исследования незаменимы при оценке качества и безопасности пищевых продуктов, имеющих очень сложный химический состав. Например, газожидкостная хроматография (ГЖХ) является наиболее важным методом для изучения состава жирных кислот природных масел и жиров, а также липидов, выделенных из различных продуктов питания. Кроме того, ГЖХ используется при определении содержания жирорастворимых витаминов, синтетических красителей, консервантов, аминокислот, углеводов, ароматических веществ пищевых продуктов, пестицидов и др. [4, 5].
Методы капиллярного электрофореза анализа сложных смесей основаны на использовании элек-трокинетических явлений (электромиграции ионов и других заряженных частиц и электроосмосе) для разделения и определения компонентов. Данный метод позволяет определять аминокислотный состав белков пищевых продуктов, состав органических кислот, содержание фруктозы, глюкозы, сахарозы.
Разработаны и внедрены ферментативные методы анализа . Их применяют при определении лимонной и яблочной кислот для соков; состава моно- и дисахаридов в молочных продуктах питания и плодово-ягодных полуфабрикатах.
Однако используемые в настоящее время методы анализа далеко не всегда позволяют исследовать пищевые продукты достаточно глубоко. Необходимость создания и постоянного усовершенствования специфичных и чувствительных методов, не требующих большого количества материала для анализа и пригодных для рутинной диагностики, неоспорима [5].
Освоение в последние годы методов ДНК-диагностики послужило стимулом для разработки и внедрения в практику высокочувствительных методик оценки качества и экспертизы продуктов питания, основанных на методе полимеразной цепной реакции (ПЦР) [3]. Полимеразная цепная реакция – это метод амплификации (многократное воспроизведение) in vitro, с помощью которого в течение нескольких часов можно выделить и размножить определенную последовательность ДНК в количестве, превышающем исходное в 10 раз. В основе метода лежит многократное копирование с помощью фермента ДНК-полимеразы определенного фрагмента ДНК по принципу комплементарности [6].
ПЦР-анализ состоит из трех основных процедур: подготовка пробы исследуемого материала, которая в большинстве случаев сводится к изоляции ДНК и ее очистке; амплификация (собственно ПЦР) и детекция продуктов амплификации. Ключевым этапом ПЦР является амплификация – направленная репликация фрагмента ДНК. Каждый цикл амплификации состоит из трех этапов: денатурация ДНК; отжиг праймеров (их присоединение к м-ДНК); элонгация праймеров (синтез). Многократное (циклическое) повторение этих трех стадий приводит к обогащению реакционной смеси молекулами ДНК-мишени, поскольку в каждом новом цикле в качестве матрицы выступает не только исходная, но и вновь синтезированная ДНК.
При создании ПЦР-тест-системы одной из основных задач является правильный подбор затравочных молекул или праймеров. Праймеры – искусственно синтезированные олигонуклеотиды, имеющие, как правило, размер от 15 до 30 п.н., идентичные соответствующим участкам ДНК-мишени. Они играют ключевую роль в образовании продуктов реакции амплификации. Правильно подобранные праймеры обеспечивают специфичность и чувствительность тест-системы [2].
Цель исследования . Подбор затравочных молекул для ПЦР-тест-системы, позволяющей идентифицировать растительное сырье в продуктах питания.
Объекты и методы исследования. В качестве объектов исследования были выбраны клубника и вишня. Для поиска последовательностей генов, к которым необходимо подобрать праймеры, удобно исполь- зовать биоинформационную базу данных NCBI. NCBI (National Centerfor Biotechnological Information, USA) – национальный центр биотехнологической информации, в числе прочего предоставляет сведения о структуре генома живых организмов – о нуклеотидных и аминокислотных последовательностях. Результаты анализа представлены в таблице 1.
Таблица 1
Анализ нуклеотидных последовательностей генома клубники и вишни
|
Наименование сырья |
Количество выбранных нуклеотидных последовательностей, присутствующих во всех геномах |
Степень сродства по скору, % |
|
Клубника (Fragaria ) |
69 |
95 |
|
Вишня (Prunussubg. Cerasus) |
25 |
95 |
Для исследования были использованы следующие сорта клубники: Fragariamoschata; Fragariaorientalis; Fragariavesca; Fragariaxananassa; Fragariavirginianasubsp. Glauca; Fragarianubicola, Fragari-adaltoniana; Fragaria sp.; Fragariachiloensis; Fragarianipponica; Fragariapentaphylla; Fragariamoupinensis; Fragar-ianilgerrensis; Fragariaiinumae; Fragariatibetica; Fragariacorymbosa. При анализе геномов Fragaria выбраны небольшие последовательности, присутствующие во всех геномах. В ходе анализа было выявлено, что общее количество нуклеотидных последовательностей в системе, представленных в Gene Bank, для клубники составило 69, наибольшее сродство по скору – 95 %.
Также проведен анализ геномов Prunussubg. Cerasus, в ходе которого выбраны небольшие последовательности, присутствующие во всех геномах. Анализируя данные, выявили 25 последовательностей для вишни, которые имеют наибольшее сродство по скору (95%).
На следующем этапе исследований в программе Bio Edit было проведено выравнивание и сравнение гомологии нуклеотидных последовательностей клубники и вишни. Результаты представлены на рисунках 1–2.

Рис. 1. Равнение и гомология нуклеотидных последовательностей клубники в программе Bio Edit

Рис. 2. Равнение и гомология нуклеотидных последовательностей вишни в программе Bio Edit
Как показал анализ, все нуклеотидные последовательности клубники и вишни обладают высоким сродством и степенью гомологии 98 %. Выбрали участки последовательностей, идентичные друг к другу, для подбора универсальных праймеров (рис. 3–4).
CGGCTCCTCGCCCCCTCCTCCCGGGAGGCGGACGTCTCGCGCGTCGCGCTCCGGCGCTTCCGCCTGGCCGA CCCTTCCGGGCGTACCGAACACCGGCGTGAATTGCGCCAAGGAACTTGAATGAAAGAGCGTTCCCCCGCCGT CCCGGAGACGGAGACCGCGCGGGTGGTTCGTCGTCTTCAGTATGTCTAAACGACTCTCGGCAACGGATATCTC GGCTCTCGCATCGATGAAGAACGTAGCGAAATGCGATACTTGGTGTGAATTGCAGAATCCCGTGAACCATCGA GTCTTTGAACGCAAGTTGCGCCCGAAGCCGTTAGGCCGAGGGCACGTCTGCCTGGGCGTCACACGTCGTTGC CCCCCCGACCCCTTCGGGAGCCGGACGGGACGGATGATGGCCTTCCCGTGTGCCCCGTCACGCGGTTGGCA TAAATACCGAGTCCTYGGCGACCGGCGTCGCGGCAATCGGTGGTTGTCAAACCTCGGTGCCTTGTCGCGTGC GTGAGTCGATCGCGGGAC
Рис. 3. Последовательности клубники
AACCTGCCTAGCAGAACGACCCGAGAACTAGTTTCAAAGCGGGGGATGAGGGGTCTTGCGGCTCCTTGTCCCT TTATCTCGGGGGGGTTGCATTGCGTTCGCGCAACCGACCCTTCCTGCGTACAAACGAACACCGGCGCGAATTG CGCCAAGGAACCTGAATGAGAGAGCGCGTCCCCGTTGCACCGGAAACGGTGCGCGCGGGCGGCGTCGTCAT CTTCAAATATGTCAAAACGACTCTCGGCAACGGATATCTCGGCTCTCGCATCGATGAAGAACGTAGCGAAATGC GATACTTGGTGTGAATTGCAGAATCCCGTGAACCATCGAGTCTTTGAACGCAAGTTGCGCCCGAAGCCATTAGG CCGAGGGCACGCCTGCCTGGGCGTCACACGTCGTTGCACCCCCACTACTCCCTCGGGATTGCGGGGTGCGGA TGATGGCCTCCCGTACGCTCCGTCGCGCGGTTGGCATAAATACCAAGTCCTCGGCGACGCACGCCACGACAAT CGGTGGTTGCGAAACCTCGGTTGCCCGTCGTGTGCGGTCGTCGCGCATCGGGGGCTCGAAAAAATGCTTGGC TCCGGCTTGGC
Рис. 4. Последовательности вишни
Разработка праймеров является самым ответственным звеном в ПЦР. Требуется подобрать такой фрагмент молекулы ДНК, который бы отличался генетической консервативностью и присутствовал бы только в исследуемом гене. При этом длина такого фрагмента должна составлять 15–30 нуклеотидов.
К выбранным участкам нуклеотидных последовательностей индивидуально подобрали праймеры, которые исключали бы перекрест при идентификации гена. Первыми выбрали праймеры с параметрами ПЦР для клубники, которые представлены на рисунке 5. Далее выбрали праймеры для идентификации вишни (рис. 6).
А
Нуклеотидный код (IUPAC)
5'-

-3'
Перевёрнутая комплементарная цепь (5' —► 3'): GTC CGC СТС CCG GGA GGA G
5' модификация (если есть)
3' модификация (если есть)
Выберите тип олигонуклеотида | оцДНК [Я
50 нМ Праймер
50 мМ Соли (Na+)
Величина поглощения при 260 нм: 1|
ОП расчитывается только для одноцепочечной ДНК или РНК
| ПОСЧИТАТЬ! | | Поменять цепи | | BLAST2 | | mfold |
Физические константы
Расчёт температуры плавления (Ты)
Длина: | 19|
Молекулярный вес: | 5790.8j (?)
Содержание GC: | 79| %
1 мл раствора с ОП равной | 1| при 260 нм
является | ~ содержит | олигонуклеотида.
5.329, микромолярным (?) и
30.9| микрограмм(а)
Простой метод (?)
С корректировкой по концентрации солей (?)
| 59| °C
По алгоритму ближайших соседей (?)
Нуклеотидный код (IUPAC)
5'-

-3'
Перевёрнутая комплементарная цепь (5* —► 3'): GCC TTG TCG CGT GCG TGA
5' модификация (если есть)
3' модификация (если есть)
Выберите тип олигонуклеотида | оцДНК |^1
50 нМ
50 мМ
Праймер
Соли(Na+)
Величина поглощения при 260 нм: |1
ОП расчитывается только для одноцепочечной ДНК или РНК
| ПОСЧИТАТЬ! I I Поменять цепи | | BLAST2 | | mfold |
Физические константы
Расчёт температуры плавления (Тм)
Молекулярный вес: |
Содержание GC: |
1 мл раствора с ОП равной [
5478.6 С?)
при 260 нм
| 55| °C
Простой метод (?)
является [ содержит | олигонуклеотида.
5.1 б| микромолярным (?) и
28.з| микрограмм(а)
I 61| °C
С корректировкой по концентрации солей (?)
| 58| °C
По алгоритму ближайших соседей (?)
Б
Рис. 5. Универсальные праймеры для идентификации клубники: А – левый праймер; Б – правый праймер
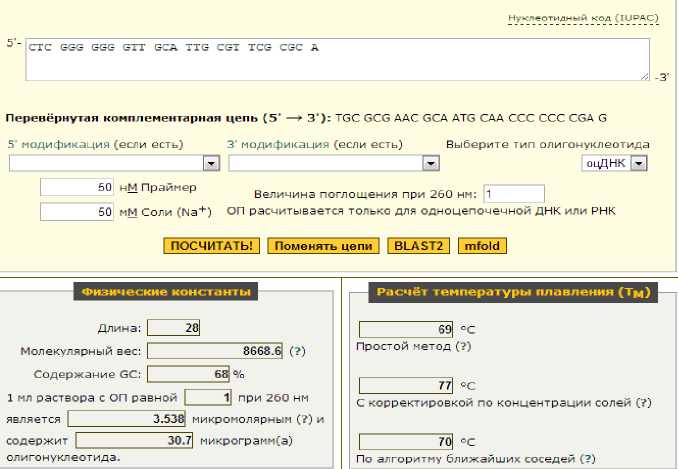
А
5'-

-3'
Перевёрнутая комплементарная цепь (5‘ —• 3'): TGC CCG TCG TGT GCG GTC GTC GCG СА
5' модификация (если есть)
3‘ модификация (если есть)
Выберите тип олигонуклеотида о^ НК U
50 нМ Праймер _ _,_ .
Величина поглощения при 260 нм: 1
50 мМ Соли (Na+) ОП расчитывается только для одноцепочечной ДНК или РНК
| ПОСЧИТАТЬ! | | Поменять цепи | | BIAST2 | | mfold |
Физические константы
Расчёт температуры плавления ( 1м)
Длина:[
Молекулярный вес: [
Содержание GC: Г
1 мл раствора является | содержит |
ОП равной Г
7976.2| (?) 73|о/о
Т| при 260 нм
I —69| °C
Простой метод (?)
олигонуклеотида.
3.5Э5| микромолярным (?) и
28.7| микрограмм(а)
I Ё| °C
С корректировкой по концентрации солей (?)
| —Й] "С
По алгоритму ближайших соседей (?)
Б
Рис. 6. Универсальные праймеры для идентификации вишни: А – левый праймер; Б – правый праймер
Выбранные универсальные непересекающиеся праймеры для определения методом ПЦР растительного сырья (клубники, вишни) представлены в таблице 2.
Универсальные праймеры для тест-системы ПЦР
Таблица 2
|
Наименование сырья |
Длина, п.н. |
Праймеры |
|
Клубника |
19 |
CTCCTCCCGGGAGGCGGAC |
|
18 |
TCACGCACGCGACAAGGC |
|
|
Вишня |
28 |
CTCGGGGGGGTTGCATTGCGTTCGCGCA |
|
26 |
TGCGCGACGACCGCACACGACGGGCA |
Таким образом, проанализированы нуклеотидные последовательности генов растительного сырья (клубники, вишни). С помощью компьютерного моделирования и анализа выбраны универсальные праймеры для идентификации методом ПЦР клубники и вишни.


