Атеротромботический и лакунарный инсульты у пациентов пожилого возраста: особенности клинических проявлений и тромбоцитарного гемостаза
Автор: Голдобин Виталий Витальевич, Клочева Елена Георгиевна, Сироткина Ольга Васильевна, Вавилова Татьяна Владимировна, Ласковец Анастасия Борисовна
Журнал: Ученые записки Петрозаводского государственного университета @uchzap-petrsu
Рубрика: Медицинские науки
Статья в выпуске: 6 (135), 2013 года.
Бесплатный доступ
Ишемический инсульт чаще возникает у лиц пожилого и старческого возраста. Патогенез атеротромботического и лакунарного инсультов определяется взаимодействием тромбоцита с эндотелиоцитом сосуда, что объясняет назначение антиагрегантных препаратов для вторичной профилактики. Цель исследования - изучение клинических данных и показателей тромбоцитарного гемостаза у пациентов пожилого возраста, перенесших атеротромботический и лакунарный инсульты. Обследованы 35 больных с инсультом (66,3 ± 3,9 года) и 13 лиц без инсульта (63,6 ± 5,2 года). Всем обследуемым выполнено стандартное клинико-лабораторное обследование, позволяющее верифицировать патогенетический вариант инсульта, исследование тромбоцитарного гемостаза: аденозиндифосфат-индуцированная агрегометрия и проточная цитометрия экспрессии рецепторов к фибриногену, фактору Виллебранда и Р-селектина, а также молекулярно-генетическое исследование. Данные агрегометрии при стимуляции 2,5 и 5 мкмоль аденозиндифосфата свидетельствовали о более высокой активности тромбоцитов у здоровых лиц (85,3 ± 28,1 и 54,1 ± 20,0 %, р
Ишемический инсульт, тромбоциты, агрегация, р-селектин, рецепторы к фибриногену, тромбоцитарный гликопротеин 1ba
Короткий адрес: https://sciup.org/14750477
IDR: 14750477 | УДК: 616.831-005.4:616-005
Atherothrombotic and lacunar strokes in elderly patients: clinical manifestations and platelet haemostasis
Occurrence of ischemic stroke incidences increases with aging. The relations between platelets and endothelial cells are pivotal in pathogenesis of atherothrombotic and lacunar stroke, therefore, antiplatelet drugs’ administration is common for the purpose of prevention of secondary strokes. The goal of the study was to investigate clinical manifestation and platelet homeostasis parameters in elderly patients with atherothrombotic and lacunar strokes. 35 patients with stroke (66,3 ± 3,9 years) and 13 persons without stroke (63,6 ± 5,2) were examined. We performed routine clinical examination and laboratory investigation to reveal pathogenetic variants of stroke. Platelet homeostasis investigation: adenosindiphosphate-induced agregometry and flow-cytometry of receptor expression for fibrinogen; von Willebrand factor and P-selectin, and moleculargenetic test were carried out. Agregometry with stimulation by 2,5 and 5 mmol adenosindiphosphate revealed high reactive activity of platelets in a healthy group (85,3 ± 28,1% and 54,1 ± 20,0%, р
Текст научной статьи Атеротромботический и лакунарный инсульты у пациентов пожилого возраста: особенности клинических проявлений и тромбоцитарного гемостаза
Медико-социальная значимость церебрального ишемического инсульта связана с высокими показателями инвалидизации и летальности пациентов [1]. Частота развития первичного ишемического инсульта (ИИ) увеличивается в пожилом возрасте: в когортных исследованиях показано развитие инсульта у 2 % лиц в возрасте 45–64 лет, у 8 % лиц 64–74 лет и у 11 % лиц возраста 75 лет и более [13]. До настоящего времени механизмы развития ИИ окончательно не ясны. Определяющую роль в патогенезе атеротром-ботического и лакунарного инсультов играет взаимодействие тромбоцитов с эндотелиоци-тами сосудистой стенки [3]. Важной составляющей вторичной профилактики атеротромбо-тического и лакунарного инсультов является назначение антитромбоцитарных препаратов. Однако на современном этапе профилактики эффективность антиагрегантной терапии составляет 25 % [6], а повторный ИИ развивается в течение 5 лет у 16–42 % больных [2], [6], что указывает на необходимость определения особенностей терапии для пациентов c различными патогенетическими вариантами ИИ. Выделение классификационных подгрупп атеротромботи-ческого инсульта (АТИ) и лакунарного инсульта (ЛИ) связано с нарушением кровоcнабжения мозга на различных уровнях: атеротромбозом магистральных артерий при АТИ и поражением мелких пенетрирующих артерий при ЛИ, чаще вследствие липогиалиноза.
Целью данного исследования являлось изучение клинических данных и показателей тромбоцитарного гемостаза у пациентов пожилого возраста, перенесших атеротромботический и лакунарный инсульты.
МАТЕРИАЛЫ И МЕТОДЫ
Были обследованы 35 пациентов в возрасте 66,3 ± 3,9 года (основная группа) и 13 здоровых лиц в возрасте 63,6 ± 5,2 года (контрольная группа). Набор пациентов проводился в клинике неврологии СЗГМУ им. И. И. Мечникова и в ан-гионеврологическом отделении ГУЗ «Городская больница святой преподобномученицы Елизаветы» (Санкт-Петербург).
Критериями включения в исследование являлись наличие АТИ или ЛИ в остром периоде, подтвержденное компьютерной томографией (КТ) или магнитно-резонансной томографией (МРТ) головного мозга.
Диагноз АТИ устанавливали при обнаружении стеноза соответствующей очагу артерии (> 50 % по данным дуплексного сканирования), отсутствии признаков кардиогенной эмболии и при размере очага поражения головного мозга > 20 мм при КТ или МРТ [5]. Критериями ЛИ были наличие лакунарного синдрома в клинической картине; отсутствие признаков кардиогенной эмболии, стеноза ипсилатеральной моз- говой артерии > 50 %; размер очага поражения головного мозга < 20 мм при КТ или МРТ [5].
Критериями невключения были: постоянный прием антикоагулянтных препаратов, наличие острого инфаркта миокарда, нестабильной стенокардии, фибрилляции предсердий, острой сердечной недостаточности, хронической сердечной недостаточности выше 2-й стадии по классификации Нью-Йоркской кардиологической ассоциации, пороков клапанов сердца, анамнестические данные о проведении коронарной ангиопластики или аортокоронарного шунтирования, ангиопластики брахиоцефальных артерий, каротидной эндартерэктомии, протезирования клапанов сердца. В исследование не включали пациентов с сопутствующими хроническими заболеваниями головного мозга (рассеянный склероз, болезнь Паркинсона, опухоли); заболеваниями системы крови; наличием хронической почечной недостаточности с проведением гемодиализа; лиц, постоянно принимающих антидепрессанты из группы селективных ингибиторов обратного захвата серотонина.
Для сравнения клинических и гемореологических показателей были выделены 2 группы в соответствии с вариантом ишемического инсульта: 1-ю группу составили 20 больных с АТИ в возрасте 66,5 ± 4,4 года, 2-ю группу – 15 пациентов с ЛИ в возрасте 65,9 ± 3,1 года.
Комплексное обследование включало: клинико-неврологическое, инструментальное и лабораторное исследования. На каждого больного заполнялась специально разработанная карта.
Неврологический осмотр выполняли по стандартной методике. Проводилась оценка состояния пациентов на момент поступления и при выписке по общепринятым шкалам в баллах: по шкале инсульта Американского национального института здоровья (NIHSS), которая характеризует основные нарушения при церебральном инсульте [7], [9], и по шкале Ранкина, которая позволяет оценить степень инвалидизации в повседневной жизни [8].
КТ или МРТ головного мозга выполняли всем больным на 2–5-й день от развития заболевания для верификации очага ишемии в веществе мозга, оценки его локализации и размеров.
Лабораторное исследование включало клинический анализ крови при поступлении и на 10-й день от развития ИИ, а также аденозиндифосфат (АДФ) индуцированную агрегатоме-трию и проточную цитометрию на 10-й день от развития инсульта. Венозную кровь забирали в утреннее время, натощак. В условиях процедурного кабинета под венозным жгутом проводилась венепункция локтевой вены иглой 21G со свободным током крови через вакутейнер в вакуумные полипропиленовые пробирки, содержащие в качестве антикоагулянта К2 и К3 соль этинилдиаминтетрауксусной кислоты (для гема- тологического анализа) или 3,8 % цитрат натрия (для агрегометрии и проточной цитометрии). Выполнение клинического анализа крови с подсчетом количества тромбоцитов осуществляли кондуктометрическим методом на автоматических гематологических анализаторах «Beckman Coulter LH 500» и «MaxM» (США). Показатель среднего объема тромбоцитов (MPV) рассчитывался прибором автоматически из гистограммы тромбоцитов.
АДФ-индуцированную агрегацию тромбоцитов исследовали фотометрическим методом на агрегометре «SOLAR» (Беларусь). Концентрация индуктора составляла 2,5 мкМ, 5 мкМ (АДФ производства «Sigma-Aldrich», США). Результат оценивали по изменению степени светопропу-скания в точке максимума, а также по скорости агрегации через 30 с после добавления АДФ. Перед исследованием на проточном цитометре проводили центрифугирование полученной крови при 1500 об./мин в течение 5 мин при комнатной температуре для получения богатой тромбоцитами плазмы (БТП). Обедненную тромбоцитами плазму (ОТП) получали путем центрифугирования БТП при 3000 об./мин в течение 15 мин. ОТП использовали для разведения БТП до 300 тыс. кл/мкл, если это было необходимо, а также для калибровки агрегометра на уровень Т = 100 %. Содержание гликопротеидов IIb/IIIa и Ibα на поверхности тромбоцитов, а также число клеток, экспрессирующих Р-селектин, определяли на проточном цитометре «CYTOMICS FC 500» («Beckman Coulter», США). Использовались меченые моноклональные антитела CD61-FITC, CD62P-PE (Beckman Coulter, США) и VM16d-FITC (Российский кардиологический научнопроизводственный комплекс Росмедтехнологий, РФ). Количество рецепторов IIb/IIIa и Ibα на поверхности тромбоцитов до и после индукции 10 мкМ АДФ оценивали по показателю средней интенсивности флуоресценции. Экспрессию Р-селектина на поверхности тромбоцитов оценивали как процент клеток, меченных CD62P-PE до и после индукции 10 мкМ АДФ. Математически рассчитывались параметры:
-
1) ΔIIb/IIIa, который показывает увеличение в процентах количества рецепторов IIb/IIIa на поверхности тромбоцитов после индукции АДФ;
-
2) ΔР-селектина, показывающий увеличение процента тромбоцитов, экспрессирующих Р-се-лектин после индукции АДФ.
Молекулярно-генетическое исследование включало выявление точечной мутации гена тромбоцитарного гликопротеида 1bα, локали-зованого в 13-м локусе короткого плеча 17-й хромосомы (с.3550С>T – замена С на Т в 3550-й позиции). Наличие данной миссенс-мутации приводит к замене триптофана на метионин в 145-м положении аминокислотной последова- тельности белка (Thr145Met), в результате чего изменяется функциональная активность рецептора к фактору Виллебранда, что предрасполагает к тромбообразованию и увеличивает риск развития сердечно-сосудистых заболеваний почти в 3 раза [10].
Дезоксирибонуклеиновую кислоту (ДНК) выделяли из лейкоцитов крови стандартным фенол-хлороформным методом. Лизис клеток проводили по методу Канкеля с использованием реактивов фирмы «Хеликон» (РФ). Выход ДНК составлял 40–50 мкг ДНК из 500 мкл цельной крови. Для идентификации однонуклеотидных замен использовали амплификацию соответствующего участка гена методом полимеразной цепной реакции (ПЦР) с последующим рестрикционным анализом. Амплификацию проводили на амплификаторе «Терцик» (термостат программируемый четырехканальный для проведения ПЦР анализа ТП4-ПЦР-01 – «Терцик» ТУ 9452–001–46482062–98, НПФ «ДНК-Технология», РФ) при помощи термостабильной вы-сокопроцессивной рекомбинантной Taq ДНК полимеразы фирмы «Fermentas» (Литва). В результате реакции получали фрагмент 587 полинуклеотидов, который подвергался ферментативному расщеплению с помощью рестриктазы Hin 1I (1 ед.) в рестрикционном буфере. Продукт рестрикционного анализа электрофоретически разделяли при 30 мА (150 В) в полиакриламидном геле в трис-боратном буфере. Результаты визуализировали в ультрафиолетовом свете после окрашивания бромистым этидием. В случае нормального аллельного варианта (Thr) определялись фрагменты 270 полинуклеотидов, 201 полинуклеотид и 1163 полинуклеотида, при мутации образуются фрагменты 386 полинуклеотидов и 201 полинуклеотид (Met).
Статистическую обработку результатов выполняли с использованием пакета программ Statistica 6,0 for Windows (StatSoft Inc.). Изучаемые количественные признаки представлены в виде М ± σ, где М – среднее, σ – одно стандартное отклонение. Проверка нормальности распределения проводилась по критерию Шапиро – Уилкса. Для проверки гипотезы о равенстве средних для двух групп использовались параметрические (t-Стьюдента для независимых выборок; t-Стьюдента для связанных выборок) или непараметрические (χ2, Манна – Уитни, Вилкок-сона) критерии. Различия считались статистически значимыми при p < 0,05.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Основные клинические проявления ИИ у обследованных пациентов представлены на рисунке. У больных с АТИ выявлялись афазия, гемианопсия, нехарактерные для ЛИ.
Значения NIHSS и шкалы Ранкина в 1-й и 2-й группах при поступлении и при выписке
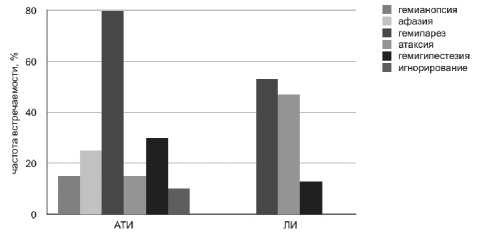
Клинические проявления инсульта у пациентов 1-й и 2-й групп представлены в табл. 1. Наблюдалось достоверно (р < 0,05) более высокое значение NIHSS при поступлении у больных с АТИ, что свидетельствовало о более тяжелом состоянии указанных пациентов. Также у пациентов с АТИ был выявлен значимо (р < 0,05) более высокий балл по шкале Ранкина при выписке, что указывало на выраженное нарушение функциональной независимости. Полученные различия могут быть объяснены большим размером очага при АТИ по сравнению с ЛИ, что предполагает более тяжелое течение заболевания [5].
Таблица 1
Значения клинических шкал у пациентов с различными вариантами ИИ
|
Группа пациентов |
NIHSS, балл |
Шкала Ранкина, балл |
||
|
при поступлении |
при выписке |
при поступлении |
при выписке |
|
|
1-я |
7,6 ± 3,1* |
3,4 ± 2,0 |
2,7 ± 0,7 |
1,8 ± 0,7* |
|
2-я |
4,8 ± 2,6* |
2,3 ± 1,7 |
2,3 ± 0,6 |
1,3 ± 0,5* |
Примечание. * – p < 0,05.
Наблюдалось достоверное уменьшение показателей клинических шкал при выписке по сравнению со значениями при поступлении в обеих группах (р < 0,05), что указывало на благоприятное течение ИИ у обследованных пациентов.
Количество тромбоцитов у пациентов 1-й группы при поступлении составило 233,7 ± 60,6 × 109 / л, MPV – 10,0 ± 1,0 фл, на 10-й день соответственно 225,2 ± 40,0 × 109 / л и 10,4 ± 1,0 фл. У больных 2-й группы указанные показатели были 244,7 ± 59,1 × 109 / л, 8,7 ± 0,9 фл, 217,7 ± 39,8 × 109 / л и 9,0 ± 1,1 фл. Достоверного различия тромбоцитарных показателей гемограммы при поступлении и при выписке у пациентов 1-й и 2-й групп не наблюдалось (р > 0,05). В течение первых 10 суток заболевания было выявлено снижение MPV в обеих группах (р < 0,05), что свидетельствовало об уменьшении размеров тромбоцитов. MPV рассматривают как один из маркеров функционального исхода ишемического инсульта. Снижение значений данного показателя в динамике заболевания может указывать на благоприятный прогноз инсульта у обследованных пациентов [12].
Исследование агрегации тромбоцитов показало более (р < 0,05) высокие значения степени агрегации при стимуляции 2,5 и 5 мкмоль АДФ у здоровых лиц по сравнению с основной группой (табл. 2). Полученные данные могут быть связаны с влиянием постоянно проводимой антиагрегантной терапии в основной группе, изменяющим взаимодействие тромбоцита с индуктором агрегации.
Таблица 2
Агрегометрические показатели у обследуемых с ишемическим инсультом и лиц контрольной группы
|
Индуктор агрегации |
Пациенты с инсультом |
Контрольная группа |
||
|
Степень,% |
Скорость, % / мин |
Степень, % |
Скорость, % / мин |
|
|
2,5 мкмоль АДФ |
54,1 ± 20,0* |
23,7 ± 9,1 |
85,3 ± 28,1* |
29,8 ± 14,1 |
|
5 мкмоль АДФ |
64,9 ± 19,6* |
26,7 ± 10,0 |
83,8 ± 23,7* |
32,8 ± 14,9 |
Примечание. * – p < 0,05.
Степень агрегации тромбоцитов при стимуляции 2,5 мкмоль АДФ в 1-й группе составила 54,4 ± 18,1 %, во 2-й – 53,8 ± 23,0 %; скорость агрегации была соответственно 24,7 ± 9,1 % / мин и 22,3 ± 9,3 % / мин. При стимуляции 5 мкмоль АДФ степень агрегации в 1-й группе была равна 65,6 ± 21,2 %, во 2-й – 64,0 ± 17,8 %; скорость агрегации составила соответственно 26,9 ± 10,3 % / мин и 26,5 ± 9,8 % / мин. Достоверных различий агрегометрических данных у пациентов 1-й и 2-й групп выявлено не было (р > 0,05).
Показатели экспрессии тромбоцитами Р-се-лектина приведены в табл. 3. Наблюдалось достоверно (р < 0,05) более высокое количество тромбоцитов, экспрессирующих Р-селектин после стимуляции АДФ в основной группе по сравнению с контрольной. Экспрессия Р-селектина является специфическим маркером активации тромбоцита, отражающим его конформационные изменения, поскольку в неактивированном состоянии Р-селектин депонирован в α-гранулах тромбоцита [11]. Выявление активации тромбоцитов у пациентов с ИИ по сравнению с контрольной группой при проточной цитометрии может свидетельствовать о предпочтительности данного метода по сравнению со стандартной аг-регометрией. Достоверного различия показателей экспрессии Р-селектина у больных 1-й и 2-й групп выявлено не было (р > 0,05).
Таблица 3
Экспрессия Р-селектина на тромбоцитах в обследуемых группах
|
Группа |
Тромбоциты, экспрессирующие Р-селектин, % |
||
|
базальный уровень |
стимулированный АДФ |
∆ |
|
|
Основная |
6,0 ± 5,7 |
36,1 ± 17,9* |
82,4 ± 14,3 |
|
Контрольная |
4,4 ± 4,5 |
24,1 ± 12,8* |
77,6 ± 18,6 |
Примечание. * – p < 0,05.
В табл. 4 представлены результаты проточной цитометрии (в единицах интенсивности флуоресценции) с определением экспрессии рецепторов IIb/IIIа на поверхности тромбоцита. У пациентов с ИИ наблюдалось более высокое значение D, чем в контрольной группе. До 80 % рецепторов IIb/ IIIa равномерно распределены на мембране тромбоцитов, остальные 20 % находятся в канальцевой системе «внутри тромбоцита» [4]. Таким образом, можно предположить, что полученное высокое значение Δ для пациентов с инсультом связано с наличием у них большей пластичности мембраны активированных тромбоцитов.
|
Таблица 4 Количество рецепторов IIb/IIIa на тромбоцитах в сравниваемых группах |
|||
|
Группа |
Интенсивность флюоресценции |
||
|
базальная |
стимулированная АДФ |
∆, % |
|
|
Основная |
7,4 ± 1,4 |
8,2 ± 1,9 |
12,4 ± 5,0* |
|
Контрольная |
7,5 ± 1,5 |
8,3 ± 2,3 |
8,4 ± 6,9* |
Примечание. * – p < 0,05.
Сравнение уровней экспрессии рецепторов IIb/IIIа на поверхности тромбоцита у пациентов 1-й и 2-й групп значимых различий не выявило (р > 0,05).
Экспрессия рецепторов к фактору Виллебранда на тромбоците (в единицах интенсивности флуоресценции) в основной группе составила 4,3 ± 2,5, в контрольной – 4,9 ± 1,2, достоверного различия выявлено не было (р > 0,05). Экспрессия рецепторов к фактору Виллебранда на тромбоците в 1-й группе была 3,8 ± 1,4, во 2-й – 4,9 ± 3,4, значимого различия не выявлено (р > 0,05).
Гетерозиготное носительство мутантной аллели с.3550С>T наблюдалось у 9 (аллельная частота 12,9 %) пациентов с инсультом и у одного (3,8 %) обследуемого контрольной группы, достоверного различия не было (р > 0,05). В 1-й группе мутантную аллель выявили у 8 (20,0 %) пациентов, что значимо (р < 0,05) больше, чем во 2-й – один больной (6,7 %).
В 1-й группе наблюдалась прямая достоверная корреляция (r = 0,608; p = 0,012) балла NIHSS при выписке с экспрессией рецепторов Ibα на тромбоците, что указывало на худшее восстановление пациентов с более высокой экспрессией рецепторов к фактору Виллебранда на тромбоците. Тромбо-образование определяется взаимодействием фактора Виллебранда со специфическими рецепторами клеток крови, в первую очередь тромбоцитов, и образованием комплекса фактор Виллебранда – рецептор к фактору Виллебранда – IX–V. В доступной нам литературе нет данных об экспрессии рецепторов к фактору Виллебранда на тромбоците у пациентов с АТИ. Перспективным направлением терапии у данных пациентов могут стать препараты, направленные на блокаду рецептора к фактору Виллебранда или комплекса фактор Виллебранда – рецептор к фактору Виллебранда.
Во 2-й группе наблюдалась прямая достоверная корреляция балла по шкале Ранкина при выписке с показателями агрегации тромбоцитов: скоростью агрегации тромбоцитов при индукции 2,5 мкмоль АДФ (r = 0,800; p = 0,005), значением D P-селектина (r = 0,722; p = 0,018). Полученная корреляционная связь указывала на худшее восстановление функциональной независимости больных ЛИ с повышенной агрегацией и активацией тромбоцитов.
ЗАКЛЮЧЕНИЕ
Проведенное исследование показало, что у пациентов пожилого возраста с атеротромбо-тическим и лакунарным инсультами наблюдается активация тромбоцитарного звена гемостаза. Стандартная агрегометрия недостаточно информативна для оценки активации тромбоцитов у данных больных. Прогностическое значение для течения острого периода инсульта у пациентов пожилого возраста с атеротромботическим ишемическим инсультом может иметь экспрессия рецептора к фактору Виллебранда на тромбоците. У больных с лакунарным инсультом на восстановление могут оказывать влияние показатели, характеризующие агрегацию и активацию тромбоцитов.
ATHEROTHROMBOTIC AND LACUNAR STROKES IN ELDERLY PATIENTS:
CLINICAL MANIFESTATIONS AND PLATELET HAEMOSTASIS
Список литературы Атеротромботический и лакунарный инсульты у пациентов пожилого возраста: особенности клинических проявлений и тромбоцитарного гемостаза
- Гусев Е. И., Скворцова В. И., Стаховская Л. В. Эпидемиология инсультав России//Журнал неврологиии психиатрии (Приложение «Инсульт»). 2003. С. 4-9.
- Сус лина З. А., Пир адов М. А. Инсульт: диагностика, лечение, профилактика. М.: МЕДпресс-информ, 2009. 288 с.
- Суслина З. А., Танашян М. М., Ионова В. Г. Ишемический инсульт: кровь, сосудистая стенка, антитромботическая терапия. М.: Медицинская книга, 2005. 248 с.
- Шитикова А. С. Тромбоцитарный гемостаз. СПб.: Изд-во СПб ГМУ, 2000. 227 с.
- Adams H. P. Jr., Bendixen B. H., Kappelle L. J. et al. Classification of sup-type of acute ischemic Stroke. Definition for use ina multicenter clinical trial. TOAST. Trial of Org 10172 in acute stroke treatment//Stroke. 1993. Vol. 24. № 1. P. 35-41.
- Antithrombotic Trialists’ Collaboration. Collaborative meta-analysis of randomised trials of antiplatelet therapy for prevention of death, myocardial infarction, and stroke in high risk patient//BMJ. 2002. Vol. 324. № 7329. P. 71-86.
- Biller J., Love B., Marsh III Е. et al. Spontaneous improvement after acute ischemic stroke//Stroke. 1990. Vol. 21. № 7. P. 1008-1012.
- Bonita R., Beaglehole R. Modification ofRankin Scale: recovery ofmotor function after stroke//Stroke. 1988. Vol. 19. № 12. P. 1497-1500.
- Bгott T., Adams H. P., Olinger C. P. et al. Measurement of acute cerebral infarction:a clinical examination scale//Stroke. 1989. Vol. 20. № 7. P. 864-870.
- Gonzalez-Conejero R., Lozano M. L.,Rivera J. et al. Polymorphisms of platelet membrane glycoprotein Ib associated with arterial thrombotic disease//Blood. 1998. Vol. 92. № 8. P. 2771-2776.
- Harrison P., Cramer E. M. Platelet a-granules//Blood Rev. 1993. Vol. 7. № 1. P. 52-62.
- Mayda-Domac F., Misirli H., Yilmaz M. Prognostic role of mean platelet volume and platelet count in ischemic and hemorrhagic stroke//J. Stroke Cerebrovasc. Dis. 2010. Vol. 19. № 1. Р. 66-72.
- Pleis J. R., Lethbridge-Cejku M. Summary health statistics for US adults: National Health Interview Survey, 2006. National Center for Health Statistics//Vital Health Stat. 2007. № 235. P. 1-153.


