Атипичный гемолитико-уремический синдром в клинической практике
Автор: Рогозина Лариса Александровна, Давыдкин Игорь Леонидович, Данилова Олеся Евгеньевна, Фатенков Олег Вениаминович, Гиматдинова Гелия Рифкатовна, Хайретдинов Раис Кеттдусович
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Клиническая медицина
Статья в выпуске: 1, 2023 года.
Бесплатный доступ
Атипичный гемолитико-уремический синдром (аГуС) это системное заболевание из группы тромботических микроангиопатий (ТМА), в основе которого лежит неконтролируемая активация альтернативного пути комплемента наследственной или приобретенной природы, приводящая к генерализованному тромбообразованию в сосудах микроциркуляторного русла. Хроническая активация альтернативного пути комплемента приводит к повреждению эндотелиальных клеток, эритроцитов и тромбоцитов и, как следствие, к тромботической микроангиопатии и системному мультиорганному поражению. В настоящее время почти в половине случаев триггер аГуС выявить не удается. В лечении с целью купирования симптомов в качестве препаратов первой линии применяются свежезамороженная плазма (СЗП), что позволяет устранить дефицит собственных белков фактора комплемента Н и I (CFH и CFI), мембранного кофакторного протеина (MCP), и комплекс стабильных и лабильных белков факторов гемостаза, что позволяет остановить тромбообразование в микроциркуляторном русле. Применение СЗП является подготовительным этапом перед антикомплементарной терапией. Прогноз заболевания всегда серьезный и ассоциирован с тяжелыми осложнениями и высокой смертностью. Не менее чем у 6 % пациентов развивается полиорганная недостаточность с признаками генерализованной ТМА, поражением ЦНС, органов ЖКТ, легких и, безусловно, почек. Представлено собственное клиническое наблюдение больной и аГуС.
Тромботическая микроангиопатия, атипичный гемолитико-уремический синдром, adamts-13, комплемент
Короткий адрес: https://sciup.org/14127224
IDR: 14127224 | УДК: 616-005.6.616.151.294+616.61-008.64 | DOI: 10.34014/2227-1848-2023-1-6-13
Atypical hemolytic uremic syndrome: a case study
Atypical hemolytic uremic syndrome (aHUS) is a systemic disease, a type of thrombotic microangiopathy (TMA). It is based on uncontrolled activation of the alternative complement pathway of a hereditary or acquired nature, leading to generalized thrombosis in the microvasculature. Chronic activation of the alternative complement pathway leads to the damage of endothelial cells, erythrocytes and platelets and, as a result, to thrombotic microangiopathy and systemic multiorgan damage. Currently, in roughly half of the cases, it is impossible to identify aHUS triggers. Fresh frozen plasma (FFP) is used as first-line drug to reverse the symptoms. It helps to eliminate the deficiency of self-proteins complement factor H and complement factor I (CFH and CFI), membrane cofactor protein (MCP), and stable and labile proteins factors of hemostasis, and to stop thrombosis in the microvasculature. FFP administration is a preparatory step before anticomplementary therapy. Disease prognosis is always serious and is associated with severe complications and high mortality. At least 6 % of patients develop multiple organ failure with generalized TMA, injury of the central nervous system, gastrointestinal tract, lungs, and kidneys. The paper describes a clinical case of a patient with aHUS.
Текст научной статьи Атипичный гемолитико-уремический синдром в клинической практике
В настоящее время тромботическая микроангиопатия (ТМА) включает в себя большую многообразную группу состояний, для которой характерна общая гистологическая картина, но разные механизмы развития [1, 2]. В основе ТМА лежат образование тромбов и эндотелиальные повреждения, приводящие к тяжелым органным повреждениям, главным образом – к почечной недостаточности с тромбоцитопенией и микроангиопатической гемолитической анемией (МАГА) [3–8]. Генетический дефект металлопротеазы (ADAMTS-13), расщепляющей фактор Виллебранда, из-за сниженной активности способствует образова- нию микротромбов [9]. Вследствие массивного тромбообразования потребляется большое количество тромбоцитов, что обусловливает их количественное уменьшение, в результате распространенный процесс в микроциркулятор-ном русле приводит к массивному ишемическому повреждению различных органов: сердца, почек, желудочно-кишечного тракта [10].
С течением времени все больше расширяется список возможных этиологических факторов, приводящих к неконтролируемой активации комплемента в альтернативном пути. Сегодня накоплено достаточно данных о взаимосвязи новой коронавирусной инфекции
(COVID-19) и тромботической микроангиопатии [11, 12]. Учитывая механизмы повреждения микрососудистого русла, особенно важно своевременно диагностировать ТМА и провести патогенетическое лечение, что, однако, затруднено, так как требуются глубокий клинико-лабораторный анализ, а также контроль ряда генетических факторов.
В данной статье мы представляем клинический случай атипичного гемолитико-уремического синдрома (аГУС) у пациентки, получавшей терапию препаратом «Экулизумаб» в условиях нефрологического отделения Клиник СамГМУ.
Описание клинического случая. Пациентка Б., 49 лет, жительница Самарской области. С 10-х чисел июля 2020 г. стала отмечать нарастающую одышку на фоне лихорадки в течение 8 дней до 37,8–39,5 °С. При госпитализации в инфекционную клинику диагностирована коронавирусная инфекция, вызванная COVID-19, с поражением 30 % легких. Подтверждение ПЦР-диагностикой не получено, вирус не идентифицирован. Дальнейшее лечение получала в терапевтическом отделении Чапаевской ЦРБ, где находилась с диагнозом «внебольничная двусторонняя бактериальновирусная пневмония средней степени тяжести, дыхательная недостаточность 1 степени», откуда выписана через 7 дней для прохождения амбулаторного лечения.
В течение последующих 24 дней после выписки из стационара наблюдались жалобы на выраженную слабость, мучительную тошноту, многократную рвоту желчью, боль в животе, преимущественно в правом подреберье, жидкий стул до 5–7 раз в сут. В анализах крови сохранялся лейкоцитоз ((11…17)×109/л), в биохимическом анализе крови впервые выявлены повышение креатинина (224 мкмоль/л), увеличение мочевины (13,1 ммоль/л).
С подозрением на обострение хронического панкреатита пациентка доставлена в хирургическое отделение. В связи с диагностированным острым повреждением почек (олигурия, креатинин сыворотки крови 644 мкмоль/л) на фоне снижения количества тромбоцитов (32×109/л) 03.09.2020 переведена в нефрологическое отделение Клиник СамГМУ.
При поступлении состояние пациентки соответствовало средней степени тяжести. В сознании. Кожный покров бледный, отеки нижних конечностей, передней брюшной стенки, в легких с обеих сторон – влажные хрипы в нижних отделах, частота дыхания – 21 в 1 мин, частота сердечных сокращений (ЧСС) – 102 уд./мин, АД – 150/120 мм рт. ст. При обследовании отмечена быстро нарастающая анемия (гемоглобин 93–67 г/л), тромбоцитопения (32×109/л), в биохимическом анализе крови – повышение креатинина (644 мкмоль/л), уровни трансаминаз были в пределах нормы (АСТ 12 ЕД/л, АЛТ 34 ЕД/л), гипокалиемия (2,7 ммоль/л), гипонатриемия (132 ммоль/л). В общем анализе мочи – протеинурия (5,0 г/л), микрогематурия. Тяжесть состояния определялась выраженной анемией, тромбоцитопенией, острым повреждением почек, что потребовало начала заместительной почечной терапии сеансами продленной вено-венозной гемодиафильтрации (ПВВГДФ).
В течение последующих дней наблюдалась трудно корригируемая артериальная гипертензия (АД 190/100 мм рт. ст.). Сочетание тромбоцитопении и анемии позволило заподозрить тромботическую микроангиопатию, что потребовало проведения некоторых анализов, показавших следующие результаты: проба Кумбса – негативная, шизоциты в крови – 17 %, резкое снижение концентрации гаптоглобина до 0,11 г/дл (норма 2–14 г/дл), ЛДГ – 1050 ЕД/л (норма 240–480 ЕД/л). При дополнительном обследовании были выявлены диффузные изменения почек с увеличением размеров с обеих сторон (справа 120×62 мм, слева 122×66 мм). С учетом развития полиор-ганной недостаточности у пациентки с признаками микроангиопатического гемолиза и тромбоцитопении была констатирована тромботическая микроангиопатия. В целях исключения вторичной ТМА проводилась дифференциальная диагностика системной красной волчанки (СКВ), антифосфолипидного синдрома (АФС) (первичного и вторичного), ВИЧ-инфекции, онкопатологии и ДВС-син-дрома (по шкале ISTH явного ДВС-синдрома набрано 3 балла). Сходные клинико-лабораторные проявления первичных форм ТМА по- требовали исключения тромботической тромбоцитопенической пурпуры (ТТП), для чего проведено исследование на ADAMТS-13, уровень которой составил 13–49 % (референсные значения 93–113 %), что в итоге позволило диагностировать аГУС. Еще одним доводом в пользу развития комплементопосредованной ТМА послужила выявленная гипокомплементемия – снижение концентрации С3-компонента комплемента до 0,55 г/л (норма 0,9–1,8 г/л), что свидетельствует о его повышенном потреблении. Генетический анализ выявил наличие антител к фактору Н (17,8 AU/ml), что дало основание подтвердить наличие атипичного гемолитико-уремического синдрома. К сеансам ПВВГДФ, трансфузиям отмытых эритроцитов (11 сеансов гемотрансфузий), ан- тибактериальной и дезинтоксикационной терапии с 03.09.2020 по 12.09.2020 добавили лечение свежезамороженной плазмой (СЗП) в режиме плазмообмена № 2 из расчета 80 мл на 1 кг веса с последующими инфузиями СЗП до 12-го дня госпитализации, с 06.09.2020 был добавлен гепарин 5000 ЕД подкожно 3 раза в день. Для лечения артериальной гипертензии использовались ингибиторы АПФ, бета-блокаторы, антагонисты кальция.
На 12-е сут после начала лечения появилась тенденция к незначительному улучшению: рост числа тромбоцитов в крови до 96×109/л, увеличение диуреза (2,5 л/сут), снижение ЛДГ до 690 МЕ/л на фоне снижения уровня креатинина сыворотки в крови до 240 мкмоль/л (рис. 1).
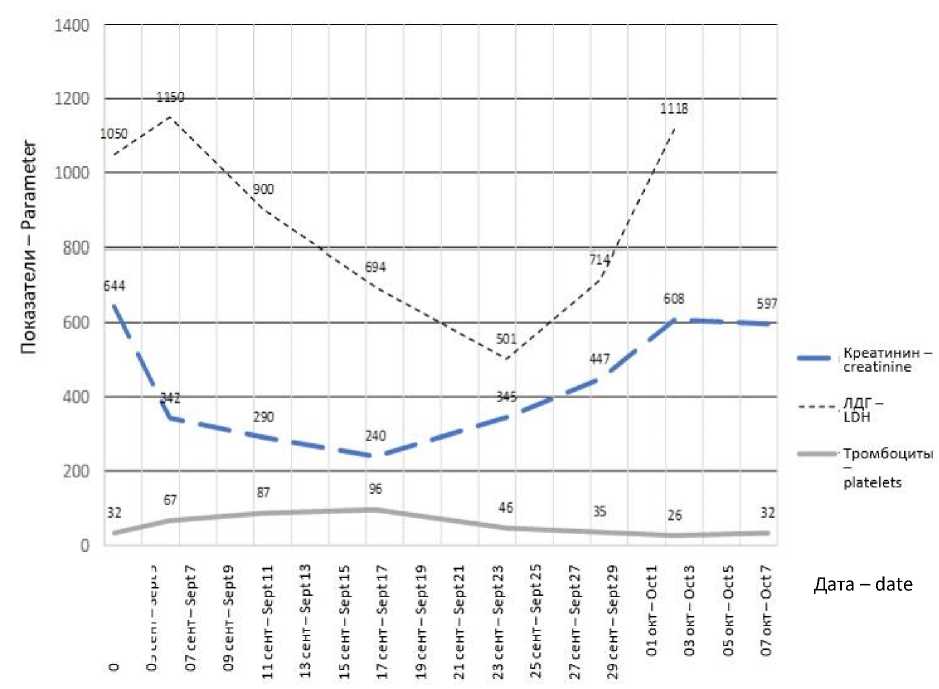
Рис. 1. Динамика уровня креатинина, ЛДГ, тромбоцитов при госпитализации
Fig. 1. Changes in creatinine, LDH, and platelet levels on hospital admission
К 16-му дню госпитализации получено экспертное заключение из ФГАОУ ВО Первый МГМУ им. М.И. Сеченова Минздрава Рос- сии, завизированное профессором С.В. Моисеевым, профессором Н.Л. Козловской, доцентом Ю.М. Коротчаевой, где учтены осо- бенности клинико-лабораторной картины, включающие дебют после перенесенной пневмонии, предположительно вирусной этиологии, наличие полиорганной недостаточности, показатель ADAMS-13 (13–49 %), что подтвердило диагноз атипичного гемолитико-уремического синдрома (аГУС) и позволило включить пациентку в региональный сегмент Федерального регистра лиц, страдающих жизнеугрожающими и хроническими прогрессирующими редкими (орфанными) заболеваниями, приводящими к сокращению жизни граждан, и запустить алгоритм получения жизненно важного препарата «Экулизумаб». В целях иммунизации против Neisseria meningitidis пациентка 22.09.2020 вакцинирована препаратом «Менактра».
Однако через 12 дней после отмены инфузий СЗП (с 25.09.2020) констатирован рецидив – явления интоксикации, поражение ЦНС, абдоминальный, тромбогеморрагический синдромы: лихорадка до 38–39 °С, петехии, обширные экхимозы на передней поверхности бедер, руках, потеря сознания, множественные судорожные припадки, неконтролируемый уровень артериального давления (190– 220 на 100–120 мм рт. ст.). В общем анализе крови – гемолитическая анемия (эритроциты 2,06×1012/л, гемоглобин 39 г/л), лейкоцитоз (17,01×1012/л), повышение ЛДГ (1180 МЕ/л), увеличение СРБ до 144 мг/л (норма 5 мг/л). В последующем лечение проводилось в условиях отделения реанимации и интенсивной терапии. Тяжелое состояние пациентки было обусловлено наличием полиорганной недостаточности, в основном за счет поражения ЦНС, и присоединившейся клиникой острого живота, что в итоге повлияло на решение консилиума о проведении диагностической лапаротомии с подозрением на тромбоз мезентериальных сосудов с последующим решением вопроса дальнейшей тактики. В результате исследования исключена хирургическая патология. На фоне антибиотикотерапии («Меронем», «Левофлоксацин») проведена индукционная терапия «Экулизумабом» – 900 мг 1 раз в неделю № 2 (28.09.2020, 05.10.2020), которая к успешному исходу не привела. Несмотря на проведение антикомплементарной терапии, пациентка скончалась.
Патологоанатомический диагноз: D 59.3 Атипичный гемолитико-уремический синдром. Кровоизлияния: субэпикардиально, суб-плеврально, в брыжейке кишечника, тромбоз мелких ветвей легочной артерии. Острое нарушение мозгового кровообращения по геморрагическому типу в правой гемисфере головного мозга с прорывом в желудочки и вторичными ишемическими изменениями левой гемисферы. Отек головного мозга. Вклинение ствола.
Обсуждение. Вышеизложенное клиническое наблюдение демонстрирует сложности диагностики аГУС у больного, обследование которого проводилось в два этапа. На первом этапе установлен симптомокомплекс, подтвердивший ТМА, в ходе дальнейшей дифференциальной диагностики исключены основные формы первичной ТМА, для которых характерны сходные клинико-лабораторные проявления. На протяжении госпитализации были исключены вторичные причины ТМА: СКВ (отрицательный волчаночный антикоагулянт и негативные показатели аутоиммунного воспаления), катастрофический АФС (b2-гликопротеин-1, антитела к кардиолипину не выявлены) и ВИЧ-инфекция, что позволило исключить вторичный механизм ТМА. Триггером ТМА в данном случае могла послужить неподтвержденная вирусная инфекция, предположительно SARS-CoV-2 [13–15].
Многообразие клинической картины в совокупности с длительным анамнезом заболевания и достаточно поздним введением препарата «Экулизумаб» не привели к успеху, вследствие чего не удалось избежать потери пациентки. Описанный нами клинический опыт дает основание предположить, что разбор неудачного случая поможет помочь распознать данную патологию на более ранних этапах.
Внесение аГУС в программу льготного обеспечения пациентов, страдающих 14 редкими и высокозатратными нозологиями, способствует доступности и более раннему началу антикомплементарной терапии у данной категории пациентов.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Вклад авторов
Концепция и дизайн исследования: Рогозина Л.А., Давыдкин И.Л.
Участие в исследовании, обработка материала: Фатенков О.В., Гиматдинова Г.Р.
Статистическая обработка данных: Рогозина Л.А., Данилова О.Е., Хайретдинов Р.К.
Анализ и интерпретация данных: Рогозина Л.А., Данилова О.Е.
Написание и редактирование текста: Хайретдинов Р.К., Гиматдинова Г.Р., Рогозина Л.А.
Список литературы Атипичный гемолитико-уремический синдром в клинической практике
- Fakhouri F., Roumenina L., Provot F. Pregnancy-associated hemolytic uremic syndrome revisited in the era of complement gene mutations. J. Am. Soc. Nephrol. JASN. 2010; 21 (5): 859-867.
- Fakhouri F., Vercel C., Fremeaux-Bacchi V. Obstetric Nephrology: AKI and Thrombotic Microangiopathies in Pregnancy. Clin. J. Am. Soc. Nephrol. 2012; 7: 2100-2106. URL: https://pubmed.ncbi. nlm.nih.gov/ (дата обращения: 09.09.2022). DOI: 10.2215/CJN.13121211.
- Акиньшина С.В., Бицадзе В.О., Гадаева З.К., Макацария А.Д. Значение тромботической микроан-гиопатии в патогенезе акушерских осложнений. Акушерство, гинекология и репродукция. 2015; 9 (1): 62-71.
- Коротчаева Ю.В., Козловская Н.Л., Бондаренко Т.В. Акушерский атипичный гемолитико-уреми-ческий синдром: трудный диагноз? Архив акушерства и гинекологии им. В.Ф. Снегирева. 2015; 2: 36-41.
- Мочалова М.Н., Белокриницкая Т.Е., Хавень Т.В. Клинический случай тромботической микроан-гиопатии в акушерской практике. Сеченовский вестник. 2017; 2 (28): 28-32.
- Слуханчук Е.В., Бицадзе В.О., Хизроева Дж.О. COVID-19 и тромботическая микроангиопатия. Акушерство, гинекология и репродукция. 2021; 15 (6): 639-657.
- Kentouche K., Voigt A., Schleussner E. Pregnancy in Upshaw-Schulman syndrome. Hamostaseologie. 2013; 33 (2): 144-148.
- Torok T.J., Holman R.C., Chorba T.L. Increasing mortality from thrombotic thrombocytopenic purpura in the United States - analysis of national mortality data, 1968-1991. Am. J. Hematol. 1995; 50: 84-90.
- Yoko Yoshida, Hideki Kato, Yoichiro Ikeda, Masaomi Nangaku. Pathogenesis of Atypical Hemolytic Uremic Syndrome. Atheroscler Thromb. 2019; 26 (2): 99-110. DOI: 10.5551/jat.RV17026.
- Meri S. Complement activation in diseases presenting with thrombotic microangiopathy. Eur. J. Intern. Med. 2013; 24 (6): 496-502.
- Алтынова В.Х., ЭмироваХ.М., Нигматуллина Н.Б. Атипичный гемолитико-уремический синдром в педиатрической практике. Клиническая фармакология и терапия. 2016; 25 (3): 83-89.
- Козловская Н.Л. Атипичный гемолитико-уремический синдром: современные представления о патогенезе, клинике, подходах к диагностике и лечению. Тромбоз, гемостаз и реология. 2019; 4 (80): 13-20.
- Bitzan М., Zieg J. Influenza-associated thrombotic microangiopathies. Pediatr Nephrol. 2018; 33 (11): 2009-2025.
- Harin Rhee, Sang Heon Song, Yong Jae Lee. Pandemic H1N1 influenza A viral infection complicated by atypical hemolytic uremic syndrome and diffuse alveolar hemorrhage. Clin Exp Nephrol. 2011; 15 (6): 948-952. URL: https://pubmed.ncbi.nlm.nih.gov/ (дата обращения: 09.09.2022). DOI: 10.1007/s10157-011-0516-z.
- Ganesan C., Sharon E. Maynard Acute kidney injury in pregnancy: the thrombotic microangiopathies. J. Nephrol. 2011; 24 (5): 554-563. URL: https://pubmed.ncbi.nlm.nih.gov/21240869/ (дата обращения: 09.09.2022). DOI: 10.5301/JN.2011.6250.


