Аутофагия как природно-оздоровительный механизм
Автор: Малозмов О.Ю., Зайцева А.А., Андреев А.Л., Харламов А.И.
Журнал: Теория и практика современной науки @modern-j
Рубрика: Медицина и здоровье
Статья в выпуске: 9 (63), 2020 года.
Бесплатный доступ
В статье рассматривается один из природообусловленных процессов сохранения гомеостаза - аутофагия. Рассмотрены типы аутофагии. Показана роль данного природного феномена и факторы, способствующие его инициации.
Аутофагия, голодание, двигательная активность
Короткий адрес: https://sciup.org/140275701
IDR: 140275701 | УДК: 616-003
Autophagy as a natural health mechanism
The article deals with one of the natural processes of preserving homeostasis - autophagy. Types of autophagy are considered. The role of this natural phenomenon and the factors contributing to its initiation are shown.
Текст научной статьи Аутофагия как природно-оздоровительный механизм
В настоящее время, как, впрочем, и во многие предшествующие эпохи, людей интересовали вопросы здорового существования и продления самой жизни. Многое в данной сфере сводится к рационализации в образе жизни, аспектами которой являются: адекватная двигательная активность, рациональность в питании, своевременная медицинская помощь, снижение влияния заведомо вредных, опасных для здоровья аддикций и многое другое. В данном случае обратимся к рассмотрению феномена «аутофагии» – одного из интересных природных процессов, происходящем на клеточном уровне, позволяющем снизить риск многих заболеваний, способствующем здоровому психофизическому долголетию человека.
Процесс аутофагии это неотъемлемая часть жизнедеятельности любой клетки. Понятна заинтересованность в исследовании данного феномена, поскольку аутофагия является ключевым физиологическим процессом диссимиляции – выведением из клеток, повреждённых органелл, агрегированных белков и внутриклеточных патогенов [2]. Аутофагия (с греч. «самопоеда-ние») – это процесс утилизации клеточных органелл и макромолекул [1].
Основным стимулом к усилению процессов аутофагии может служить наличие чужеродных веществ, дефектных белков и агентов, а так же нехватка питательных веществ [2]. Кроме того аутофагия может быть индуцирована окислительным или токсическим стрессом. Из этого следует, что основным активатором аутофагии служит голодание, которое запускает процесс утилизации клеточных органелл и макромолекул. Голодание для клетки является стрессором, который выступает как активатор аутофагии. Таким образом, обеспечивается альтернативный источник внутриклеточных строительных блоков и субстратов, а также энергия для обеспечения непрерывного выжи- вания клеток. На сегодня процесс аутофагии представляют как один из видов программируемой клеточной смерти наряду с такими процессами, как апоптоз и некроптоз.
В 2016 году японский учёный Ясинори Осуми получил нобелевскую премию за «Открытие механизмов аутофагии». Именно он изучил механизм аутофагии, проводя исследования на дрожжевых грибах, обнаружив гены ATG (Autophagy-related Genes), отвечающих за индукцию, протекание и регуляцию аутофагии. В свете сегодняшних знаний механизм аутофагии представляет следующее. В ыделяют три типа аутофагии: микроаутофагия, макроаутофагия и шаперон-зависимая аутофагия (рис.1).
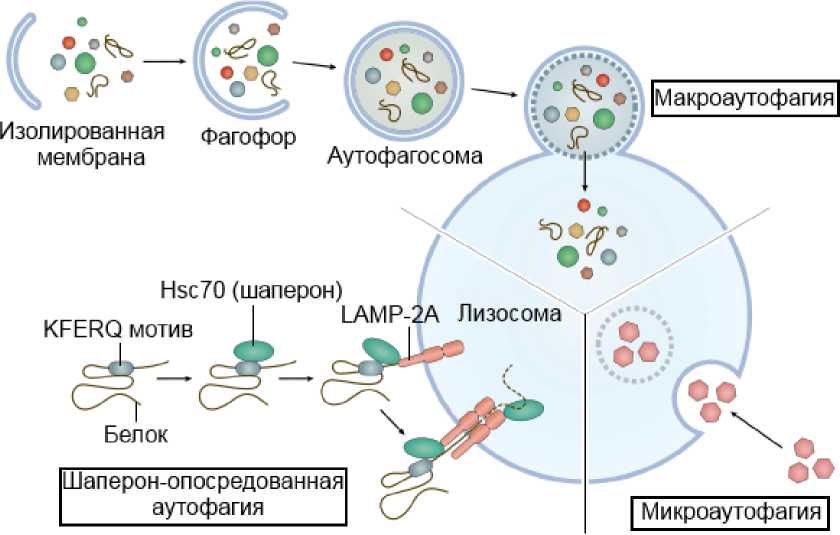
Рис.1. Типы аутофагии.
Процесс микроаутофагии заключается в том, что макромолекулы и остатки клеточных мембран за счёт инвагинации поступают в лизосому. Таким образом, сама клетка в период нехватки энергии или в отсутствие так называемого «строительного материала» может заставлять распадаться белки. Данный тип аутофагии детально описан у дрожжей, но довольно слабо изучен у млекопитающих [5].
При макроаутофагии локус цитоплазмы с содержимым клетки изолируется мембранным компартментом. В итоге данный участок отграничивает- ся от остальной цитоплазмы двухмембранным барьером. Такой вид двухмембранных органелл является так называемыми аутофагосомами. В свою очередь аутофаголизосомы формируются за счёт соединения лизосомами с аутофагосой, в которых органеллы и другое содержимое аутофагосом разлагается. Именно данный вид аутофагии находится под контролем уникальных генов Atg (autophagyrelated gene), регулирующих процесс деградации митохондрий, эндоплазматического ретикулума, пероксисом, рибосом, а также различных белков, липидов и РНК [5].
Третий тип аутофагии - шаперон-зависимая, осуществляющая транспортировку частично денатурировавших белков из цитоплазмы через мембрану лизосомы во внутрь, где эти белки расщепляются. В процесс вовлечены цитоплазматические белки-шапероны семейства hsp-70 (heat shock protein 70), вспомогательные белки и LAMP-2 (lysosome-associated membrane protein type 2A), контролирующие данный процесс. Аутофагия подразделяется на стадии такие, как: инициация, элонгация, формирование аутофагосомы и, на завершающем этапе, формирование аутолизосомы [5].
На рисунке 2 достаточно лаконично представлены основные процессы и состояния, происходящие при участии рассматриваемого феномена и способствующие избеганию заболеваний.
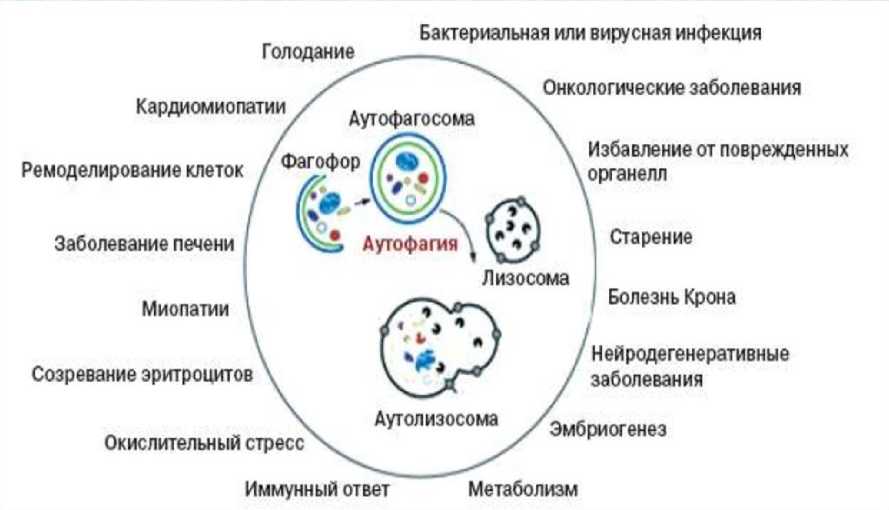
Рис.2. Процессы, происходящие при участии аутофагии.
Понятно, что данный феномен является одним из природных источников поддержания гомеостаза, сохранения здоровья. Возникает закономерный вопрос: как активировать аутофагию для целей борьбы со старением и со старческими заболеваниями ?
Зная гены, отвечающие за процесс аутофагии, можно выборочно инактивировать их у испытуемых организмов (C.elegans), тем самым можно выявить, какие изменения произойдут с организмом, например, при полном отсутствии этих генов. К примеру, если отключить ген atg-7 и atg-12, являющиеся генами аутофагии, c помощью интерферирующих РНК, то в итоге происходит значительное уменьшение продолжительности жизни C.elegans. Ингибирование фактора TOR, подавляющего аутофагию, приводит к активации макроаутофагии, а так же к росту продолжительности жизни подопытных животных [6].
Шаперон-зависимая аутофагия как способ омоложения . В организме человека есть белок LAMP-A, являющийся рецептором клеточных лизосом, благодаря которому осуществляется шаперон-зависимая аутофагия. С возрастом уменьшается количество белка LAMP-A, в результате чего понижается действие шаперон-зависимой аутофагии, а в цитоплазме клеток происходит накопление повреждённых органелл. По результатам эксперимента доктора Куэрво было установлено, что при введении двадцати мышам двухмесячного возраста (возраст, соответствующий 80 годам человека) рецептора LAMP-A уменьшается количество дефектных белков в клетках, и восстанавливается функционирование органов животных. Таким образом, учёным удалось улучшить деятельность печени, можно сказать, что они в прямом смысле этого слова «омолодили» орган. Доктор Куэрво надеется, что это открытие будет способствовать предотвращению процесса старания путём уменьшения количества рецептора LAMP-A. В её планах создать препарат, замедляющего процессы старения и предотвращающего различные заболевания [7].
Основным активатором аутофагии является белок Beclin-1. Профессор Левин в своей лаборатории открыл белок Beclin-1 – главный активатор аутофагии. Данный белок необходим для выживания в период голодания у нематод, поскольку он играет главную роль в процессе аутофагии у низших эукариотов. Пониженная же экспрессия Beclin-1 у человека приводит к повышению вероятности заболевания болезнью Альцгеймера.
Белок Beclin-1 содержит BH3 домен, который обеспечивает связывание этого белка с антиапоптотическими гомологами белка Bcl-2. Таким образом, при создании комплекса Beclin-1/Bcl-2 инактивируется аутофагия. Комплекс Bcl-2/Bcl-XL играет основную роль в регуляции работы белка Beclin-1 в процессе аутофагии. При лечении нейродегенеративных заболеваний можно использовать вещества, которые будут приводить к распаду комплекс Bcl-2/Bcl-XL. Этим можно активировать аутофагию, а при других заболеваниях можно наоборот ингибировать аутофагию [8].
Роль аутофагии при старении в период голодания . При наблюдении за нематодами, подверженными голоданию, выяснилось, что они живут существенно дольше, в сравнении с теми, у которых была пища постоянно. Возникает вопрос, отвечает ли за это аутофагия? Для выяснения этого вопроса учёные инактивировали у долгоживущих нематод-мутантов гены bec-1 и vps-34 (эти гены кодируют белки, участвующие в процессе аутофагии). В итоге нематоды, с нарушенным процессом аутофагии, жили примерно одинаково, как нормально питающиеся нематоды. Следовательно, именно ауто фагия обеспечивает продление жизни у «голодающих» нематод.
Из этого можно сделать вывод, что аутофагия способствует предотвращению процессов старения в организме, поэтому она занимает важную нишу в медицине, ведь благодаря ей мы можем выглядеть моложе, иметь более здоровое тело за счёт активации её с помощью голодания [9].
Основные способы вызвать процесс аутофагии в организме человека: 1) аэробные физические упражнения, 2) краткосрочное голодание и ограничение калорий.
Было установлено, что при аэробных физических упражнениях происходит увеличение аутофагии в мышцах и нервной ткани. Связано это с тем, что при физических нагрузках на организм клетка испытает стресс, способствующий активации аутофагии. Таким образом, физические нагрузки играют немаловажную роль в активации аутофагии, а значит – замедлению старения организма. Кроме того в одном из наблюдений было установлено, что при физических нагрузках аутофагия так же активируется и в мозге, предотвращая развитие нейродегенеративных заболевай путём утилизации деструктивных белков из нейрона. Поэтому даже утренние пробежки могут быть одним из факторов активации аутофагии и улучшения общего состояния организма.
Как было показано выше, голодание является неотъемлемой частью активации аутофагии . Именно этот процесс может способствовать переработке дефектных органелл, деструктивных белков и даже раковых клеток, обеспечивая должную жизнедеятельность клетки при отсутствии внешних источников энергии. Следует также отметить, что голодание может довольно значительно снизить риск возникновения когнитивных расстройств, деменции, болезни Альцгеймера и болезни Паркинсона.
Польза аутофагии для организма заключается в следующем.
-
1. Продление продолжительности жизни . Аутофагия препятствует процессам старения за счёт самоуничтожения «ненужных» ей органелл, усиливая тем самым метаболические процессы в организме человека. В частности, аутофагия задействована в удалении дисфункциональных митохондрий (митофагия), которые производят большое количество вредных активных форм кислорода, расщепляющих клетки. Таким образом, данный процесс продлевает жизнь за счёт деструкции внутриклеточных патогенов.
-
2. Защита от психических расстройств . Действие аутофагии наблюдается во всех тканях организма. В нервной ткани роль аутофагии также очень высока, поскольку благодаря ей осуществляется профилактика нейро-дегенеративных заболеваний, в частности такого заболевания, как Альцгей-
- мер. Доказательством этому служат, опубликованные результаты аутопсии (посмертного вскрытия) мозга людей, страдающих при жизни депрессией или шизофренией, у которых был выявлен недостаток основных проводящих путей аутофагии.
-
3. Помощь в борьбе с инфекционными заболеваниями . Аутофагия использует такие механизма защиты от инфекций, как удаление чужеродного микроорганизма из самой клетки, в том числе и выведение токсина из клетки, а так же она регулирует иммунный ответ организма. Инфекционные микробы (такие как микобактерии туберкулёза и стрептококк группы А), а также вирусы (такие как ВИЧ), удаляются из организма при помощи процессов аутофагии.
-
4. Помощь в регулировании воспаления . Аутофагия способна усиливать или ослаблять воспалительный процессы в организме. При увеличении воспалительного процесса аутофагия сигнализирует о повышенной концентрации титра антител в организме заболевшего человека. Уменьшение воспаления свидетельствует об утилизации антигенов из клетки, то есть действие иммунного ответа.
-
5. Участие в профилактике онкологических заболеваний . Аутофагия может замедлять рост раковых клеток на начальных стадиях канцерогенеза. Например, мыши с генетически модифицированным (нарушенным) уровнем аутофагии более склонны к раковым заболеваниям. Аутофагия выступает в роли супрессора развития новообразований. Например, экспрессия экзоген-
- ного Beclin-1 (одного из главных регуляторов молекулярных механизмов аутофагии) снижает пролиферативную способность опухолевых клеток in vitro, а также их канцерогенный потенциал in vivo [4].
Поскольку многие нейродегенеративные заболевания связаны с накоплением отмерших нейронов и повреждённых белков, то результатом становится утрата умственных способностей. Аутофагия выступает в роли защитника организма от подобных заболеваний. У пациентов с болезнью Хантингтона (генетическое заболевание нервной системы) аутофагия удаляет белок гентингтин (НТТ), у пациентов с болезнью Альцгеймера – амилоид β (созданный из белка АРР), у пациентов с болезнью Паркинсона - о -синуклеин (SNCA), а у пациентов с деменцией – тау-белок (МАРТ) [3].
Итак, можно подытожить основные выводы из вышеизложенного.
-
1. Аутофагия наблюдается во многих процессах жизнедеятельности клеток, и её нарушения наблюдаются при многих заболеваниях.
-
2. На клеточном уровне аутофагия проявляется в: 1) поддержании гомеостаза во время неустойчивости питательной среды, 2) удаляет дисфункциональные, вредные органеллы. На организменном уровне аутофагия способствует: 1) уменьшению онкогенеза, 2) поддержанию функции нейронов, 3) уменьшению воспаления, 4) улучшению мобилизации липидов, 5) улучшению эффероцитоза. В целом – продлевает жизнь.
-
3. Медико-биологическое знание находится ещё в начале изучения данного механизма и в способности его применения на человеческом организме (например, в виде препаратов). Поэтому исследователям предстоит большой объём работы в развитии использования данного механизма в лечении больных.
-
4. Эксперименты и доказанные гипотезы о положительном воздействии аутофагии на организм, говорят о том, что мы можем самостоятельно запускать данный процесс.
-
5. Даже имеющаяся неполная информация об этом феномене даёт представление о его важности для любого организма на планете.
Список литературы Аутофагия как природно-оздоровительный механизм
- Зенков Н.К. Аутофагия как механизм защиты при окислительном стрессе / Н.К. Зенков, А.В. Чечушков, П.М. Кожин, Г.Г. Мартинович, Н.В. Кандалинцева, Е.Б. Меньщикова // Бюллетень сибирской медицины. - 2019. - №18. - С.195-214.
- Ковалёва О.В. Аутофагия: клеточная гибель или способ выживания? / О.В. Ковал'ва, М.С. Шитова, И.Б. Зборовская // Клиническая онкогематология. - 2014. - №2. - С.103-113.
- Аутофагия сила естественного очищения [Электронный ресурс]. - Режим доступа: http://mayorov.online/ (дата обращения 15.04.20).
- Liang X.H., Jackson S., Seaman M. et al. Induction of autophagy and inhibition of tumorigenesis by beclin 1. Nature 1999; 402: 672-6.
- Anding A.L., Baehrecke E.H. Cleaning house: Selective autophagy of organelles. Dev. Cell. 2017; 41 (1): 10-22. 10.1016/j.devcel. 2017.02.016. DOI: 10.1016/j.devcel.2017.02.016
- Mijaljica D., Prescott M., Devenish R.J. MicroAutophagy in mammalian cells: Revisiting a 40-year-old conundrum. Autophagy 2011; 7: 673-82.
- Ravikumar, B., Futter, M., Jahreiss, L., Korolchuk, V. I., Lichtenberg, M., Luo, S., Massey, D. C. O., Menzies, F. M., Narayanan, U., Renna, M., Jimenez-Sanchez, M., Sarkar, S., Underwood, B., Winslow, A. and Rubinsztein, D. C. Mammalian macroautophagy at a glance. Gournal of Cell Science. Volume 122 (11) June 1, 2009.
- Restoration of chaperone-mediated autophagy in aging liver improves cellular maintenance and hepatic function [Электронный ресурс]. - Режим доступа: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2722716/?tool=pubmed (дата обращения 15.04.20).
- A C.elegans mutant that lives twice as long as wild type. [Электронный ресурс]. - Режим доступа: https://www.ncbi.nlm.nih.gov/pubmed/8247153?ordinalpos=75&itool=EntrezSystem2.PEntrez.Pubmed.Pubmed_ResultsPanel.Pubmed_DefaultReportPanel.Pubmed_RVDocSum (дата обращения 15.04.2020).


