Азиатский нозематоз пчел, вызванный микроспоридией Nosema (Vairimorpha) ceranae: современные представления, патогенез, профилактика, диагностика и лечение обзор)
Автор: Тимофеев С.А., Игнатьева А.Н., Долгих В.В.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Обзоры, проблемы
Статья в выпуске: 2 т.58, 2023 года.
Бесплатный доступ
Азиатский нозематоз - паразитарное заболевание медоносных пчел, вызываемое облигатным внутриклеточным паразитом микроспоридией Nosema ceranae . Эта инфекция распространена по всему миру и может приводить к снижению производства меда, резкому сокращению популяции взрослых особей в пчелиных семьях и их окончательной гибели (M. Higes с соавт., 2007; P.J. Marín-García с соавт., 2022). Цель настоящего обзора - представление актуальных данных об азиатском нозематозе и его возбудителе, а также о современных методах диагностики, лечения и профилактики в пчеловодстве . Паразит преимущественно передается между пчелами фекально-оральным путем и заражает клетки среднего отдела кишечника насекомых (R. Galajda с соавт., 2021). Вертикальная трансмиссия паразита также возможна, поскольку споры N. ceranae обнаруживались в клетках яичников зараженных маток (C. Alaux с соавт., 2011). Патогенез N. ceranae связан с разрушением зараженных клеток; перестройкой обменных процессов хозяина для обеспечения нужд паразита; дефицитом у больных пчел запасных ресурсов и жизненно важных метаболитов; гормональным дисбалансом; негативными последствиями части иммунных реакций на развитие патогена, такими как окислительный стресс (L. Paris с соавт., 2017). Способность N. ceranae специфично блокировать защитные реакции пчел, в частности апоптоз зараженных клеток и продукцию антимикробных пептидов, может усиливать патогенный характер азиатского нозематоза (K. Antúnez с соавт., 2009; C. Kurze с соавт., 2015). Методика диагностики инфекции включает в себя первичную детекцию паразита с помощью световой микроскопии, в том числе с применением различных красителей (N.J. Ryan с соавт., 1993), и дальнейшее установление видовой принадлежности микроспоридии с помощью молекулярных методов, таких как стандартная полимеразная цепная реакция (ПЦР) или петлевая изотермическая амплификация. Наиболее эффективным препаратом для лечения нозематозов пчел длительное время оставался антибиотик фумагиллин, несмотря на то, что у N. ceranae описаны случаи формирования устойчивости к этому препарату (W.-F. Huang, с соавт., 2013; I. Tlak Gajger с соавт., 2018). Однако обнаружение остатков фумагиллина в меде пчел после обработки и его токсичность для человека привели к запрету этого препарата в ряде стран и прекращению его производства в 2018 году (I. Tlak Gajger с соавт., 2018). В связи с этим в последние годы проведено множество исследований, направленных на поиск новых способов терапии нозематозов. Например, для лечения этого заболевания использовали экстракты из различных грибов и растений; пробиотики, такие как эвгенол, хитозан, нарингенин, протексин; ингибиторы функционирования протеасом иксазомиб и цитрат иксазомиба (V. Chaimanee с соавт., 2021; S.S. Klassen с соавт., 2021; E.M. Huntsman с соавт., 2021). Несмотря на то, что многие из опробованных методик показали обнадеживающие результаты, безопасного аналога фумагиллина, схожего с ним по эффективности борьбы с нозематозом, пока не найдено. В статье также приводятся рекомендации по уходу за ульями для профилактики азиатского нозематоза в пчеловодстве.
Nosema ceranae, vairimorpha ceranae, apis mellifera, нозематоз, микроспоридии, заболевания пчел, диагностика, патогенез, лечение, профилактика
Короткий адрес: https://sciup.org/142238880
IDR: 142238880 | УДК: 638.14/.15:579.62 | DOI: 10.15389/agrobiology.2023.2.274rus
Nosemosis type c of bees caused by microsporidia Nosema (Vairimorpha) ceranae: current views, pathogenesis, prevention, diagnosis and treatment (review)
Nosemosis type C is a parasitic disease of honey bees caused by the obligate intracellular parasite microsporidia Nosema (Vairimorpha) cerana. This disease is widespread worldwide and can lead to a decrease in honey production, a sharp reduction in the population of adults in bee families and their final death (M. Higes et al., 2007; P.J. Marín-García et al., 2022). The purpose of this review is to present up-to-date data on this disease and its causative agent, as well as on modern methods of diagnosis, prevention and treatment in beekeeping. The parasite is mainly transmitted between bees by the fecal-oral route and infects the cells of the middle intestine of insects (R. Galajda et al., 2021).. Vertical transmission of the parasite is also possible, as N. ceranae spores have been found in ovarian cells of infected queens (C. Alaux et al., 2011). The pathogenesis of N. ceranae is associated with the destruction of infected cells, the restructuring of the host’s metabolic processes to meet the needs of the parasite, the shortage of spare resources and vital metabolites in sick bees. hormonal imbalance; negative consequences of part of the immune responses to the pathogen invasion, such as oxidative stress (L. Paris et al., 2017). Ability of N. ceranae specifically inhibits such protective reactions of bees as activation of apoptosis of infected cells and production of antimicrobial peptides can enhance the pathogenic nature of nosemosis type C (K. Antunez et al., 2009; C. Kurze et al., 2015). The method of diagnosis of infection includes the primary detection of the parasite using light microscopy, including with the use of various dyes (N.J. Ryan et al., 1993), and further determination of the species of microsporidia using molecular methods such as standard polymerase chain reaction (PCR) or loop-mediated isothermal amplification (LAMP). The most effective drug for the treatment of nosemosis of bees for a long time remained the antibiotic fumagillin, despite the fact that N. ceranae can acquire resistance to this drug (W.-F. Huang et al., 2013; I. Tlak Gajger et al., 2018). However, the discovery of residues of this drug in honey produced by bees after treatment and its toxicity to humans led to the prohibition of this drug in a number of countries and the cessation of its production in 2018 (I. Tlak Gajger et al., 2018). In this regard, many studies have been conducted in recent years aimed at finding new ways to treat nosemosis. For example, extracts from various fungi and plants, probiotics such as eugenol, chitosan, naringenin, proteksin, proteasome function inhibitors ixazomib, and ixazomib citrate are considered as agents for the treatment of this disease (V. Chaimanee et al., 2021; S.S. Klassen et al., 2021; E.M. Huntsman et al., 2021). Despite the fact that many of the tested methods have shown encouraging results, a safe analogue of fumagillin, similar to it in terms of the effectiveness of the fight against nosemosis, has not yet been found. The article also provides recommendations for the care of beehives for the prevention of nosemosis type C in beekeeping.
Текст обзорной статьи Азиатский нозематоз пчел, вызванный микроспоридией Nosema (Vairimorpha) ceranae: современные представления, патогенез, профилактика, диагностика и лечение обзор)
-
* Работа выполнена при поддержке РНФ (грант ¹ 18-16-00054).
насекомым-фитофагам трансгенных растений и их пыльцы, глобальное изменение климата и т.д. Возможной причиной сокращения популяций медоносных пчел также называют болезни, вызванные различными патогенами и паразитами (6, 7).
Nosema ceranae — облигатный внутриклеточный паразит пчел, относящийся к микроспоридиям (группа одноклеточных организмов, родственных грибам). Впервые вид был описан в 1996 году у китайской восковой пчелы Apis cerana (8) и в настоящее время считается инфекционным для представителей таксонов безжалых пчел ( Meliponini ), настоящих ос ( Vespidae ) и некоторых видов шмелей и пчел, включая все подвиды медоносной пчелы A. mellifera (9-12). Проведенная в 2020 году филогенетическая ревизия родов Nosema и Vairimorpha показала, что N. ceranae корректно относить ко второму роду (13). Тем не менее, поскольку в подавляющем большинстве современных работ продолжают использовать традиционное наименование паразита Nosema ceranae , мы также будем придерживаться этого названия в рамках представленного обзора.
N. ceranae широко распространен в пчеловодческих хозяйствах большинства стран. Он считается доминирующим видом микроспоридий, заражающим медоносных пчел, который вытеснил N. аpis — естественного патогена A. mellifera (14-16). Заболевание, вызываемое этим паразитом, — азиатский нозематоз, или нозематоз типа C (type С nosemosis), — связывают с резким сокращением популяции взрослых особей в колониях пчел, снижением производства меда и даже коллапсом колоний (12, 17).
Цель настоящего обзора — представление актуальных данных об азиатском нозематозе и его возбудителе, а также о современных методах его диагностики, лечения и профилактики в пчеловодстве .
Биология и патогенез Nosema ceranae. Инфекционной стадией жизненного цикла N. ceranae , способной существовать во внешней среде, как и у всех микроспоридий, служат споры, размер которых около 4,7½2,7 мкм (8). Споры попадают в организм пчелы с пищей, а также, вероятно, при контактном взаимодействии с другими зараженными пчелами, например при груминге (18). Во время этого процесса пчелы очищают друг друга, что помогает им избавляться от других паразитов, таких как Varroa destructor , но груминг может приводить и к распространению нозематоза. В средней кишке насекомого, защищенной лишь перитрофической мембраной, происходит внедрение зародыша (спороплазмы) паразита в клетку эпителия с помощью сложно организованного аппарата экструзии споры. Внутри клетки хозяина спороплазма превращается в меронт, и после нескольких циклов деления начинается процесс формирования новых спор, которые выводятся из зараженных клеток в просвет кишечника при разрушении энтероцитов и служат источником заражения других клеток того же насекомого или других особей. Обнаружение в клетках кишечного эпителия пчел пустых оболочек спор N. ceranae , не содержащих зародыша паразита, также может свидетельствовать о том, что экструзия спор и заражение соседних клеток кишечника насекомого проходит внутри зараженной клетки (19, 20).
Вертикальная трансмиссия паразита также возможна, поскольку споры N. ceranae обнаруживались в клетках яичников зараженных маток (21, 22). Заражение этих клеток обычно происходит при контакте с инфицированными рабочими пчелами (23), таким же образом заражаются трутни (24). Считается, что в природных и хозяйственных ульях заражаются только взрослые особи пчел, однако в лабораторных условиях было показано развитие нозематоза у предкуколок, зараженных N. ceranae, на стадии 3-суточной личинки (25).
Несмотря на то, что N. ceranae , кроме кишечника, была обнаружена в разных органах рабочих пчел (26, 27), их заражение никогда не было доказано на гистологическом уровне. Авторы (28) недавнего детального исследования тропизма N. ceranae в медоносной пчеле предполагают, что описанные выше результаты были получены из-за контаминации проб тканей спорами паразита из-за несовершенства методик препарирования или разрушения кишечника насекомого на поздней стадии заражения. То есть, скорее всего, кишечник служит единственным органом, в котором происходит развитие N. ceranae (28). При этом развитие паразита происходит только в энтероцитах, но не в стволовых клетках, необходимых для возобновления кишечного эпителия (29).
Как в естественных условиях, так и при искусственном заражении N. ceranae в кишечнике инфицированного насекомого наблюдается патология со схожими симптомами (30). Зараженные клетки эпителия демонстрируют признаки деградации — появление вакуолей в цитоплазме, нарушение целостности клеточных мембран, конденсацию и уменьшение размера клеточного ядра, обычно сопровождаемые гиперхроматозом (чрезмерным увеличением содержания хроматина) и пикнозом (сморщиванием клеточного ядра в процессе конденсации хроматина). Перитрофическая мембрана исчезает полностью или значительно фрагментируется. В нижележащем участке щеточной каймы иногда наблюдается разрыв клеточной плазматической мембраны. В наиболее инфицированных эпителиальных клетках ядро смещено апикально. В некоторых клетках хозяина незрелые и зрелые стадии N. ceranae могут обнаруживаться в инвагинациях ядерной оболочки. В зараженных клетках активно идут литические процессы, о чем свидетельствуют многочисленные вакуоли и агрегаты рибосом и лизосом, а также утрата частиц гликогена (19, 30). Потеря гликогена и рыхлая агрегация рибосом — возможные последствия повреждения митохондрий (31). Использование запасов гликогена может указывать на то, что инфицированная клетка переключилась с более эффективного способа производства энергии (например, окислительного фосфорилирования) на менее эффективный аноксибионтный гликолиз, возможно, для компенсации истощения АТФ, который поглощается паразитом из зараженных клеток (32). Дефицит АТФ ведет к нарушению транспорта ионов через мембрану зараженной клетки, что приводит к накоплению в клетке избытков натрия, отсоединению рибосом от шероховатого эндоплазматического ретикулума и, в конечном счете, к некрозу (14, 31).
Воздействие на метаболизм клетки хозяина и его специфичная перенастройка для увеличения доступности питательных веществ и энергетических ресурсов для паразита — характерная черта паразитизма микроспоридий (32). При заражении N. ceranae в клетках кишечника A. mellifera наблюдается активация гена альфа-глюкозидазы и трех генов, участвующих в транспорте трегалозы, а также подавление генов, кодирующих трегалазу и глюкозо-метанол-холиноксидоредуктазу (33, 34). Эти изменения метаболизма приводят к увеличению доступности трегалозы для паразита, которая считается основным источником глюкозы для микроспоридий (32).
N. ceranae также специфично воздействует на защитные реакции хозяина на клеточном уровне. Зараженные клетки кишечника могут подвергаться апоптозу до того, как паразит успевает завершить полный цикл развития. N. ceranae, по-видимому, способна блокировать этот процесс, о чем свидетельствует увеличение транскрипции различных ингибиторов апоптоза в зараженных клетках (33-35). Это предположение подтверждается тем, что у устойчивой к нозематозу линии пчел не наблюдалось ингибирования апоптоза при экспериментальном заражении (36). Еще одним клеточным механизмом защиты от заражения микроспоридиями служит оксидативный стресс — продукция зараженными клетками активных форм кислорода, способных уничтожать внутриклеточных паразитов. Этот механизм, по всей видимости, неэффективен против инфекции N. ceranae, поскольку паразит активно развивается, несмотря на наблюдаемый окислительный стресс и повреждение клеток кишечника, за счет продукции каталазы, глутатионпероксидазы и глутатион-S-трансферазы (34, 37). Однако, вероятно, N. ceranae все же воздействует на зараженные клетки пчелы и подавляет реакции окислительного стресса, так как при искусственной индукции последнего пестицидами заражение N. ceranae снижало количество активных форм кислорода и уменьшало повреждение клеток кишечника A. mellifera (38).
На уровне организма азиатский нозематоз у пчел может протекать бессимптомно или причинять значительный вред. Во многом это зависит от внешних условий, в которых существуют пчелы, от колебаний температуры и влажности (16, 39). В лаборатории заражение пчел дозой 105 спор/особь приводило к 100 % смертности насекомых к 8-м сут после инфицирования (19). Одно из важных последствий нозематоза у пчел — энергетический стресс, вызванный нарушением работы поврежденного кишечника и изменением углеводного обмена зараженных клеток. Несмотря на то, что инфицированные пчелы потребляют больше пищи, чем незараженные, они, по-видимому, не могут утилизировать избыточное количество потребляемых углеводов, большинство из которых используется патогеном для завершения жизненного цикла (12, 17, 40). С энергетическим стрессом связывают высокую смертность рабочих пчел во время сбора нектара, что требует значительных энергетических затрат (40, 41). Инфицированные пчелы собирают нектар менее эффективно, чем здоровые, чаще не возвращаются в улей из-за нарушения ориентации в пространстве (42). Зараженные рабочие пчелы также проводят больше времени вне улья, реализуя рискованное поведение, такое как грабежи (43). Интересно, что подобных эффектов не наблюдали при искусственном заражении линии пчел, устойчивой к нозематозу (44). С энергетическим стрессом вследствие нозематоза связывают деградацию у пчел-кормилиц гипофарингиальных желез, производящих секрет для кормления личинок, и обеднение самого секрета (40, 41). Несмотря на то, что степень заражения у трутней обычно ниже, чем у рабочих пчел, последствия нозематоза и энергетического стресса у них обычно проявляется более выраженно и их смертность от этой инфекции выше (45).
Ряд других изменений в организме зараженных пчел и последствий нозематоза связывают с иммунным ответом на инфекцию. Описанный выше окислительный стресс напрямую влияет на уменьшение продолжительности жизни зараженных пчел (40). N. сeranae, по-видимому, подавляет другие защитные реакции насекомых на организменном уровне. У зараженных пчел снижается экспрессия многих генов, связанных с иммунным ответом, в том числе кодирующих антимикробные пептиды и гормоны. Подавление экспрессии наблюдалось для таких белков, как абаецин, дефензин, гименоптецин, глюкозодегидрогеназа, вителлогенин, серинпротеаза 40, каталаза (34, 46). Кроме того, отмечалось подавление экспрессии компонентов путей активации иммунного ответа Toll и Imd и рецепторов распознавания паттерна (47). Подобное подавление иммунного ответа у зараженных пчел наблюдалось не только в лабораторных экспериментах и сельскохозяйственных ульях, но и в природных популяциях (48). Однако в других исследованиях, наоборот, при заражении N. сeranae увеличивалась экспрессия различных компонентов иммунного ответа пчел, в том числе многих генов, указанных выше (49, 50). Этот факт позволяет предположить, что на иммунный ответ могут влиять многие факторы, такие как инфекционная нагрузка, которая значительно различается между исследованиями; продолжительность анализов; биоматериал, в котором изучали экспрессию генов (целые пчелы, брюшная полость, желудочки и т.д.); возраст пчел при заражении и во время исследования. Механизмы взаимодействия N. ceranae с иммунной системой хозяина и их роль в патогенезе требуют дальнейшего изучения.
В зависимости возраста пчелы выполняют разные функции в улье. Например, молодые особи чистят, строят и кормят расплод внутри колонии, тогда как внешние задачи зарезервированы за старшими пчелами (51). Инфекция N. ceranae провоцирует гормональный дисбаланс, приводит к нарушению поведения и ускоряет развитие зараженных пчел. Распределение функций между особями разных возрастов в первую очередь регулируется соотношением продукции в организме пчелы ювенильного гормона и вителлогенина. У рабочих пчел, инфицированных N. ceranae , повышалось содержание ювенильного гормона, что приводило к их преждевременному переходу от кормления к поиску пищи вне улья (51, 52).
Заражение N. ceranae может быть одним из факторов, влияющих на социальную демографию колонии. Зараженные пчелы погибают из-за разрушения тканей организма, не могут вернуться в улей из-за энергетического стресса или покидают улей, чтобы ограничить передачу инфекции здоровым рабочим пчелам. Молодые пчелы раньше переходят к поиску нектара из-за гормонального дисбаланса, а в улье нарушается процесс кормления личинок и других особей. Потеря инфицированных рабочих пчел с течением времени может спровоцировать ускоренное старение и преждевременный поиск корма и у неинфицированных молодых насекомых, занятых кормлением. Молодые собиратели менее эффективны в добыче пищи, чем собиратели нормального возраста, что становится угрозой для продовольственной безопасности колонии. Кульминация этих эффектов может в конечном итоге привести к внезапной гибели колонии (17, 19, 53).
Детекция Nosema ceranae и диагностика азиатского нозематоза у пчел. В пчелиной семье клинические и субклинические проявления азиатского нозематоза выражаются в более длительном периоде размножения в холодные месяцы, в увеличении доли рамок с расплодом относительно числа пчел-кормилиц в теплые месяцы и снижении производства меда. Зараженные семьи ослабевают, доля взрослых пчел снижается, что приводит к гибели семьи в течение 1,5-2 лет (12, 54). Ни одно из этих проявления не специфично для инфекции N. ceranae и может быть вызвано другими заболеваниями, что требует дифференциальный диагностики для определения нозематоза (16).
Первым этапом для детекции N. ceranae в улье служит микроскопический анализ фекалий, мазков из вскрытого подмора и гомогенатов кишечника на наличие спор. Их характерная яйцевидная форма (рис.) позволяет легко идентифицировать заражение микроспоридиями. Для облегчения обнаружения паразита в препарате применяют специфичные красители, которые связываются с хитином оболочки спор микроспоридий, — трихром и калькофлуор белый, а также неспецифичный краситель толуидиновый синий (55, 56).
Недавно был предложен метод для первичной микроскопической детекции N. ceranae в полевых условиях без лабораторного оборудования. На основе обычного смартфона, ультрафиолетовых светодиодов и набора простейших линз авторы разработали прибор весом 374 г, позволяющий эффективно выявлять споры N. ceranae в образцах при окрашивании современной модификацией калькофлуора белого (57). Споры N. ceranae незначительно отличаются от спор N. apis морофологически (последние имеют более округлую форму), поэтому для надежной дифференциации указанных видов необходимы молекулярные методы детекции (12, 16).
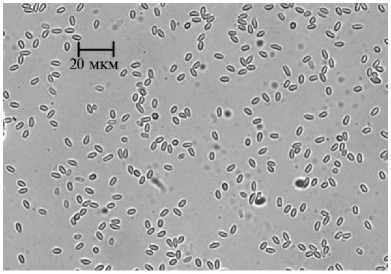
Микрофотография спор Nosema ceranae из гомогената кишечника зараженный пчелы Apis mellif-era (световая просвечивающая микроскопия, Axio Imager M1, «Carl Zeiss», Германия, увеличение ½100; снимок сделан А.Н. Игнатьевой).
Основная методика, позволяющая детектировать нозематоз у пчел и установить конкретную видовую принадлежность паразита – стандартная полимеразная цепная реакция (ПЦР) или ПЦР в реальном времени (real-time PCR, qPCR) (58, 59). Для этого необходимо использовать праймеры, специфичные для N. ceranae, N. apis, а также для обоих видов одновременно. С полным списком праймеров, которые используют в диагностике нозематоза, можно ознакомиться в работе R. Galajda с со-авт. (18). Детекция с помощью ПЦР позволяет установить факт зараже- ния улья при исследовании не только инфицированных пчел или их экскрементов, но и продуцируемого меда, в котором также обнаруживаются споры паразита, сохраняющие инфекционность (60, 61). Разработанный недавно сверхбыстрый протокол выявления N. ceranae с помощью ПЦР в реальном времени позволяет устанавливать заражение пчел на этапе 24 клеток паразита во всем организме насекомого, тогда как микроскопическая детекция обычно эффективна на этапе массовой спорогонии, когда формируются десятки тысяч клеток N. ceranae (62). Кроме того, молекулярная диагностика с помощью ПЦР дает возможность оценить степень заражения в 8 раз точнее, чем подсчет спор при микрокопировании. Недавно разработан еще один метод диагностики нозематоза, схожий с ПЦР, но не требующий применения стационарного лабораторного оборудования, который основан на петлевой изотермической амплификации (loop-mediated isothermal amplification, LAMP) (63).
Профилактика и лечение азиатского нозематоза в пчеловодстве. В недавних работах ученых из Италии и Испании были сформулированы основные принципы оптимального пчеловодства для минимизации рисков появления различных заболеваний и сохранения здоровья пчел на пасеках (64, 65). По нашему мнению, в этих работах представлены наиболее актуальные на сегодняшний день рекомендации.
К профилактике нозематоза относятся следующие мероприятия: приобретение маток у заводчиков, в чьих семьях не обнаружено заражения N. ceranae ; сбор образцов пчел-фуражиров или мусора из улья ранней осенью или весной для диагностики нозематоза с помощью микроскопического исследования и ПЦР; укрепление и оздоровление семей осенью и весной с помощью стимуляторов или кормовых добавок; дезинфицирование инструментов и оборудования для пчеловодства перед использованием — металлические инструменты можно стерилизовать прожиганием, а для дезинфекции ульев применять окуривание ледяной уксусной кислотой, 5 % гидроксидом натрия (каустическая сода), 0,5 % гипохлоритом натрия
(отбеливатель) и 1,65 % раствором аммиака; исключение кормления здоровых семей медом и пыльцой от зараженных N. ceranae семей; замена маток минимум каждые 2 года, за исключением тех, которые имеют высокую генетическую ценность; содержание новых семей отдельно от уже имеющихся не менее 1 мес для контроля на наличие болезней и инвазий и предотвращения их передачи; ежегодное обновление 30 % сотов в улье; минимизация стресса у пчел (следует избегать зимних проверок ульев, ограничить использование дымокура, необходимо правильное кормление пчел и т.д.); немедленное удаление улья с пасеки в случае гибели пчелиной семьи.
Наиболее эффективным средством для лечения как классического, так и азиатского нозематоза служит антибиотик фумагиллин, выделенный из гриба Aspergillus fumigatus и позволяющий значительно снизить зараженность колонии и риск ее разрушения (66-68). В зависимости от географического положения и состояния семьи рекомендуется обрабатывать зараженные семьи от одного (осенью во время кормления) до двух раз в год (осенью и весной, в случае тяжелых инфекций). В то время как осенняя обработка направлена на поддержание жизни семьи в холодное время года, весенняя проводится для улучшения состояния здоровья взрослых пчел, которые смогут должным образом заботиться о следующем поколении особей, выращенных весной. Тем не менее известны случаи, когда при крайне высокой степени зараженности колонии пчел азиатским нозематозом использование фумагиллина не останавливало распространения инфекции и не повышало выживаемость колоний зимой, независимо от дозы или метода обработки (69, 70). Для N. ceranae также описаны случаи формирования устойчивости к этому антибиотику (68, 71). Кроме того, важно отметить, что фумагиллин нельзя считать полностью безопасным для человека, и обнаружение его остатков в меде после обработки ульев привело к запрету применения препарата в Европе, а в 2018 году Канадская компания «Medivet Pharmaceuticals Ltd.» прекратила его производство (72).
В последнее время значительное число исследований посвящено поиску средств терапии нозематоза у пчел (табл.)
Результаты исследований, направленных на поиск новых средств терапии азиатского нозематоза, вызываемого микроспоридией Nosema ceranae, у пчел Apis mellifera (2021 год)
Вещество, метод Эффект Ссылка
Биодобавка, содержащая пшеничные отруби, Статистически значимое снижение зараженности (73) эфирные масла, корицу, декстрозу, пивные колонии нозематозом примерно на 10 % дрожжи, лецитин, насыщенные и ненасыщенные жирные кислоты, растительные белки, незаменимые аминокислоты, липиды и витаминно-минеральный комплекс на основе витамина B
Различные комбинации экстрактов 7 видов лекарственных растений
12 экстрактов различных лекарственных растений
Экстракт гриба Agaricus bisporus
Смесь экстрактов из 20 % черники, 40 % полыни, (74)
10 % дубового мха, 10 % орегано, 10 % хмеля, 5 % лаврового листа и 5 % анисового иссопа была наиболее эффективна против N. ceranae и приводила к более чем 2-кратному снижению инфекционной нагрузки у зараженных пчел
9 из 12 экстрактов подавляли развитие инфек- (75)
ции, продукция спор N. ceranae в зараженных пчелах уменьшалась в 4-6 раз
Добавление экстракта увеличивало выживаемость (76)
зараженных пчел примерно на 10 % и уменьшало продукцию спор в зараженных пчелах на треть.
Показано иммуностимулирующие действие экстракта, увеличивающего у зараженных пчел экспрессию генов, кодирующих абецин, гименоптае-цин, апидецин и вителлогенин
Прополис, вырабатываемый A. mellifera и Tetrigona apicalis
Пребиотики из пищевых волокон, камедь акации, инулин и фруктоолигосахарид, а также коммерческие пробиотики Ветафарм, концентрат протексина с одним бактериальным штаммом ( Enterococcus faecium ) и концентрат протексина с несколькими штаммами бактерий ( Lactobacillus acidophilus , L. plantarum , L. rhamnosus , L. delbrueckii , Bifidobacterium bifidum , Streptococcus salivarius и E. faecium )
Пробиотики эвгенол, хитозан, нарингенин, протексин
Шрот из семян Brassica nigra и Eruca sativa , содержащий фиксированное количество различных глюкозинолатов
Шрот из семян Brassica nigra и Eruca sativa , содержащий фиксированное количество различных глюкозинолатов.
Хитозан и пептидогликан
Проведен скрининг некоторых растительных экстрактов, продуктов микробной ферментации, органических кислот, отходов пищевой цепи, бактериоцинов и грибов
Проведен нокдаун гена A. mellifera , кодирующего переносчик ионов железа трансферрин
Двуцепочечные РНК, комплементарные участкам генов N. ceranae , кодирующих белки оболочки спор
Ингибиторы функционирования протеасом — иксазомиб и цитрат иксазомиба
Продолжение таблицы Прополис от обоих видов пчел более чем в 2 раза (77)
снизил смертность пчел, на 20-40 % — инфицирование, на 70-80 % — инфекционность по сравнению с показателями у необработанных пчел и привел к значительно большему содержанию белка в гипофарингеальных железах и гемолимфе у обработанных пчел, чем у необработанных
Камедь акации вызвала наибольшее снижение (78)
числа спор N. ceranae (67 %), но также значительно увеличила смертность пчел (62,2 %). Штамм
-
E. faecium давал аналогичное снижение числа спор (59 %), не влияя на смертность. Применение одиночного штамма представляется многообещающим, поскольку он может уменьшить размножение N. ceranae и увеличить выживаемость инфицированных пчел даже по сравнению со здоровыми неинфицированными особями Обработки эвгенолом, нарингенином и протекси- (79)
ном значительно снизили заражение N. ceranae и увеличили производство меда. Протексин также увеличивал численность взрослых пчел, а хитозан был неэффективен
Более чем 2-кратное снижение зараженности(80)
пчел в лабораторных условиях
Снижение зараженности пчел по сравнению с(81)
контролем в полевых условиях, проявляющееся в меньшей степени, чем при применении этой методики в лаборатории
Стимуляция иммунных реакций пчел, увеличение(82)
экспрессии генов антимикробных пептидов, более чем 2-кратное снижение зараженности микроспоридиями
Некоторые из вводимых ингредиентов, такие как(83)
уксусная кислота в высокой концентрации, п-ку-маровая кислота и Saccharomyces sp. штамм KIA1, показали относительную эффективность в борьбе с нозематозом
Снижение транскрипционной активности в клет-(84)
ках N. ceranae , уменьшение потери железа, усиление иммунитета и улучшение выживаемости зараженных пчел
Более чем 2-кратное снижение зараженности и(85)
увеличение выживаемости пчел в лабораторных условиях
Значительное снижение зараженности пчел и по-(86)
вышение их выживаемости, сравнимое по эффективности с действием фумагиллина
Пр им еч ан и е. В случаях, когда не указано иного, экспериментальная процедура заключалась в добав- лении действующего вещества при кормлении зараженных пчел.
Таким образом, азиатский нозематоз медоносных пчел, вызываемый облигатным внутриклеточным паразитом — микроспоридией Nosema ceranae распространен по всему миру. Инфекция приводит к нарушению функционирования кишечника, гормональному дисбалансу и энергетическому стрессу. Эти факторы могут менять поведение зараженных насекомых, нарушая естественное для улья распределения обязанностей между пчелами разных возрастов. Кульминация таких эффектов способна в конечном итоге привести к внезапной гибели колонии. Диагностика азиатского нозематоза обычно включает микроскопический анализ препаратов кишечника насекомых и последующий молекулярный анализ с помощью ПЦР или ее аналогов. Наиболее результативным средством лечения заболевания служит антибиотик фумагиллин, который, однако, токсичен для человека и запрещен во многих странах. Поиску новых методов терапии нозематоза в настоящее
время уделяется особое внимание, но пока безопасной и эффективной альтернативы фумагиллину обнаружить не удалось.
Список литературы Азиатский нозематоз пчел, вызванный микроспоридией Nosema (Vairimorpha) ceranae: современные представления, патогенез, профилактика, диагностика и лечение обзор)
- Gallai N., Salles J.M., Settele J., Vaissiere B.E. Economic valuation of the vulnerability of world agriculture confronted with pollinator decline. Ecological Economics, 2009, 68(3): 810-821 (doi: 10.1016/j.ecolecon.2008.06.014).
- Klein A.M., Vaissiere B.E., Cane J.H., Steffan-Dewenter I., Cunningham S.A., Kremen C., Tscharntke T. Importance of pollinators in changing landscapes for world. Proceedings of the Royal Society B: Biological Sciences, 2007, 274(1608): 303-313 (doi: 10.1098/rspb.2006.3721).
- Potts S.G., Biesmeijer J.C., Kremen C., Neumann P., Schweiger O., Kunin W.E. Global polli-nator declines: trends, impacts and drivers. Trends in Ecology & Evolution, 2010, 25(6): 345-353 (doi: 10.1016/j.tree.2010.01.007).
- Potts S.G., Imperatriz-Fonseca V., Ngo H.T., Aizen M.A., Biesmeijer J.C., Breeze T.D., Dicks L.V., Garibaldi L.A., Hill R., Settele J., Vanbergen A.J. Safeguarding pollinators and their values to human well-being. Nature, 2016, 540: 220-229 (doi: 10.1038/nature20588).
- Brodschneider R., Gray A., Adjlane N., Ballis A., Brusbardis V., Charrière J-D., Chlebo R., Coffey M.F., Dahle B., de Graaf D.C., Dražić M.M., Evans G., Fedoriak M., Forsythe I., Gregorc A., Grzęda U., Hetzroni A., Kauko L., Kristiansen P., Martikkala M., Martín-Hernán-dez R., Medina-Flores C.A., Mutinelli F., Raudmets A., Ryzhikov V.A., Simon-Delso N., Ste-vanovic J., Uzunov A., Vejsnæs F., Wöhl S., Zammit-Mangion M., Danihlík J. Multi-country loss rates of honey bee colonies during winter 2016/2017 from the COLOSS survey. Journal of Apicultural Research, 2018, 57(3): 452-457 (doi: 10.1080/00218839.2018.1460911).
- Goulson D., Nicholls E., Botias C., Rotheray E.L. Bee declines driven by combined stress from parasites, pesticides, and lack of flowers. Science, 2015, 347(6229): 1255957 (doi: 10.1126/sci-ence.1255957).
- Spivak M., Mader E., Vaughan M., Euliss N.H. Jr. The plight of the bees. Environmental Science & Technology, 2011, 45(1): 34-38 (doi: 10.1021/es101468w).
- Fries I., Feng F., Da Silva A., Slemenda S.B., Pieniazek N.J. Nosema ceranae n. sp. (Microspora, Nosematidae), morphological and molecular characterization of a microsporidian parasite of the Asian honey bee Apis cerana (Hymenoptera, Apidae). European Journal of Protistology, 1996, 32(3): 356-365 (doi: 10.1016/S0932-4739(96)80059-9).
- Porrini M.P., Porrini L.P., Garrido P.M., Neto С., Porrini D.P., Muller F., Nuñez L.A., Alva-rez L., Iriarte P.F., Eguaras M.J. Nosema ceranae in South American native stingless bees and social wasp. Microbial Ecology, 2017, 74: 761-764 (doi: 10.1007/s00248-017-0975-1).
- Plischuk S., Martín-Hernández R., Prieto L., Lucía M., Botías C., Meana A., Abrahamo-vich A.H., Lange C., Higes M. South American native bumblebees (Hymenoptera: Apidae) in-fected by Nosema ceranae (Microsporidia), an emerging pathogen of honeybees (Apis mellifera). Environmental Microbiology Reports, 2009, 1(2): 131-135 (doi: 10.1111/j.1758-2229.2009.00018.x).
- Fürst M.A., McMahon D.P., Osborne J.L., Paxton R.J., Brown M.J. Disease associations between honeybees and bumblebees as a threat to wild pollinators. Nature, 2014, 506: 364-366 (doi: 10.1038/nature12977).
- Martín-Hernández R., Bartolome C., Chejanovsky N., Le Conte Y., Dalmon A., Dussaubat C., Dussaubat C., Meana A., Pinto M., Soroker V., Higes M. Nosema ceranae in Apis mellifera: a 12 years post-detection perspective: Environmental Microbiology, 2018, 20(4): 1302-1329 (doi: 10.1111/1462-2920.14103).
- Tokarev Y.S., Huang W.F., Solter L.F., Malysh J.M., Becnel J.J., Vossbrinck C.R. A formal redefinition of the genera Nosema and Vairimorpha (Microsporidia: Nosematidae) and reassign-ment of species based on molecular phylogenetics. Journal of Invertebrate Pathology, 2020, 169: 107279 (doi: 10.1016/j.jip.2019.107279).
- Goblirsch M. Nosema ceranae disease of the honey bee (Apis mellifera). Apidologie, 2017, 49: 131-150 (doi: 10.1007/s13592-017-0535-1).
- Grupe A.C., Quandt C.A. A growing pandemic: a review of Nosema parasites in globally distrib-uted domesticated and native bees. PLoS Pathogens, 2020, 16(6): e1008580 (doi: 10.1371/jour-nal.ppat.1008580).
- Marín-García P.J., Peyre Y., Ahuir-Baraja A.E., Garijo M.M., Llobat L. The role of Nosema ceranae (Microsporidia: Nosematidae) in honey bee colony losses and current insights on treatment. Veterinary Sciences, 2022, 9(3): 130 (doi: 10.3390/vetsci9030130).
- Higes M., Martín-Hernández R., Botías C., Bailón E.G., González-Porto A.V., Barrios L., Del Nozal M.J., Bernal J.L., Jiménez J.J., Palencia P.G., Meana A. How natural infection by Nosema ceranae causes honeybee colony collapse. Environmental Microbiology, 2008, 10(10): 2659-2669 (doi: 10.1111/j.1462-2920.2008.01687.x).
- Galajda R., Valenčáková A., Sučik M., Kandráčová P. Nosema disease of european honey bees. Journal of Fungi, 2021, 7(9): 714 (doi: 10.3390/jof7090714).
- Higes M., García-Palencia P., Martín-Hernández R., Meana A. Experimental infection of Apis mellifera honeybees with the microsporidia Nosema ceranae (Microsporidia). Journal of Inverte-brate Pathology, 2007, 94(3): 211-217 (doi: 10.1016/j.jip.2006.11.001).
- Higes M., Martín-Hernández R., Garrido-Bailón E., González-Porto A.V., García-Palencia P., Meana A., Del Nozal M.J., Mayo R., Bernal M.J. Honeybee colony collapse due to Nosema ceranae in professional apiaries. Environmental Microbiology Reports, 2009, 1(2): 110-113 (doi: 10.1111/j.1758-2229.2009.00014.x).
- Alaux C., Folschweiller M., McDonnell C., Beslay D., Cousin M., Dussaubat C., Brunet J.-L., Le Conte Y. Pathological effects of the microsporidium Nosema ceranae on honey bee queen physiology (Apis mellifera). Journal of Invertebrate Pathology, 2011, 106(3): 380-385 (doi: 10.1016/j.jip.2010.12.005).
- Traver B.E., Williams M.R., Fell R.D. Comparison of within hive sampling and seasonal activity of Nosema ceranae in honey bee colonies. Journal of Invertebrate Pathology, 2012, 109(2): 187-193 (doi: 10.1016/j.jip.2011.11.001).
- Higes M., Martín-Hernández R., García-Palencia P., Marín P., Meana A. Horizontal transmis-sion of Nosema Ceranae (Microsporidia) from worker honeybees to queens (Apis mellifera). Envi-ronmental Microbiology, 2009, 1(6): 495-498 (doi: 10.1111/j.1758-2229.2009.00052.x).
- Traver B.E., Fell R.D. Nosema ceranae in drone honey bees (Apis mellifera). Journal of Invertebrate Pathology, 2011, 107(3): 234-236 (doi: 10.1016/j.jip.2011.05.016).
- Eiri D.M., Suwannapong G., Endler M., Nieh J.C. Nosema ceranae can infect honey bee larvae and reduces subsequent adult longevity. PLoS ONE, 2015, 10(5): e0126330 (doi: 10.1371/jour-nal.pone.0126330).
- Copley T.R., Jabaji S.H. Honeybee glands as possible infection reservoirs of Nosema ceranae and Nosema apis in naturally infected forager bees. Journal of Applied Microbiology, 2012, 112(1): 15-24 (doi: 10.1111/j.1365-2672.2011.05192.x).
- Chen Y.P., Evans J.D., Charles M., Robin G., Michael Z., Gundensen-Rindal D., Pettis J.S. Morphological, molecular, and phylogenetic characterization of Nosema ceranae, a microsporid-ian parasite isolated from the European honey bee, Apis mellifera. Journal of Eukaryotic Microbi-ology, 2009, 56(2): 142-147 (doi: 10.1111/j.1550-7408.2008.00374.x).
- Higes M., García-Palencia P., Urbieta A., Nanetti A., Martín-Hernández R. Nosema apis and Nosema ceranae tissue tropism in worker honey bees (Apis mellifera). Veterinary Pathology, 2020, 57(1): 132-138 (doi: 10.1177/0300985819864302).
- Panek J., Paris L., Roriz D., Mone A., Dubuffet A., Delbac F., Diogon M., El Alaoui H. Impact of the microsporidian Nosema ceranae on the gut epithelium renewal of the honeybee, Apis mel-lifera. Journal of Invertebrate Pathology, 2018, 159: 121-128 (doi: 10.1016/j.jip.2018.09.007).
- García-Palencia P., Martín-Hernández R., González-Porto A.V., Marin P., Meana A., Higes M. Natural infection by Nosema ceranae causes similar lesions as in experimentally infected caged-worker honey bees (Apis mellifera). Journal of Apicultural Research, 2010, 49: 278-283 (doi: 10.3896/IBRA.1.49.3.08).
- Kumar V., Abbas A.K., Aster J.C. Cell injury, cell death, and adaptations. In: Robbins basic pathology. 9th ed. Elsevier Saunders, Philadelphia, 2012.
- Timofeev S., Tokarev Y., Dolgikh V. Energy metabolism and its evolution in Microsporidia and allied taxa. Parasitology Research, 2020, 119: 1433-1441 (doi: 10.1007/s00436-020-06657-9).
- Dussaubat C.J., Brunet L., Higes M., Colbourne J.K., Lopez J., Choi J.H., Martín-Hernández R., Botías C., Cousin M., McDonnell C., Bonnet M., Belzunces L.P., Moritz R.F.A., Le Conte Y., Alaux C. Gut pathology and responses to the microsporidium Nosema ceranae in the honey bee Apis mellifera. PLoS ONE, 2012, 7(5): e37017 (doi: 10.1371/journal.pone.0037017).
- Aufauvre J., Misme-Aucouturier B., Viguès B., Texier C., Delbac F., Blot N. Transcriptome analyses of the honeybee response to Nosema ceranae and insecticides. PLoS ONE, 2014, 9(3): e91686 (doi: 10.1371/journal.pone.0091686).
- Martín-Hernández R., Higes M., Sagastume S., Juarranz Á., Dias-Almeida J., Budge G.E., Meana A., Boonham N. Microsporidia infection impacts the host cell’s cycle and reduces host cell apoptosis. PLoS ONE, 2017, 12(2): e0170183 (doi: 10.1371/journal.pone.0170183).
- Kurze C., Le Conte Y., Dussaubat C., Erler S., Kryger P., Lewkowski O., Müller T, Widder M, Moritz R.F.A. Nosema tolerant honeybees (Apis mellifera) escape parasitic manipulation of apop-tosis. PLoS ONE, 2015, 10(10): e0140174 (doi: 10.1371/journal.pone.0140174).
- Dussaubat C., Maisonnasse A., Crauser D., Beslay D., Costagliola G., Soubeyrand S., Kretzch-mar A., Le Conte Y. Flight behavior and pheromone changes associated to Nosema ceranae infection of honey bee workers (Apis mellifera) in field conditions. Journal of Invertebrate Pathol-ogy, 2013, 113(1): 42-51 (doi: 10.1016/j.jip.2013.01.002).
- Paris L., Roussel M., Pereira B., Delbac F.E., Diogon M. Disruption of oxidative balance in the gut of the western honeybee Apis mellifera to the intracellular parasite Nosema ceranae and to the insecticide fipronil. Microbial Biotechnology, 2017, 10(6): 1702-1717 (doi: 10.1111/1751-7915.12772).
- Higes M., Martín-Hernández R., Martínez-Salvador A., Garrido-Bailón E., González-Porto A.V., Meana A., Bernal J.L., Del Nozal M.J., Bernal J.A. Preliminary study of the epidemiological factors related to honey bee colony loss in Spain. Environmental Microbiology Reports, 2010, 2(2): 243-250 (doi: 10.1111/j.1758-2229.2009.00099.x).
- Vidau C., Panek J., Texier C., Biron D.G., Belzunces L.P., Le Gall M., Broussard C., Delbac F., El Alaouiab H. Differential proteomic analysis of midguts from Nosema ceranae-infected honey-bees reveals manipulation of key host functions. Journal of Invertebrate Pathology, 2014, 121: 89-96 (doi: 10.1016/j.jip.2014.07.002).
- Mayack C., Naug D. Individual energetic state can prevail over social regulation of foraging in honeybees. Behavioral Ecology and Sociobiology, 2013, 67: 929-936 (doi: 10.1007/s00265-013-1517-6).
- Kuszewska K., Woyciechowski M. Risky robbing is a job for short-lived and infected worker honeybees. Apidologie, 2014, 45: 537-544 (doi: 10.1007/s13592-014-0267-4).
- Wolf S., McMahon D.P., Lim K.S., Pull C.D., Clark S.J., Paxton R.J., Osborne J.L. So near and yet so far: harmonic radar reveals reduced homing ability of Nosema infected honeybees. PLoS ONE, 2014, 9(8): e103989 (doi: 10.1371/journal.pone.0103989).
- Kurze C., Mayack C., Hirche F., Stangl G.I., Le Conte Y., Kryger P., Moritz R.F. Nosema spp. infections cause no energetic stress in tolerant honeybees. Parasitology Research, 2016, 115: 2381-2388 (doi: 10.1007/s00436-016-4988-3).
- Retschnig G., Williams G.R., Mehmann M.M., Yañez O., de Miranda J.R., Neumann P. Sex specific differences in pathogen susceptibility in honey bees (Apis mellifera). PLoS ONE, 2014, 9(1): e85261 (doi: 10.1371/journal.pone.0085261).
- Antúnez K., Martín-Hernández R., Prieto L., Meana A., Zunino P., Higes M. Immune suppres-sion in the honey bee (Apis mellifera) following infection by Nosema ceranae (Microsporidia). Environmental Microbiology, 2009, 11(9): 2284-2290 (doi: 10.1111/j.1462-2920.2009.01953.x).
- Li W., Chen Y., Cook S.C. Chronic Nosema ceranae infection inflicts comprehensive and persis-tent immunosuppression and accelerated lipid loss in host Apis mellifera honey bees. International Journal for Parasitology, 2018, 48(6): 433-444 (doi: 10.1016/j.ijpara.2017.11.004).
- Lourenço A.P., Guidugli-Lazzarini K.R., de Freitas N.H.A., Message D., Bitondi M. M.G., Simoes Z.L.P., Teixeira E.W. Immunity and physiological changes in adult honey bees (Apis mellifera) infected with Nosema ceranae: the natural colony environment. Journal of Insect Phys-iology, 2021, 131: 104237 (doi: 10.1016/j.jinsphys.2021.104237).
- Schwarz R.S., Evans J.D. Single and mixed species trypanosome and microsporidia infections elicit distinct, ephemeral cellular and humoral immune responses in honey bees. Developmental & Comparative Immunology, 2013, 40(3-4): 300-310 (doi: 10.1016/j.dci.2013.03.010).
- Li W., Evans J.D., Li J., Su S., Hamilton M., Chen Y. Spore load and immune response of honey bees naturally infected by Nosema ceranae. Parasitology Research, 2017, 116: 3265-3274 (doi: 10.1007/s00436-017-5630-8).
- Dussaubat C., Maisonnasse A., Alaux C., Tchamitchan S., Brunet J.L., Plettner E., Belzunces L.P., Le Conte Y. Nosema spp. Infection alters pheromone production in honey bees (Apis mellifera). Journal of Chemical Ecology, 2010, 36: 522-525 (doi: 10.1007/s10886-010-9786-2).
- Goblirsch M., Huang Z.Y., Spivak M. Physiological and behavioral changes in honey bees (Apis mellifera) induced by Nosema ceranae infection. PLoS ONE, 2013, 8: e58165 (doi: 10.1371/jour-nal.pone.0058165).
- Perry C.J., Søvik E., Myerscough M.R., Barron A.B. Rapid behavioral maturation accelerates failure of stressed honey bee colonies. Proceedings of the National Academy of Sciences USA, 2015, 112(11): 3427-3432 (doi: 10.1073/pnas.1422089112).
- Higes M., Martín-Hernandez R., Meana A. Nosema ceranae in Europe: an emergent type C nosemosis. Apidologie, 2010, 41: 375-392 (doi: 10.1051/apido/2010019).
- Ryan N.J., Sutherland G., Coughlan K., Globan M., Doultree J., Marshall J., Baird R.W., Peder-sen J., Dwyer B. A new trichrome-blue stain for detection of microsporidial species in urine, stool, and nasopharyngeal specimens. Journal of Clinical Microbiology, 1993, 31(12): 3264-3269 (doi: 10.1128/jcm.31.12.3264-3269.1993).
- Weber R., Bryan R.T., Owen R.L., Wilcox C.M., Gorelkin L., Visvesvara G.S. Improved light-microscopical detection of microsporidia spores in stool and duodenal aspirates. The enteric op-portunistic infections working group. The New England Journal of Medicine, 1992, 326: 161-166 (doi: 10.1056/NEJM199201163260304).
- Snow J.W., Ceylan Koydemir H., Karinca D.K., Liang K., Tseng D., Ozcan A. Rapid imaging, detection, and quantification of Nosema ceranae spores in honey bees using mobile phone-based fluorescence microscopy. Lab on a Chip, 2020, 19(5): 789-797 (doi: 10.1039/c8lc01342j).
- Evans J.D., Schwarz R.S., Chen Y.P., Budge G., Cornman R.S., De la Rua P., de Miranda J.R., Foret S., Foster L., Gauthier L., Genersch E., Gisder S., Jarosch A., Kucharski R., Lopez D., Man Lun C., Moritz R.F.A., Maleszka R., Muñoz I., Pinto M.A. Standard methods for molecular research in Apis mellifera. Journal of Agricultural Research, 2013, 52(4): 1-54 (doi: 10.3896/IBRA.1.52.4.11).
- Erler S., Lommatzsch S., Lattorff H.M.G. Comparative analysis of detection limits and specificity of molecular diagnostic markers for three pathogens (Microsporidia, Nosema spp.) in the key pollinators Apis mellifera and Bombus terrestris. Parasitology Research, 2012, 110: 1403-1410 (doi: 10.1007/s00436-011-2640-9).
- MacInnis C.I., Keddie B.A., Pernal S.F. Nosema ceranae (Microspora: Nosematidae): A sweet surprise? Investigating the viability and infectivity of N. ceranae spores maintained in honey and on beeswax. Journal of Economic Entomology, 2020, 113(5): 2069-2078 (doi: 10.1093/jee/toaa170).
- Salkova D., Shumkova R., Balkanska R., Palova N., Neov B., Radoslavov G., Hristov P. Mo-lecular detection of Nosema spp. in honey in Bulgaria. Veterinary Sciences, 2022, 9(1): 10 (doi: 10.3390/vetsci9010010).
- Truong A-T., Sevin S., Kim S., Yoo M.S., Cho Y.S., Yoon B. Rapidly quantitative detection of Nosema ceranae in honeybees using ultra-rapid real-time quantitative PCR. Journal of Veterinary Science, 2021, 22(3): e40 (doi: 10.4142/jvs.2021.22.e40).
- Lannutti L., Mira A., Basualdo M., Rodriguez G., Erler S., Silva V., Gisder S., Genersch, E., Florin-Christensen M., Schnittger L. Development of a loop-mediated isothermal amplification (LAMP) and a direct LAMP for the specific detection of Nosema ceranae, a parasite of honey bees. Parasitology Research, 2020, 119: 3947-3956 (doi: 10.1007/s00436-020-06915-w).
- Gochnauer T.A., Furgala B. Chemotherapy of nosema disease, compatibility of fumagillin with other chemicals. The American Bee Journal, 1969, 109: 309-311.
- Pietropaoli M., Skerl M.S., Cazier J., Riviere M.P., Tiozzo B., Eggenhoeffner R., Gregorc A., Haefeker W., Higes M., Ribarits A. BPRACTICES project: towards a sustainable European bee-keeping. Bee World, 2020, 97(3): 66-69 (doi: 10.1080/0005772X.2020.1757220).
- Formato G., Rivera-Gomis J., Bubnic J., Martín-Hernández R., Milito M., Croppi S., Higes M. Nosemosis prevention and control. Applied Sciences, 2022, 12(2): 783 (doi: 10.3390/app12020783).
- Mendoza Y., Diaz-Cetti S., Ramallo G., Santos E., Porrini M., Invernizzi C. Nosema ceranae winter control: study of the effectiveness of different fumagillin treatments and consequences on the strength of honey bee (Hymenoptera: Apidae) colonies. Journal of Economic Entomology, 2017, 110(1): 1-5 (doi: 10.1093/jee/tow228).
- Williams G.R., Sampson M.A., Shutler D., Rogers R.E.L. Does fumagillin control the recently detected invasive parasite Nosema ceranae in western honey bees (Apis mellifera)? Journal of In-vertebrate Pathology, 2008, 99(3): 342-344 (doi: 10.1016/j.jip.2008.04.005).
- van den Heever J.P., Thompson T.S., Curtis J.M., Ibrahim A., Pernal S.F. Fumagillin: an over-view of recent scientific advances and their significance for apiculture. Journal of Agricultural and Food Chemistry, 2014, 62(13): 2728-2737 (doi: 10.1021/jf4055374).
- van den Heever J.P., Thompson T.S., Curtis J.M., Pernal S.F. Stability of dicyclohexylamine and fumagillin in honey. Food Chemistry, 2015, 179: 152-158 (doi: 10.1016/j.foodchem.2015.01.111).
- Huang W.-F., Solter L.F., Yau P.M., Imai B.S. Nosema ceranae escapes fumagillin control in honey bees. PLoS Pathogens, 2013, 9(3): e1003185 (doi: 10.1371/journal.ppat.1003185).
- Tlak Gajger I., Ribarić J., Smodiš Škerl M., Vlainić J., Sikirić P. Stable gastric pentadecapeptide BPC 157 in honeybee (Apis mellifera) therapy, to control Nosema ceranae invasions in apiary conditions. Journal of Veterinary Pharmacology and Therapeutics, 2018, 41(4): 614-621 (doi: 10.1111/jvp.12509).
- Jovanovic N.M., Glavinic U., Delic B., Vejnovic B., Aleksic N., Mladjan V., Stanimirovic Z. Plant-based supplement containing B-complex vitamins can improve bee health and increase colony performance. Preventive Veterinary Medicine, 2021, 190: 105322 (doi: 10.1016/j.prevet-med.2021.105322).
- Pașca C., Matei I.A., Diaconeasa Z., Rotaru A., Erler S., Dezmirean D.S. Biologically active extracts from different medicinal plants tested as potential additives against bee pathogens. Anti-biotics, 2021, 10(8): 960 (doi: 10.3390/antibiotics10080960).
- Chaimanee V., Kasem A., Nuanjohn T., Boonmee T., Siangsuepchart A., Malaithong W., Sinpoo C., Disayathanoowat T., Pettis J.S. Natural extracts as potential control agents for Nosema ceranae infection in honeybees, Apis mellifera. Journal of Invertebrate Pathology, 2021, 186: 107688 (doi: 10.1016/j.jip.2021.107688).
- Glavinic U., Rajkovic M., Vunduk J., Vejnovic B., Stevanovic J., Milenkovic I., Stanimirovic Z. Effects of Agaricus bisporus mushroom extract on honey bees infected with Nosema ceranae. In-sects, 2021, 12(10): 915 (doi: 10.3390/insects12100915).
- Naree S., Benbow M.E., Suwannapong G., Ellis J.D. Mitigating Nosema ceranae infection in western honey bee (Apis mellifera) workers using propolis collected from honey bee and stingless bee (Tetrigona apicalis) hives. Journal of Invertebrate Pathology, 2021, 185: 107666 (doi: 10.1016/j.jip.2021.107666).
- Borges D., Guzmán-Novoa E., Goodwin P.H. Effects of prebiotics and probiotics on honey bees (Apis mellifera) infected with the microsporidian parasite Nosema ceranae. Microorganisms, 2021, 9(3): 481 (doi: 10.3390/microorganisms9030481).
- Klassen S.S., VanBlyderveen W., Eccles L., Kelly P.G., Borges D., Goodwin P.H., Petukhova T., Wang Q., Guzmán-Novoa E. Nosema ceranae Infections in honey bees (Apis mellifera) treated with pre/probiotics and impacts on colonies in the field. Veterinary Sciences, 2021, 8(6): 107 (doi: 10.3390/vetsci8060107).
- Nanetti A., Ugolini L., Cilia G., Pagnotta E., Malaguti L., Cardaio I., Matteo R., Lazzer L. Seed meals from Brassica nigra and eruca sativa control artificial Nosema ceranae infections in Apis mellifera. Microorganisms, 2021, 9(5): 949 (doi: 10.3390/microorganisms9050949).
- Ugolini L., Cilia G., Pagnotta E., Malaguti L., Capano V., Guerra I., Zavatta L., Albertazzi S., Matteo R., Lazzeri L., Righetti L., Nanetti A. Glucosinolate bioactivation by Apis mellifera work-ers and its impact on Nosema ceranae infection at the colony level. Biomolecules, 2021, 11(11): 1657 (doi: 10.3390/biom11111657).
- Braglia C., Alberoni D., Porrini M.P., Garrido P.M., Baffoni L., Di Gioia D. Screening of dietary ingredients against the honey bee parasite Nosema ceranae. Pathogens, 2021, 10(9): 1117 (doi: 10.3390/pathogens10091117).
- Valizadeh P., Guzman-Novoa E., Petukhova T., Goodwin P.H. Effect of feeding chitosan or peptidoglycan on Nosema ceranae infection and gene expression related to stress and the innate immune response of honey bees (Apis mellifera). Journal of Invertebrate Pathology, 2021, 185: 107671 (doi: 10.1016/j.jip.2021.107671).
- He N., Zhang Y., Duan X.L., Li J.H., Huang W.F., Evans J.D., DeGrandi-Hoffman G., Chen Y.P., Huang S.K. RNA Interference-mediated knockdown of genes encoding spore wall proteins confers protection against Nosema ceranae infection in the European honey bee, Apis mellifera. Microorganisms, 2021, 9(3): 505 (doi: 10.3390/microorganisms9030505).
- Rodríguez-García C., Heerman M.C., Cook S.C., Evans J.D., DeGrandi-Hoffman G., Banmeke O., Zhang Y., Huang S., Hamilton M., Chen Y.P. Transferrin-mediated iron seques-tration suggests a novel therapeutic strategy for controlling Nosema disease in the honey bee, Apis mellifera. PLoS Pathogens, 2021, 17(2): e1009270 (doi: 10.1371/journal.ppat.1009270).
- Huntsman E.M., Cho R.M., Kogan H.V., McNamara-Bordewick N.K., Tomko R.J.Jr., Snow J.W. Proteasome inhibition is an effective treatment strategy for microsporidia infection in honey bees. Biomolecules, 2021, 11(11): 1600 (doi: 10.3390/biom11111600).


