Безопасность и некоторые морфологические и биохимические показатели крови кур-несушек при использовании препаратов фармазина
Автор: Салашная Е.А., Зуев Н.П.
Статья в выпуске: 4 т.248, 2021 года.
Бесплатный доступ
В статье рассмотрены основные показатели безопасности применения препаратов фармазина (фармазина и биофарма-200) на сельскохозяйственной птице. В организме кур при использовании фармазина и биофарма-200 в крови регистрировали повышение содержания эритроцитов, а в них гемоглобина. Кроме того, безопасность применения изучаемых препаратов для потребления человеком обусловлена тем, что их концентрация относительно быстро уменьшается вкуриных яйцах. Фармазин и его производные (биофарм-200) являются перспективными для использования в птицеводстве и могут быть рекомендованы для дальнейшего изучения с этой целью.
Куры, макролиды, фармазин, безопасность, кровь
Короткий адрес: https://sciup.org/142230941
IDR: 142230941 | УДК: 591.1:615.281:636.5 | DOI: 10.31588/2413-4201-1883-248-4-186-190
Safety and some morphological and biochemical indicators of blood in nese chickens when using pharmasin preparations
The article discusses the main safety indicators for the use of pharmaceuticalsin preparations (pharmacin and biopharm-200) on poultry. In the body of chickens, when using pharmacin and biopharm-200, an increase in the content of erythrocytes, and in them hemoglobin, was recorded in the blood. In addition, the safety of the study drugs for human consumption is due to the fact that their concentration decreases relatively quickly in chicken eggs. Pharmazin and its derivatives (biopharm-200) are promising for use in poultry farming and can be recommended for further study for this purpose.
Текст научной статьи Безопасность и некоторые морфологические и биохимические показатели крови кур-несушек при использовании препаратов фармазина
В последнее время в птицеводстве широкое применение нашли многие антимикробные препараты, особенно, фторхинолоны [7 ,8, 10] и макролиды [2, 3], а среди последних препараты тилозина, и в частности, фармазин. Вместе с тем, недостаточно изучено их физиологобиохимическое действие на организм сельскохозяйственной птицы, что имеет большое теоретическое и практическое значение [6].
Из группы макролидов широкое применение имеют производные фармазина – различные модификации биофарма (биофарм – 80, биофарм – 120 и биофарм – 200). Фармакокинетика ранее изученных макролидных препаратов заключается в том, что они равномерно распределяются во всех органах и быстро выводятся из организма, характеризуются печеночно-кишечной рециркуляцией и не обладают кумулятивными свойствами. Макролиды также проявляют антимикробную активность в отношении гемофильной палочки, эшерихий, сальмонелл, клебсиелл, протея, бордетелл, иерсиний, кампилобактерий, стафилококков [2, 3]. Как правило, бруцеллы, коринобактерии, хламидии, микоплазмы, микобактерии, анаэробные стафилококки являются умеренно чувствительными. Следует подчеркнуть, что в пределах чувствительных видов возможны значительные колебания в степени этого показателя возбудителя в зависимости от факторов вирулентности штамма, структуры и физико-химических свойств препарата. Кроме того, выраженный постантибиотический эффект ранее активной концентрации препаратов является существенным. Тилозинсодержащие препараты повышают чувствительность бактерий к фагоцитозу. Бактерицидная активность препаратов увеличивается при совместном применении с препаратами аминогликозидной, тетрациклиновой и макролидной групп, что выражается в сокращении времени достижения максимального бактерицидного эффекта и уменьшении доз использования. Вместе с тем, недостаточно полно изучено их влияние на гематологические и физиологобиохимические показатели крови кур. Как это осуществлено в отношении других средств, применяемых в птицеводстве [1, 4, 9].
Целью работы было: изучить некоторые физиолого-биохимические изменения и безопасность применения препаратов группы макролидов (фармазин и биофарм-200) при их использовании в птицеводстве.
Материал и методы исследований.
Предыдущими исследованиями было установлено, что микроорганизмы Escherichiacoli и Salmonellacholeraesuis оказались достаточно чувствительными к соединениям тилозина, с точки зрения перспективы дальнейшего использования [2, 3]. Учитывая перспективность использования биофарма в птицеводстве и особенности биологии кур [5], были проведены исследования по изучению острой токсичности препарата и его влияния на физиолого-биохимические показатели крови кур-несушек. Острую токсичность препарата изучали набеспородных белых мышахвесом 17-21 г.
В эксперименте на курах-несушках было изучено влияние препаратов на морфолого-биохимические показатели крови при их введении в дозе и сроках, используемых для лечения птицы: в 1-ой группе (30 голов) фармазинэнтерально 20 мг/кг, во второй (30 голов) – биофарм – 200 энтерально в дозе 70 мг/кг массы тела. Лекарства применяли вместе с кормом в течение 10 дней. Перед введением препаратов, на 1-й,15-й и 30-й сутки исследований у кур из подкрыльцовой вены брали кровь для проведения морфологических и биохимических исследований: определение содержания эритроцитов на счетчике частиц Культер-Каунтер, а гемоглобина – гемоглобин цианидным методом, общего белка – рефрактометрическим методом, кальция и фосфора на атомно-абсорбционном спектрофотометре.
На 1-й, 15-й и 30-й сутки опыта от кур собирали фекалии, в которых определяли цвет, запах, консистенцию (органолептически).
Концентрацию водородных ионов определяли – лакмусовой бумагой, содержание белка – проба Вишнякова-
Трибуле, жира и крахмала – микроскопически, общепринятыми методами, наличие углеводов (глюкозы), крови, билирубина, кетоновых тел, протеина – качественными реакциями с реактивами AmesCompany (США).
Фармакокинетикутилозин содержащих препаратов изучали с определением действующего вещества биофарма-200 и фармазина-тилозина. Препарат назначали в течение 10 дней в терапевтической дозе. После прекращения его введения у подопытной птицы забирали яйца и в них исследовали содержание действующего вещества биофарма – тилозина. В качестве контроля использовали яйца, полученные от кур, не получавших препараты.
Исследования ДВ – тилозина, было проведено спектрофотометрическим методом на спектрофотометре СФ-26 по методике, разработанной в лаборатории фармакологии и фармации ВНИВИПФиТ Антиповым В.А. с соавторами (1982).
Результат исследований.
Результаты определения безвредности (острой токсичности) биофарма-200 представлены в таблице 1, из которой видно, что препарат относится к малотоксичным средствам.
Таблица 1 – Определение безвредности препарата биофарм – 200
|
Пероральное введение |
Подкожное введение |
||||||
|
доза, мг/кг |
количество животных |
пало |
доза, мг/кг |
количество животных |
пало |
||
|
голов |
% |
голов |
% |
||||
|
2100 |
6 |
- |
- |
400 |
6 |
- |
- |
|
2700 |
6 |
2 |
33,4 |
500 |
6 |
1 |
16,7 |
|
3100 |
6 |
3 |
50,1 |
600 |
6 |
1 |
16,7 |
|
3400 |
6 |
3 |
50,1 |
700 |
6 |
2 |
33,4 |
|
4300 |
6 |
3 |
50,0 |
800 |
6 |
3 |
50,1 |
|
4500 |
6 |
4 |
66,7 |
900 |
6 |
4 |
56,8 |
|
5300 |
6 |
5 |
83,3 |
1000 |
6 |
4 |
56,8 |
|
5700 |
6 |
5 |
83,3 |
1100 |
6 |
5 |
73,5 |
|
6100 |
6 |
5 |
83,3 |
1200 |
6 |
6 |
100 |
|
6200 |
6 |
6 |
100 |
||||
|
ЛД50=4300 мг/кг |
ЛД50=900 мг/кг |
||||||
Проведенными исследованиями была установлена стимулирующая активность изучаемых препаратов в отношении содержания эритроцитов, гемоглобина, кальция и фосфора в пределах физиологических границ. Закономерности фармакокинетики и остаточные количества действующего вещества фармазина и биофарма-200 (тилозина) в куриных яйцах представлены в таблице 2.
Таблица 2 – Содержание тилозина в яйцах кур-несушек
|
Сутки |
Концентрация тилозина при использовании фармазина, мкг/мл |
Концентрация тилозинапосле использования биофарма-200, мкг/мл |
|
1 |
1,48 |
1,07 |
|
2 |
1,48 |
0,48 |
|
3 |
0,53 |
0,44 |
|
4 |
0,34 |
0,27 |
|
5 |
0,31 |
0,25 |
|
6 |
0,35 |
0,17 |
|
7 |
0,21 |
Отсутствует |
|
8 |
Отсутствует |
Отсутствует |
Из данных таблицы 2 видно, что при использовании биофарма-200 (композиционный препарат, включающий фармазин) на 7-е сутки, в куриных яйцах, его не обнаруживают, тогда как при применении фармазина в отдельности действующее вещество препарата присутствует и только на 8-е сутки, он инактивируется.
Изменения некоторых показателей крови кур-несушек при введении фармазина и его композиционного средства биофарма-200 (состава фармазин плюс биовит-200), представлены на диаграмме 1.
По нашим данным, у кур, получавших биофарм-200 (фармазин+биовит-200), наблюдалось увеличение содержания эритроцитов, гемоглобина, общего белка, кальция и фосфора.
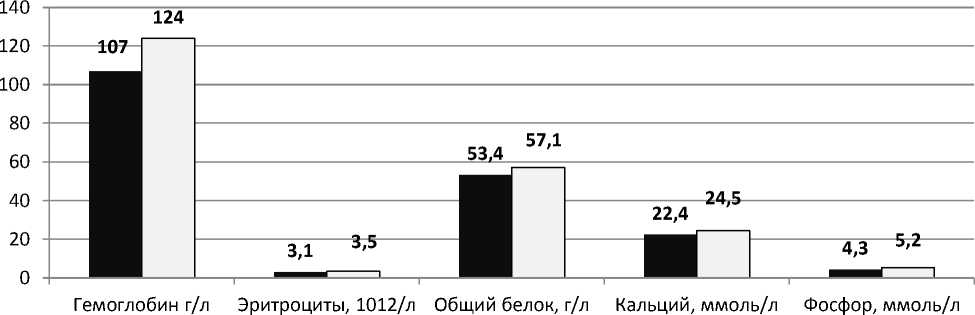
Рисунок 1 – Некоторые морфологические и введении фармазина и биофарма– 200
Проведенными качественными реакциями фекалий птиц было установлено, что цвет, запах и консистенция соответствовали возрасту птицы. Концентрация водородных ионов, содержание белка, жира и крахмала, наличие глюкозы не имели патологический характер. Кровь, билирубин, кетоновые тела не обнаружены.
Заключение. Таким образом, на основании полученных результатов исследований можно сделать вывод, что фармазин и биофарм-200 не оказывает биохимические показатели крови кур при общего токсического действия на кур, что обусловлено тем, что их концентрация относительно быстро уменьшается яйцах.
Применение этих препаратов стимулировало увеличение содержания эритроцитов, а в них гемоглобина. Фармазин и его производные (биофарм-200), являются перспективными для использования в птицеводстве и могут быть рекомендованы для дальнейшего изучения с этой целью.
Резюме
В статье рассмотрены основные показатели безопасности применения препаратов фармазина (фармазина и биофарма-200) на сельскохозяйственной птице. В организме кур при использовании фармазина и биофарма-200 в крови регистрировали повышение содержания эритроцитов, а в них гемоглобина. Кроме того, безопасность применения изучаемых препаратов для потребления человеком обусловлена тем, что их концентрация относительно быстро уменьшается вкуриных яйцах. Фармазин и его производные (биофарм-200) являются перспективными для использования в птицеводстве и могут быть рекомендованы для дальнейшего изучения с этой целью.
Список литературы Безопасность и некоторые морфологические и биохимические показатели крови кур-несушек при использовании препаратов фармазина
- Галиев, Д.М. Влияние кормовой добавки "БШ" на гематологические показатели цыплят бройлеров / Д.М. Галиев, Е.В. Шацких // Развитие научной, творческой и инновационной деятельности молодежи. Сборник статей по материалам X Всероссийской (национальной) научнопрактической конференции молодых ученых, посвященной 75-летию Курганской ГСХА имени Т.С. Мальцева. -2018. - С. 36-40.
- Зуев, Н.П. Получение и разработка антимикробных композиций на основе тилозин содержащих препаратов / Н.П. Зуев, В.Д. Буханов // Материалы первого съезда ветеринарных фармакологов России 21 -23 июня 2007 года. - Воронеж: Изд. "РАСХН, ВНИВИПФ и Т". - С. 311-316.
- Зуев, Н.П. Терапевтическая эффективность композиционных тилозин содержащих препаратов в остром опыте / Н.П. Зуев, В.Д. Буханов // Материалы первого съезда ветеринарных фармакологов России 21 -23 июня 2007 г. -Воронеж: Изд. "РАСХН, ВНИВИПФ и Т". 2007. - С. 307-311.
- Молоканова, О.В. Биохимический состав крови цыплят-бройлеров при включении в рацион протеолитического фермента сибенза ДП 100 / О.В. Молоканова, Е.В. Шацких // Пермский аграрный вестник. - 2019. - № 3 (27). - С. 108-116.
- Сидоренко, Л.И. Биология кур / Л.И. Сидоренко, В.И. Щербатов. -Краснодар: Изд. "КубГАУ", 2016. - 244 с.
- Сурай, П.Ф. От регуляции витагенов к оптимизации иммунного ответа: новые подходы к иммуномодуляции в птицеводстве / П.Ф. Сурай, В.И. Фисинин, И.И. Кочиш // Мировое и российское птицеводство: состояние, динамика развития, инновационные перспективы. Материалы XX Международной конференции. Российское отделение Всемирной научной ассоциации по птицеводству, НП "Научный центр по птицеводству". - 2020. - С. 56-66.
- Падейская, Е.Н. Антимикробные препараты группы фторхинолонов в клинической практике / Е.Н. Падейская, В.П. Яковлев. - М.: Изд. Логата, 1998. - 351 с.
- Моисеева, А.А. Влияние энрофлоксацина на динамику белой крови птиц раннего возраста / А.А. Моисеева, А.А. Присный, В.Н. Скворцов // Теория и практика ветеринарной фармации, экологии и токсикологии в АПК. Материалы международной научнопрактической конференции, посвященной 100-летию кафедры фармакологии и токсикологии СПбГУВМ. - Санкт-Петербург. - 2021. - С. 168-170.
- Фисинин, В.И. Эффективность воздействия антиоксиданта на зоотехнические. Гематологические показатели выращивания и состояние печени бройлеров / В.И. Фисинин [и др.] // Птица и птицепродукты. - 2021. - № 3. - С. 48-50.
- Юрин, Д.В. Переносимость энрофлоксацина при парентеральном введении / Д.В. Юрин, В.Н. Скворцов // В сборнике: Актуальные проблемы науки в агропромышленном комплексе. Сборник статей 72-й международной научнопрактической конференции. - Караваево. -2021. - С. 175-179.


