Биологические эффекты, связанные с поступлением в организм цыплят-бройлеров наночастиц хрома в разной дозировке
Автор: Лебедев С.В., Гавриш И.А., Губайдуллина И.З., Шабунин С.В.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Ультрадисперсные кормовые добавки
Статья в выпуске: 4 т.54, 2019 года.
Бесплатный доступ
Хром - важный химический элемент для человека и животных, его эссенциальность проявляется в снижении количества глюкозы и холестерина в крови, уменьшении жировых отложений. Всасывание хрома зависит от его источника, размера частиц и состава рациона, при этом уменьшение размера частиц Cr позволяет увеличить скорость усвоения хрома в организме. Перспективность замены традиционных источников микроэлементов на органические и ультрадисперсные формы металлов определяется высокой удельной площадью поверхности последних, большей реакционной способностью и биодоступностью. В настоящей работе мы впервые показали, что наночастицы (НЧ) Cr2O3 в дозах от 50 до 100 мкг/кг корма не обладают токсичным действием, влияют на формирование продуктивных качеств через стимулирование выработки пищеварительных ферментов и оказывают положительное действие на абсорбцию элемента в тушке цыплят-бройлеров. Нашей целью была биологическая аттестация различных доз наночастиц хрома в рационе цыплят-бройлеров ( Gallus gallus ) по активности пищеварительных ферментов, биохимическим и микробиологическим показателям...
Цыплята-бройлеры, антиоксидантные ферменты, продуктивность, концентрация cr, биохимические показатели крови, пищеварительные ферменты
Короткий адрес: https://sciup.org/142222198
IDR: 142222198 | УДК: 636.52/.58:591.1:636.085.12:546.763 | DOI: 10.15389/agrobiology.2019.4.820rus
Effects caused by different doses of dietary chromium nanoparticles fed to broiler chickens
Chromium is important chemical element for humans and animals which essentiality is manifested in reducing the amount of glucose and cholesterol in blood, reducing body fat. Factors which influence the absorption of chromium are source, size and composition of diet. Reducing size of Cr particles allows one to increase absorption. Replacement of traditional sources of microelements for organic and ultrafine metal forms is prospective due to their surface area, higher reactivity and bioavailability. In this paper, we show for the first time that Cr2O3 nanoparticles (NPs) at doses of 50 to 100 µg/kg of feed have no toxic effect, improve productive performance through stimulation of digestive enzymes and have positive effect on accumulation of the element in broiler chicken carcass. Our goal was to estimate effects of various doses of dietary chromium nanoparticles on the activity of digestive enzymes, biochemical blood parameters and gut microbiota in Arbor Aikres broiler chickens ( Gallus gallus ) (OAO Orenburg Poultry Farm, 2018)...
Текст научной статьи Биологические эффекты, связанные с поступлением в организм цыплят-бройлеров наночастиц хрома в разной дозировке
Хром — важный химический элемент для человека и животных, его эссенциальность, согласно нормам (1), проявляется в снижении концентрации глюкозы и холестерина в крови, уменьшении жировых отложений, стимуляции развития мышечной ткани (2). Недостаточное поступле- ние хрома в организм, связанное с типом и качеством питания, сопровождается замедлением роста и ухудшением толерантности к глюкозе (3). Cr стимулирует функцию инсулина, усиливая функцию рецепторов чувствительных к инсулину клеток (4-6).
Важный инструмент в регуляции обмена поступившего в организм хрома — его способность приникать через кишечную стенку. Этот процесс ускоряется при уменьшении размера частиц хрома и наличии пищеварительных агентов (витамины, фитаты, аминокислоты). Хром имеет чрезвычайно низкую переваримость, плохо всасывается (для органических форм — 25 %, неорганических — 3 %), при этом всасывание Cr3+ происходит в основном через почки (80-95 %) (7) с потерями при депонировании в волосяном покрове, выведении через сальные железы и с желчью (45 %) (8), что свидетельствует о быстром поглощении и рекреации Cr. Независимо от увеличения дозы хрома в рационе (40-240 мкг/сут) степень его усвоения остается постоянной — 0,4-2,0 % (9). Органический Cr оказывает более благоприятное воздействие на птицу по сравнению с неорганическими формами из-за повышенной абсорбции и биодоступности (10). Следовательно, факторы, обусловливающие всасывание хрома, — это его источник, размер частиц и состав рациона, при этом уменьшение размера частиц Cr позволяет увеличить скорость усвоения хрома в организме.
Перспективность замены традиционных источников микроэлементов на органические и ультрадисперсные формы металлов определяется высокой удельной площадью поверхности последних, большей реакционной способностью и биодоступностью. Учитывая малые размеры и высокую проникающую способность наночастиц (НЧ), необходимо помнить, что каждый отдел желудочно-кишечного тракта имеет уникальную среду со специфическим набором энзимов и рН (11). Наночастицы должны быть в состоянии преодолеть эти препятствия, чтобы проявить биологическую активность в тонком отделе кишечника (11).
Биологическое действие наночастиц хрома связано с участием в метаболизме нуклеиновых кислот, увеличением площади мышц, накоплением хрома в тканях, уменьшением количества жира (12, 13). В экспериментах на птице добавление хрома в рацион увеличивало количество белка в мышцах груди и бедра и снижало содержание холестерина в мышцах (14).
Следует отметить, что отчеты о влиянии различных источников хрома на активность пищеварительных энзимов у животных встречаются редко, хотя изучение возможности использования НЧ в качестве модуляторов активности пищеварительных ферментов представляется перспективным. Известно, что в молекулах ферментов существует несколько регуляторных центров, специализированных по отношению к различным эффекторам (15). По мнению ряда исследователей, быстрые конформационные переходы могут происходить в результате действия модификаторов (16). Альтернативные формы микроэлементов могут быть необходимым инструментом в управлении процессами пищеварения для улучшения конверсии питательных веществ, повышения продуктивности и пищевой ценности птицеводческой продукции.
В настоящей работе нами впервые было показано, что НЧ Cr2O3 в дозах от 50 до 100 мкг/кг корма не обладают токсичным действием, влияют на формирование продуктивных качеств через стимулирование выработки пищеварительных ферментов и оказывают положительное действие на абсорбцию элемента в тушке цыплят-бройлеров.
Нашей целью была биологическая аттестация различных доз наночастиц хрома в рационе цыплят-бройлеров (Gallus gallus) по активности пищеварительных ферментов, биохимическим и микробиологическим показателям.
Методика. Исследования проводили на цыплятах-бройлерах кросса Арбор Айкрес (ОАО «Птицефабрика Оренбургская», , 2018 год). Экспериментальную часть работы выполняли в соответствии с протоколами Женевской конвенции, принципами надлежащей лабораторной практики (Национальный стандарт Российской Федерации ГОСТ Р 53434-2009), правилами лабораторной практики при проведении доклинических исследований в РФ (ГОСТ 3 51000.4-96) и «The Guide for Care and Use of Laboratory Animals» (National Academy Press Washington, D.C., 1996). Птицу содержали в клетках КУН-05 площадью 4050 см2 (90½45½45 см) и маркировали пластиковыми ножными бирками. На основании ежесуточного взвешивания методом пар-аналогов сформировали 5 групп: одну контрольную и четыре опытных (n = 30, масса от 160 до 180 г). Птицу кормили 2 раза в сутки рационом, приготовленным с учетом рекомендаций (17) в соответствии с потребностью в разные возрастные периоды.
Состав основного рациона (ОР) в стартовый и ростовой период был следующим: зерно пшеницы (соответственно 27,1 и 41,2 %), кукуруза (16 и 22 %), шрот соевый (25 и 15 %), шрот подсолнечный (18 и 8 %), масло подсолнечное (5 и 2,8 %), монохлоргидрат лизина, 98 % (0,35 и 0,17 %), DL-метионин (0,10 и 0,13 %), L-треонин (0,03 и 0,54 %), соль поваренная (0,28 и 0,3 %), монокальцийфосфат (0,7 и 0,7 %), мел кормовой (0,5 и 0,4 %), известняковая мука (1,0 и 0,7 %), премикс (2 %) (ООО «Коудайс МКорма», Россия). Поение осуществлялось вволю. Взвешивание проводили еженедельно. Контрольная птица на протяжении всего эксперимента получала основной рацион. Птицам опытных групп в период эксперимента (14-42-е сут) в основной рацион дополнительно вводили НЧ Cr2O3 (d = 91 нм, удельная поверхность — 9 м2/г, Z-потенциал — 93±0,52 мВ, содержание Cr — 99,8 %, метод получения — плазмохимический синтез; ООО «Платина», г. Москва, Россия) в следующих дозах: I группа — 50, II — 100, III — 200 и IV — 400 мкг/кг. Дозировки корма были выбраны с учетом ранее полученного положительного эффекта влияния хрома на ростовые и биохимические показатели цыплят-бройлеров (18, 19). Комбикорм готовили методом ступенчатого смешивания, НЧ вводили после диспергирования в физиологическом растворе (УЗДН-2Т, «НПП Академприбор», Россия; 35 кГц, 300 Вт, 10 мкА, 30 мин).
Кровь для анализа брали перед убоем в 21- и 42-суточном возрасте утром натощак из подкрыльцовой вены. Сыворотку крови исследовали на автоматическом анализаторе СS-T240 («DIRUI Industrial Co., Ltd», Китай) с использованием коммерческих наборов для ветеринарии ДиаВетТест (ООО «Диакон-Вет», Россия) и Randox Laboratories Limited («Randox Laboratories, Ltd.», Великобритания).
Биоматериал получали после декапитации бройлеров под нембута-ловым наркозом на 21-е и 42-е сут. Проводили послеубойную анатомическую разделку тушек, измеряли абсолютную и относительную массу внутренних органов с последующим измельчением и озолением (Multiwave 3000, «Anton Paar», Австрия). Микроэлементный анализ осуществляли методами атомно-эмиссионной спектрометрии (Optima 2000 V, «Perkin Elmer», США) и масс-спектрометрии (Elan 9000, «Perkin Elmer», США) согласно рекомендациям производителя.
Для оценки активности пищеварительных ферментов непосредственно после вскрытия извлекали кишечник, отбирали в стерильные пробирки поджелудочную железу и 12-перстную кишку. Активность панкреа-822
тических ферментов измеряли на автоматическом биохимическом анализаторе СS-T240 («Dirui Industrial Co., Ltd», Китай) с использованием коммерческих биохимических наборов для ветеринарии ДиаВетТест (ООО «Диакон-Вет», Россия), активность протеазы — методом гидролиза казеина (20).
Качественный и количественный состав микробиоценоза кишечника бройлеров определяли по стандартной методике (21). В работе использовали Эндо-агар («ООО НИЦФ», Россия) для энтеробактерий с нормальной ферментативной активностью и условно-патогенных лактозонегативных энтеробактерий, мясо-пептонный агар (МПА) (ООО «НИЦФ», Россия) — для аэробной флоры, Рогоза-агар («Himedia», Индия) — для лактобактерий, Бифидо-агар («Himedia», Индия) — для молочнокислых бактерий (бифидобактерий), желточно-солевой агар (ЖСА) (ООО «НИЦФ», Россия) — для подсчета стафилоккоков, ВСА-агар («Himedia», Индия) — для патогенных сальмонелл. Посевы инкубировали в течение 24-72 ч при температуре 37 ° С. Число микроорганизмов каждой группы в 1 г кишечного содержимого (M) подчитывали по формуле M = N ½ 10n, где N — число колоний, n — разведение материала. Окончательный результат в расчете на 1 г содержимого слепой кишки выражали как KOE/г.
Статистический анализ выполняли методом ANOVA (программный пакет Statistica 10.0, «StatSoft, Inc.», США) и в программе Microsoft Excel. Статистическую достоверность различий сравниваемых показателей оценивали по t -критерию Стьюдента. Достоверными считали значения при р < 0,05. Данные представлены как средние значения ( M) и стандартные ошибки средних (±SEM).
Результаты. За период эксперимента расход корма на 1 кг прироста живой массы в контроле составил 1,85 кг, в зависимости от дозы НЧ Cr2O3 разница с контролем составляла от 8 до 16 %. Наибольшими ростовыми показателями характеризовалась птица в III и IV опытных группах (табл. 1). Аналогичный ростостимулирующий эффект был получен другими авторами при испытании в качестве добавки НЧ Fe, Cu, Zn (22, 23). Имеются данные об отрицательном действии препарата хрома в дозе 400 г/т на продуктивность и сохранность бройлеров (24), тогда как дозы до 1200 мкг/кг положительно влияют на живую массу и эффективность потребления корма (18, 19, 25).
1. Показатели роста и содержание хрома в биосубстратах и тушке цыплят-бройлеров кросса Арбор Айкрес в зависимости от дозы наночастиц Cr2O3 в рационе ( М ±SЕМ, n = 30, опыт в условиях вивария, 42-е сут эксперимента)
|
Показатель |
Группа |
||||
|
контроль |
I |
II |
III |
IV |
|
|
Начальная масса, г |
224±2,4 |
230±4,3 |
234±3,0 |
224±3,2 |
232±23,1 |
|
Конечная масса, г |
2266±20,3 |
2366±40,1 |
2431±36,4 |
2533±59,8 |
2536±78,2 |
|
Расход корма, г: |
|||||
|
всего |
3774,30 |
3649,80 |
3739,53 |
3855,70 |
3853,97 |
|
на 1 кг прироста |
1,85 |
1,71 |
1,70 |
1,67 |
1,55 |
|
Содержание Cr, мкг/кг: |
|||||
|
в рационе |
540±1,5 |
587±1,5 |
637±2,5* |
736±2,7* |
937±2,4** |
|
в помете |
433±3,5 |
373±4,6 |
466±6,1 |
363±4,2 |
366±3,8 |
|
в тушке |
108±0,2 |
125±2,4** |
129±4,1** |
132±3,2* |
145±2,8** |
|
Соотношение Cr: |
|||||
|
корм/помет |
1,2 |
1,5 |
1,3 |
2,0 |
2,5 |
|
корм/тушка |
5,0 |
4,6 |
4,9 |
5,5 |
6,4 |
|
П р и м е ч а н и е. Описание групп см. в разделе «Методика». *, ** Различия с контролем статистически значимы соответственно при р < 0,05 |
и р < 0,01. |
||||
Известно, что биологическая роль минеральных веществ в организме зависит от их биохимической доступности. В нашем эксперименте при максимальных дозах введения 200 и 400 мкг/кг содержание Cr в туш- ке бройлеров было на 28,2 и 25,6 % выше, чем в контроле, на фоне снижения его доли в помете на 15 %. Коэффициент Crкорм/Crпомет был наибольшим в группах с высоким содержанием хрома в рационе, что свидетельствует об его лучшем использовании. В то же время степень усвоения из корма, выраженная коэффициентом Crкорм/Crтушка, находилась в диапазоне 4,6-6,4, что указывает на отсутствие агломераций (образования более крупных по размерам вторичных частиц), характерных для наночастиц, поступающих в организм в высоких дозах, а также о наличии регуляторного механизма в метаболизме хрома (23). Учитывая, что в клетках тканей кишечника эффективность поглощения наночастиц размером 100 нм в 15-250 раз выше, чем более крупных микрочастиц (26), отложение хрома благодаря проникновению в цитоплазму (27) может увеличиваться за счет дефицита транспортного белка трансферрина и образования в 12-перстной, слепой и толстой кишке стабильных трудно адсорбируемых гидратов (28).
Введение НЧ Cr2O3 в рацион цыплят-бройлеров сопровождалось отсутствием окислительного стресса, на что указывала активность каталазы (КАТ), супероксиддисмутазы (СОД) и концентрация малонового диальдегида (табл. 2) в сыворотке крови. В частности, на фоне снижения СОД во всех опытных группах достоверные различия (р ≤ 0,05) с контролем были характерны для II группы (51,3 %), содержание КАТ было стабильно низким и уменьшалось в ответ на увеличение дозы НЧ Cr2O3 в рационе. Отсутствие токсичности и ростостимулирующий эффект НЧ Cr2O3 определялись нарастанием количества NO-метаболитов во II и III опытных группах соответственно на 18,8 и 9,2 % относительно контроля (р ≤ 0,05). В других группах различия по сравнению с контрольной не превышали 5 %.
2. Активность каталазы (КАТ) , супероксиддисмутазы (СОД) , концентрация малонового диальдегида (МД) и NO-метаболитов в сыворотке крови у цыплят-бройлеров кросса Арбор Айкрес в зависимости от дозы наночастиц Cr2O3 в рационе ( М ±SЕМ, n = 30, опыт в условиях вивария, 42-е сут)
|
Показатель |
Группа |
||||
|
контроль |
I |
II 1 |
III |
IV |
|
|
СОД, % ингибирования |
|||||
|
аутоокисления адреналина |
568±68,6 |
405±57,0 |
277±18,6* |
509±28,6 |
435±48,0 |
|
КАТ, мкмоль Н2О2•л - 1•мин - 1 |
2363±54,9 |
1050±82,8* |
1871±51,38* |
1510±47,4* |
1116±64,1* |
|
МД, нмоль/мл |
0,65±0,260 |
0,36±0,006 |
0,41±0,120 |
0,29±0,090 |
0,18±0,040 |
|
NO-метаболиты, мкмоль/л |
59,8±2,53 |
61,4±3,42 |
73,6±3,62* |
65,8±1,51* |
62,9±1,83 |
П р и м еч а ни е. Описание групп см. в разделе «Методика».
* Различия с контролем статистически значимы при р ≤ 0,05.
Различия в механизме действия НЧ хрома в разных дозировках приводили к неодинаковым изменениям биохимических показателей крови (табл. 3). Эффект НЧ Cr2O3 выражался в стимуляции активности аланин-аминотрасферазы (АлАТ) и аспартатаминотрансферазы (АсАТ) на 14-е сут. Так, активность АлАТ во II и IV группах была практически в 2 раза выше, чем в контроле (р ≤ 0,05). Для АсАт на 21-е сут достоверные различия были характерны для всех опытных групп (см. табл. 3).
3. Биохимические показатели сыворотки крови у цыплят-бройлеров кросса Арбор Айкрес на 21-е и 42-е сут в зависимости от дозы наночастиц Cr2O3 в рационе ( М ±SЕМ, n = 30, опыт в условиях вивария)
|
Показатель |
Группа |
||||
|
контроль |
I 1 |
II 1 |
III |
IV |
|
|
Н а 21-е сут |
|||||
|
АлАТ, Ед/л |
7,3±0,50 |
8,3±2,40 |
14,2±1,00*** |
7,1±3,20 |
13,2±1,70** |
|
АсАТ, Ед/л |
52,5±33,00 |
80,2±50,10* |
190,4±76,90** |
188,7±33,20** |
106,4±20,00** |
|
Глюкоза, ммоль/л |
14,0±0,40 |
14,8±0,80 |
14,4±1,60 |
15,3±0,50 |
14,8±0,50 |
|
Холестерин, ммоль/л |
3,0±0,10 |
3,4±0,20 |
2,9±0,60 |
2,7±0,30 |
3,2±0,30 |
|
Триглицериды, ммоль/л |
0,6±0,20 |
0,6±0,20 |
1,6±0,20* |
0,6±0,30 |
1,2±0,10* |
Продолжение таблицы 3
|
Амилаза, Ед/л |
436±19,1 |
422±195,1 |
303±64,1 |
403±25,7 |
617±42,9* |
|
Липаза, Ед/л |
6,4±0,30 |
7,2±0,30 Н а 42-е сут |
6,8±0,30 |
7,9±0,80 |
8,3±2,40 |
|
АлАТ, Ед/л |
23,0±2,10 |
17,1±1,00 |
26,3±1,10 |
24,0±2,40 |
15,4±1,10 |
|
АсАТ, Ед/л |
70,5±6,10 |
152,0±8,50*** |
63,8±7,80 |
69,4±13,70 |
116,6±20,90** |
|
Глюкоза, ммоль/л |
15,4±0,40 |
14,3±0,60 |
13,4±1,10 |
14,0±0,50 |
14,2±0,20 |
|
Холестерин, ммоль/л |
3,8±0,30 |
3,3±0,10 |
3,0±0,30 |
3,1±0,30 |
3,9±0,40 |
|
Триглицериды, ммоль/л |
0,6±0,10 |
0,4±0,20 |
0,3±0,10 |
1,1±0,30* |
2,1±0,70* |
|
Амилаза, Ед/л |
173±5,6 |
180±5,6 |
157±10,4 |
166±1,2 |
186±1,2 |
|
Липаза, Ед/л |
2,7±0,80 |
2,3±0,80 |
1,4±0,70 |
2,8±0,70 |
5,4±4,50** |
П р и м е ч а н и е. Описание групп см. в разделе «Методика». АлАТ — аланинаминотрансфераза, АсАТ — аспартатаминотрансфераза.
*, **, *** Различия с контролем статистически значимы при р ≤ 0,05; р ≤ 0,01 и р ≤ 0,001.
К окончанию эксперимента активность АлАТ в сыворотки крови у цыплят-бройлеров (при статистически недостоверной разнице с контролем) снижалась в группах с минимальной и максимальной нагрузкой НЧ Cr2O3, тогда как АсАТ — наоборот, увеличилась на 53,7 и 39,6 % (р ≤ 0,05). Высокая активность эндогенных трансфераз может быть признаком нарушения функции печени, почек и поджелудочной железы, но, учитывая отсутствие маркеров воспаления (показатели СОД и КАТ), допустимо предположить, что метаболическая функция хрома связана с тонкими механизмами участия в стимулировании выработки хромодулина (LMWCCr) (29). Хромодулин акцептирует молекулы хрома, связанные биологическими молекулами, в том числе трансферрином, и стимулирует гепатопротекторную активность (30). Изменения показателей по глюкозе и холестерину при поступлении хрома с рационом мы не отмечали.
Маркером энергетического и липидного обмена служит концентрация в крови триглицеридов. На 21-е сут у бройлеров, получавших в составе рациона НЧ Cr2O3 в дозе 100 и 400 мкг/кг, этот показатель был больше соответственно на 61,6 и 48,5 % по сравнению с контролем. Эффект пролонгировался к концу учетного периода, что не подтверждает результаты исследований (31), где высокое содержание холестерина и триглицеридов было характерно для хромдефицитных состояний. Такая неоднозначная реакция организма, возможно, связана как с высокой биодоступностью наночастиц хрома, так и с перестройкой ферментативной системы (32).
Активность амилолитических ферментов в крови на 21-е сут оказалась наибольшей в IV группе, разница с контрольными значениями составила 29,5 % (р ≤ 0,05). В других группах существенных отклонений не обнаружили. Аналогичная динамика была характерна для липазы. В группах, получавших наибольшие дозы НЧ Cr2O3 (200 и 400 мкг/кг), активность этого фермента на 21-е и 42-е сут оказалась на 19-30 % выше, чем в контроле. Увеличение активности сывороточных ферментов может быть результатом синтеза или ресинтеза микронутриентов, повышения проницаемости клеточных мембран и транслокации пищеварительных ферментов в кровяное русло (33).
Ряд авторов (33, 34) постулируют, что циркулирующие с кровотоком ферменты представляют собой депо для последующей рекреции поджелудочной железой. Второй механизм появления панкреатических гидролаз в крови — их резорбция из выводных протоков железы (так называемое уклонением ферментов), третий механизм — резорбция ферментов из тонкой кишки (35).
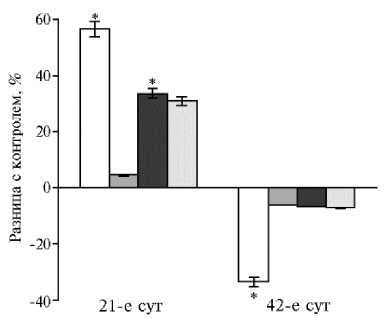
Гормоны и биологически активные вещества, вырабатываемые поджелудочной железой, необходимы для эффективного поглощения питательных веществ через слизистую оболочку кишечника. На 21-е сут для ферментов поджелудочной железы был характерен рост активности липазы (до 96 % во всех опытных группах). Пик активности амилазы и протеазы соответствовал дозам НЧ Cr 100 и 400 мкг/кг (р ≤ 0,05). Дозозависимая разница на 42-е сут эксперимента выражалась в ингибировании амилазы в диапазоне доз от 100 до 400 мкг/кг на фоне увеличения активности липазы и протеазы при низких и высоких концентрациях НЧ Cr (рис. 1).
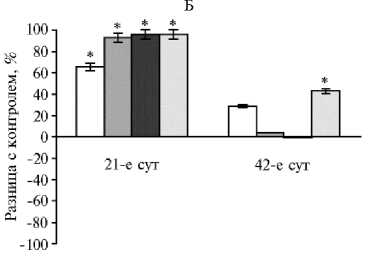
Рис. 1. Разница с контролем в активности амилазы (А) , липазы (Б) и протеазы (В) в поджелудочной железе у цыплят-бройлеров кросса Арбор Айкрес при добавлении в рацион наночастиц Cr 2 O 3 в разных дозах: a — 50 мкг/кг, б — 100 мкг/кг, в — 200 мкг/кг, г — 400 мкг/кг ( М ±SЕМ, n = 30, опыт в условиях вивария).
* Различия с контролем статистически значимы при р ≤ 0,05.
А
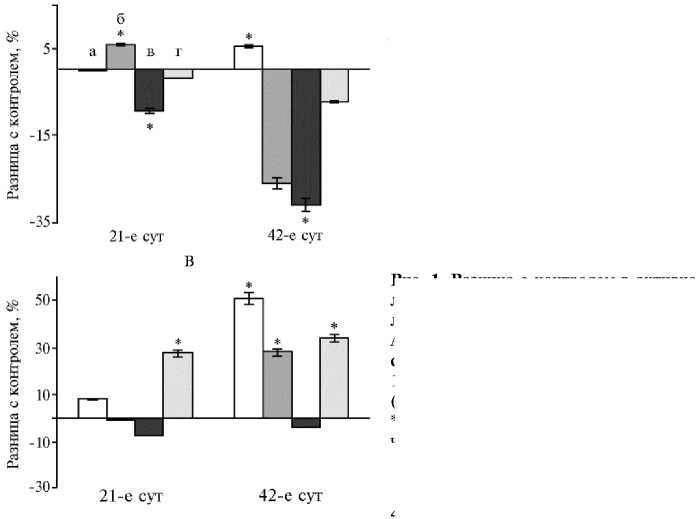
В этот возрастной период (на 42-е сут эксперимента) функциональное напряжение инкреции ферментов под воздействием НЧ Cr обусловлено снижением активности амилазы и липазы в поджелудочной железе на фоне роста протеолитической активности. Реадсорбция ферментов в кровь, а затем в просвет тонкого кишечника рассматривается как возможная адаптация энтеропанкреатической регуляции в разные возрастные периоды (36). С этим механизмом, вероятно, связано наблюдаемое нами изменение активности ферментов в 12-перстной кишке на значения, диаметрально противоположные соответствующим показателям в поджелудочной железе.
Таким образом, мы показали, что у цыплят-бройлеров, потреблявших в составе рациона HЧ Сr, происходят дозозависимые разнонаправленные изменения активности пищеварительных ферментов в поджелудочной железе в разные возрастные периоды. Наши данные о модификации ферментативной активности в присутствии наночастиц согласуется с результатами, полученными другими авторами (37-39). В их опытах образование комплекса химотрипсина с НЧ селена способствовало смещению рН гидролитической активности в щелочную область с одновременным увеличением максимальной ферментативной активности в сравнении со свободным ферментом.
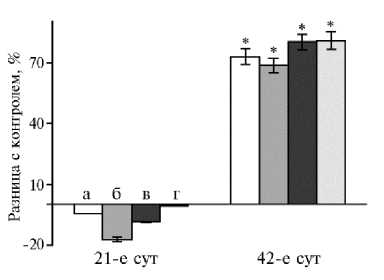
Эскалацию ферментов через кишечник с сохранением активности подтвердили результаты анализа помета (рис. 2). Активность амилазы в помете на 21-е сут снижалась, но возрастала к концу учетного периода. Активность липазы не изменялась в первый период и нарастала на 7075 % на 42-е сут (p ≤ 0,05). Активность протеазы, наоборот, была выше контроля на 21-е сут с последующим снижением к концу эксперимента.
На 21-е сут контрольная группа имела самое низкое значение рН кишечного содержимого, в то время как в других группах эта величина изменялась в пределах рН 4,62-7,53. На 42-е сут только в группе, получавшей НЧ Cr2O3 400 мкг/кг, показатель кислотности отличался от контрольного и составил рН 9,34. Сохранение и увеличение активности амилазы и липазы при таком рН может быть примером адаптации ферментов, а также их стабилизации наночастицами. Снижение активности амилазы в IV группе, вероятно, свидетельствует о чувствительности этого фермента к изменению кислотно-щелочного баланса среды.
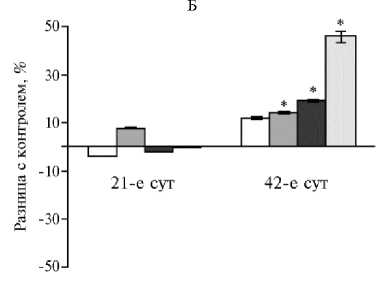
Рис. 2. Разница с контролем в активности амилазы (А) , липазы (Б) и протеазы (В) в помете у цыплят-бройлеров кросса Арбор Айкрес при введении в рацион наночастиц Cr 2 O 3 в разных
А
В
дозах: a — 50 мкг/кг, б — 100 мкг/кг, в
—
200 мкг/кг, г — 400 мкг/кг ( М ±SЕМ, n = 30, опыт в условиях вивария).
* Различия с контролем статистически значимы при р ≤ 0,05.
Одна из причин снижения функции кишечного пищеварения у птиц — избыточной рост микробной флоры в просвете кишечника, что приводит к снижению продвижения химуса и преждевременной деконъюгации первичных желчных кислот (40). Избыточная микробная флора может вызывать повреждения эпителия тонкой кишки, поскольку метаболиты некоторых микроорганизмов цитотоксичны. Определение численности микроорганизмов в слепой кишке бройлеров — важный этап монито- ринга жизнеспособности организма (41). В слепой кишке бройлеров на 21-е сут в группе, получавшей 400 мкг Cr/кг корма, снижалось общее число микроорганизмов (на 88,4 %) (p ≤ 0,05), численность энтеробактерий и бифидобактерий (соответственно на 28,0 и 65,4 %) (p ≤ 0,05), а также возрастала представленность сальмонелл (на 21,7 %, р ≤ 0,05) (табл. 4). При дозе 50 мкг/кг снижалась численность бифидобактерий и лактобактерий (соответственно на 35,6 и 53,8 %) (p ≤ 0,05), доза 100 мкг/кг увеличивала количество энтеробактерий, но снижала число сальмонелл, 200 мкг/кг — способствовала росту численности стафиллококков, энтеробактерий, сальмонелл, одновременно уменьшая число бифидобактерий и лактобактерий. На 42-е сут в I группе число бифидобактерий продолжало снижаться с одновременным сокращением численности стафиллококков и сальмонелл.
Во II группе возрастало число энтеробактерий и снижалось — бифидобактерий. В III группе уменьшалась представленность бифидобактерий, в IV группе на 42-е сут (так же, как на 21-е сут) — энтеробактерий, бифидобактерий и сальмонелл.
-
4. Численность различных групп микроорганизмов в слепой кишке у цыплят-бройлеров кросса Арбор Айкрес на 21-е и 42-е сут в зависимости от дозы наночастиц Cr2O3 в рационе ( М ±SЕМ, n = 30, опыт в условиях вивария)
Группа
Общее микробное число
Стафил-лококки
Энтеробактерии
Сальмонеллы
Бифидобактерии
Лактобактерии
Целлюлозоразлагающие бактерии
Контроль
37,6±3,20
0,5±0,10
Н 8,9±0,60
а 21-е сут 15,0±0,70
6,2±0,40
1,4±0,20
0,9±0,20
I
40,0±5,10
0,9±0,10
11,7±1,20
16,5±0,80
4,0±0,30*
0,6±0,09*
1,1±0,40
II
44,8±2,30
1,3±0,20
12,8±1,20*
10,3±0,30*
6,6±0,50
0,9±0,20
0,8±0,20
III
42,6±3,10
2,3±0,20*
15,1±2,10*
20,2±1,40*
3,0±0,20*
0,2±0,01*
1,1±0,30
IV
4,1±0,60*
0,9±0,10
6,4±0,30*
19,2±1,00*
2,1±0,20*
1,7±0,40
0,5±0,10
Контроль
48,6±4,10
3,1±0,60
Н 15,1±0,60
а 42-е сут
2,5±0,30
31,0±2,60
67,0±5,90
2,1±0,30
I
56,1±4,90
1,2±0,10*
18,6±1,30
0,9±0,10*
20,0±2,90*
52,3±4,80
1,8±0,40
II
46,6±3,80
2,2±0,20
19,2±1,10*
0
20,7±2.50*
56,3±5,50
1,9±0,20
III
60,6±5,80
2,0±0,10
17,4±1,90
3,5±0,60
18,7±2,70*
52,3±5,30
2,3±0,30
IV
62,2±5,20
1,8±0,10
12,3±0,80*
0,7±0,20*
17,7±3,10*
62,2±6,80
2,2±0,40
П р и м еч а ни е. Описание групп см. в разделе «Методика». * Различия с контролем статистически значимы при р ≤ 0,05.
В этом контексте наблюдаемый «энзиматический выброс» свидетельствует о нарушениях в микроэкологии кишечника, что обусловлено рядом причин: (усиленная перистальтика, измененный состав химуса, поступающего в толстый кишечник, гиперпродукция щелочных секретов при патологиях) (39). Известно, что под влиянием микробных протеолитических ферментов рН фекалий сдвигается в сторону щелочных значений, способствуя сохранению активности ферментов в кишечнике (38, 42, 43).
Множественные физиологические эффекты НЧ Cr, отмеченные ранее на крысах (44) и в настоящем исследовании на цыплятах-бройлерах, связаны с физико-химическими свойствами наночастиц, облегчающими их взаимодействие с биологическими объектами (45).
Итак, наночастицы Cr2O3 в рационе не токсичны, на что указывает отсутствие изменений в активности каталазы, супероксиддисмутазы и в накоплении малонового диальдегида. При этом хром действует как антиоксидант, повышая концентрации NO-метаболитов в сыворотке крови. Биологическая роль наночастиц хрома при включении в рацион цыплят-бройлеров в дозах 50 и 100 мкг/кг корма проявляется в стимулировании роста, выработки пищеварительных ферментов и снижении затрат корма. При высоких концентрациях НЧ в разные возрастные периоды (21-е сут и 42-е сут) происходило частичное подавление всасываемости пищеварительных ферментов в кровь и их активности в кишечнике (амилаза) при сохранении активности в помете (амилаза, липаза) за счет ослабления роста микроорганизмов (бифидобактерий, стафиллококков и сальмонелл) и сдвига рН в щелочную сторону.
Список литературы Биологические эффекты, связанные с поступлением в организм цыплят-бройлеров наночастиц хрома в разной дозировке
- National research council. Mineral tolerance of animals. Second revised edition. National Academy Press, Washington DC, 2005 ( ). DOI: 10.17226/11309
- Anderson R.A., Bryden N.A., Polansky M.M. Lack of toxicity of chromium chloride and chromium picolinate in rats. J. Am. Coll. Nutr., 1997, 16: 273-279 ( ). DOI: 10.1080/07315724.1997.10718685
- Simonoff M., Llabador Y., Hamon C., Peers A.M., Simonoff G.N. Low plasma chromium in patients with coronary artery and heart diseases. Biol. Trace Elem. Res., 1984, 6: 431-439 ( ). DOI: 10.1007/BF02989260
- Anderson R.A. Chromium. In: Trace elements in human and animal nutrition. 5th edition. Academic Press, San Diego, CA, 1987.
- Linder M.C. Nutrition and metabolism of the trace elements. In: Nutritional biochemistry and metabolism: with clinical applications /M.C. Linder (ed.). Prentice Hall, NY, 1991.
- Onderci M., Sahin K., Sahin N., Cikim G., Vijaya J., Kucuk O. Effects of dietary combination of chromium and biotin on growth performance, carcass characteristics, and oxidative stress markers in heat-distressed Japanese quail. Biol. Trace Elem. Res., 2005, 106(2): 165-176 ( ).
- DOI: 10.1385/BTER:106:2:165
- National Research Council. Nutrient Requirements of Swine. 10th revised edition. National Academy Press, Washington DC, 1998 ( ).
- DOI: 10.17226/6016
- Doisy R.J., Streeten D.H.P., Souma M.L., Kalafer M.E., Rekant S.L., Dalakos T.G. Metabolism of chromium 51 in human subjects (Vol. 155). Marcel Dekker, NY, 1971.
- Оберлис Д., Харланд Б., Скальный А. Биологическая роль макро- и микроэлементов у человека и животных. СПб, 2008.
- Moeini M.M., Bahrami A., Ghazi S., Targhibi M.R. The effect of different levels of organic and inorganic chromium supplementation on production performance, carcass traits and some blood parameters of broiler chicken under heat stress condition. Biol. Trace Elem. Res., 2011, 144(1-3): 715-724 ( ).
- DOI: 10.1007/s12011-011-9116-8
- Ban C., Park S.J., Lim S., Choi S.J., Choi Y.J. Improving flavonoid bioaccessibility using an edible oil-based lipid nanoparticle for oral delivery. J. Agric. Food Chem., 2015, 63(21): 5266-5272 ( ).
- DOI: 10.1021/acs.jafc.5b01495
- Wang M.Q., Xu Z.R. Effect of chromium nanoparticle on growth performance, carcass characteristics, pork quality and tissue chromium in finishing pigs. Asian Australasian Journal of Animal Sciences, 2004, 17: 1118-1122 ( ).
- DOI: 10.5713/ajas.2004.1118
- Wang M.Q., Xu Z.R., Zha L.Y., Lindemann M.D. Effects of chromium nanocomposite supplementation on blood metabolites, endocrine parameters and immune traits in finishing pigs. Animal Feed Science and Technology, 2007, 139(1-2): 69-80 ( ).
- DOI: 10.1016/j.anifeedsci.2006.12.004
- Motozono Y., Hatano K., Sugawara N., Ishibashi T. Effects of dietary chromium picolinate on growth, carcass quality and serum lipids of female broilers. Nihon Chikusan Gakkaiho, 1998, 69(7): 659-665 ( ).
- DOI: 10.2508/chikusan.69.659
- Уголев А.М., Кузьмина В.В. Пищеварительные процессы и адаптации у рыб. М., 1993.
- Уголев А.М. Мембранное пищеварение: полисубстратные процессы, организация и регуляция. М., 1972.
- Методические рекомендации по кормлению сельскохозяйственной птицы /Под ред. В.И. Фисинина. Сергиев Посад, 2009.
- Lie T.F., Yeh H.S., Lu F.Y., Fu C.M. Nanoparticles of chromium picolinate enhance chromium digestibility and absorption. Journal of the Science of Food and Agriculture, 2009, 89(7): 1164-1167 ( ).
- DOI: 10.1002/jsfa.3569
- Sahin K., Sahin N., Onderci M., Gursu F., Cikim G. Optimal dietary concentration of chromium for alleviating the effect of heat stress on growth, carcass qualities, and some serum metabolites of broiler chickens. Biol. Trace Elem. Res., 2002, 89(1): 53-64 ( ).
- DOI: 10.1385/BTER:89:1:53
- Батоев Ц.Ж. Фотометрическое определение активности протеолитических ферментов в поджелудочной железе, соке по уменьшению концентрации казеина. Сборник научных трудов Бурятского СХИ (Улан-Удэ), 1971, 25: 122-126.
- Газиумарова Л.Д., Титов Л.П., Клюйко Н.Л. Бактериологическая диагностика дисбактериоза кишечника: инструкция по применению. Л.-Минск, 2010.
- Sizova E.A., Miroshnikov S.A., Lebedev S.V., Kudasheva A.V., Ryabov N.I. To the development of innovative mineral additives based on alloy of Fe and Co antagonists as an example. Agricultural Biology [Sel'skokhozyaistvennaya biologiya], 2016, 51(4): 553-562 ( ).
- DOI: 10.15389/agrobiology.2016.4.553eng
- Sizova E.A., Miroshnikov S.A., Lebedev S.V., Levakhin Y.I., Babicheva I.A., Kosilov V.I. Comparative tests of various sources of microelements in feeding chicken-broilers. Agricultural Biology [Sel'skokhozyaistvennaya Biologiya], 2018, 53(2): 393-403 ( ).
- DOI: 10.15389/agrobiology.2018.2.393eng
- Егоров И.А., Петросян А., Андрианова Е.Н. Био-ХромТМ в кормлении птицы. Птицеводство, 2011, 12: 3-5.
- Samanta S., Haldar S., Ghosh T.K. Production and carcase traits in broiler chickens given diets supplemented with inorganic trivalent chromium and an organic acid blend. British Poultry Science, 2008, 49(2): 155-163 ( ).
- DOI: 10.1080/00071660801946950
- Sahoo S.K., Labhasetwar V. Nanotech approaches to drug delivery and imaging. Drug Discovery Today, 2003, 8(24): 1112-1120 ( ).
- DOI: 10.1016/S1359-6446(03)02903-9
- Davda J., Labhasetwar V. Characterization of nanoparticle uptake by endothelial cells. International Journal of Pharmaceutics, 2002, 233(1-2): 51-59 ( ).
- DOI: 10.1016/S0378-5173(01)00923-1
- Oberleas D., Harland B.F. Impact of phytic acid on nutrient availability. In: Phytase in animal nutrition and waste management. N.Y., 1996.
- Vincent J.B. The biochemistry of chromium. The Journal of Nutrition, 2000, 130(4): 715-718 ( ).
- DOI: 10.1093/jn/130.4.715
- Clodfelder B.J., Emamaullee J., Hepburn D.D., Chakov N.E., Nettles H.S., Vincent J.B. The trail of chromium (III) in vivo from the blood to the urine: the roles of transferrin and chromodulin. Journal of Biological Inorganic Chemistry, 2001, 6(5-6): 608-617 ( ).
- DOI: 10.1007/s007750100238
- Striffler J.S., Polansky M.M., Anderson R.A. Overproduction of insulin in the chromium-deficient rat. Metabolism, 1999, 48(8): 1063-1068 ( ).
- DOI: 10.1016/S0026-0495(99)90207-X
- Anderson R.A., Kozlovsky A.S. Chromium intake, absorption and excretion of subjects consuming self-selected diets. The American Journal of Clinical Nutrition, 1985, 41(6): 571-577 ( ).
- DOI: 10.1093/ajcn/41.6.1177
- Rothman S., Liebow C., Isenman L.C. Conservation of digestive enzymes. Physiol. Rev., 2002, 82(1): 1-18 ( ).
- DOI: 10.1152/physrev.00022.2001
- Kawabata A., Matsunami M., Sekiguchi F. Gastrointestinal roles for proteinase-activated receptors in health and disease. Br. J. Pharmacol., 2008, 153(Suppl. 1): S230-S240 ( ).
- DOI: 10.1038/sj.bjp.0707491
- Рансбергер К. Теория системной энзимотерапии. Опыт и перспективы системной энзимотерапии. Красноярск, 2003.
- Фисинин В.И., Егоров И.А., Вертипрахов В.Г., Грозина А.А., Ленкова Т.Н., Манукян В.А., Егорова Т.А. Активность пищеварительных ферментов в дуоденальном химусе и плазме крови у исходных линий и гибридов мясных кур при использовании биологически активных добавок в рационе. Сельскохозяйственная биология, 2017, 52(6): 1226-1233 ( ).
- DOI: 10.15389/agrobiology.2017.6.1226rus
- Ершов Д.Ю., Киппер А.И., Боровикова Л.Н., Гаркушина И.С., Матвеева Н.А., Писарев О.А. Равновесие сорбции химотрипсина на наночастицах селена. Сорбционные и хроматографические процессы, 2011, 6(11): 923-925.
- Tahami Z., Hosseini S.M., Bashtani M. Effect of organic acids supplementation on some gastrointestinal tract characteristics and small intestine morphology of broiler chickens. Anim. Prod. Res., 2014, 3(3): 1-9.
- Дзагуров Б.А., Журавлева И.О., Кцоева З.А. Влияние pH среды на активность пищеварительных ферментов химуса двенадцатиперстной кишки цыплят-бройлеров при бентонитовых подкормках. Известия Горского государственного аграрного университета, 2013, 3(50): 131-133.
- Куваева И.Б. Обмен веществ организма и кишечная микрофлора. М., 1976.
- Miller K.P., Wang L., Benicewicz B.C., Decho A.W. Inorganic nanoparticles engineered to attack bacteria. Chem. Soc. Rev., 2015, 44(21): 7787-7807 ( ).
- DOI: 10.1039/c5cs00041f
- Arakha M., Pal S., Samantarrai D., Panigrahi T.K., Mallick B.C., Pramanik K., Jha S. Antimicrobial activity of iron oxide nanoparticle upon modulation of nanoparticle-bacteria interface. Scientific Reports, 2015, 5: 14813 ( ).
- DOI: 10.1038/srep14813
- Feng Z.V., Gunsolus I.L., Qiu T.A., Hurley K.R., Nyberg L.H., Frew H., Torelli M.D. Impacts of gold nanoparticle charge and ligand type on surface binding and toxicity to Gram-negative and Gram-positive bacteria. Chem. Sci., 2015, 6(9): 5186-5196 ( ).
- DOI: 10.1039/c5sc00792e
- Лебедев С.В., Гавриш И.А., Губайдуллина И.З. Морфо-биохимические показатели и активность пищеварительных ферментов у крыс линии Wistar под влиянием различных источников хрома. Сельскохозяйственная биология, 2019, 54(2): 304-315 ( ).
- DOI: 10.15389/agrobiology.2019.2.304rus
- Slepicka P., Kasalkova N.S., Siegel J., Kolska Z., Bacakova L., Svorcik V. Nano-structured and functional-ized surfaces for cytocompatibility improvement and bactericidal action. Biotechnology Advances, 2015, 6(33): 1120-1129 ( ).
- DOI: 10.1016/j.biotechadv.2015.01.001


