Биомеханика артерий шеи и головы: развитие аневризм и отрыв атеросклеротических бляшек при сочетанных патологиях
Автор: Доль А.В.
Журнал: Российский журнал биомеханики @journal-biomech
Статья в выпуске: 3 (105) т.28, 2024 года.
Бесплатный доступ
На сегодняшний день основной причиной смертности в мире остаются заболевания сердечно-сосудистой системы. При этом сочетанная патология артерий шеи и головы, при которой атеросклерозом поражены сонные артерии, а также наблюдается изменение кровотока в позвоночных артериях или в виллизиевом круге (ВК) в силу аплазии соединительной артерии, существенно повышает риск образования аневризм и их последующего разрыва. Оценка степени риска возникновения осложнений при таком типе патологического состояния может позволить врачу своевременно приступить к профилактическим мерам в конкретных клинических случаях. В работе представлены результаты моделирования различных вариантов сочетанных патологий в артериях шеи и головы. Рассматриваемый сегмент включает участки общих сонных, наружных и внутренних сонных артерий (ВСА), а также сосуды виллизиева круга и базилярную артерию. Основной идеей исследования было создание прогнозной модели, позволяющей оценить риски развития аневризм в виллизиевом круге и отрыва атеросклеротических бляшек в сонных артериях. Такая система может быть полезна врачам в рутинной практике при планировании тактики лечения у пациентов с сочетанными патологиями артериального русла. На основе анализа литературы выявлен ряд патологий артериальной системы шеи и головы, наиболее часто встречающихся в различных комбинациях: с точки зрения геометрических особенностей рассматривались стенозы ВСА 30 и 70 % и аплазия (отсутствие) одной из соединительных артерий. Кроме того, учитывается характер кровотока в базилярной артерии, который при синдроме позвоночно-подключичного обкрадывания может менять направление. На основе анализа массовых кровотоков и касательных напряжений выделяли две степени риска образования аневризм. Высокий риск соответствует случаям, для которых обе этих величины статистически значимо отличались от нормы. Средний риск соответствует случаям, для которых статистически значимо от нормы отличалась только одна из величин. Для моделей, содержащих атеросклеротические бляшки, были сведены в таблицы данные о касательных и нормальных напряжениях на поверхностях атеросклеротических бляшек. На основе анализа выборок для каждого случая был определен риск отрыва бляшки с каждой стороны, выявлено 11 сочетаний патологических состояний с повышенным риском.
Артерия, виллизиев круг, сонная артерия, аневризма, атеросклеротическая бляшка, мкэ
Короткий адрес: https://sciup.org/146282986
IDR: 146282986 | УДК: 531/534: | DOI: 10.15593/RZhBiomeh/2024.3.02
Biomechanics of neck and head arteries: the development of aneurysms and the separation of atherosclerotic plaques with combined pathologies
The paper presents the results of modelling various variants of combined pathologies in the cerebral and carotid arteries. The main idea of the study was to create a prognostic model allowing to estimate the risks of aneurysm development in circle of Willis and atherosclerotic plaque detachment in the carotid arteries. Such a system may be useful to physicians in routine practice when planning treatment tactics in patients with combined arterial pathologies. The arterial system of the neck and head: sections of the common carotid artery (CCA), external carotid artery (ECA), internal carotid artery (ICA) and the vessels of the circle of Willis, including the anterior, middle and posterior cerebral arteries, the anterior communicating artery (ACA), the posterior communicating artery (PCA) and the basilar artery (BA). Based on the literature analysis, a number of pathologies of the cerebral and carotid arteries, most frequently occurring in various combinations, were identified: stenoses of the ICA and aplasia (absence) of one of the connecting arteries were considered from the point of view of geometrical features. In addition, the character of blood flow in the basilar artery, which can change its direction in steal-syndrome, was taken into account. Based on the analysis of mass blood flow and wall shear stress, two degrees of risk of aneurysm formation were distinguished. High risk corresponds to cases for which both of these values were statistically significantly different from the norm. Medium risk corresponds to cases for which only one of the values was statistically significantly different from the norm. For models containing atherosclerotic plaques, data on shear and normal stresses on the surfaces of atherosclerotic plaques were tabulated. The risk of plaque detachment on each side was determined for each case by analysing the result sets.
Текст научной статьи Биомеханика артерий шеи и головы: развитие аневризм и отрыв атеросклеротических бляшек при сочетанных патологиях
В соответствии с данными Всемирной организации здравоохранения, основной причиной смертности в мире остаются заболевания сердечно-сосудистой системы [1]. В России наблюдается схожая картина [2]. По данным исследователей из Центрального научно-исследовательского института организации и информатизации здравоохранения, смертность от болезней системы кровообращения составляет 28 % у мужчин и 31 % у женщин [1]. Всего же ежегодно порядка 10–11 % населения в России умирает от инсультов и других цереброваскулярных болезней [2].
Различают ишемический и геморрагический инсульты: первый характеризуется повреждением вещества головного мозга вследствие уменьшения притока крови, а второй – вследствие излияния крови в мозг.
В соответствии с клиническими данными [2] в России до 80–90 % нетравматических субарахноидальных (под паутинной оболочкой мозга) кровоизлияний (САК) происходят из-за разрыва внутричерепных (интракраниальных) аневризм. Разрыв аневризм приводит либо к неврологическим расстройствам различной степени тяжести, связанным с повреждением тканей головного мозга, либо к смерти. Особенно важным является тот факт, что САК выводят из строя население работоспособного возраста (40–60 лет). Смертность при субарахноидальном кровоизлиянии составляет порядка 40–50 % [3; 4].
Наличие у пациента аневризмы сосудов головного мозга часто диагностируется лишь постфактум, то есть непосредственно в случае разрыва или значительного увеличения ее в размерах. Это связано с тем, что заболевание протекает практически бессимптомно, а для выявления аневризмы часто необходимо проводить томографическое обследование с введением контрастного вещества. Данный метод является дорогостоящим, некомфортным для пациента и имеет ряд противопоказаний, в связи с чем врач назначает такое исследование лишь в тех случаях, когда выявить причину неудовлетворительного состояния не удается с использованием прочего диагностического оборудования (УЗИ, рентгенография, компьютерная томография). В связи с этим аневризмы виллизиева круга (ВК) во многих случаях не диагностируются практически до момента разрыва.
В работе исследуется артериальная система шеи и головы: участки общих сонных (ОСА), наружных (НСА) и внутренних сонных (ВСА) артерий, а также сосуды виллизиева круга, включающие передние, средние и задние мозговые артерии, переднюю соединительную (ПСА) и задние соединительные артерии (ЗСА), а также базилярную артерию (БА).
На основе анализа литературы выявлен ряд патологий артериальной системы шеи и головы, наиболее часто встречающихся в различных комбинациях [5–8]:
с точки зрения геометрических особенностей рассматривались стенозы ВСА и аплазия (отсутствие) одной из соединительных артерий.
К наиболее часто встречающимся вариантам разомкнутого ВК могут быть отнесены следующие: с отсутствующей передней, одной из задних или одновременно обеих задних соединительных артерий [7–9]. В данной работе рассматриваются также 3 основных варианта состояния ВСА: норма (без стеноза), стеноз 30 % и стеноз 70 %. Такие пороговые значения стенозов выбраны как наиболее часто встречающиеся в литературе [10–13]. Стеноз 30 % считается гемодинамически незначимым, при этом данное значение признается физиологами пороговым, после которого существенно возрастает риск возникновения осложнений [12]. Стеноз 70 % характеризуется как гемодинамически значимый, при этом также отмечается, что данное значение является пороговым в смысле существенного увеличения риска клинических осложнений и необходимости хирургического вмешательства [11].
Во многих исследовательских работах, посвященных изучению аневризм сосудов головного мозга, отмечается, что одной из причин образования аневризмы служит атеросклероз сонных артерий [14–16]. В результате сужения просвета сонной артерии происходит изменение объемного кровотока на входе в вилли-зиев круг, что влечет за собой перераспределение потоков крови за счет его компенсаторных функций. Именно это, по мнению некоторых исследователей, может служить отправной точкой формирования аневризм. Однако механизм влияния стенозов сонных артерий на процесс возникновения и роста аневризм артерий ВК изучен мало. Не осуществлены биомеханические исследования данного механизма. В литературе есть предположения клиницистов и описаны клинические случаи, показывающие наличие такой связи [5; 6; 17].
Одним из патологических состояний, существенно влияющих на гемодинамику сосудов ВК, является синдром позвоночно-подключичного обкрадывания (СППО) или стил-синдром ( steal -синдром) [18; 19]. Впервые ретроградный кровоток (РК) был описан еще в 1960 г. Л. Конторни [20], а уже через год M. Райвич [21] связал этот феномен с транзиторной ишемической атакой, тем самым указав на связь РК с церебральным кровообращением. Сам термин « steal -синдром» впервые ввел в середине XX в. невролог C.M. Фишер [22]. Суть описанного явления заключается в том, что в силу патологических изменений в подключичной артерии (чаще всего вследствие атеросклеротических отложений [23]) возникает РК в позвоночной артерии со стороны поражения, а также в ряде случаев установившийся РК в базилярной артерии (БА).
Выделяют три стадии выраженности синдрома позвоночно-подключичного обкрадывания [24], причем при третьей, наиболее выраженной стадии, наблюдается установившийся постоянный РК. Пиковые значения скоростей при РК в базилярной артерии, как правило, ниже, чем при антеградном (нормальном), однако крайние значения диапазона ретроградных пиков близки к нормальным значениям для антеградного кровотока (АК) у контрольной группы здоровых пациентов [25].
Как следствие, у пациента при таком типе кровотока может теряться до 20 % кровоснабжения головного мозга [18]. А при развитии в этом случае вертебробазилярной недостаточности, то есть обратимого нарушения функций мозга, вызванного уменьшением кровоснабжения, в 30 % случаев приводит к инсульту в течение 5 лет [26]. При этом отмечается, что инсульты на фоне СППО носят гемодинамический характер, то есть напрямую связаны с существенным изменением кровообращения.
Существуют также работы, показывающие, что, как правило, до 84 % описанных клинических случаев с синдромом позвоночно-подключичного обкрадывания указывают на наличие у таких пациентов стенозов сонных артерий, вызванных атеросклеротическими отложениями [27–29].
Диагностирование атеросклероза и СППО проводится с помощью ряда стандартных медицинских процедур, не требующих больших финансовых и временных затрат. При этом основным методом диагностики является ультразвуковая допплерография, доступная практически в любой современной клинике.
Существует множество работ, посвященных исследованию отрыва атеросклеротических бляшек в сонных артериях и факторов, оказывающих влияние на этот процесс. Здесь и далее под отрывом бляшки будем понимать нарушение целостности фиброзной покрышки, которая отделяет содержимое бляшки от сосудистого русла. Такой надрыв покрышки приводит к выбросу в поток крови содержимого бляшки и дальнейшему образованию тромбов. В целом ряде работ исследователи указывают, что высокие эквивалентные напряжения, а также низкие касательные напряжения на поверхности бляшки являются индикаторами повышенного риска отрыва [30–33]. При этом значение 300 кПа для эквивалентных напряжений рассматривается как пороговое [30; 34], на которое можно ориентироваться при оценке риска. Однако при анализе литературы не встретилось работ, связывающих изменение напряженно-деформированного состояния стенки, пораженной атеросклеротической бляшкой, с наличием сопутствующих патологий сосудов ВК.
Целью исследования является создание прогнозной модели для оценки риска развития аневризм у конкретного пациента с сочетанной патологией артерий шеи и головы, а также риска разрыва фиброзной покрышки атеросклеротической бляшки с дальнейшей эмболизацией. Для реализации цели работы необходимо построить геометрическую модель системы, определить граничные условия, провести серию чис- ленных расчетов различных вариантов патологических состояний и выявить закономерности и связи между атеросклерозом сонных артерий, СППО и образованием аневризм.
Материалы и методы
Рассматриваемая система артерий шеи и головы схематично представлена на рис. 1.
Сочетания патологических состояний артериальной системы с учетом вариантов строения ВК, а также степеней и локализаций поражения ВСА атеросклерозом приведены в табл. 1.
На основе компьютерной томограммы (КТ) с контрастированием в программном пакете SolidWorks была создана геометрическая модель рассматриваемого участка сосудистого русла, после чего на основе литературных данных о толщине артерий [35] строилась модель стенок.
Ранее был рассмотрен ряд вариантов сочетанных патологических состояний в системе артерий шеи и головы [36], что позволило выявить комбинации, существенно повышающие риск образования аневризм. Позже была найдена работа [17] с описанным клиническим случаем сочетанной патологии (стеноз сонной артерии и аневризма задней соединительной артерии), который зеркально повторял один из вариантов сочетания с повышенным риском. Было сделано предположение, что необходимо рассматривать симметричную модель сосудистого русла, так как патологические состояния в силу симметрии системы также могут развиваться с обеих сторон с одинаковой вероятностью. Поэтому построенная пациент-ориентированная модель была рассечена сагиттальной плоскостью, и одна половина зеркально отражена, в результате чего получили симметричную систему сосудов.
В качестве граничных условий на входе в ОСА и БА задавались профили скорости кровотока. Торцы сосудов жестко фиксировались. На границе двух сред (крови и стенки) задавались условия прилипания [37]. На внешней стенке артерии принимается давление, равное нулю.
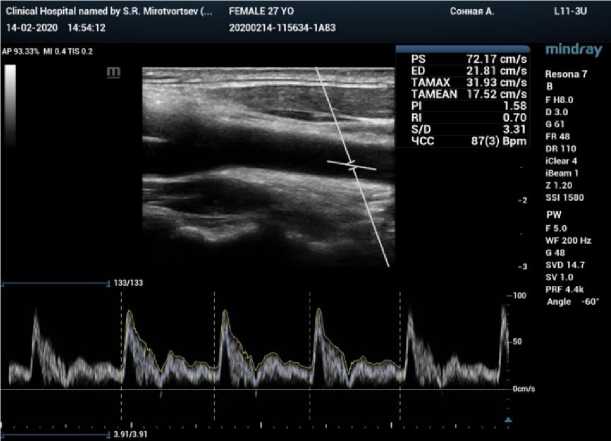
Графики скоростей и давлений на входе в сосуд были получены по данным ультразвукового исследования (УЗИ). В ходе УЗИ здорового пациента (женщина, 27 лет, без патологий сосудистого русла) на срезе сосуда в средней части сечения ставилась метка, и в отмеченной точке аппаратом УЗИ автоматически строился график, который в дальнейшем строился график, который в дальнейшем обрабатывался и задавался в виде входных значений (рис. 2).
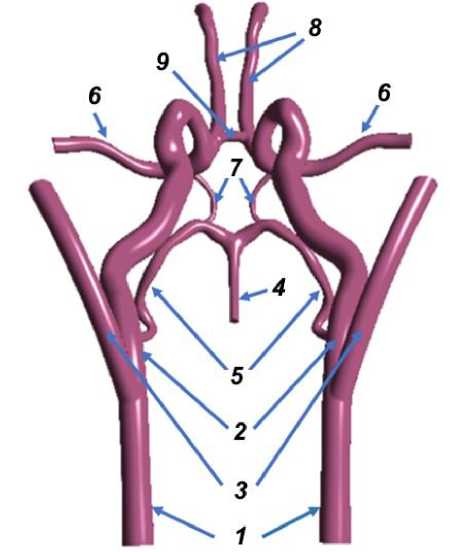
Рис. 1. Рассматриваемый участок артериального русла: 1 – общая сонная артерия; 2 – внутренняя сонная артерия;
3 – наружная сонная артерия; 4 – базилярная артерия;
5 – задняя мозговая артерия; 6 – средняя мозговая артерия; 7 – задняя соединительная артерия; 8 – передняя мозговая артерия; 9 – передняя соединительная артерия
Таблица 1
Модели с различными сочетаниями патологий
|
Варианты строения ВК |
Варианты стенозов ВСА |
|
|
Замкнутый |
Обе артерии в норме («норма») |
|
|
Отсутствует правая ЗСА |
Стеноз правой 30 % |
|
|
Отсутствует левая ЗСА |
Стеноз правой 70 % |
|
|
Отсутствуют обе ЗСА |
Стеноз левой 30 % |
|
|
Отсутствует ПСА |
Стеноз левой 70 % |
|
|
– |
Стеноз правой 30 %, стеноз левой 30 % |
|
|
– |
Стеноз правой 30 %, стеноз левой 70 % |
|
|
– |
Стеноз правой 70 %, стеноз левой 30 % |
|
|
– |
Стеноз правой 70 %, стеноз левой 70 % |
а
Рис. 2. График скорости в общей сонной артерии:
а – данные УЗИ; б – оцифрованный и заданный в качестве граничных условий график скорости
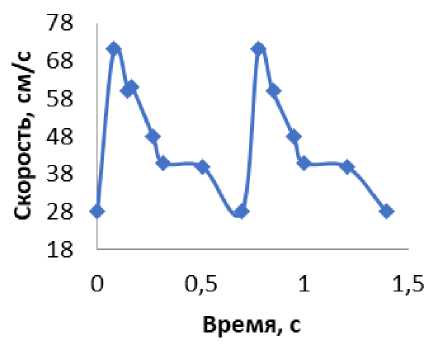
б
По данным современных исследований, у здоровых пациентов без патологических изменений в артериях шеи и головы кровоснабжение головного мозга осуществляется за счет кровотока во внутренних сонных (примерно 2/3 от всего объема) и позвоночных (примерно треть) артериях [38]. Исходя из этих данных, график скорости на входе в ОСА был отмасштабирован таким образом, чтобы входной объемный кровоток в базилярной артерии обеспечивал 1/3 кровоснабжения артерий ВК в норме (с учетом отношения радиусов ОСА и БА был подобран масштабирующий коэффициент, равный 0,77). При этом пиковое значение скорости крови в базилярной артерии в систолу составило 56 см/с, что хорошо согласуется с данными литературы [38; 39].
Свойства живых тканей
|
Ткани |
Плотность, кг/м3 [35; 44; 45] |
Модуль Юнга, МПа [43; 44; 46] |
Коэффициент Пуссона [45] |
|
Виллизиев круг |
1378 |
0,55 |
0,4 |
|
Сонные артерии |
1378 |
0,35 |
0,4 |
|
Бляшки мягкие |
1080 |
0,29 |
0,49 |
|
Бляшки твердые |
1300 |
0,85 |
0,49 |
|
Стенка ОСА (материал Муни – Ривлина) |
C 10 = – 0,193 МПа, C 01 = 0,267 МПа, C 20 = 0,04 МПа, C 11 = – 0,192 МПа, C 02 = 0,331 МПа |
||
В случае наличия у пациента СППО и, как следствие, ретроградного кровотока в БА пиковые значения скоростей крови в базилярной артерии могут быть сравнимы со скоростями при антеградном кровотоке [25; 40], поэтому в случае РК в базилярной артерии было принято решение использовать график скорости, полученный для АК (менялось только направление движения крови на торце).
На выходах из участка сосудистого русла задавались условия типа windkessel [41], моделирующие сопротивление нижележащих по течению участков артериальной системы.
Кровь считалась вязкой несжимаемой ньютоновской жидкостью со свойствами: ρ = 1050 кг/м3, μ = 0,005 Па · с. В работе [42] было показано, что для моделирования крупных сосудов шеи и головы усложнение модели крови не оказывает существенного влияния на результаты.
Моделирование участка сосудистого русла, включающего сонные артерии и виллизиев круг, проводилось в трехмерной постановке, однако в случаях, когда был выявлен повышенный риск разрыва покрышки атеросклеротической бляшки, необходимо было проводить дополнительные расчеты напряженно-деформированного состояния участка сосуда в 2 D . В случае трехмерной постановки для всех участков модели, соответствующих мягким тканям (артерии, бляшки), использовалась модель идеально упругого изотропного материала. В случае расчета в двумерной постановке стенка сонной артерии моделировалась гиперупругим материалом Муни – Ривлина (5-параметрическая модель). Модули Юнга сосудистых стенок и бляшек, а также набор констант для модели Муни – Ривлина были определены ранее и опубликованы в работе [43]. Значения констант, определяющих свойства материалов, приведены в табл. 2.
Построенная геометрическая модель для каждой комбинации патологий импортировалась в программ- ный пакет Ansys, широко применяемый в различных областях биомеханики [47; 48], где численно методами конечных элементов и конечных объемов решалась связанная задача теории упругости и гидродинамики. Основная система уравнений подробно описана в работах [45; 49; 50].
С целью оценки риска образования аневризм анализировались массовые кровотоки в обеих ЗСА и ПСА, а также касательные напряжения ( WSS ) на стенках этих артерий, средние касательные напряжения за период пульсации ( TAWSS ), а также oscillatory shear index ( OSI ) [51–53].
Для оценки риска отрыва бляшек анализировали максимумы эквивалентных напряжений и касательные напряжения на поверхностях покрышек. В случае расчета напряженно-деформированного состояния бляшки в двумерной постановке анализировали поле эквивалентных напряжений.
Результаты расчетов сводились в таблицы (для массовых кровотоков, для касательных и эквивалентных напряжений), после чего выборки, соответствующие отдельным вариантам состояния сонных артерий, попарно сравнивались между собой U -критерием Манна – Уитни [54]. За эталонное состояние системы принималось нормальное строение ВК, а также строение ВК с аплазией одной или нескольких соединительных артерий.
Результаты
Типичное представление полученных данных приведено в табл. 3, 4. В связи с большим объемом табличных результатов все итоговые таблицы не приводятся, ниже будет представлен результат обработки всего объема данных.
Статистически значимо большие (по сравнению с эталонными) значения в таблицах выделены желтым, а меньшие – синим цветом. Зеленым выделены столбцы, соответствующие эталону (норме).
Пример характерных полей распределения TAWSS и OSI приведен на рис. 3.
На основе анализа всех табличных данных о массовых кровотоках и касательных напряжениях были составлены таблицы с оценкой степени риска образования аневризм для каждого рассмотренного случая
Массовые кровотоки (в кг/с · 10-4) через ПСА (антеградный кровоток в БА)
Таблица 3
|
Кровоток |
Норма |
Правая 30 % |
Правая 70 % |
Левая 30 % |
Левая 70 % |
Правая 30 %, левая 30 % |
Правая 30 %, левая 70 % |
Правая 70 %, левая 30 % |
Правая 70 %, левая 70 % |
|
Систола |
|||||||||
|
Замкнутый круг |
0,14 |
0,15 |
2,14 |
0,15 |
2,14 |
0,15 |
2,06 |
2,06 |
0,09 |
|
Без правой ЗСА |
0,21 |
0,43 |
2,74 |
0,05 |
1,96 |
0,25 |
1,68 |
2,42 |
0,47 |
|
Без левой ЗСА |
0,21 |
0,05 |
1,96 |
0,43 |
2,74 |
0,25 |
2,42 |
1,68 |
0,47 |
|
Без обеих ЗСА |
0,12 |
0,13 |
2,36 |
0,13 |
2,36 |
0,13 |
2,22 |
2,22 |
0,12 |
|
Диастола |
|||||||||
|
Замкнутый круг |
0,12 |
0,06 |
1,45 |
0,06 |
1,45 |
0,17 |
1,57 |
1,57 |
0,11 |
|
Без правой ЗСА |
0,30 |
0,41 |
2,00 |
0,17 |
1,19 |
0,32 |
1,08 |
1,85 |
0,43 |
|
Без левой ЗСА |
0,30 |
0,17 |
1,19 |
0,41 |
2,00 |
0,32 |
1,85 |
1,08 |
0,43 |
|
Без обеих ЗСА |
0,06 |
0,03 |
1,54 |
0,03 |
1,54 |
0,08 |
1,62 |
1,62 |
0,08 |
WSS (в Па) на стенке ПСА в систолу
Таблица 4
|
Кровоток |
Норма |
Правая 30 % |
Правая 70 % |
Левая 30 % |
Левая 70 % |
Правая 30 %, левая 30 % |
Правая 30 %, левая 70 % |
Правая 70 %, левая 30 % |
Правая 70 %, левая 70 % |
|
Антеградный |
– |
– |
– |
– |
– |
– |
– |
– |
– |
|
Замкнутый круг |
0,41 |
0,43 |
0,47 |
0,43 |
0,47 |
0,41 |
0,43 |
0,43 |
0,33 |
|
Без правой ЗСА |
0,42 |
0,42 |
0,52 |
0,41 |
0,47 |
0,41 |
0,44 |
0,49 |
0,33 |
|
Без левой ЗСА |
0,42 |
0,41 |
0,47 |
0,42 |
0,52 |
0,41 |
0,49 |
0,44 |
0,33 |
|
Без обеих ЗСА |
0,42 |
0,42 |
0,49 |
0,42 |
0,49 |
0,41 |
0,50 |
0,50 |
0,39 |
|
Ретроградный |
– |
– |
– |
– |
– |
– |
– |
– |
– |
|
Замкнутый круг |
0,35 |
0,26 |
0,41 |
0,26 |
0,41 |
0,34 |
0,41 |
0,41 |
0,24 |
|
Без правой ЗСА |
0,56 |
0,54 |
0,33 |
0,58 |
0,76 |
0,55 |
0,74 |
0,34 |
0,47 |
|
Без левой ЗСА |
0,56 |
0,58 |
0,76 |
0,54 |
0,33 |
0,55 |
0,34 |
0,74 |
0,47 |
|
Без обеих ЗСА |
0,42 |
0,42 |
0,49 |
0,42 |
0,49 |
0,41 |
0,50 |
0,50 |
0,39 |
|
Нулевой |
– |
– |
– |
– |
– |
– |
– |
– |
– |
|
Замкнутый круг |
0,41 |
0,43 |
0,47 |
0,43 |
0,47 |
0,41 |
0,43 |
0,43 |
0,33 |
|
Без правой ЗСА |
0,42 |
0,42 |
0,52 |
0,41 |
0,47 |
0,41 |
0,44 |
0,49 |
0,33 |
|
Без левой ЗСА |
0,42 |
0,41 |
0,47 |
0,42 |
0,52 |
0,41 |
0,49 |
0,44 |
0,33 |
|
Без обеих ЗСА |
0,42 |
0,42 |
0,49 |
0,42 |
0,49 |
0,41 |
0,50 |
0,50 |
0,39 |
сочетанной патологии (табл. 5, 6). Красным выделены ячейки с высоким, а желтым – со средним риском образования аневризм на соответствующем участке.
Для моделей, содержащих атеросклеротические бляшки, были сведены в таблицы данные о касательных и нормальных напряжениях на поверхностях атеросклеротических бляшек.
Нормальность распределения выборок оценивали критерием Колмогорова – Смирнова [55]. Распределение обеих выборок (значений касательных и нормальных напряжений) оказалось отличным от нормального.
На основе анализа выборок для каждого случая был определен риск отрыва бляшки с каждой стороны (табл. 7).
В таблице сокращения АК, РК, ОК соответствуют антеградному, ретроградному и отсутствующему кровотокам.
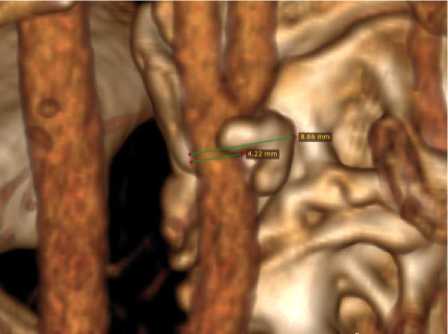
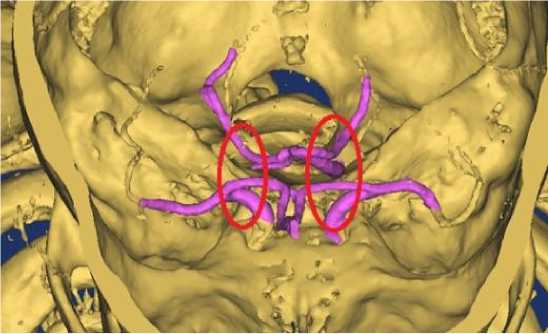
Был рассмотрен частный случай сочетанной патологии, определена степень стеноза в ВСА (50 % с обеих сторон) и подтверждена аплазия обеих ЗСА (рис. 4).
Был проведен расчет напряженно-деформированного состояния артериального русла в трехмерной постановке, определен риск отрыва бляшки, после чего выполнено численное моделирование бляшки в двумерной постановке. Результаты расчета приведены на рис. 5. Максимальное напряжение составило 141 кПа.
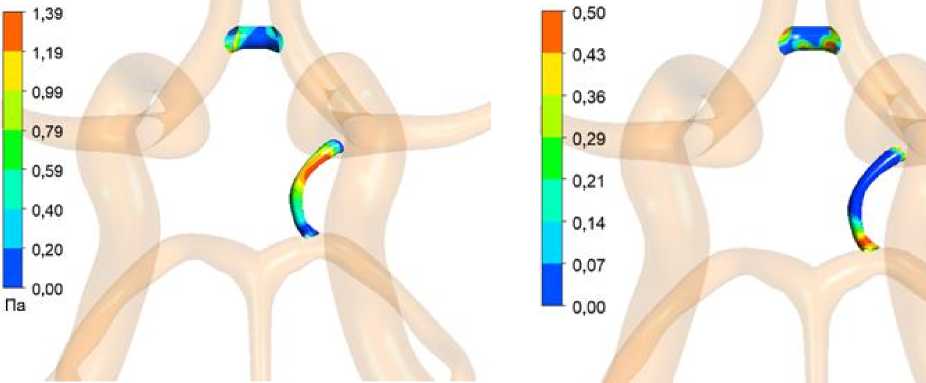
а б
Рис. 3. Поля распределения TAWSS ( а ) и OSI ( б ) на ПСА и правой ЗСА
Таблица 5
Оценка рисков для передней соединительной артерии
|
Кровоток |
Норма |
Правая 30 % |
Правая 70 % |
Левая 30 % |
Левая 70 % |
Правая 30 %, левая 30 % |
Правая 30 %, левая 70 % |
Правая 70 %, левая 30 % |
Правая 70 %, левая 70 % |
|
Антеградный |
– |
– |
– |
– |
– |
– |
– |
– |
– |
|
Замкнутый круг |
|||||||||
|
Без правой ЗСА |
|||||||||
|
Без левой ЗСА |
|||||||||
|
Без обеих ЗСА |
|||||||||
|
Ретроградный |
– |
– |
– |
– |
– |
– |
– |
– |
– |
|
Замкнутый круг |
|||||||||
|
Без правой ЗСА |
|||||||||
|
Без левой ЗСА |
|||||||||
|
Без обеих ЗСА |
|||||||||
|
Нулевой |
– |
– |
– |
– |
– |
– |
– |
– |
– |
|
Замкнутый круг |
|||||||||
|
Без правой ЗСА |
|||||||||
|
Без левой ЗСА |
|||||||||
|
Без обеих ЗСА |
Обсуждение
В работе представлены результаты моделирования различных вариантов сочетанных патологий в артериях шеи и головы. Основной идеей исследования было создание прогнозной модели, позволяющей оценить риски развития аневризм в виллизиевом круге и отрыва атеросклеротических бляшек в сонных артериях. Такая система может быть полезна врачам в рутинной практике при планировании тактики лечения у пациентов с сочетанными патологиями артериального русла. Подобные системы поддержки принятия врачебных решений в сосудистой хирургии уже применяются, к примеру, в ФГБНУ
«Научно-исследовательский институт комплексных проблем сердечно-сосудистых заболеваний» [17], однако в приведенном примере оценка риска исхода и выбор тактики лечения основываются на статистических данных, а не на численном моделировании. Кроме того, описания систем оценки именно риска образования аневризм или отрыва атеросклеротических бляшек при сочетанных патологиях в литературе пока не обнаружено.
Безусловно, в клинической практике у оперирующих хирургов, как правило, не возникает сложностей при оценке рисков в случаях с гемодинамически значимыми стенозами ВСА или уже имеющимися аневризмами соединительных
Оценка рисков для задних соединительных артерий
|
Кровоток |
Норма |
Правая 30 % |
Правая 70 % |
Левая 30 % |
Левая 70 % |
Правая 30 %, левая 30 % |
Правая 30 %, левая 70 % |
Правая 70 %, левая 30 % |
Правая 70 %, левая 70 % |
|
Антеградный |
– |
– |
– |
– |
– |
– |
– |
– |
– |
|
Левая ЗСА |
|||||||||
|
Замкнутый круг |
|||||||||
|
Без правой ЗСА |
|||||||||
|
Без ПСА |
|||||||||
|
Правая ЗСА |
|||||||||
|
Замкнутый круг |
|||||||||
|
Без левой ЗСА |
|||||||||
|
Без ПСА |
|||||||||
|
Ретроградный |
– \ |
– |
– |
– |
– |
– |
– |
– |
– |
|
Левая ЗСА |
|||||||||
|
Замкнутый круг |
|||||||||
|
Без правой ЗСА |
|||||||||
|
Без ПСА |
|||||||||
|
Правая ЗСА |
|||||||||
|
Замкнутый круг |
|||||||||
|
Без левой ЗСА |
|||||||||
|
Без ПСА |
|||||||||
|
Нулевой |
– \ |
– |
– |
– |
– |
– |
– |
– |
– |
|
Левая ЗСА |
|||||||||
|
Замкнутый круг |
|||||||||
|
Без правой ЗСА |
|||||||||
|
Без ПСА |
|||||||||
|
Правая ЗСА |
|||||||||
|
Замкнутый круг |
|||||||||
|
Без левой ЗСА |
|||||||||
|
Без ПСА |
|||||||||
артерий. Кроме того, существуют и внедрены в практику соответствующие клинические рекомендации, где четко прописаны алгоритмы действий врача при различных отдельно взятых патологических состояниях сосудистого русла, но влияние, к примеру, разомкнутого ВК или наличия СППО на исход лечения в них не оценивается [56].
Cами врачи отмечают, что сочетанная патология всегда, даже при наличии гемодинамически незначимых стенозов ВСА или аплазии одной из соединительных артерий, вызывает ряд вопросов по тактике лечения и может повлечь серьезные осложнения даже при изначальном удовлетворительном результате хирургического лечения [13; 17; 27; 29].
Врачами-кардиологами отдельно отмечается, что при стенозах ВСА менее 50 % необходимо дополнительно исследовать атеросклеротические бляшки на возможность отрыва, так как даже гемодинамически незначимые бляшки могут стать причиной эмболиче- ского инсульта [13]. С позиции биомеханики наличие любого сужения в сосудах существенно влияет на гемодинамику рассматриваемого участка артериального русла, поэтому необходимо рассматривать каждый клинический случай отдельно, учитывая все индивидуальные особенности пациента.
Синдром позвоночно-подключичного обкрадывания, очевидно, также значительно влияет на гемодинамику артерий головы, однако до сих пор не проведено комплексного исследования влияния данного патологического состояния на процесс формирования аневризм в виллизиевом круге.
При отсутствии сопутствующих патологий аплазия участков ВК чаще всего никак не проявляется, вследствие чего пациент может даже не знать о такой особенности строения сосудов долгое время до возникновения сопутствующих заболеваний. При этом разомкнутый виллизиев круг встречается по разным данным у 60–70 % населения [57; 58]. Поэтому в
Оценка рисков отрыва бляшек
|
Бляшка в левой ВСА |
Бляшка в правой ВСА |
|
Стеноз левой ВСА 30 %, без правой ЗСА, АК, РК, ОК |
Стеноз правой ВСА 30 %, без левой ЗСА, АК, РК, ОК |
|
Стеноз правой ВСА 30 %, стеноз левой ВСА 30 %, АК |
Стеноз правой ВСА 30 %, стеноз левой ВСА 30 %, АК |
|
Стеноз правой ВСА 70 %, стеноз левой ВСА 30 %, АК |
Стеноз правой ВСА 30 %, стеноз левой ВСА 70 %, АК |
|
Стеноз правой ВСА 30 %, стеноз левой ВСА 30 %, без ПСА, АК |
Стеноз правой ВСА 30%, стеноз левой ВСА 30 %, без ПСА, АК |
|
Стеноз правой ВСА 70 %, стеноз левой ВСА 70 %, без обеих ЗСА, АК, РК, ОК |
Стеноз правой ВСА 70 %, стеноз левой ВСА 70 %, без обеих ЗСА, АК, РК, ОК |
|
Стеноз левой ВСА 30 %, без ПСА, АК |
Стеноз правой ВСА 30 %, без ПСА, АК |
|
Стеноз правой ВСА 30 %, стеноз левой ВСА 70 %, без правой ЗСА, РК |
Стеноз правой ВСА 70 %, стеноз левой ВСА 30 %, без левой ЗСА, РК |
|
Стеноз правой ВСА 70 %, стеноз левой ВСА 30 %, без левой ЗСА, РК |
Стеноз правой ВСА 30 %, стеноз левой ВСА 70 %, без правой ЗСА, РК |
|
Стеноз левой ВСА 70 %, без правой ЗСА, РК |
Стеноз правой ВСА 70 %, без левой ЗСА, РК |
|
Стеноз левой ВСА 70 %, без ПСА, РК |
Стеноз правой ВСА 70 %, без ПСА, РК |
|
Стеноз правой ВСА 30 %, стеноз левой ВСА 30 %, без правой ЗСА, ОК |
Стеноз правой ВСА 30 %, стеноз левой ВСА 30 %, без левой ЗСА, ОК |
а
Рис. 4. Конкретный случай сочетанной патологии: а - данные КТ с параметрами стеноза; б - визуализация сосудов ВК с отсутствующими ЗСА (места аплазии выделены красными эллипсами)
б
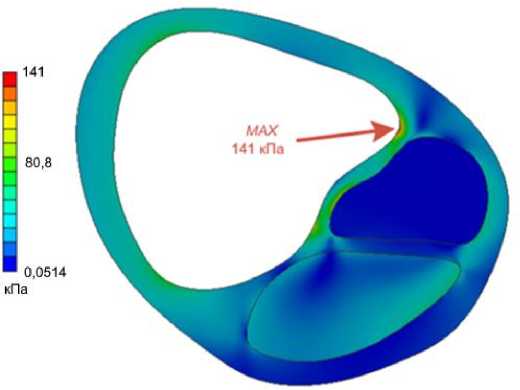
Рис. 5. Диаграмма распределения эквивалентных напряжений в двумерной модели
данной работе за эталонное или нормальное состояние сосудов ВК принимается состояние без стенозов ВСА. Отсутствие одной из соединительных артерий также считается нормой. И уже с результатами моделирования эталона (различных вариантов нормы) могут попарно сравниваться полученные значения для патологически измененных моделей.
Массовые кровотоки, касательные напряжения на стенках артерий, средние касательные напряжения за период пульсации ( TAWSS ), а также oscillatory shear index ( OSI) были выбраны для анализа как наиболее показательные и часто встречающиеся в работах, посвященных исследованию артериального русла и процессам образования и разрыва аневризм [36; 51; 52].
Риск развития аневризм оценили в передней соединительной и задних соединительных артериях, так как именно там чаще всего наблюдается их появление [9; 59].
Анализ максимальных значений TAWSS и OSI на соединительных артериях и поверхностях бляшек не дал показательных результатов, так как не было выявлено статистически значимых отличий по этим величинам. Однако авторы в работах [51; 52] оценивают именно зоны концентрации этих величин, поэтому был проведен качественный анализ полей TAWSS и OSI на стенках и поверхностях бляшек.
В ряде случаев, которые соответствовали, как правило, статистически значимо отличимым от нормы патологическим состояниям, наблюдаются зоны концентрации высоких значений OSI (в литературе повышенными считаются значения около 0,5 [51]) и низких TAWSS (см. рис. 3). Именно в этих участках потенциально могут образовываться аневризмы. К примеру, в работе [60] описана аневризма, локализованная в области примыкания передней соединительной к передней мозговой артерии.
На основе анализа массовых кровотоков и касательных напряжений выделяли две степени риска образования аневризм. Высокий риск (соответствующие ячейки в табл. 5, 6 отмечены красным) соответствует случаям, для которых обе эти величины статистически значимо отличались от нормы. Средний риск (желтые ячейки) соответствует случаям, для которых статистически значимо от нормы отличалась только одна из величин. Следует отметить, что для всех случаев с высоким риском и большинства случаев со средним риском на диаграммах распределения TAWSS и OSI визуализировались области локальных экстремумов на соответствующих участках артерий.
Выявленные случаи сочетанных патологических состояний с высоким риском образования аневризм хорошо согласуются с клиническими данными: найден ряд описанных в литературе случаев, соответствующих табл. 5, 6 [17; 60].
При оценке риска отрыва атеросклеротических бляшек проанализировали поля эквивалентных и касательных напряжений. Выборки всех значений касательных ( WSS ) и эквивалентных напряжений на поверхностях бляшек оказались распределены ненормально, поэтому критическими значениями считали величины, выходящие за границы третьего квартиля. Также выделили ряд значений, выходящих за границы девятого дециля (10 % самых высоких эквивалентных или касательных напряжений).
В связи с тем, что и эквивалентные, и касательные напряжения позволили выявить одинаковый набор сочетанных патологий, существенно отличающихся от общей массы, было принято решение определять сам факт повышенного риска отрыва бляшки, а в соответствующих случаях делать пациент-ориентированный расчет одной или нескольких плоских моделей бляшки с более детальным разбиением ее на составляющие с конкретными свойствами. Свойства компонент бляшки на основе КТ могут быть определены по ре- грессионной зависимости модуля Юнга от чисел Хаунсфилда, полученной ранее [43].
В табл. 7 видно, что часть случаев с повышенным риском отрыва бляшек включает гемодинамически незначимые стенозы, а риск там, по всей видимости, повышается за счет изменения характера движения крови из-за аплазии соединительных артерий в ВК или наличием СППО.
В качестве отработки методики выполнен уточняющий расчет для пациента с двусторонним поражением внутренних сонных артерий (50 % справа, 50 % слева). Пациент наблюдается несколько лет, бляшки сильно кальцинированы, стабильны. Для проверки того, попадает ли данный случай в группу с повышенным риском, были построены модели бляшек, соответствующие степени стеноза данного пациента. Далее был проведен расчет гемодинамики в трехмерной постановке. Максимальные эквивалентные напряжения на бляшках составили порядка 8000 Па, что соответствует десятому децилю в общей выборке и, соответственно, случаю с повышенным риском отрыва. Таким образом, в данном случае требовался уточняющий расчет в 2 D -постановке.
На основе данных КТ по срезу, соответствующему поперечному сечению бляшки примерно посередине ее продольного размера, была построена уточненная двумерная модель просвета сосуда с бляшкой, определены механические характеристики элементов бляшки. Расчет напряженно-деформированного состояния при действии распирающего внутрисосудистого давления, соответствующего нормальному давлению для пациента, определенному по УЗИ, показал максимум эквивалентных напряжений на покрышке в 141 кПа. По данным литературы, к разрыву фиброзной покрышки приводят напряжения в 300 кПа и более [10; 31; 61; 62]. Поэтому, несмотря на повышенный риск отрыва в соответствии с полученной классификацией (табл. 7), риск отрыва исключен посредством уточненного расчета, что и подтверждается клиническими наблюдениями.
Следует отметить, что у данного пациента значения стенозов отличаются от определенных в работе в качестве базовых 30 и 70 %. Очевидно, что у большинства пациентов не будет точного соответствия выбранным в работе базовым значениям стеноза. В связи с этим в качестве продолжения работы выдвинута идея обучения нейронной сети, которая сможет на основе уже имеющихся рассчитанных вариантов определять степень риска образования аневризм и отрыва атеросклеротических бляшек для промежуточных значений стенозов ВСА.
Заключение
Была проведена серия численных экспериментов по моделированию гемодинамики артерий шеи и го- ловы при наличии сочетанных патологий и выявлены закономерности и связи между атеросклерозом сонных артерий, СППО и образованием аневризм. В результате анализа полей касательных и нормальных напряжений, а также массовых кровотоков на отдельных участках сосудистого русла для каждой комбина-
Список литературы ции патологических состояний была определена степень риска образования аневризм в области передней и задних соединительных артерий. Кроме того, были определены комбинации патологических состояний, при которых повышается риск разрыва фиброзной покрышки атеросклеротической бляшки.
-
1. Воробьев, Р.В. Аналитический обзор проблемы здорового старения в странах европейского региона воз и российской федерации / Р.В. Воробьев, А.В. Короткова // Социальные аспекты здоровья населения. – 2016. – № 5.
-
2. Здравоохранение в России: cтат.сб. / С.Ю. Никитина, Т.Л. Харькова, В.Ж. Чумарина, И.Н. Шаповал,
-
3. A prospective study of acute cerebrovascular disease in the community: the Oxfordshire community stroke project 1981–6. 2. Incidence, case fatality rates and overall outcome at 1 year of cerebral infarction, primary intracerebral and subarachnoid haemorrhage / J. Bamford, P. Sandercock, M. Dennis, J. Burn, C. Warlow // J Neurol Neurosurg Psychiatry. – 1990. – Vol. 53, no. 16. – P. 22.
-
4. Incidence of intracerebral and subarachnoid haemorrhage in southern Sweden / O.G. Nilsson, A. Lindgren, N. Ståhl, L. Brandt, H. Säveland // J Neurol Neurosurg Psychiatry. – 2000. – Vol. 69. – P.601–607.
-
5. Li, Y. Spontaneous regression of an intracranial aneurysm after carotid endarterectomy / Y. Li, T.D. Payner, A.A. Cohen-Gadol // Surg Neurol Int. – 2012. – Vol. 3. – P. 66.
-
6. Espinosa, G. Endovascular treatment of carotid stenosis associated with incidental intracranial aneurysm /
G. Espinosa, L. Dzieciuchowicz, L. Grochowicz // Annals of Vascular Surgery. – 2009. – Vol. 23, no. 5. –
-
7. The role of circle of willis anatomy variations in cardioembolic stroke - a patient-specific simulation based study / D. Mukherjee, N. Jani, J. Narvid, S.C. Shadden // Ann. Biomed. Eng. – 2018. – Vol. 46, no. 8. – P. 1128–1145.
-
8. Dzmitry, V. Comparative study of the arterial circle of Willis in individuals with or without cerebrovascular disorders / V. Dzmitry, I. Tokina // MOJ. Anat. Physio. – 2023. – Vol. 10, no. 1. – P. 14–16.
-
9. Anatomical variations in the circle of Willis are associated with increased odds of intracranial aneurysms: The Tromsø study / L.B. Hindenes, T. Ingebrigtsen, J.G. Isaksen, A.K. Håberg, L.-H. Johnsen, M. Herder, E.B. Mathiesen, T.R. Vangberg // Journal of the Neurological Sciences. – 2023. – Vol. 452. – P. 120740
-
10. How critical is fibrous cap thickness to carotid plaque stability? a flow–plaque interaction model / Z.-Y. Li,
S.P.S. Howarth, T. Tang, J.H. Gillard // Stroke. – 2006. – Vol. 37. – P. 1195–1199.
-
11. Walker, J. Ultrasound based measurement of ‘carotid stenosis > 70 %’: an audit of uk practice / J. Walker, A.R. Naylor // Eur. J. Vasc. Endovasc. Surg. – 2006. – Vol. 31. – P. 487–490.
-
12. Carotid stenosis by digital subtraction angiography: reproducibility of the european carotid surgery trial and the north american symptomatic carotid endarterectomy trial measurement methods and visual interpretation / R. Vanninen, H. Manninen, K. Koivisto, H. Tulla, K. Partanen, M. Puranen // Am. J. Neuroradiol. – 1994. – Vol. 15, no. 9. – P. 1635–1641.
13. Российский консенсус по диагностике и лечению пациентов со стенозом сонных артерий /
М.А. Чернявский, О.Б. Иртюга, С.Н. Янишевский,
А.С. Алиева, К.А. Самочерных, К.Б. Абрамов,
Т.В. Вавилова, В.А. Лукьянчиков, Д.И. Курапеев,
А.Г. Ванюркин, Д.В. Чернова, Н.К. Шелуханов,
А.В. Козленок, З.А. Кавтеладзе, М.В. Малеванный,
Р.А. Виноградов, Т.Н. Хафизов, Г.Е. Иванова,
Н.В. Жуковская, А.А. Фокин, И.М. Игнатьев,
А.А. Карпенко, П.В. Игнатенко, Д.А. Астапов,
В.Ю. Семенов, В.А. Порханов, В.В. Крылов,
Д.Ю. Усачев, А.В. Светликов, Б.Г. Алекян,
Р.С. Акчурин, А.М. Чернявский, А.О. Конради,
Е.В. Шляхто // Российский кардиологический журнал. –
2022. – Т. 27, № 11. – С. 76–86.
-
14. Khan, U.A. Risk of intracerebral aneurysm rupture during carotid revascularization / U.A. Khan, J. Shalhoub, A.H. Davies // Journal of Vascular Surgery. – 2012. – Vol. 56, no. 6. – P. 1739–1747.
-
15. Small, unruptured intracranial aneurysms and management of symptomatic carotid artery stenosis. North American symptomatic carotid endarterectomy trial group / L.J. Kappelle, M. Eliasziw, A.J. Fox, H.J. Barnett // Neurology. – 2000. – Vol. 55. – P. 307–309.
-
16. Extracranial severe carotid stenosis and incidental
intracranial aneurysms / E. Ballotta, G. Da Giau, R. Manara, C. Baracchini // Annals of Vascular Surgery. – 2006. – Vol. 20. – P. 5–8.
-
17. Клинический случай лечения сочетанной патологии: разрыв аневризмы средней мозговой артерии на фоне стеноза внутренней сонной и коронарных артерий / А.Н. Казанцев, Р.С. Тарасов, К.П. Черных, Р.Ю. Лидер, Н.Э. Заркуа, Г.Ш. Багдавадзе, Ю.П. Линец // Патология кровообращения и кардиохирургия. – 2020. – Т. 24, № 2. – С. 109–118.
-
18. Заваруев, А.В. Синдром позвоночно-подключичного обкрадывания / А.В. Заваруев // Журнал неврологии и психиатрии. – 2017. – Т. 1. – С. 72–77.
-
19. Potter, B.J. Subclavian steal syndrome / B.J. Potter,
D.S. Pinto, // Circulation. – 2014. – Vol. 129. –
P. 2320–2323.
-
20. Contorni, L. Il Circolo collaterals vertebro-vertebral nella obliterazionedell’arteria subclavian all sua origine /
L. Contorni // Minerva Chira. – 1960. – Vol. 15. – P. 268–271.
-
21. Reversal of blood flow through the vertebral artery and its effect on cerebral circulation / M. Reivich, H.E. Holling, B. Roberts, J.F. Toole // The New England Journal of Medicine. – 1961. – Vol. 265. – P. 878–885.
-
22. Fisher, C.M. New vascular syndrome, “subclavian steal” / C.M. Fisher // N Engl J Med. – 1961. – Vol. 265.
– P. 912–913.
-
23. Todua, F. Subclavian Steal Effect / F. Todua, D. Gachechiladze // Noninvasive Radiologic Diagnosis of Extracranial Vascular Pathologies. – 2018. – Springer,
-
24. A review of subclavian steal syndrome with clinicalcorrelation / S. Osiro, A. Zurada, J. Gielecki, M.M. Shoja, R.S. Tubbs, M. Loukas // Med Sci Monit. – 2012. – Vol. 18, no. 5. – P. 57–63.
-
25. Transcranial Doppler ultrasonography of the basilar artery in patients with retrograde vertebral artery flow / C. Harper, P.A. Cardullo, A.K. Weyman, R.B. Patterson // Journal of Vascular Surgery. – 2008. – Vol. 48, no. 4. – P. 859–864.
-
26. Flossmann, E. Prognosis of vertebrobasilar transient ischaemic attack and minor stroke / E. Flossmann // Brain. – 2003. – Vol. 126, no. 9. – P. 1940–1954.
-
27. Отдаленные результаты хирургического лечения больных с окклюзией I сегмента подключичных артерий / П.О. Казанчян, В.А. Попов, Ю.А. Стеняев, Ю.В. Дебелый, Т.В. Рудакова, Е.А. Валиков, Р.Н. Ларьков, А.В. Дерзанов // Ангиология и сосудистая хирургия. – 2002. – Т. 8, № 4. – С. 94–101.
-
28. Эндартерэктомия при атеросклеротическом стенозе внутренней сонной артерии / Д.К. Лунев, А.В. Покровскийĭ, Д.Н. Джибладзе, Т.И. Глазунова, В.Л. Буяновский // Журнал невропатологии и психиатрии им. С.С. Корсакова. – 1991. – Т. 91, № 7. – С. 66–68.
-
29. Серажитдинов, А.Ш. Особенности хирургической тактики при одномоментной реконструкции сонной и подключичной артерий / А.Ш. Серажитдинов, В.В. Владимирский, В.И. Лифенцов // Ангиология и сосудистая хирургия. – 2010. Т. 16, № 3. – С. 113–116.
-
30. Finet, G. Biomechanical interaction between cap thickness, lipid core composition and blood pressure in vulnerable coronary plaque: impact on stability or instability / G. Finet, J. Ohayon, G. Rioufol // Coron Artery Dis. – 2004. – Vol. 15, no. 1. – P. 13–20.
-
31. Prediction of atherosclerotic plaque life – Perceptions from fatigue analysis / P. Paritala, T. Yarlagadda, J. Wang, Y. Gu, Z. Li // Procedia Manufacturing. – 2019. – Vol. 30. – P. 522–529.
-
32. A three dimensional finite element analysis of stress distribution in a coronary atherosclerotic plaque: in vivo prediction of plaque rupture location / J. Ohayon, G. Finet, F. Treyve, G. Rioufol, O. Dubreuil // Biomech Appl Comput Assist Surg. – 2005. – Vol. 37. – P. 225–241.
-
33. On the sensitivity of wall stresses in diseased arteries to variable material properties / S.D. Williamson, Y. Lam, H.F. Younis, H. Huang, S. Patel, M.R. Kaazempur-Mofrad, R.D. Kamm // J Biomech Eng. – 2003. – Vol. 125, no. 1. – P. 147–155.
-
34. Distribution of circumferential stress in ruptured and stable atherosclerotic lesions. A structure analysis with histopathological correlation / G.C. Cheng, H.M. Loree, R.D. Kamm, M.C. Fishbein, R.T. Lee // Circulation. – 1993. – Vol. 87, no. 4. – P. 1179–1187.
-
35. Modeling of human circle of Willis with and without aneurisms / D. V. Ivanov, A.V. Dol, O. Pavlova,
A.V. Aristambekova // Acta Bioeng. Biomech. – 2014. – Vol. 16, no 2. – P. 121–129.
-
36. Численное исследование влияния стеноза внутренних сонных артерий на гемодинамику артерий виллизиевого круга / А.В. Доль, Д.В. Иванов, А.С. Бахметьев, С.И. Киреев, Д.Н. Майстренко, А.А. Гудзь // Российский журнал биомеханики. – 2021. – Т. 25, № 4. – С. 356–368.
-
37. Non-Newtonian biomagnetic fluid flow through a stenosed bifurcated artery with a slip boundary condition / Y. Xu, J. Zhu, L. Zheng, X. Si // Appl. Math. Mech.-Engl. Ed. – 2020. – Vol. 41. – P. 1611–1630.
-
38. Королева, М.В. Показатели кровотока в магистральных артериях головы у женщин различных фитнес-групп / М.В. Королева, В.В. Королева, Г.А. Шорин // Человек. Спорт. Медицина. – 2008. – №19 (199). – С. 109–113.
-
39. Aaslid, R. Noninvasive transcranial Doppler ultrasound recording of flow velocity in basal cerebral arteries / R. Aaslid, T.-M. Markwalder, H. Nornes // Journal of Neurosurgery Page Range. – 1982. – Vol. 57, no. 6. – P. 769–774.
-
40. Tan, T.Y. Hemodynamic effects of subclavian steal phenomenon on contralateral vertebral artery / T.Y. Tan, U. Schminke, T.Y. Chen // J Clin Ultrasound. – 2006. – Vol. 34. – P. 77–81.
-
41. Westerhof, N. The arterial Windkessel / N. Westerhof, J.W. Lankhaar, B.E. Westerhof // Med Biol Eng Comput. – 2009. – Vol. 47, no. 2. – P. 131–141.
-
42. Razavi, S.E. Numerical simulation of the blood flow behavior in the circle of Willis / S.E. Razavi, R. Sahebjam // BioImpacts. – 2014. – Vol. 4, no. 2. – P. 89–94.
-
43. Доль, А.В. Механические свойства атеросклеротических бляшек, покрышек и стенок: испытания на мобильном стенде / А.В. Доль // Российский журнал биомеханики. – 2023. – Т. 27, № 3. – С. 81–88.
-
44. Иванов, Д.В. Определение механических свойств артерий виллизиевого многоугольника / Д.В. Иванов, О.А. Фомкина // Российский журнал биомеханики. – 2008. – Т. 12, № 4. – С. 75–83.
-
45. Экспериментальное и численное моделирование структуры потока в модели дистального анастомоза бедренной артерии / В.М. Молочников, Г.Г. Хубулава, Е.И. Калинин, Н.Д. Пашкова, И.В. Никифоров // Российский журнал биомеханики. – 2023. – Т. 27, № 3. – С. 36–52.
-
46. Трехмерный конечно-элементный анализ влияния
-
47. Иванов, Д.В. Биомеханические основы прогнозирования протекания каротидного атеросклероза / Д.В. Иванов, А.В. Доль, Ю.И. Кузык // Российский журнал биомеханики. – 2017. – Т. 21, № 1. – С. 29–40.
-
48. Экспериментальное и численное моделирование структуры потока в модели дистального анастомоза бедренной артерии / В.М. Молочников, Г.Г. Хубулава, Е.И. Калинин, Н.Д. Пашкова, И.В. Никифоров // Российский журнал биомеханики. – 2023. – Т. 27, № 3. – С. 36–52.
-
49. Трехмерный конечно-элементный анализ влияния
-
50. Доль, А.В. Математические модели движения крови в системе сосудов с упругими стенками / А.В. Доль, Ю.П. Гуляев, Д.В. Иванов // Успехи современного естествознания. – 2014. – № 9. – С. 79–84.
-
51. Численное моделирование течения жидкости в венозном клапане при пробе Вальсальвы / Я.А. Гатаулин, Е.Д. Никитин, А.Д. Юхнев, Д.А. Росуховский // Российский журнал биомеханики. – 2022. – № 3. – С. 78–86.
-
52. Abdominal aortic hemodynamics in young healthy adults at rest and during lower limb exercise: quantification using image-based computer modeling / B.T. Tang, C.P. Cheng, M.T. Draney, N.M. Wilson, P.S. Tsao, R.J. Herfkens, C.A. Taylor // Am. J. Physiol. Heart Circ. Physiol. – 2006. – Vol. 291. – P. H668–H676.
-
53. Alterations in wall shear stress predict sites of neointimal hyperplasia after stent implantation in rabbit iliac arteries / J.F. LaDisa Jr., L.E. Olson, R.C. Molthen, D.A. Hettrick, P.F. Pratt, M.D. Hardel, J.R. Kersten, D.C. Warltier, P.S. Pagel // Am. J. Physiol. Heart Circ. Physiol. – 2005. – Vol. 288. – P. H2465–H2475.
-
54. Исследование структуры кровотока в
персонифицированных моделях ответвления шунта от бедренной артерии / А.Д. Юхнев, А.А. Маринова, Е.М. Смирнов, Я.А. Гатаулин, Л.Г. Тихомолова, А.А. Врабий, А.А. Супрунович // Российский журнал биомеханики. – 2023. – Т. 27, № 4. – С. 25–39.
-
55. Nachar, N. The Mann-Whitney U: A test for assessing whether two independent samples come from the same
distribution / N. Nachar // Tutorials in Quantitative Methods for Psychology. – 2008. – Vol. 4. – P. 1–13.
-
56. Hanusz, Z. Normalization of the Kolmogorov–Smirnov and Shapiro–Wilk tests of normality / Z. Hanusz, J. Tarasińska // Biometrical Letters. – 2015. – Vol. 52.
-
57. Численное моделирование полного протеза коленного сустава с силиконовой прослойкой / А. Мааче, М. Амаджи, Х. Амеддах, Х. Мазуз // Российский журнал биомеханики. – 2024. – Т. 28, № 1. – С. 77–87.
-
58. The association of the circle of Willis anomaly and risk of stroke in patients with carotid artery disease / E.Ö. Göksu, P. Koç, E. Küçükseymen, A. Ünal, F. Genç, E.S. Gencer, A. Yaman // Arq Neuropsiquiatr. – 2017. – Vol. 75, no. 7. – P. 429–432.
-
59. Circle of Willis anomalies in stroke patients related with symptomatic carotid artery disease / S. Kamışlı, Ö. Kamışlı, U. Teker, Y. Kablan, K. Saraç, C. Özcan // Turkish J Cerebrovasc Dis. – 2012. – Vol. 18, no. 1. – P. 6–9.
-
60. Lazzaro, M.A. The role of circle of Willis anomalies in cerebral aneurysm rupture / M.A. Lazzaro, B. Ouyang, M. Chen // Journal of NeuroInterventional Surgery. – 2012. – Vol. 4. – P. 22–26.
-
61. Simultaneous internal carotid artery stenosis and ipsilateral anterior communicating artery saccular aneurysm treatment: a case report / A.V. Korotkikh, D.A. Nekrasov, A.A. Khilchuk, S.G. Scherbak, A.M. Sarana // Radiology Case Reports. – 2020. – Vol. 15, no. 7. – P. 1083–1086.
-
62. Distribution of circumferential stress in ruptured and stable atherosclerotic lesions. A structural analysis with histopathological correlation / G.C. Cheng, H.M. Loree, R.D. Kamm, M.C. Fishbein, R.T. Lee // Circulation. – 1993. – Vol. 87. – P. 1179–1187.
-
63. The impact of calcification on the biomechanical stability of atherosclerotic plaques / H. Huang, R. Virmani, H. Younis, A.P. Burke, R.D. Kamm, R.T. Lee // Circulation. – 2001. Vol. 103. – P. 1051–1056.
Л.И. Агеева, Г.А. Александрова, Н.М. Зайченко,
Г.Н. Кириллова, С.А. Леонов, Е.В. Огрызко, И.А. Титова, Пак Ден Нам; Стат.сб. / Росстат. – М., 2019. – С. 170.
P. 688.e1–688.e5.
Cham. – P. 195–200.
утраты дентального имплантата на распределение напряжения в имплантационном протезе нижней челюсти / Р.А. Розов, К.У. Хигучи, Дж. Брунски, В.Н. Трезубов, А.А. Смердов, М.Л. Мишнев // Российский журнал биомеханики. – 2023. – Т. 27, № 3. – С. 24–35.
утраты дентального имплантата на распределение напряжения в имплантационном протезе нижней челюсти / Р.А. Розов, К.У. Хигучи, Дж. Брунски, В.Н. Трезубов, А.А. Смердов, М.Л. Мишнев // Российский журнал биомеханики. – 2023. – Т. 27, № 3. – С. 24–35.
Финансирование. Работа выполнена при финансовой поддержке Благотворительного фонда В. Потанина (проект № ГСАД-0013/23 от 23.01.2023).
Список литературы Биомеханика артерий шеи и головы: развитие аневризм и отрыв атеросклеротических бляшек при сочетанных патологиях
- Воробьев, Р.В. Аналитический обзор проблемы здорового старения в странах европейского региона воз и российской федерации / Р.В. Воробьев, А.В. Короткова // Социальные аспекты здоровья населения. – 2016. – № 5.
- Здравоохранение в России: cтат.сб. / С.Ю. Никитина, Т.Л. Харькова, В.Ж. Чумарина, И.Н. Шаповал, Л.И. Агеева, Г.А. Александрова, Н.М. Зайченко, Г.Н. Кириллова, С.А. Леонов, Е.В. Огрызко, И.А. Титова, Пак Ден Нам; Стат.сб. / Росстат. – М., 2019. – С. 170.
- A prospective study of acute cerebrovascular disease in the community: the Oxfordshire community stroke project 1981–6. 2. Incidence, case fatality rates and overall outcome at 1 year of cerebral infarction, primary intracerebral and subarachnoid haemorrhage / J. Bamford, P. Sandercock, M. Dennis, J. Burn, C. Warlow // J Neurol Neurosurg Psychiatry. – 1990. – Vol. 53, no. 16. – P. 22.
- Incidence of intracerebral and subarachnoid haemorrhage in southern Sweden / O.G. Nilsson, A. Lindgren, N. Ståhl, L. Brandt, H. Säveland // J Neurol Neurosurg Psychiatry. – 2000. – Vol. 69. – P.601–607.
- Li, Y. Spontaneous regression of an intracranial aneurysm after carotid endarterectomy / Y. Li, T.D. Payner, A.A. Cohen-Gadol // Surg Neurol Int. – 2012. – Vol. 3. – P. 66.
- Espinosa, G. Endovascular treatment of carotid stenosis associated with incidental intracranial aneurysm / G. Espinosa, L. Dzieciuchowicz, L. Grochowicz // Annals of Vascular Surgery. – 2009. – Vol. 23, no. 5. – P. 688.e1–688.e5.
- The role of circle of willis anatomy variations in cardio-embolic stroke - a patient-specific simulation based study / D. Mukherjee, N. Jani, J. Narvid, S.C. Shadden // Ann. Biomed. Eng. – 2018. – Vol. 46, no. 8. – P. 1128–1145.
- Dzmitry, V. Comparative study of the arterial circle of Willis in individuals with or without cerebrovascular disorders / V. Dzmitry, I. Tokina // MOJ. Anat. Physio. – 2023. – Vol. 10, no. 1. – P. 14–16.
- Anatomical variations in the circle of Willis are associated with increased odds of intracranial aneurysms: The Tromsø study / L.B. Hindenes, T. Ingebrigtsen, J.G. Isaksen, A.K. Håberg, L.-H. Johnsen, M. Herder, E.B. Mathiesen, T.R. Vangberg // Journal of the Neurological Sciences. – 2023. – Vol. 452. – P. 120740
- How critical is fibrous cap thickness to carotid plaque stability? a flow–plaque interaction model / Z.-Y. Li, S.P.S. Howarth, T. Tang, J.H. Gillard // Stroke. – 2006. – Vol. 37. – P. 1195–1199.
- Walker, J. Ultrasound based measurement of ‘carotid stenosis > 70 %’: an audit of uk practice / J. Walker, A.R. Naylor // Eur. J. Vasc. Endovasc. Surg. – 2006. – Vol. 31. – P. 487–490.
- Carotid stenosis by digital subtraction angiography: reproducibility of the european carotid surgery trial and the north american symptomatic carotid endarterectomy trial measurement methods and visual interpretation / R. Vanninen, H. Manninen, K. Koivisto, H. Tulla, K. Partanen, M. Puranen // Am. J. Neuroradiol. – 1994. – Vol. 15, no. 9. – P. 1635–1641.
- Российский консенсус по диагностике и лечению пациентов со стенозом сонных артерий / М.А. Чернявский, О.Б. Иртюга, С.Н. Янишевский, А.С. Алиева, К.А. Самочерных, К.Б. Абрамов, Т.В. Вавилова, В.А. Лукьянчиков, Д.И. Курапеев, А.Г. Ванюркин, Д.В. Чернова, Н.К. Шелуханов, А.В. Козленок, З.А. Кавтеладзе, М.В. Малеванный, Р.А. Виноградов, Т.Н. Хафизов, Г.Е. Иванова, Н.В. Жуковская, А.А. Фокин, И.М. Игнатьев, А.А. Карпенко, П.В. Игнатенко, Д.А. Астапов, В.Ю. Семенов, В.А. Порханов, В.В. Крылов, Д.Ю. Усачев, А.В. Светликов, Б.Г. Алекян, Р.С. Акчурин, А.М. Чернявский, А.О. Конради, Е.В. Шляхто // Российский кардиологический журнал. – 2022. – Т. 27, № 11. – С. 76–86.
- Khan, U.A. Risk of intracerebral aneurysm rupture during carotid revascularization / U.A. Khan, J. Shalhoub, A.H. Davies // Journal of Vascular Surgery. – 2012. – Vol. 56, no. 6. – P. 1739–1747.
- Small, unruptured intracranial aneurysms and management of symptomatic carotid artery stenosis. North American symptomatic carotid endarterectomy trial group / L.J. Kappelle, M. Eliasziw, A.J. Fox, H.J. Barnett // Neurology. – 2000. – Vol. 55. – P. 307–309.
- Extracranial severe carotid stenosis and incidental intracranial aneurysms / E. Ballotta, G. Da Giau, R. Manara, C. Baracchini // Annals of Vascular Surgery. – 2006. – Vol. 20. – P. 5–8.
- Клинический случай лечения сочетанной патологии: разрыв аневризмы средней мозговой артерии на фоне стеноза внутренней сонной и коронарных артерий / А.Н. Казанцев, Р.С. Тарасов, К.П. Черных, Р.Ю. Лидер, Н.Э. Заркуа, Г.Ш. Багдавадзе, Ю.П. Линец // Патология кровообращения и кардиохирургия. – 2020. – Т. 24, № 2. – С. 109–118.
- Заваруев, А.В. Синдром позвоночно-подключичного обкрадывания / А.В. Заваруев // Журнал неврологии и психиатрии. – 2017. – Т. 1. – С. 72–77.
- Potter, B.J. Subclavian steal syndrome / B.J. Potter, D.S. Pinto, // Circulation. – 2014. – Vol. 129. – P. 2320–2323.
- Contorni, L. Il Circolo collaterals vertebro-vertebral nella obliterazionedell’arteria subclavian all sua origine / L. Contorni // Minerva Chira. – 1960. – Vol. 15. – P. 268–271.
- Reversal of blood flow through the vertebral artery and its effect on cerebral circulation / M. Reivich, H.E. Holling, B. Roberts, J.F. Toole // The New England Journal of Medicine. – 1961. – Vol. 265. – P. 878–885.
- Fisher, C.M. New vascular syndrome, “subclavian steal” / C.M. Fisher // N Engl J Med. – 1961. – Vol. 265. – P. 912–913.
- Todua, F. Subclavian Steal Effect / F. Todua, D. Gachechiladze // Noninvasive Radiologic Diagnosis of Extracranial Vascular Pathologies. – 2018. – Springer, Cham. – P. 195–200.
- A review of subclavian steal syndrome with clinicalcorrelation / S. Osiro, A. Zurada, J. Gielecki, M.M. Shoja, R.S. Tubbs, M. Loukas // Med Sci Monit. – 2012. – Vol. 18, no. 5. – P. 57–63.
- Transcranial Doppler ultrasonography of the basilar artery in patients with retrograde vertebral artery flow / C. Harper, P.A. Cardullo, A.K. Weyman, R.B. Patterson // Journal of Vascular Surgery. – 2008. – Vol. 48, no. 4. – P. 859–864.
- Flossmann, E. Prognosis of vertebrobasilar transient ischaemic attack and minor stroke / E. Flossmann // Brain. – 2003. – Vol. 126, no. 9. – P. 1940–1954.
- Отдаленные результаты хирургического лечения больных с окклюзией I сегмента подключичных артерий / П.О. Казанчян, В.А. Попов, Ю.А. Стеняев, Ю.В. Дебелый, Т.В. Рудакова, Е.А. Валиков, Р.Н. Ларьков, А.В. Дерзанов // Ангиология и сосудистая хирургия. – 2002. – Т. 8, № 4. – С. 94–101.
- Эндартерэктомия при атеросклеротическом стенозе внутренней сонной артерии / Д.К. Лунев, А.В. Покровскийĭ, Д.Н. Джибладзе, Т.И. Глазунова, В.Л. Буяновский // Журнал невропатологии и психиатрии им. С.С. Корсакова. – 1991. – Т. 91, № 7. – С. 66–68.
- Серажитдинов, А.Ш. Особенности хирургической тактики при одномоментной реконструкции сонной и подключичной артерий / А.Ш. Серажитдинов, В.В. Владимирский, В.И. Лифенцов // Ангиология и сосудистая хирургия. – 2010. Т. 16, № 3. – С. 113–116.
- Finet, G. Biomechanical interaction between cap thickness, lipid core composition and blood pressure in vulnerable coronary plaque: impact on stability or instability / G. Finet, J. Ohayon, G. Rioufol // Coron Artery Dis. – 2004. – Vol. 15, no. 1. – P. 13–20.
- Prediction of atherosclerotic plaque life – Perceptions from fatigue analysis / P. Paritala, T. Yarlagadda, J. Wang, Y. Gu, Z. Li // Procedia Manufacturing. – 2019. – Vol. 30. – P. 522–529.
- A three dimensional finite element analysis of stress distribution in a coronary atherosclerotic plaque: in vivo prediction of plaque rupture location / J. Ohayon, G. Finet, F. Treyve, G. Rioufol, O. Dubreuil // Biomech Appl Comput Assist Surg. – 2005. – Vol. 37. – P. 225–241.
- On the sensitivity of wall stresses in diseased arteries to variable material properties / S.D. Williamson, Y. Lam, H.F. Younis, H. Huang, S. Patel, M.R. Kaazempur-Mofrad, R.D. Kamm // J Biomech Eng. – 2003. – Vol. 125, no. 1. – P. 147–155.
- Distribution of circumferential stress in ruptured and stable atherosclerotic lesions. A structure analysis with histopathological correlation / G.C. Cheng, H.M. Loree, R.D. Kamm, M.C. Fishbein, R.T. Lee // Circulation. – 1993. – Vol. 87, no. 4. – P. 1179–1187.
- Modeling of human circle of Willis with and without aneurisms / D. V. Ivanov, A.V. Dol, O. Pavlova, A.V. Aristambekova // Acta Bioeng. Biomech. – 2014. – Vol. 16, no 2. – P. 121–129.
- Численное исследование влияния стеноза внутренних сонных артерий на гемодинамику артерий виллизиевого круга / А.В. Доль, Д.В. Иванов, А.С. Бахметьев, С.И. Киреев, Д.Н. Майстренко, А.А. Гудзь // Российский журнал биомеханики. – 2021. – Т. 25, № 4. – С. 356–368.
- Non-Newtonian biomagnetic fluid flow through a stenosed bifurcated artery with a slip boundary condition / Y. Xu, J. Zhu, L. Zheng, X. Si // Appl. Math. Mech.-Engl. Ed. – 2020. – Vol. 41. – P. 1611–1630.
- Королева, М.В. Показатели кровотока в магистральных артериях головы у женщин различных фитнес-групп / М.В. Королева, В.В. Королева, Г.А. Шорин // Человек. Спорт. Медицина. – 2008. – №19 (199). – С. 109–113.
- Aaslid, R. Noninvasive transcranial Doppler ultrasound recording of flow velocity in basal cerebral arteries / R. Aaslid, T.-M. Markwalder, H. Nornes // Journal of Neurosurgery Page Range. – 1982. – Vol. 57, no. 6. – P. 769–774.
- Tan, T.Y. Hemodynamic effects of subclavian steal phenomenon on contralateral vertebral artery / T.Y. Tan, U. Schminke, T.Y. Chen // J Clin Ultrasound. – 2006. – Vol. 34. – P. 77–81.
- Westerhof, N. The arterial Windkessel / N. Westerhof, J.W. Lankhaar, B.E. Westerhof // Med Biol Eng Comput. – 2009. – Vol. 47, no. 2. – P. 131–141.
- Razavi, S.E. Numerical simulation of the blood flow behavior in the circle of Willis / S.E. Razavi, R. Sahebjam // BioImpacts. – 2014. – Vol. 4, no. 2. – P. 89–94.
- Доль, А.В. Механические свойства атеросклеротических бляшек, покрышек и стенок: испытания на мобильном стенде / А.В. Доль // Российский журнал биомеханики. – 2023. – Т. 27, № 3. – С. 81–88.
- Иванов, Д.В. Определение механических свойств артерий виллизиевого многоугольника / Д.В. Иванов, О.А. Фомкина // Российский журнал биомеханики. – 2008. – Т. 12, № 4. – С. 75–83.
- Экспериментальное и численное моделирование структуры потока в модели дистального анастомоза бедренной артерии / В.М. Молочников, Г.Г. Хубулава, Е.И. Калинин, Н.Д. Пашкова, И.В. Никифоров // Российский журнал биомеханики. – 2023. – Т. 27, № 3. – С. 36–52.
- Трехмерный конечно-элементный анализ влияния утраты дентального имплантата на распределение напряжения в имплантационном протезе нижней челюсти / Р.А. Розов, К.У. Хигучи, Дж. Брунски, В.Н. Трезубов, А.А. Смердов, М.Л. Мишнев // Российский журнал биомеханики. – 2023. – Т. 27, № 3. – С. 24–35.
- Иванов, Д.В. Биомеханические основы прогнозирования протекания каротидного атеросклероза / Д.В. Иванов, А.В. Доль, Ю.И. Кузык // Российский журнал биомеханики. – 2017. – Т. 21, № 1. – С. 29–40.
- Экспериментальное и численное моделирование структуры потока в модели дистального анастомоза бедренной артерии / В.М. Молочников, Г.Г. Хубулава, Е.И. Калинин, Н.Д. Пашкова, И.В. Никифоров // Российский журнал биомеханики. – 2023. – Т. 27, № 3. – С. 36–52.
- Трехмерный конечно-элементный анализ влияния утраты дентального имплантата на распределение напряжения в имплантационном протезе нижней челюсти / Р.А. Розов, К.У. Хигучи, Дж. Брунски, В.Н. Трезубов, А.А. Смердов, М.Л. Мишнев // Российский журнал биомеханики. – 2023. – Т. 27, № 3. – С. 24–35.
- Доль, А.В. Математические модели движения крови в системе сосудов с упругими стенками / А.В. Доль, Ю.П. Гуляев, Д.В. Иванов // Успехи современного естествознания. – 2014. – № 9. – С. 79–84.
- Численное моделирование течения жидкости в венозном клапане при пробе Вальсальвы / Я.А. Гатаулин, Е.Д. Никитин, А.Д. Юхнев, Д.А. Росуховский // Российский журнал биомеханики. – 2022. – № 3. – С. 78–86.
- Abdominal aortic hemodynamics in young healthy adults at rest and during lower limb exercise: quantification using image-based computer modeling / B.T. Tang, C.P. Cheng, M.T. Draney, N.M. Wilson, P.S. Tsao, R.J. Herfkens, C.A. Taylor // Am. J. Physiol. Heart Circ. Physiol. – 2006. – Vol. 291. – P. H668–H676.
- Alterations in wall shear stress predict sites of neointimal hyperplasia after stent implantation in rabbit iliac arteries / J.F. LaDisa Jr., L.E. Olson, R.C. Molthen, D.A. Hettrick, P.F. Pratt, M.D. Hardel, J.R. Kersten, D.C. Warltier, P.S. Pagel // Am. J. Physiol. Heart Circ. Physiol. – 2005. – Vol. 288. – P. H2465–H2475.
- Исследование структуры кровотока в персонифицированных моделях ответвления шунта от бедренной артерии / А.Д. Юхнев, А.А. Маринова, Е.М. Смирнов, Я.А. Гатаулин, Л.Г. Тихомолова, А.А. Врабий, А.А. Супрунович // Российский журнал биомеханики. – 2023. – Т. 27, № 4. – С. 25–39.
- Nachar, N. The Mann-Whitney U: A test for assessing whether two independent samples come from the same Distribution / N. Nachar // Tutorials in Quantitative Methods for Psychology. – 2008. – Vol. 4. – P. 1–13.
- Hanusz, Z. Normalization of the Kolmogorov–Smirnov and Shapiro–Wilk tests of normality / Z. Hanusz, J. Tarasińska // Biometrical Letters. – 2015. – Vol. 52.
- Численное моделирование полного протеза коленного сустава с силиконовой прослойкой / А. Мааче, М. Амаджи, Х. Амеддах, Х. Мазуз // Российский журнал биомеханики. – 2024. – Т. 28, № 1. – С. 77–87.
- The association of the circle of Willis anomaly and risk of stroke in patients with carotid artery disease / E.Ö. Göksu, P. Koç, E. Küçükseymen, A. Ünal, F. Genç, E.S. Gencer, A. Yaman // Arq Neuropsiquiatr. – 2017. – Vol. 75, no. 7. – P. 429–432.
- Circle of Willis anomalies in stroke patients related with symptomatic carotid artery disease / S. Kamışlı, Ö. Kamışlı, U. Teker, Y. Kablan, K. Saraç, C. Özcan // Turkish J Cerebrovasc Dis. – 2012. – Vol. 18, no. 1. – P. 6–9.
- Lazzaro, M.A. The role of circle of Willis anomalies in cerebral aneurysm rupture / M.A. Lazzaro, B. Ouyang, M. Chen // Journal of NeuroInterventional Surgery. – 2012. – Vol. 4. – P. 22–26.
- Simultaneous internal carotid artery stenosis and ipsilateral anterior communicating artery saccular aneurysm treatment: a case report / A.V. Korotkikh, D.A. Nekrasov, A.A. Khilchuk, S.G. Scherbak, A.M. Sarana // Radiology Case Reports. – 2020. – Vol. 15, no. 7. – P. 1083–1086.
- Distribution of circumferential stress in ruptured and stable atherosclerotic lesions. A structural analysis with histopathological correlation / G.C. Cheng, H.M. Loree, R.D. Kamm, M.C. Fishbein, R.T. Lee // Circulation. – 1993. – Vol. 87. – P. 1179–1187.
- The impact of calcification on the biomechanical stability of atherosclerotic plaques / H. Huang, R. Virmani, H. Younis, A.P. Burke, R.D. Kamm, R.T. Lee // Circulation. – 2001. Vol. 103. – P. 1051–1056.


