Биопленки углеводородокисляющих бактерий антропогенно нарушенных почв г. Когалыма
Автор: Коробейникова А.С., Голубев Д.М., Тарасюк А.К., Уткин Д.В., Нечаева О.В., Глинская Е.В.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 4, 2025 года.
Бесплатный доступ
Определены биологические свойства и условия формирования биопленок углеводородокисляющими бактериями для их дальнейшего применения в очистке от нефтезагрязнений и рекультивации антропогенно нарушенных почв. Объектом исследования явились углеводородокисляющие микроорганизмы, выделенные из проб почв г. Когалыма: Bacillus alcalophilus WS-3027B, B. funiculus LY-2403G, B. halodurans MH-3011N, B. niacini TC-8101S, B. psychrodurans LV-1106E, Curtobacterium flaccumfaciens AE-0851V. Для выявления способности бактерий образовывать биопленки использовали метод определения степени формирования биопленок в стационарной фазе роста путем окрашивания кристаллическим фиолетовым по методу O'Toole et al. Обнаружено, что среди нефтеокисляющих микроорганизмов штаммы B. alcalophilus WS-3027B и C. flaccumfaciens AE-0851V характеризуются плотной продукцией биопленки, штаммы B. halodurans MH-3011N, B. niacini TC-8101S, B. funiculus LY-2403G, B. psychrodurans LV-1106E – умеренной продукцией биопленки. Установлены оптимальные условия образования биопленок исследуемыми микроорганизмами. Проведенное изучение биопленкообразования углеводородокисляющих бактерий открывает перспективы использования данных штаммов в качестве активных деструкторов нефтепродуктов при биоремедиации загрязненных почв.
Биопленки, углеводородокисляющие микроорганизмы, почва, нефтяное загрязнение, биоремедиация
Короткий адрес: https://sciup.org/147252648
IDR: 147252648 | УДК: 579.2 | DOI: 10.17072/1994-9952-2025-4-406-414
Biofilms of hydrocarbon-oxidizing bacteria from anthropogenic soils in Kogalym
The article is devoted to the determination of the biological properties and conditions of biofilm formation by hydrocarbon-oxidizing bacteria for their further use in oil pollution treatment and remediation of anthropogenic disturbed soils. The object of the study is hydrocarbon-oxidizing microorganisms isolated from soil samples from Kogalym: Bacillus alcalophilus WS-3027B, B. funiculus LY-2403G, B. halodurans MH-3011N, B. niacini TC-8101S, B. psychrodurans LV-1106E, Curtobacterium flaccumfaciens AE-0851V. Biofilm formation activities were evaluated by the crystal violet staining method for assessing biofilm formation degree in the stationary phase according to O'Toole et al. Among the hydrocarbon-oxidizing microorganisms, B. alcalophilus WS-3027B and C. flaccumfaciens AE-0851V were found to form dense biofilms, while B. halodurans MH-3011N, B. niacini TC-8101S, B. funiculus LY-2403G, and B. psychrodurans LV-1106E exhibited moderate biofilm production. Optimal conditions for the formation of biofilms by the studied microorganisms have been established. The conducted study of biofilm formation of hydrocarbon-oxidizing bacteria opens up prospects for the use of these strains as active destructors of petroleum products in the bioremediation of contaminated soils.
Текст научной статьи Биопленки углеводородокисляющих бактерий антропогенно нарушенных почв г. Когалыма
Нефть является наиболее востребованным энергетическим ресурсом и основой мирового экономического прогресса и процветания, однако, попадая в окружающую среду, она оказывает негативное воздействие, подвергая риску как качество жизни человечества, так и биосферу в целом [Luo et al., 2024]. Разливы нефти пагубно сказываются на плодородии почвы и приводят к потере сельскохозяйственных угодий [Ajona, Vasanthi, 2021]. Вследствие этого требуется применение современных стратегий в проведении очистительных мероприятий для удаления нефти и нефтепродуктов из почв [Tayyeb at al., 2024; Плешакова и др., 2025].
Углеводородные компоненты нефти, благодаря своей химической стабильности и высокой устойчивости к различным биологическим превращениям, являются опасными загрязнителями окружающей среды, трудности удаления их из почвы связаны со сложностью состава и гидрофобностью [Adeniji, Okoh, Okoh, 2017; Vu, Mulligan, 2022; Hegazy at al., 2024].
Физико-химические подходы к удалению разлитой нефти, несмотря на свое частое применение, обычно оказываются непрактичными как с экономической, так и экологической точки зрения [Rosenberg, 1993]. Поэтому биоремедиация, осуществляемая с помощью микроорганизмов, является наиболее подходящим вариантом очистки почвы от нефти и нефтепродуктов [Ajona, Vasanthi, 2021]. Этот метод основан на способности микроорганизмов вовлекать углеводороды в процессы метаболизма, используя их в качестве источника углерода и энергии и приводя к их минерализации с образованием углекислого газа, воды и безвредных соединений [Bala et al., 2022].
Многие бактерии, обитающие в почве, способны образовывать на поверхности клеточной стенки слизистый слой, защищающий их от действия неблагоприятных факторов окружающей среды (механического повреждения, высушивания, осмотического стресса и т.д.). Кроме того, за счет слизеобразования колонии микроорганизмов прочно удерживаются на твердой поверхности, способны к агрегации и образованию биопленок [Сопрунова, Нгуен Виет Тьен, 2010]. Биопленка представляет собой слой иммобилизованных клеточных полимеров, состоящих из полисахаридов, белков, нуклеиновых кислот, липидов и гумуса [Gupta, Thakur, 2016]. Именно благодаря биопленкам бактерии получают ряд преимуществ, таких как способность к адгезии, возможность обмена метаболитами и устойчивость к стрессам окружающей среды [Santos et al., 2018]. Исследование бактериальных биопленок и условий их формирования позволит глубже изучить экологию микроорганизмов и поможет в разработке биопрепаратов, направленных на очищение загрязненных углеводородами нефти почв [Verma et al., 2023; van Hoogstraten et al., 2024]. Оптимальная температура образования биопленки для большей части бактериальных организмов – в пределах от 20 до 30°C. Снижение температуры ниже 9‒10°C резко ухудшает условия деятельности микроорганизмов [Прикладная экобиотехнология, 2012]. Кроме того, рН среды также оказывает влияние на формирование биопленки [Hostaka, Ciznár, Stefkovicová, 2010; Спирина, Русакова, 2021]. Способность угле-водородокисляющих бактерий к образованию биопленок в почвах с различными значениями рН (кислыми, нейтральными, щелочными) в широком диапазоне температур является важным фактором при разработке препаратов для биоремедиации почв от нефтезагрязнений.
Цель исследования – определить биологические свойства и условия формирования биопленок угле-водородокисляющими бактериями.
Материалы и методы исследования
Объектом исследования явились 6 штаммов углеводородокисляющих бактерий ( Bacillus alcalophilus WS - 3027B , B. funiculus LY - 2403G , B. niacini TC-8101S , B. psychrodurans LV-1106E , B. halodurans MH-3011N , Curtobacterium flaccumfaciens AE-0851V), выделенных из проб почв, отобранных на территории г. Когалыма Ханты-Мансийского автономного округа (ХМАО) Тюменской обл.
Город Когалым расположен в зоне вечной мерзлоты. Климат г. Когалыма, находящийся под непосредственным влиянием Арктики, характеризуется как резко континентальный (субарктический) с суровой продолжительной зимой и коротким теплым летом. Температура почвы на глубине 20 см составляет в среднем 8‒9°С [График температуры: эл. ресурс]. Почва на территории г. Когалыма относится к группе дистрик-гистосолей – торфяно-болотных почв верховых болот, характеризующихся кислой средой [Кле-банович, 2015; Почвы Когалыма: эл. ресурс; Дистрик-гистосоль: эл. ресурс].
В связи с этим представляет интерес изучение способности к формированию биопленок у представителей указанных выше видов при данных климатических и эдафических факторах.
Для оценки степени формирования биопленок использовали агаровые бактериальные культуры в стационарной фазе роста. Бактерии выращивали на ГРМ-агаре рН 7.2 (ФБУН ГНЦ ПМБ Роспотребнадзора, Оболенск) при температуре 28°С в течение 24 ч. Бактериальные взвеси готовили в 0.9% растворе хлорида натрия в концентрации, соответствующей 10 единицам отраслевого стандартного образца мутности (ОСО 42-28-59-85П (10 МЕ), ФГБУ «НЦЭСМП» Минздрава России), эквивалентной концентрации 1.1×108 КОЕ/мл Bacillus sp. [СО мутности…: эл. ресурс]. Взвеси микроорганизмов переносили в ГРМ-бульон (ФБУН ГНЦ ПМБ Роспотребнадзора, Оболенск) с рН, равной 3, 5, 7, 8 и 9, до конечной концентрации 5×107 КОЕ/мл. Культуры микроорганизмов в бульоне вносили по 200 мкл в лунки полистироловых 96-луночных плоскодонных планшетов для культивирования клеток и тканей (Jet Bio-Filtration, Китай, РУ № ФСЗ 2012/12495 от 02.06.2020 г.) и инкубировали при температурах 6, 28, 37, 42°С без встряхивания в течение 72 ч. В лунки отрицательного контроля вносили 200 мкл ГРМ-бульона рН 7.2. Далее из лунок планшетов отбирали среду с планктонными клетками, лунки промывали в течение 2‒3 мин стерильным физиологическим раствором в объеме 200 мкл. Физиологический раствор полностью удаляли из лунок и высушивали планшеты в течение 20 мин. Окраску биопленок на поверхности лунок проводили по методу O'Toole, основанному на способности красителя кристаллического фиолетового связываться с клетками и внеклеточным матриксом биопленок [O'Toole, Kaplan, Kolter, 2000]. Для этого в лунки планшетов вносили по 200 мкл отфильтрованного 0.2% раствора кристаллического фиолетового в 96% этиловом спирте и инкубировали в течение 15 мин при комнатной температуре. Краситель удаляли из лунок. Несвязавшийся краситель отмывали троекратно водопроводной водой. Планшеты высушивали 30 мин. Затем в лунки добавляли 96% раствор этанола в объеме 200 мкл для элюции связанного с биопленкой красителя. Растворитель отбирали, помещали в чистые плоскодонные планшеты и измеряли оптическую плотность при длине волны 595 нм. В качестве контроля использовали лунки, инкубированные с чистой средой, подвергнутые аналогичным манипуляциям.
Количественную оценку образования биопленки в каждой лунке проводили по формуле [Adeniji, Okoh, Okoh, 2017]:
OD отн =OD абс /OD с , где OD отн – относительная оптическая плотность красителя, OD абс – абсолютная оптическая плотность красителя, OD с – оптическая плотность (OD) отрицательного контроля+3 sd.
Умеренную продукцию биопленки считали при 2×OD
с
≤OD
отн
≤4×OD
с
, плотную продукцию считали при 4×OD
с
Статистическую обработку полученных данных осуществляли с применением общепринятых статистических методов [Урбах, 1975; Лакин, 1990] в программе Microsoft Office Excel (Microsoft, США).
Результаты и их обсуждение
Полученные результаты представлены на рисунке и в таблице.
По нашим данным, максимальная продукция биопленки наблюдается у всех штаммов в температурном оптимуме их роста: B. halodurans MH-3011N – при 37°С, B. niacini TC-8101S – 30°С, B. alcalophilus WS-3027B – 30°С, B. funiculus LY-2403G – 22°С, B. psychrodurans LV-1106E – 22°С, C. flaccumfaciens AE-0851V – 30°С [Bacterial Diversity: эл. ресурс]. Среди изучаемых углеводородокисляющих микроорганизмов 2 штамма – Bacillus alcalophilus WS-3027B и C. flaccumfaciens AE-0851V – характеризуются плотной продукцией биопленки по (Stepanovic, Vuković, Hola [2007]), остальные 4 штамма – B. halodurans MH-3011N, B. niacini TC-8101S, B. funiculus LY-2403G, B. psychrodurans LV-1106E характеризуются умеренной продукцией биопленки (см. таблицу). Для большинства исследованных штаммов максимальная продукция биопленки наблюдалась при нейтральных и щелочных показателях среды. Это согласуется с литературными данными об адаптации гало- и алкалофильных бактерий к высоким значениям рН, к кото- рым относятся B. halodurans MH-3011N, B. alcalophilus WS-3027B, к высоким значениям рН [Irwin, 2020;
Alkalihalobacillus : эл. ресурс].
(а)
(б)
(в)
(г)
(д)
(е)
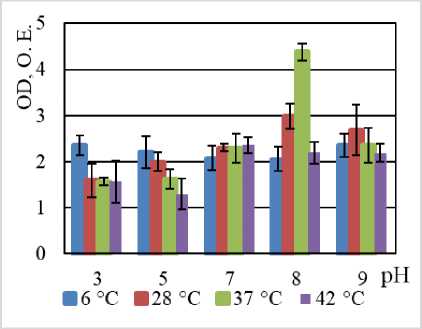
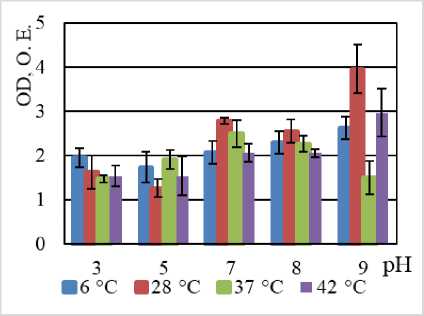
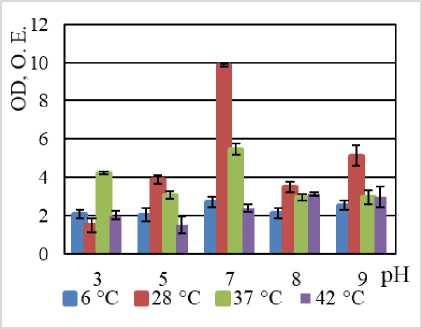
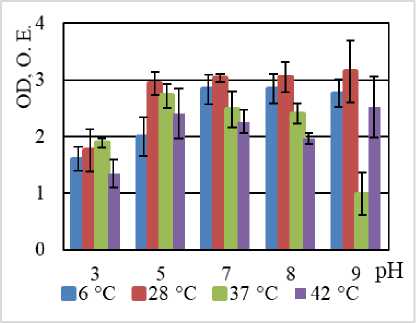
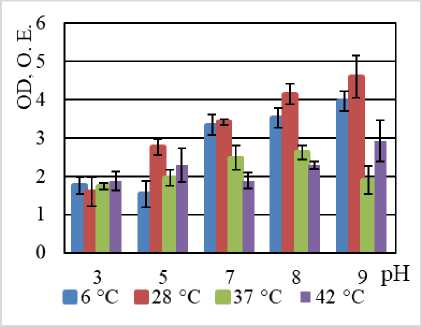
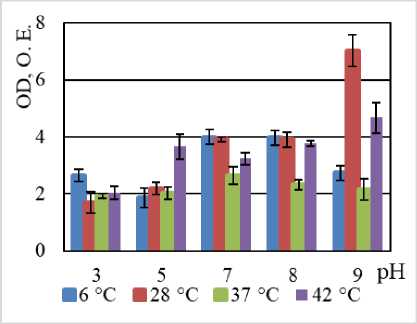
Способность к биопленкообразованию штаммами:
B. halodurans MH-3011N (а), B. niacini TC-8101S (б), B. alcalophilus WS - 3027B (в), B. funiculus LY - 2403G (г), B. psychrodurans LV-1106E (д), C. flaccumfaciens AE-0851V (е)
Biofilm-forming capability of the strains:
B. halodurans MH-3011N (a), B. niacini TC-8101S (b), B. alcalophilus WS - 3027B (c),
B. funiculus LY - 2403G (d), B. psychrodurans LV-1106E (e), C. flaccumfaciens AE-0851V (e)]
Условия биопленкообразования микроорганизмами [Conditions of biofilm formation by microorganisms]
|
Штамм |
Характеристика |
|
B. halodurans MH-3011N |
Наибольшая продукция биопленки наблюдается в щелочной среде (рН 8) при температуре 37°С. При кислых рН (рН=3.5) максимальная продукция биопленки наблюдается при температуре 6°С. Продукция биопленки умеренная. |
|
B. niacini TC-8101S |
Наибольшая продукция биопленки наблюдается в щелочной среде (рН 9) при температуре 28°С. При кислых рН (рН=3) максимальная продукция биопленки наблюдается при температуре 6°С. Продукция биопленки умеренная. |
|
B. alcalophilus WS - 3027B |
Наибольшая продукция биопленки наблюдается в нейтральной среде (рН 7) и в щелочной среде (рН 9) при температуре 28°С. Штамм характеризуется плотной продукцией биопленки (ODc>4). |
|
B. funiculus LY - 2403G |
Равномерная продукция биопленки наблюдается в широком диапазоне рН (от 5 до 9) при температуре 28 и 6°С. Продукция биопленки умеренная. |
|
B. psychrodurans LV-1106E |
Наибольшая продукция биопленки наблюдается в щелочной среде (рН 9) при температуре 28 и 6°С. Продукция биопленки умеренная. |
|
C. flaccumfaciens AE-0851V |
Наибольшая продукция биопленки наблюдается в щелочной среде (рН 9) при температуре 28°С. При кислых рН (рН 3) максимальная продукция биопленки наблюдается при температуре 6°С. Штамм характеризуется плотной продукцией биопленки (ODc>4). |
В то же время представляет интерес поиск штаммов, сохраняющих способность к формированию биопленки в экстремальных условиях субарктического пояса при низких температурах и кислой среде подзолистых почв, подзолов и верховых торфяников для практического использования при биоремедиации почв от нефтезагрязнений углеводородами. Установлено, что в кислых средах у всех штаммов сохранялась умеренная продукция биопленки.
Максимальная продукция биопленки у большинства штаммов наблюдалась при оптимальной температуре роста 28°С. Однако ряд штаммов сохраняли умеренную продукцию биопленки при низких температурах в кислых и слабокислых средах – условиях, имитирующих вечную мерзлоту. Следовательно, наиболее подходящими видами для биоремедиации почв г. Когалыма с учетом биопленкообразования и экологических условий (кислые почвы, низкие температуры) оказались B. halodurans MH-3011N, B. ni-acini TC-8101S , C. flaccumfaciens AE-0851V (таблица). В то же время вид C. flaccumfaciens AE-0851V в качестве свободноживущих бактерий длительно не сохраняется в почве, т. к. не образует спор [ Curto-bacterium flaccumfaciens : эл. ресурс].
Заключение
Таким образом, проведена оценка эффективности биопленкообразования 6 штаммов углеводородо-кисляющих микроорганизмов родов Bacillus и Curtobacterium , выделенных из проб почв г. Когалыма. Установлено, что штаммы углеводородокисляющих бактерий способны к максимальной продукции биопленки в оптимальных для своего роста условиях. В то же время отмечено, что представители B. halodurans MH-3011N, B. niacini TC-8101S , C. flaccumfaciens AE-0851V характеризуются умеренной способностью к пленкообразованию при низких температурах и кислых значениях рН среды, что свидетельствует о перспективности их использования при разработке биопрепаратов для биоремедиации почв от нефтезагрязнений в условиях субарктического пояса.
Полученные в результате исследования данные можно использовать для комплексного подхода при биоремедиации урбосистем и прогнозирования состояния антропогенно нарушенных территорий. Проведенное изучение биопленкообразования углеводородокисляющих бактерий, выделенных из проб почв г. Когалыма, открывает перспективы использования представителей данных видов в качестве активных деструкторов нефтепродуктов.


