Биосовместимость кальцийфосфатных материалов биогенного происхождения при имплантации в область дефектов костей собак
Автор: Талашова Ирина Александровна, Силантьева Тамара Алексеевна, Кононович Наталья Андреевна, Лунева Светлана Николаевна
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 4, 2016 года.
Бесплатный доступ
Цель. Оценить биосовместимость имплантационных кальцийфосфатных материалов из костной ткани быков в зависимости от их состава. Материалы и методы. В эксперименте на животных (собаки) оценивали биосовместимость трех имплантационных кальцийфосфатных материалов, произведенных по оригинальной технологии. Материалы получены из бычьей костной ткани путем ее деминерализации и осаждения из раствора солей фосфатов кальция. Для улучшения характеристик биосовместимости в их состав дополнительно вводили белки с молекулярной массой от 20 до 30 кДа, выделенные из сыворотки крови собак с активным остеогенезом. Выделение проводили с применением методов высаливания, диализа и гель-проникающей хроматографии. Кальцийфосфатные материалы и их композиты имплантировали в дефекты метафизов трубчатых костей. Исследование выполнено с применением методов инфракрасной спектроскопии, рентгеновского электронно-зондового микроанализа, световой и сканирующей электронной микроскопии. Количественно и качественно определяли химический состав материалов, характер и интенсивность репаративного костеобразования. Гистоморфометрически оценивали диаметр частиц имплантатов в составе тканей, заполняющих область дефекта губчатой кости. Результаты. Установлено, что имплантируемые материалы в разной степени обладали свойствами биодеградации, остеоиндукции и остеокондукции. Кальцийфосфатные материалы, наиболее приближенные по своему составу к костной ткани, имели высокую степень биосовместимости. Заключение. Предложенные кальцийфосфатные материалы могут найти применение в клинической практике при возмещении посттравматических дефектов, коррекции патологических состояний, сопровождающихся остеопорозом и потерей костного вещества.
Кальцийфосфатные материалы, биосовместимость, остеоиндукция, остеокондукция, биодеградация, биоинтеграция
Короткий адрес: https://sciup.org/142121934
IDR: 142121934 | УДК: [546.41''181.1:606:611.018.4]-089.84-092.9 | DOI: 10.18019/1028-4427-2016-4-95-103
Biogenic calcium phosphate materials implanted into canine bone defects and their biocompatibility
Purpose To study the biocompatibility of implantation calcium phosphate (CP) materials from bovine bone tissue and its dependence on their composition Materials and methods The authors studied the biocompatibility of three implantation calcium phosphate materials obtained by an original technology on experimental animals (dogs). The materials obtained from bovine bone tissue by its demineralization and sedimentation out of the CP salts solutions. Serum proteins (SP) of the molecular mass of 20-30 kDa that were isolated from blood serum of the dogs with active osteogenesis were added to CP composition in order to improve the characteristics of biocompatibility. The isolation was performed using the methods of salting-out, dialysis and gel permeation chromatography. CP materials and their composites were implanted into the defects of long bone metaphyses. The study was performed using the methods of infrared spectroscopy, X-ray electron probe microanalysis, and light and scanning electron microscopy. Chemical composition of CP materials, reparative osteogenesis character and its intensity were determined quantitatively and qualitatively. The diameter of the implant particles of the tissues that filled the cancellous defect area were evaluated histomorphometrically. Results It was found that the implanted materials differed in biodegradation, osteoinduction and osteoconduction properties. CP materials that were the closest to bone tissue by their composition had a higher degree of biocompatibility Conclusion The proposed CP materials can be used in clinical practice for filling posttraumatic defects and correction of the pathological conditions accompanied by osteoporosis or bone loss.
Текст научной статьи Биосовместимость кальцийфосфатных материалов биогенного происхождения при имплантации в область дефектов костей собак
Биосовместимые имплантационные материалы для восстановления костной ткани человека в течение длительного периода времени востребованы в практической ортопедии и травматологии. Определенные ограничения в использовании аутогенной губчатой костной ткани, «золотого» стандарта костной пластики, предопределяют поиск новых остеопластических материалов как биологического, так и искусственного происхождения [1, 2]. Эти материалы должны обладать свойствами остеоиндуктивности, то есть стимулировать дифференциацию некоммитированных и коммитированных клеток в остеогенном направлении, а также остеокондуктивности, образуя плотные поверхностные контакты с новообразованной костной тканью [3-6]. Вышеуказанные свойства обеспечивают биоинтеграцию, или способность материала форми-
ровать механически прочную конструкцию совместно с вновь образованной костью [7]. Биодеградация, или способность к элиминации совместно с провизорными костными трабекулами в процессе физиологической реорганизации, также является обязательным свойством имплантационного материала [8]. Комплекс перечисленных качеств объединяется понятием биосовместимости или способности биоматериала выполнять необходимые функции в процессе заживления дефектов кости для получения положительного клинического результата [9]. Кальцийфосфатные соединения (CP), в том числе полученные из нативного костного матрикса, в значительной степени соответствуют этому комплексу требований [10, 11]. При имплантации в дефекты губчатой кости собак и овец подтверждена их низкая иммуногенность и хорошая биосовместимость
[12, 13]. Для любых имплантационных CP материалов имеют значение химический состав, размер и форма частиц [5, 14]. В связи с этим, достижение положительных результатов напрямую зависит от технологии их производства [15]. Задачей настоящего исследования являлось изучение свойств и биосовместимости, а именно, биодеградации, остеоиндуктивности и остео-кондуктивности CP материалов, полученных с использованием трех различных технологий из костной ткани
крупного рогатого скота (КРС) и имплантированных в дефекты метафизов трубчатых костей собак. Поскольку сыворотка крови, полученная в активной фазе дистракционного остеогенеза, содержат максимальную концентрацию остеоиндуцирующих факторов [16, 17], также было проверено предположение о том, что выделенные из нее белковые компоненты (SP) окажут оптимизирующее влияние на формирование кости и биосовместимость CP материалов.
МАТЕРИАЛЫ И МЕТОДЫ
Получение СР материалов
CP соединения были получены из диафизов костей взрослых сельскохозяйственных животных (КРС) по трем различным технологиям:
-
1) CP1: деминерализация костей 0,5 N раствором HCl и седиментация СР с использованием 52,2 % водного раствора NaOH;
-
2) СР2: деминерализация костей 0,5 N раствором HCl, седиментация СР с использованием 52,2 % водного раствора NaOH и дополнительная обработка 8M водным раствором карбамида;
-
3) CP3: деминерализация костей 6 N раствором HCl и седиментация СР с использованием 0,12 % водного раствора CaO.
Полученные CP материалы стерилизовали β-излучением в дозе 20 кГр с использованием линейного резонансного ускорителя электронов LUE-8-5V (НИИЭФА, Россия).
Исследование состава CP материалов
Качественный состав разработанных CP материалов исследовали методом инфракрасной спектроскопии (IR) с использованием ИК-Фурье спектрометра (Инфралюм ФТ-02, Люмэкс, Россия). Для количественного определения кальция (Ca), фосфора (P), магния (Mg) и серы (S) в образцах CP материалов и костной ткани собак методом рентгеновского электронно-зондового анализа использовали электронно-зондовый энергодисперсионный микроанализатор Oxford INCA Energy 200 (Oxford Instruments, UK), смонтированный на сканирующем электронном микроскопе JSM-840 (JEOL, Japan); исследование проводили при ускоряющем напряжении 20 kV. Количественные данные представлены в виде значений выборочного среднего и его стандартного отклонения (M ± SD).
Разделение белков сыворотки крови
Гомологичные SP активной фазы дистракционного остеогенеза были получены из сыворотки крови собак, которым выполняли удлинение костей голени посредством аппарата Илизарова в ходе параллельного экспериментального исследования [18]. Полученную сыворотку крови разводили в два раза 0,15 М раствором NaCl, подвергали сатурации сульфатом аммония до 30 % насыщения, охлаждали и удаляли осадок путем ультрацентрифугирования (Optima LE-80K, Beckman Coulter, USA) при 40000 g в течение 15 мин. Надосадочную жидкость подвергали сатурации сульфатом аммония до 50 % насыщения для дальнейшего центрифугирования. Очищение протеинов выполняли с использованием системы для гель-проникающей хроматографии (GF) LKB (Pharmacia LKB Biotechnology AB, Sweden). Осадок, образовавшийся после второго этапа высаливания, растворяли в 8М растворе мочевины и фракционировали в соответствии с молекулярной массой с использованием GF на носителе TSK-гель TOYOPEARL HW65S (ToyoSoda, Japan).
Фракции с объемом выхода, соответствующим относительной молекулярной массе в 20-30 кДа, подвергали диализу против дистиллированной воды и лиофилизировали. Затем порции полученных SP весом от 0,02 до 0,03 г растворяли в 1 мл физиологического раствора и смешивали с 5,0-5,2 г каждого из трех СР материалов. Полученную композицию разбавляли физиологическим раствором до пастообразной консистенции. Затем каждый из CP+SP композитов помещали в стеклянный флакон, закрытый резиновой пробкой с алюминиевыми колпачками, и подвергали стерилизации β-излучением в дозе 20 кГр с использованием линейного резонансного ускорителя электронов LUE-8-5V (НИИЭФА, Россия).
Имплантация CP материалов в дефект губчатой кости собак
Эксперимент по имплантации выполнен на 24 взрослых беспородных собак обоего пола в возрасте от одного года до трех лет с массой тела 8,8 ± 3,2 кг. Моделирование несквозных конических дефектов диаметром 5-7 мм (n = 120) проксимальных метафизов плечевой и большеберцовой костей осуществляли с применением сверла. Полученные дефекты заполняли пастообразными CP материалами и CP+SP биокомпозитами: CPI (n = 16), CP2 (n = 16), CP3 (n = 16), CP1+SP (n = 16), CP2+SP (n = 16) и CP3+SP (n = 16). У семи животных, составивших контрольную группу, имплантацию материалов в костные дефекты (n = 24) не проводили. Животных выводили из эксперимента через 21 и 42 суток после операции путем внутривенного введения летальных доз 5 % раствора тиопентала натрия. Оперативные вмешательства, уход за животными и эвтаназию выполняли в соответствии с Европейской конвенцией по защите позвоночных животных, используемых для экспериментальных и других научных целей (Страсбург, 1986). Выполнение исследований было одобрено комитетом по этике ФГБУ «РНЦ «ВТО» им. акад. Г.А. Илизарова» (протокол № 3 от 12.03.2001), результаты разрешены к публикации редакционным советом (протокол № 3-28 от 27.09.2013).
Гистологическое исследование биосовместимости
Образцы тканей метафизов оперированных животных, полученные через 21 и 42 суток эксперимента, обрабатывали в соответствии с общепринятыми гистологическими методиками [19]. Репаративное костеобразование в области создания дефекта и биосовместимость CP материалов исследовали методом световой микроскопии. Целлоидиновые срезы, окрашенные гематоксилином и эозином, по Массону, исследовали в световом фотомикроскопе (OPTON Feintechnik GmbH, Germany). Оцифрованные изображения полей зрения были получены с использованием АПК ДиаМорф (ДиаМорф, Россия), смонтированном на фотомикроскопе. Оцифрованные тотальные изображения гистотопографических целлоидиновых препаратов получали с использованием сканера HP ScanJet 7400C (Hewlett-Packard, USA). Для выпол-
нения гистоморфометрических исследований применяли программное обеспечение ВидеоТесТ-Морфология (VideoTesT, Россия). Количественно оценивали объемную долю губчатой кости в дефекте (Vcb, %), объемную плотность трабекул в губчатой кости регенерата (Vtr, %), диаметр гранул имплантационного материала (Dg, мкм). Измерения выполняли не менее чем в 30 полях зрения для каждого гистологического препарата. Гранулы диаметром менее 100 мкм относили к категории «мелкие», если диаметр составлял 100-250 мкм – к категории «средние», а свыше 250 мкм – «крупные». Так как полученные
данные не отвечали нормальному распределению, для их стастистической обработки были применены методы непараметрической статистики, результаты представлены в виде медиан (Me) и их доверительных интервалов (95 % CI). Для оценки различия между группами наблюдений использовали U-критерий Манна-Уитни [20]. Различия считались статистически значимыми при р < 0,05. Статистическую обработку выполняли с использованием программы анализа данных AtteStat, версия 10.8.8 (надстройка программного продукта Microsoft Excel, свидетельство № 2002611109 от 28.06.2002).
РЕЗУЛЬТАТЫ
Инфракрасная спектроскопия CP материалов
Исследования методом IR спектроскопии показали, что CP материалы помимо неорганической составляющей, представленной кальцием и фосфором, включали в свой состав и другие группы. В CP1 это было небольшое количество карбонат-ионов – CO32-, достаточно высокое содержание протеинов, гидроксильных групп – OH, карбоксильных групп – COO и амидов (рис. 1, а). Инфракрасный спектр CP2 указывал на то, что в данном соединении практически отсутствовали вещества белковой природы, интенсивность полосы поглощения кар-бонат-ионов была низкой (рис. 1, b). Материал CP3 имел в своем составе карбонат-ионы, а также незначительное количество белковых соединений (рис. 1, c).
SEM и EPMA исследование состава и морфологии CP материалов
Исследование образцов CP материалов методами SEM и EPMA позволило установить, что все они представляли собой смесь гранулярного и порошкообразного компонентов. Гранулы имели неправильную форму, их размеры значительно варьировали (рис. 2). Результаты количетвенного анализа химических элементов представлены в таблице 1. Содержание Ca, P и Mg в материалах CP1 и CP2 было выше, чем в нативной костной ткани вследствие элиминации органических компонентов матрикса. Соотношение содаржания Ca и P было приближено к таковому в костной ткани интактных животных. По нашему мнению, присутствие S в образцах СР1 могло быть обусловлено частичным соосаждением матриксных протеинов. Материал CP3 наиболее сильно отличался от нативной костной ткани.
Гистологическое и гистоморфометрическое исследование биосовместимости CP материалов в области имплантации
21-е сутки эксперимента
Во всех экспериментальных группах после имплантации кальцийфосфатных материалов в область дефекта дно и стенки полости покрывал слой новообразованной губчатой костной ткани с грубоволокнистыми трабекулами и студенистым костным мозгом. Большую часть дефекта заполняла рыхлая волокнистая соединительная ткань, обильно васкуляризированная полнокровными синусоидными капиллярами. При имплантации CP3 в составе волокнистой соединительной ткани отмечали большое количество моноцитов и макрофагов, обширные кистозные полости. Гранулы имплантированных CP1 и CP2 материалов располагались одиночно, в составе трабекулярной костной и рыхлой соединительной тканей (рис. 3, a, b). На их поверхности обнаруживались прикрепленные многоядерные фагоциты. В группах, где использовали биокомпозиты, включающие белки сыворотки крови, отмечали плотный контакт трабекулярных и гранулярных поверхностей, прилегание капилляров соединительной и костной ткани к частицам СР материалов (рис. 3, d, e). Имплантат CP3 был
представлен скоплениями неструктурированного материала и рыхлых гранул, окруженных волокнистой соединительной тканью (рис. 3, c). Сочетание СР3 и сывороточных белков, по-видимому, увеличивало скорость резорбции имплантата, так как гранулы в составе волокнистой соединительной ткани были единичными (рис. 3, c). В обоих случаях поверхность новообразованных костных трабекул и гранул экспериментального материала резорбировали многоядерные фагоцитирующие клетки (рис. 3, f). Остео-индуктивные саойства СР материалов оценивали, измеряя Vcb и Vtr. В группах CP2 and CP2+SP были выявлены наиболее высокие значения показателей Vcb и Vtr, при этом заполнение дефекта губчатой костной тканью соответствовало таковому в контрольной группе, а Vtr превышала контрольный уровень. Имплантация материалов CP1 и CP3 статистически значимо снижала образование губчатой костной ткани в области регенерации, а Vtr не отличалась от контрольных значений. Применение CP+SP биокомпозитов значимо увеличивало заполнение дефекта губчатой костью во всех экспериментальных группах и влияло на объемную плотность трабекул (табл. 2).
42-е сутки эксперимента
На данном этапе эксперимента во всех группах в области дефекта преобладала губчатая костная ткань (рис. 4). Самые высокие показатели костеобразования были отмечены в группах с CP1, особенно при имплантации CP1+SP. Среднее значение Vcb превышало контрольные значения параметра, а Vtr приближалась к таковой в контроле. Трабекулы были сформированы пластинчатой костной тканью, в промежутках между ними располагался красный костный мозг. В группах CP2 и CP3 новообразованная губчатая костная ткань подвергалась реорганизации. Значения Vcb в области регенерации были снижены в сравнении с контролем. Введение SP в состав материала CP2 не оказывало значимого влияния на параметры костеобразования, тогда как в группе CP3+SP эти параметры были снижены по сравнению с эффектом от имплантации одного CP3 (табл. 3). Гранулы CP1 обнаруживались в составе костного вещества либо находились в плотном контакте с пластинчатыми трабекулами (рис. 5, a). Гранулы CP2 распределялись в костном веществе, межтрабекулярных промежутках и волокнистой соединительной ткани регенерата (рис. 5, b), а отдельно лежащие гранулы резорбировались многоядерными фагоцитами (рис. 5, b). Частицы материала CP3 формировали обширные скопления либо хлопьевидные включения в составе рыхлой соединительной ткани, инфильтрованной моноцитами и макрофагами (рис. 5, c). Введение SP в состав имплантационных материалов улучшало остеокондуктивность CP1 и CP2. Их гранулы контактировали как с поверхностью костных трабекул, так и с капиллярами соединительной ткани (рис. 5, d, e). В группе CP3+SP имплантационный материал полностью разорбировался (рис. 5, f).
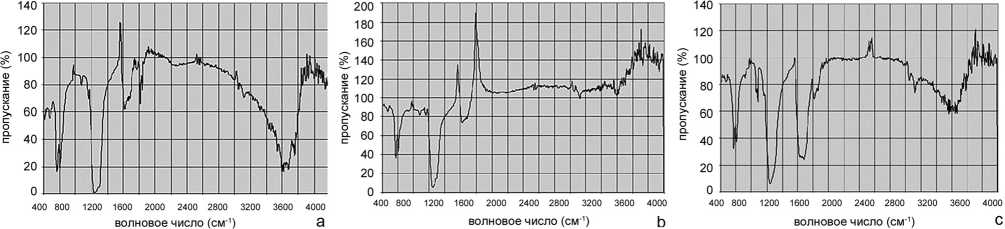
Рис. 1. IR спектры: (a) CP1, (b) CP2, (c) CP3

Рис. 2. Структура CP материалов по данным сканирующей электронной микроскопии: (a) CP1, увеличение 70×; (b) CP2, увеличение 80×; (c) CP3, увеличение 120×
Таблица 1
Содержание минеральных компонентов, M ± SD (%)
|
Ca |
P |
Mg |
S |
Са/Р |
|
|
Костная ткань |
22,8 ± 0,12 |
10,5 ± 0,09 |
0,27 ± 0,040 |
0,10 ± 0,004 |
2,17 |
|
CP1 |
33,18 ± 0,88 |
15,71 ± 0,52 |
0,43 ± 0,07 |
0,07 ± 0,03 |
2,11 |
|
CP2 |
30,20 ± 0,92 |
14,72 ± 0,82 |
0,59 ± 0,11 |
0 |
2,05 |
|
CP3 |
30,07 ± 0,87 |
10,25 ± 1,14 |
0,11 ± 0,03 |
0 |
2,93 |
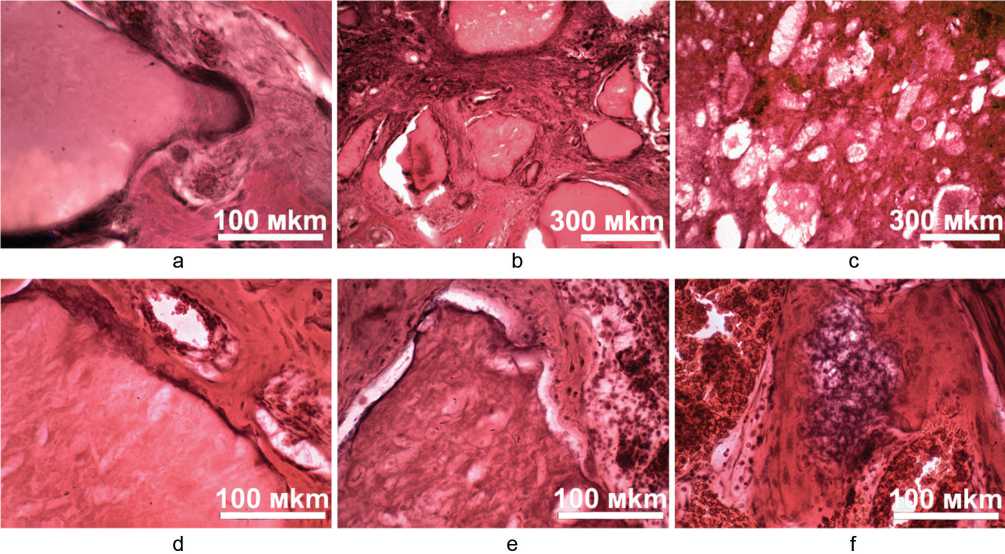
Рис. 3. Гранулы CP в тканях области дефекта на 21 сутки эксперимента: (a) CP1, (b) CP2, (c) CP3, (d) CP1+SP, (e) CP2+SP, (f) CP3+SP. Окрашивание гематоксилином и эозином; а, d-f – объектив 40x, окуляр 10×; b, c – объектив 10×, окуляр 10×
Таблица 2
Морфометрические параметры новообразованной костной ткани в области дефекта (21-е сутки эксперимента)
|
Параметр |
Контрольная группа |
|||||
|
Me |
95 % CI |
|||||
|
Vcb |
50,3 |
44,2–54,0 |
||||
|
Vtr |
29,6 |
23,7–34,6 |
||||
|
CP1 |
CP2 |
CP3 |
||||
|
Me |
95 % CI |
Me |
95 % CI |
Me |
95 % CI |
|
|
Vcb |
31,5* |
27,6–33,8 |
45,3 |
38,3–53,0 |
25,4* |
20,6–31,6 |
|
Vtr |
32,7 |
29,3–37,6 |
44,9** |
39,3–52,5 |
32,5 |
27,6–41,8 |
|
CP1+SP |
CP2+SP |
CP3+SP |
||||
|
Me |
95 % CI |
Me |
95 % CI |
Me |
95 % CI |
|
|
Vcb |
52,7 |
40,1–61,5 |
56,6 |
51,3–65,9 |
50,5 |
37,6–55,8 |
|
Vtr |
43,9** |
40,8–46,8 |
30,3 |
27,5–38,6 |
29,1 |
27,6–35,0 |
* – значимое снижение относительно контроля; ** – значимое увеличение относительно контроля.
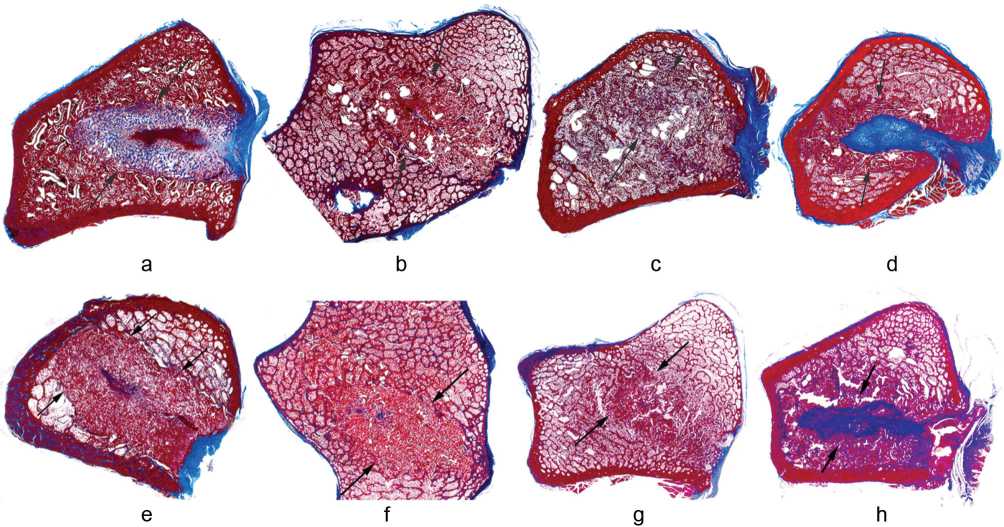
Рис. 4. Заполнение конусовидных дефектов в проксимальном метафизе большеберцовой кости: контрольная группа (a, e), CP1 (b), CP2 (c), CP3 (d), CP1+SP (f), CP2+SP (g), CP3+SP (h) на 42-е сутки эксперимента. Сканы гистотопографических целлоидиновых срезов. Окрашивание по Массону
Таблица 3
Морфометрические параметры новообразованной костной ткани в области дефекта (42-е сутки эксперимента)
|
Параметр |
Контрольная группа |
|||||
|
Me |
95 % CI |
|||||
|
Vcb |
71,3 |
62,7-79,9 |
||||
|
Vtr |
13,5 |
7,6-15,9 |
||||
|
CP1 |
CP2 |
CP3 |
||||
|
Me |
95 % CI |
Me |
95 % CI |
Me |
95 % CI |
|
|
Vcb |
85,8 |
74,5–90,4 |
67,7 |
63,4–72,0 |
58,3 |
49,8–70,4 |
|
Vtr |
12,6 |
9,6–15,5 |
29,4** |
26,0–32,2 |
32,8** |
24,1–39,6 |
|
CP1+SP |
CP2+SP |
CP3+SP |
||||
|
Me |
95 % CI |
Me |
95 % CI |
Me |
95 % CI |
|
|
Vcb |
88,1** |
84,9–91,7 |
78,7 |
74,3–85,0 |
43,5* |
36,1–49,7 |
|
Vtr |
12,5 |
10,8–18,3 |
23,9** |
20,7–26,1 |
17,6 |
15,9–18,9 |
* – значимое снижение относительно контроля; ** – значимое увеличение относительно контроля
Таблица 4
Диаметр CP гранул в области дефекта губчатой кости (мкм)
|
CP материалы |
21 день эксперимента |
42 дня эксперимента |
||
|
Me |
95 % CI |
Me |
95 % CI |
|
|
CP1 |
448 |
410–492 |
372 |
337–415 |
|
CP1+SP |
224 |
202–252 |
302 |
278–338 |
|
CP2 |
262 |
231–287 |
270 |
246–301 |
|
CP2+SP |
341 |
318–371 |
223 |
199–253 |
|
CP3 |
141 |
129–158 |
147 |
128–159 |
|
CP3+SP |
215 |
204–249 |
0 |
0 |
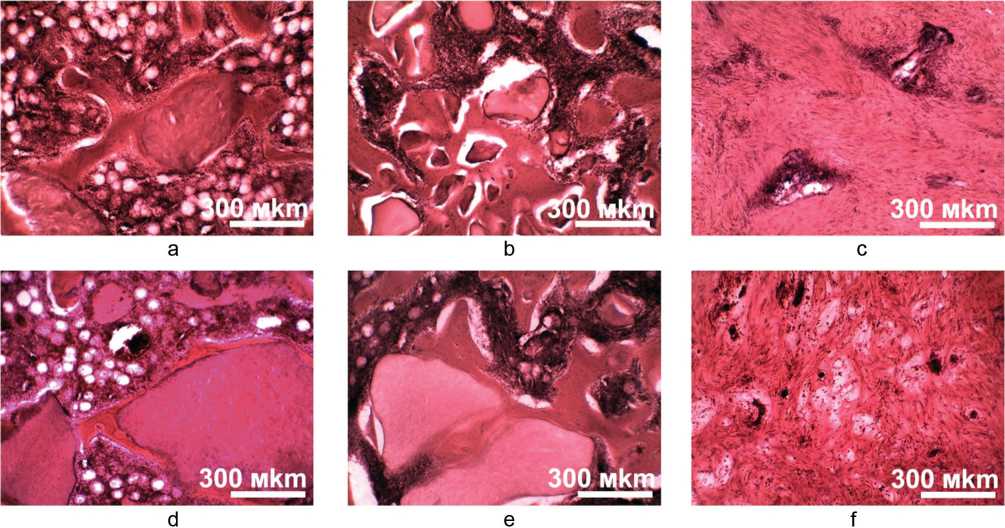
Рис. 5. Гранулы CP в тканях области дефекта на 42-е сутки эксперимента: CP1 (a), CP2 (b), CP3 (c), CP1+SP (d), CP2+SP (e), CP3+SP (f). Окрашивание гематоксилином и эозином. Объектив 10×; окуляр 10×
Гранулы CP материала в области дефекта 21-е сутки эксперимента
Исследование образцов тканей в области имплантации показало, что гранулы CP1 в их составе имели наибольший средний диаметр, составляющий около 400 мкм. Средний диаметр частиц матералов CP2 и CP3 составлял около 260 и 140 мкм соответственно. Добавление SP оказывало существенное влияние на их биодеградацию, так, среднее значение диаметра гранул CP1 снижалось приблизительно до 220 мкм,
а гранул CP2 и CP3 – напротив, возрастало, соответственно, до 340 и 215 мкм (табл. 4). Среди гранул в материалах CP1 и CP2 пребладали частицы большого и среднего диаметра, тогда как в материале CP3 – частицы среднего и малого диаметра. Добавление SP стимулировало резорбцию крупных, увеличивая этим доли мелких и средних гранул CP1 и CP2. Однако в материале CP3+SP первоочередная резорбция мелких и средних частиц приводила к снижению их доли в области имплантации (рис. 6, a).
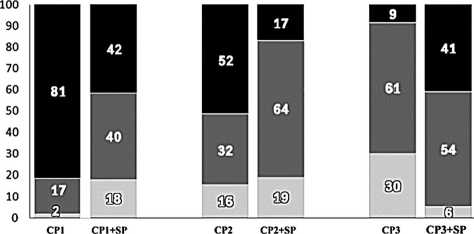
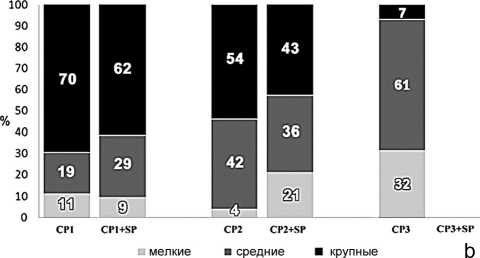
Рис. 6. Соотношение фракций гранул CP (%) в тканях области дефекта в соответствии с их размерными характеристиками: 21-е сутки эксперимента (a); 42-е сутки эксперимента (b)
42-е сутки эксперимента
Средний диаметр частиц имплантированных материалов без добавления SP не претерпевал существенных изменений в сравнении с предыдущим сроком эксперимента. Однако при использовании биокомпозитов средний диаметр гранул СР1+SP значительно увеличивался, в группе СР2+SP – напротив, снижался, а в группе CP3+SP частицы были полностью резорбированы (табл. 4). Изменения размеров частиц по сравнению с предыдущим периодом исследования отражали баланс между процессами биодеградации и биоинтеграции. При имплантации CP материалов без добавления SP
небольшое отличие размеров в сравнении с предыдущим периодом эксперимента свидетельствовало о замедлении процесса резорбции. В случае CP1 и CP2 это явление было связано с остеоинтеграцией, а в группе CP3 – с инкапсуляцией плотной волокнистой соединительной тканью. Введение в материалы SP ускоряло их биодеградацию, что проявлялось снижением доли мелких частиц и увеличением доли крупных, интегрированных в костную ткань гранул в группах CP1+SP и CP2+SP. В то же время, в группе CP3 добавление SP приводило к полной биодеградации материала и замещению его рыхлой соединительной тканью (рис. 6, b).
ДИСКУССИЯ
Анализ результатов исследования показал, что материалы CP1 и CP2 близки к нативной костной ткани по составу минерального компонента. Продукты деградации СР (ионы кальция, фосфат-ионы, полипептиды) являются естественными метаболитами и индуцируют биологические реакции, сходные с естественными процессами ремоделирования кости. Присутствие значительного количества белковых соединений в материале CP1 может оказывать стимулирующее влияние на адгезию и дифференциацию коммитированных клеток и остеобластов, определяя его остеоиндуктивные и осте-окондуктивные свойства [21]. Содержание небольшого количества Mg, как это показано для материала CP1, может оптимизировать его механические свойства, остеоиндуктивность, а также снижать степень резорбции или биодеградации [22]. Тем не менее, остеоиндуктивность CP1, по всей видимости, не является оптимальной, поскольку скорость образования костной ткани замедлена в сравнении с контрольной группой. Скорее всего, это явление связано с размером частиц CP1, составившим в среднем 400 мкм. Теоретические расчеты свидетельствуют о том, что более предпочтительный диапазон значений Dg находится в пределах 100-200 мкм. Данный размер частиц может обеспечить как высокую удельную поверхность резорбции, так и свободные промежутки между гранулами, достаточные для врастания сосудов и новообразованной костной ткани [23].
Материал CP2 содержит меньшее количество Mg, протеинов и не является остеокондуктивным. Тем не менее, в течение первых трех недель после его имплантации отмечено более активное, в сравнении с контролем, заполнение дефекта новообразованной губчатой костью, что свидетельствует о высокой остеоиндуктивности материала. Среднее значение Dg гранул CP2 на ранних этапах эксперимента составляет около 260 мкм, что приближено к оптимальным значениям для врастания вновь образованных тканей. Тем не менее, после 21 суток имплантации образование костной ткани снижается по сравнению с контрольной группой. Скорее всего, это связано с уменьшением скорости биодеградации материала, поскольку соотношения мелких, средних и крупных частиц остается неизменным вплоть до 42 суток эксперимента.
Материал CP3, в отличие от CP1 и CP2, в наибольшей степени отличается от нативной костной ткани. Он не содержит белковые соединения, а отношение
Са/Р превышает значения оптимального для СР материалов диапазона 2,0–2,5 [24], составляя 2,93. Средний диаметр Dg составляет около 140 мкм в течение всего эксперимента, что оптимально для биодеградации. Материал CP3 не является остеокондуктивным, а отсутствие макромолекул костного матрикса и Mg снижает механическую прочность гранул, что приводит к их разрушению и формированию плотных неструктурированных скоплений частиц малого диаметра. В целом, имплантация CP3 снижает скорость заполнения дефектов костной ткани. Полученные результаты подтверждают наблюдения, согласно которым CP частицы диаметром около 100 мкм и менее подавляют функционирование остеобластов [25]. Другая возможная причина низкой остеоиндуктивности может заключаться в особенностях химического состава материала CP3. Установлено, что кальцийфосфатные материалы с соотношением С/Р > 2, включающие СО, к которым относится и СР3, резорбируются, не проявляя свойств остеоиндуктивности и остеокондуктивности [24, 26].
Добавление SP к CP материалам улучшает их остеоиндукцию, остеокондукцию и ускоряет биодеградацию. Биокомпозиты CP1+SP и CP2+SP показали самую высокую биосовместимость, в то время как комбинация CP3+SP ускорила биодеградацию и способствовала улучшению остеоиндуктивности, но не оказала никакого влияния на остеокондуктивность материала. Наблюдаемые эффекты могут быть объяснены высокой сорбционной емкостью CP материалов по отношению к биологически активным соединениям, в частности, полипептидам сыворотки крови, полученным от экспериментальных животных на этапе дистракционного остеосинтеза и имеющим молекулярную массу в диапазоне от 20 до 30 кДа. Данная фракция сывороточных белков содержит остеогенные факторы роста, экспрессируемые в результате активизиции остеогенеза [17, 27, 28]. Влияние SP на минерализацию, резорбцию и биоинтеграцию при включении в состав CP материалов в последнее время широко обсуждается, при этом отмечено их стимулирующее влияние на регенерацию костной ткани [29]. В настоящее время известно несколько видов коммерческих CP материалов, однако их клиническое применение ограничено [30]. Лучшее понимание механизмов взаимодействия с биологическими тканями поможет раскрыть их потенциал для создания новой рациональной стратегии репарации костей после повреждения [31].
ЗАКЛЮЧЕНИЕ
Проведенное на собаках экспериментальное исследование показало, что остеокондуктивность, остеоиндуктивность и биодеградация разработанных нами биогенных кальцийфосфатных материалов зависит от технологии их производства. СР материалы, близкие по составу к матриксу нативной костной ткани, могут быть использованы для стимуляции костеобразования. Для улучшения характеристик остеоиндуктивности и биосовместимости их можно сочетать с гомологич-
ными белками сыворотки крови. По нашему мнению, подобные материалы должны найти свое место в лечении костной патологии, включая повреждения костей скелета, на фоне выраженного остеопороза, а также заполнения посттравматических костных дефектов, кист или компенсации дефицита костной ткани в ходе костнопластических операций.
Список литературы Биосовместимость кальцийфосфатных материалов биогенного происхождения при имплантации в область дефектов костей собак
- Pili D., Tranquilli Leali P. Biomaterials and bone//Aging Clin. Exp. Res. 2011. Vol. 23, 2 Suppl. P. 74-75.
- Bone formation with two types of grafting materials: a histologic and histomorphometric study/A.R. Rokn, M.A. Khodadoostan, A.A. Reza Rasouli Ghahroudi, P. Motahhary, M.J. Kharrazi, H.D. Bruyn, R. Afzalifar, E. Soolar, A. Soolari//Open Dent. J. 2011. Vol. 5. P. 96-104.
- Habibovic P., de Groot K. Osteoinductive biomaterials -properties and relevance in bone repair//J. Tissue Eng. Regen. Med. 2007. Vol. 1, N 1. P. 25-32.
- Osteoinductive biomaterials: current knowledge of properties, experimental models and biological mechanisms/A.M. Barradas, H. Yuan, C.A. van Blitterswijk, P. Habibovic//Eur. Cell Mater. 2011. Vol. 21. P. 407-429.
- Davies J.E. Bone bonding at natural and biomaterial surfaces//Biomaterials. 2007. Vol. 28, N 34. P. 5058-5067.
- McKee M.D. Management of segmental bony defects: the role of osteoconductive orthobiologics//J. Am. Acad. Orthop. Surg. 2006. Vol. 14, 10 Spec. No. P. 163-167.
- El-Ghannam A. Bone reconstruction: from bioceramics to tissue engineering//Expert Rev. Med. Devices. 2005. Vol. 2, N 1. P. 87-101.
- Le Geros R.Z. Biodegradation and bioresorption of calcium phosphate ceramics//Clin. Mater. 1993. Vol. 14, N 1. P. 65-88.
- Perry C.C., Patwardhan S.V., Deschaume O. From biominerals to biomaterials: the role of biomolecule-mineral interactions//Biochem. Soc. Trans. 2009. Vol. 37, Pt. 4. P. 687-691.
- Demineralized bone matrix and hydroxyapatite/tri-calcium phosphate mixture for bone healing in rats/A. Oztürk, H. Yetkin, L. Memis, E. Cila, S. Bolukbasi, C. Gemalmaz//Int. Orthop. 2006. Vol. 30, N 3. P. 147-152.
- Back-scattered electron imaging and elemental analysis of retrieved bone tissue following sinus augmentation with deproteinized bovine bone or biphasic calcium phosphate/C. Lindgren, M. Hallman, L. Sennerby, R. Sammons//Clin. Oral Implants Res. 2010. Vol. 21, N 9. P. 924-930.
- Tissue responses of calcium phosphate cement: a study in dogs/H. Yuan, Y. Li, J.D. de Bruijn, K. de Groot, X. Zhang//Biomaterials. 2000. Vol. 21, N 12. P. 1283-1290.
- An animal model in sheep for biocompatibility testing of biomaterials in cancellous bones/K.M. Nuss, J.A. Auer, A. Boos, B. von Rechenberg//BMC Musculoskelet. Disord. 2006. Vol. 7. P. 67.
- Hannink G., Arts J.J. Bioresorbability, porosity and mechanical strength of bone substitutes: what is optimal for bone regeneration?//Injury. 2011. Vol. 42, Suppl. 2. P. S22-S25.
- Badylak S.F., Freytes D.O., Gilbert T.W. Extracellular matrix as a biological scaffold material: Structure and function//Acta Biomater. 2009. Vol. 5, N 1. P. 1-13.
- Carano R.A., Filvaroff E.H. Angiogenesis and bone repair//Drug Discov. Today. 2003. Vol. 8, N 21. P. 980-989.
- The role of angiogenesis in a murine tibial model of distraction osteogenesis/R.S. Carvalho, T.A. Einhorn, W. Lehmann, C. Edgar, A. Al-Yamani, A. Apazidis, D. Pacicca, T.L. Clemens, L.C. Gerstenfeld//Bone. 2004. Vol. 34, N 5. P. 849-861.
- Шевцов В.И., Ерофеев С.А., Шрейнер А.А. Рентгенологическая динамика формирования дистракционного регенерата при удлинении конечности в условиях восьмикратной дробности дистракции//Гений Ортопедии. 2003. № 2. С. 5-9.
- Handbook of Histology Methods for Bone and Cartilage/Eds. H.A. Yuehuei, L.M. Kylie. Totowa-New Jersey: Humana Press Inc., 2003.
- Glantz S. Primer of Biostatistics. 6rd ed. New York: McGraw-Hill, 2005.
- Multiscale osteointegration as a new paradigm for the design of calcium phosphate scaffolds for bone regeneration/S.K. Lan Levengood, S.J. Polak, M.B. Wheeler, A.J. Maki, S.G. Clark, R.D. Jamison, A.J. Wagoner Johnson//Biomaterials. 2010. Vol. 31, N 13. P. 3552-3563.
- Phase composition, mechanical performance and in vitro biocompatibility of hydraulic setting calcium magnesium phosphate cement/U. Klammert, T. Reuther, M. Blank, I. Reske, J.E. Barralet, L.M. Grover, A.C. Kübler, U. Gbureck//Acta Biomater. 2010. Vol. 6, N 4. P. 1529-1535.
- Bohner M., Baumgart F. Theoretical model to determine the effects of geometrical factors on the resorption of calcium phosphate bone substitutes//Biomaterials. 2004. Vol. 25, N 17. P. 3569-3582.
- An in vitro evaluation of the Ca/P ratio for the cytocompatibility of nano-to-micron particulate calcium phosphates for bone regeneration/H. Liu, H. Yazici, C. Ergun, T.J. Webster, H. Bermek//Acta Biomater. 2008. Vol. 4, N 5. P. 1472-1479.
- The effects of calcium phosphate cement particles on osteoblast functions/D.P. Pioletti, H. Takei, T. Lin, P. Van Landuyt, Q.J. Ma, S.Y. Kwon, K.L. Sung//Biomaterials. 2000. Vol. 21, N 11. P. 1103-1114.
- Wang H., Lee J.K., Moursi A., Lannutti J.J. Ca/P ratio effects on the degradation of hydroxyapatite in vitro. J Biomed Mater Res A. 2003 Nov 1;67(2):599-608.
- Combes C., Rey C. Adsorption of proteins and calcium phosphate materials bioactivity//Biomaterials. 2002. Vol. 23, N 13. P. 2817-2823.
- Bab I., Chorev M. Osteogenic growth peptide: from concept to drug design//Biopolymers. 2002. Vol. 66, N 1. P. 33-48.
- Al-Sanabani J.S., Madfa A.A., Al-Sanabani F.A. Application of calcium phosphate materials in dentistry//Int. J. Biomater. 2013. Vol. 2013. P. 876132 DOI: 10.1155/2013/876132
- Larsson S., Hannink G. Injectable bone-graft substitutes: current products, their characteristics and indications, and new developments//Injury. 2011. Vol. 42, Suppl. 2. P. S30-S34.
- Kanczler J.M., Oreffo R.O. Osteogenesis and angiogenesis: the potential for engineering bone//Eur. Cell Mater. 2008. Vol. 15. P. 100-114.


