Численное моделирование течения жидкости в венозном клапане при пробе Вальсальвы
Автор: Гатаулин Я.А., Никитин Е.Д., Юхнев А.Д., Росуховский Д.А.
Журнал: Российский журнал биомеханики @journal-biomech
Статья в выпуске: 3 (97) т.26, 2022 года.
Бесплатный доступ
Работа посвящена численному исследованию течения жидкости в венозном клапане при пробе Вальсальвы. Данная проба является нагрузочной процедурой, а именно комплексом дыхательных действий, используемым врачами-флебологами для ультразвуковой диагностики клапанной несостоятельности. Измеряемая характеристика при пробе Вальсальвы - длительность обратного кровотока, возникающего во время закрытия клапана, по которой врач делает заключение о смыкаемости створок клапана. В работе построена численная модель венозного клапана подколенной вены на основе клинических данных. Решались нестационарные уравнения гидродинамики и движения упругой створки, при этом проба Вальсальвы моделировалась импульсным перепадом давления на входной границе участка вены с клапаном. Получены данные о поле скорости, продолжительности обратного течения, объеме утечек для разной упругости клапана, в том числе для здорового клапана и клапана с несостоятельностью. Для модели здорового клапана длительность обратного течения составила менее 1 с, а для несостоятельного клапана - более 1 с, что соответствует клиническим данным. Результаты расчетов могут быть использованы врачами-флебологами для уточнения процедуры диагностики клапанной несостоятельности.
Венозный клапан, численное моделирование, fluid-structure interaction, гемодинамика, проба вальсальвы
Короткий адрес: https://sciup.org/146282602
IDR: 146282602 | УДК: 531/534: | DOI: 10.15593/RZhBiomeh/2022.3.06
Numerical simulation of the flow through venous valve during a Valsalva maneuver
The paper presents the results of a numerical study of the flow in a model of popliteal venous valve during the Valsalva maneuver. During this procedure the increased intrathoracic pressure is transmitted from vena cavae back to venous valves causing venous reverse flow (reflux). The duration of reflux measured by ultrasound method is typically used to diagnose the presence of reflux. Reflux duration longer than 1 s of for deep veins implies valve incompetence. Numerical model of the venous valve of the popliteal vein was built on the basis of clinical data. Non-stationary equations of hydrodynamics and an elastic leaflets movement were solved. The Valsalva maneuver was simulated with the pressure impulse at the inlet boundary. Numerical data were obtained for the velocity field, the duration of the reverse flow, the reflux for different leaflet elasticity, including a healthy valve and a valve with incompetence. For a healthy valve model, the reflux duration was less than 1 s, and for an incompetent valve, it was more than 1 s. It corresponds with the clinical results. The obtained results can be used by phlebologists to improve the ultrasound diagnostics of valve incompetence.
Текст научной статьи Численное моделирование течения жидкости в венозном клапане при пробе Вальсальвы
Уильям Гарвей почти 400 лет назад доказал, что здоровый (состоятельный) венозный клапан играет ключевую роль в односторонней циркуляции крови. Данное наблюдение лежит в основе современного понимания кровообращения. Однако мало что известно о механизме работы венозных клапанов. Функция вен состоит в беспрепятственном проведении крови по направлению к сердцу и недопущении обратного ее тока [21]. Данная функция обеспечивается клапанами в просвете вены и нарушается, если створки клапана закрываются не полностью или слишком медленно, пропуская значительный объем крови в обратном направлении. В последнее время для диагностики этих нарушений применяется ультразвуковое доплеровское исследование для оценки величины и направления скорости кровотока, однако возможности такой диагностики ограничены. Створки настолько тонкие, что их не удается визуализировать, и единственный параметр, используемый врачами сегодня для оценки функции клапана, – это длительность обратного тока крови. Ее измерение проводится во время нагрузочных функциональных тестов, создающих импульс обратного перепада давления. Самый простой из них, так называемая проба Вальсальвы, или проба с натуживанием, состоит в кратковременном повышении давления на выхо-
5202-6398


Эта статья доступна в соответствии с условиями лицензии Creative Commons Attribution-NonCommercial 4.0 International
License (CC BY-NC 4.0)
This work is licensed under a Creative Commons Attribution-NonCommercial 4.0 International License (CC BY-NC 4.0)
де из клапана, которое вызывает его закрытие на период проведения пробы [11; 17; 27]. Для здорового венозного клапана проба приводит к полной остановке венозного кровотока после кратковременного обратного тока крови (менее 1 c), а для больного – обратный ток крови наблюдается более 1 с. Отсутствие возможности визуализировать движение неизмененных створок клапана и отсутствие достоверной информации о значении других характеристик кровотока, таких как объемная и пиковая скорость, создают предпосылки для математического моделирования недостающих звеньев в понимании этого фундаментального биологического процесса.
Математическое моделирование кровотока при пробе Вальсальвы выполняется в основном с помощью модели сосредоточенных параметров. Такой подход заключается в создании, подобно электрической схеме, разветвленной сети кровеносных сосудов – артерий и вен, и получении на ее основе информации о базовых характеристиках – расходах и давлениях – на каждом участке этой сети [12; 15; 19; 22; 23; 26]. Авторами этих работ смоделирована реакция отдельных частей кровеносной системы на пробу Вальсальвы при нормальных и патологических условиях, таких как, например, сердечная недостаточность, дыхательная синусовая аритмия и т.д. Однако полезная врачам локальная информация о течении – расположении и размерах застойных областей, областей турбулизации, зонах с критическими значениями давлений и сдвиговых напряжений, может быть получена только из двумерного или трехмерного численного моделирования. Существует большое количество таких публикаций для венозных клапанов в тех или иных физиологических состояниях в зависимости от упругости створок клапана, от действия окружающих вену мышц и т.д. [2; 3; 6; 8; 9; 20; 29; 28; 31]. Ранее авторами статьи были разработаны модели здорового и несостоятельного клапана подколенной вены, исследовано влияние упругости створок на поле скорости и застойную область за створками клапана [14; 30]. На основе данной модели было рассчитано течение в клапане после хирургической операции экстравазальной коррекции [13]. Результаты расчетов показали хорошее согласие с клиническими данными по амплитуде колебаний створок, положению и размерам застойной области. Работ, в которых проведено численное моделирование течения в венозном клапане при пробе Вальсальвы, авторами не обнаружено.
Цель работы – исследовать влияние упругости створок на поле скорости, продолжительность и объем обратного кровотока при пробе Вальсальвы с помощью численного моделирования течения в клапане подколенной вены.
Материалы и методы
Объектом исследования в данной работе является клапан подколенной вены человека [10; 18; 24]. Подколенная вена относится к глубоким венам. Она располо- жена между бедренной веной и венами голени. Ее длина составляет около 8 см. Известно, что в подколенной вене встречается 2–3 клапана, два из которых расположены в ее истоке и устье. Чаще всего венозные клапаны являются двустворчатыми. Доля одно- и трехстворчатых клапанов составляет менее 20 %. В работе рассматривается клапан, расположенный примерно посередине подколенной вены, и поэтому условия разветвления потока оказывают минимальное влияние на кровоток в нем. Интерес врачей к подколенной вене связан с опасностью тромбозов, которые чаще всего поражают глубокие вены нижних конечностей.
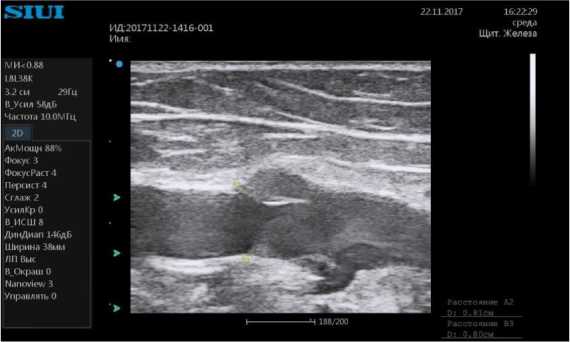
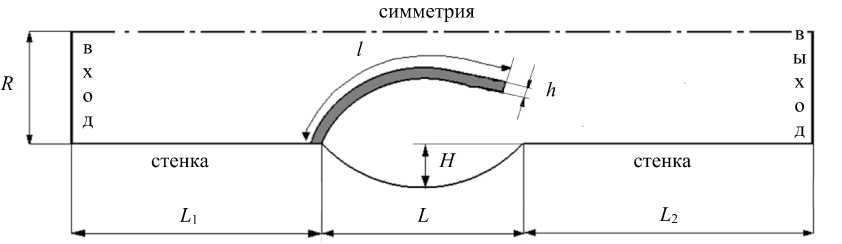
Модель клапана подколенной вены построена на основе собственных клинических измерений в плоскости симметрии клапана (рис. 1, а ). Геометрическая модель клапана характеризуется радиусом вены R , длиной l и толщиной створки h , длиной L и глубиной H синуса (расширения за клапаном). Длины областей перед клапаном L 1 и за клапаном L 2 – взяты достаточными для того, чтобы не оказывать существенного влияния на течение в клапане. Численные значения указанных параметров приведены в табл. 1. Построенная модель является симметричной. Данное допущение оправдано тем, что поток в клапане близок к плоскому, благодаря вытянутой форме створок в нормальном к центральной плоскости направлении. Кроме того, введенное допущение симметрии течения относительно оси вены исходит из того, что клапан является двустворчатым.
Таблица 1
Геометрические параметры модели клапана подколенной вены
|
R , мм |
L 1 , мм |
L 2 , мм |
L , мм |
H , мм |
h , мм |
l , мм |
|
5 |
25 |
36 |
9 |
2 |
0,5 |
10 |
Проведен сопряженный расчет течения жидкости и движения упругой створки с помощью технологии fluidstructure interaction (FSI) в обобщенной лагранже-эйлеровской постановке. Гидродинамические расчеты выполнялись в Ansys Fluent , механические – в Ansys Mechanical . Связка двух систем происходила в System Coupling в среде Ansys Workbench .
Течение жидкости моделируется с помощью уравнений движения вязкой несжимаемой жидкости (уравнений Навье – Стокса) (1)–(2):
μ
— + ((V - V m ) -V ) V =-- V p + f- V V 2 V . (1)
5 t p f p f
V- V = 0, (2)
б
Рис. 1. Изображение клапана подколенной вены в B -режиме ( а ) и расчетная область (половина геометрической модели симметричного венозного клапана) ( б )
где V - скорость жидкости в узлах динамической сетки,
Vm - скорость узлов расчетной сетки в точке, рf и цf -плотность и вязкость жидкости; рf = 1060 кг/м3, цf = 0,004 Па^с [1]. Характерное число Рейнольдса, построенное по диаметру вены и скорости течения в состоянии покоя, равно 132.
Движение створки моделируется с помощью уравнений эластодинамики для линейного однородного изотропного материала (3):
d2 d
Р = v 2 + Р fb, (3)
где d - перемещение створки, f ъ- массовая сила со стороны жидкости, § = ^( V d + ( v d ) ) - тензор деформаций, 2 - тензор напряжений, 2 = 2ц§ + 1 X tr (§) -уравнение состояния, X, ц - коэффициенты Ламэ. Эти параметры удовлетворяют следующим соотношениям (4):
. E v E
X =-------------- , ц =------- ,
(1 + v)(1 - 2v) 2(1 + v)
где E - модуль Юнга, v - коэффициент Пуассона. Механические свойства створки клапана взяты из расчет- ных работ, использующих двумерные модели клапанов [7; 29]: E = 0,2-20 МПа, v = 0,45, р = 1200 кг/м3. При разработке математических моделей в указанных исследованиях значения модуля Юнга подбирались с целью обеспечения открытия створки клапана в физиологическом диапазоне. Отметим, что измеренный модуль Юнга для здорового бычьего венозного клапана имеет значение около 10 МПа при радиальном растяжении [4].
На входной границе для расчета течения в модели здорового венозного клапана в состоянии покоя задавалась постоянная во времени среднерасходная скорость Vb 0 = 0,05 м/с [30] с плоским профилем, в расчетах с пробой Вальсальвы - импульсное изменение давления во времени A p ( t ) (рис. 4), на выходе - нулевое противодавление. На верхней границе задано условие симметрии, на нижней - условие прилипания. Стенка вены моделировалась абсолютно жесткой ввиду малости ее перемещений. На поверхности створки задавалось условие сопряжения между твердой и жидкой областями (5):
ГГ ГГ Г Г ds = df, Vs = Vf, Fs = Ff, (5)
где d - перемещение, V - скорость, F - усилие.

а

б
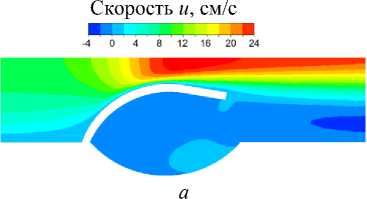
Рис. 2. Расчетные гидродинамическая и механическая сетки в фазы открытого ( а ) и закрытого ( б ) клапана
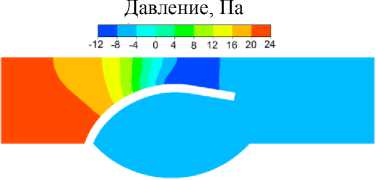
Рис. 3. Поля продольной скорости ( а ) и давления ( б ) в модели здорового венозного клапана в состоянии покоя ( E = 0,2 МПа)
На рис. 2 показаны расчетные гидродинамическая и механическая сетки в два момента времени. Сетки построены в программе Ansys Meshing. Проведены исследования на чувствительность результатов расчета к размеру сеток и шага по времени. Гидродинамическая сетка состояла из 64 558 треугольных элементов и имела сгущение к створке клапана и стенке вены. Механическая сетка состояла из 500 прямоугольных элементов. Для настройки гидродинамической сетки использовались алгоритмы Smoothing и Remeshing, которые осуществляют сглаживание и перестроение сетки и устраняют в процессе расчета появление вырожденных ячеек сетки, приводящих к остановке расчета. Решалась контактная задача о соударении створок венозного клапана, при этом вторая створка заменялась при моделировании контакта прямой пластинкой и располагалась вдоль оси вены. Шаг по времени составлял 0,01 с, на этапе решения контактной задачи временной шаг уменьшался до 0,001 с.
Результаты
Известно, что в состоянии покоя створки здорового клапана не смыкаются, полуширина проходного сечения составляет около 30 % от радиуса, а течение ввиду малых частоты и амплитуды колебаний створок практически не отличается от течения с постоянным расходом [21]. На входной границе модели задавалась постоянная во времени среднерасходная скорость Vb0 = 0,05 м/с [30]. Для получения в модели положения створки в состоянии покоя, соответствующего физиоло- гическому диапазону, расчеты проводились для разных значений модуля Юнга E створки в диапазоне 0,2–20 МПа. Расчеты начинались от заданного начального поля скорости в виде покоящейся жидкости и начального положения створки в закрытом состоянии и длились, пока клапан не откроется и характеристики течения, и положение створки не перестанут меняться во времени.
В результате расчетов было установлено, что при значении модуля Юнга E = 0,2 МПа открытие клапана соответствует физиологическому – расстояние от створки до оси составляет 30 % радиуса [21], продолжительность перехода на установившееся течение T 1 = 1 c, а перепад давления на клапане ∆ p 1 = 22 Па. На рис. 3 показаны рассчитанные для состояния покоя клапана поля продольной скорости ( а ) и давления ( б ).
Выполнены расчеты течения в модели здорового венозного клапана для граничных условий, соответствующих пробе Вальсальвы. Данные граничные условия реализуются при импульсном изменении давления на входной границе, которое состоит из трех временных участков (рис. 4). Первый – длительностью T 1 и с постоянным положительным перепадом давления ∆ p 1 – соответствует течению в состоянии покоя клапана. Указанные характеристики были получены из предыдущего расчета течения в здоровом венозном клапане в состоянии покоя. Второй участок – длительностью T 2 и с постоянным отрицательным перепадом давления ∆ p 2 – соответствует условиям пробы Вальсальвы. В начале и в конце этого участка давление линейно меняется между постоянными уровнями ∆ p 2 и ∆ p 1 в течение короткого промежутка времени τ. Третий участок – длительностью T 3 и с постоянным положительным перепадом
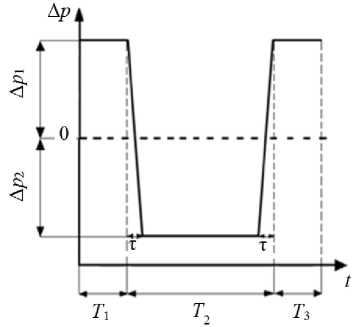
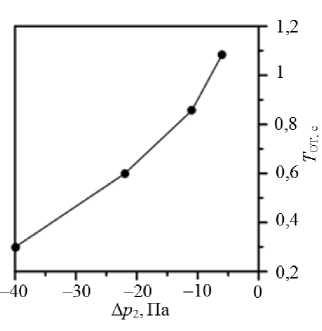
Рис. 4. Давление на входной границе участка вены Рис. 5. Зависимость длительности обратного течения с клапаном (импульсный перепад давления), моде- от величины обратного перепада давления лирующее пробу Вальсальвы
Скорость u , см/с Скорость u , см/с
.^™ 1 -24 -21 -13 -15 -12 -9-6-3 0 3

а б
Рис. 6. Поля продольной скорости для клапанов с модулем Юнга E = 0,2 МПа ( а ) и 20 МПа ( б ) в момент времени, соответствующий середине длительности пробы Вальсальвы
давления ∆ p 1 – соответствует возвращению течения к состоянию покоя. Известно, что длительность обратного течения при пробе Вальсальвы в здоровом венозном клапане составляет менее 1 с [11]. Перепад давления ∆p 2 варьировался в диапазоне от –5 до –40 Па с целью получения длительности обратного течения, близкой к соответствующему значению для здорового венозного клапана (0,5 с) [11]. Результаты расчета показаны на рис. 5.
Получено, что для значения ∆ p 2 = –22 Па длительность обратного течения составила 0,6 с, что близко к физиологическому значению, поэтому данное значение ∆ p 2 было выбрано для исследования влияния упругости створок на течение в клапане при пробе Вальсальвы. Численные значения рассчитанных параметров пробы Вальсальвы приведены в табл. 2.
Таблица 2
Параметры импульсного изменения давления на входной границе участка вены с клапаном (проба Вальсальвы)
|
T 1 , c |
T 2 , c |
T 3 , c |
τ, c |
∆ p 1 , Па |
∆ p 2 , Па |
|
1 |
3 |
1 |
0,3 |
22 |
–22 |
Для импульсного изменения давления с параметрами пробы Вальсальвы (табл. 2) выполнено исследование влияния модуля Юнга створки клапана в диапазоне от 0,2
до 20 МПа на продолжительность обратного течения T от , время закрытия клапана T закр и относительный объем утечек через клапан V от (отношение объема утечек к объему прямого тока в состоянии покоя за время пробы Вальсальвы), который рассчитывался следующим образом:
V т = J V b dt / ( V b 0 Т ) , (6)
( Тг)
где V b – среднерасходная скорость течения, V b 0 – среднерасходная скорость течения в состоянии покоя, T 2 – длительность пробы Вальсальвы.
Нужно отметить, что относительный объем утечек может быть рассчитан по результатам ультразвуковых измерений и использоваться как дополнительный параметр наряду с продолжительностью обратного тока для диагностики венозных клапанов.
На рис. 6 показаны распределения продольной скорости для клапанов с разными модулями Юнга в момент времени, соответствующий середине длительности пробы Вальсальвы (2,5 с). В клапане с E = 0,2 МПа створки закрыты, а с E = 20 МПа створки открыты, и скорость обратного тока между створками равна 24 см/с.
На рис. 7, слева, изображены расчетные изменения среднерасходной скорости во времени для клапанов с разными модулями Юнга. В течение первой секунды прямой поток через рассмотренные модели клапана нарастает, достигая установившегося состояния. В мо- а
б
в
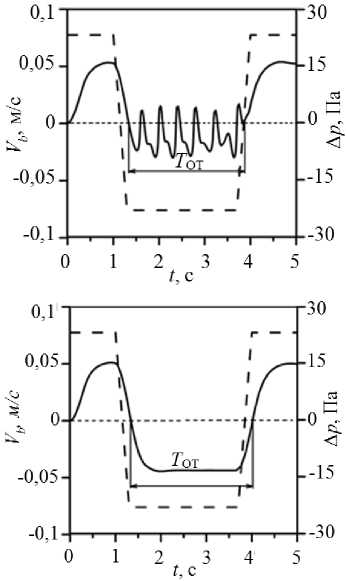
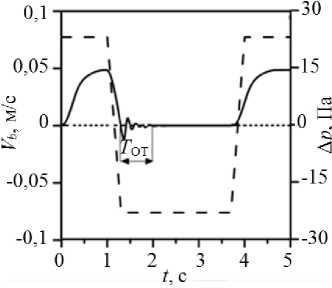
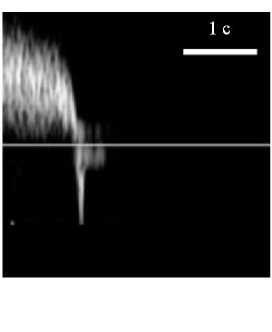
Рис. 7. Изменения среднерасходной скорости (сплошная линия) для здорового клапана (0,2 МПа) ( а ), несостоятельных клапанов 2 МПа ( б ) и 20 МПа ( в ) при воздействии обратного перепада давления (пунктирная линия) при пробе Вальсальвы (результаты собственных расчетов и ультразвуковые доплеровские измерения скорости кровотока [5; 16; 25])
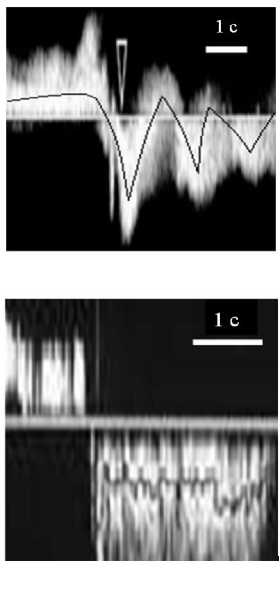
мент времени начала пробы Вальсальвы (t = 1 c) клапаны открыты. Для клапана с E = 0,2 МПа наблюдаем, что длительность обратного течения Tот = 0,6 с, что соответствует доплерограмме здорового клапана (рис. 7, а, справа) [25]. Напротив, для клапана с E = 20 МПа наблюдаем, что длительность обратного течения Tот = 2,7 с равняется времени действия обратного перепада давления при пробе Вальсальвы, что соответствует до-пплерограмме для несостоятельного клапана (рис. 7, в, справа) [16]. Промежуточный случай модели клапана, с упругостью створки 2 МПа, реализует достаточно интересную реакцию клапана на пробу Вальсальвы, при которой створки в течение всей пробы полностью не смыкаются, а совершают колебательное, медленно затухающее движение, то открывая, то закрывая клапан (рис. 7, б, слева). Этот вариант также находит свое подтвер ждение в клинических наблюдениях (рис. 7, б, справа) [5]. На рис. 8 показаны рассчитанные значения продолжительности обратного течения и относительного объема утечек. Для случаев 0,2 и 20 МПа продолжительность обратного течения и объем утечек приводят к качественно одинаковым результатам - малые Тот (<1 с) и большие значения Vот (> 0,5) соответственно. Однако в случае с E = 2 МПа картина противоположная: продолжительность обратного течения большая (Тот = 2,5 с), а объем утечек - малый (Vот = 0,19). Данный результат можно объяснить тем, что продолжительность обратного течения рассчитывается от начала и до завершения обратного течения, без учета внутренних промежутков прямого течения, в то время как объем утечек, будучи интегральной величиной, учитывает разницу объема прямого и обратного тока за это время.
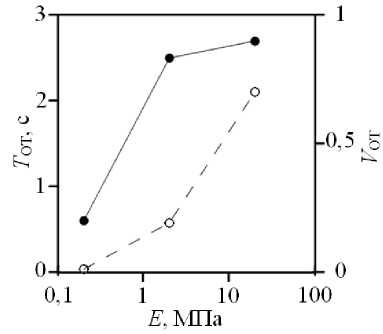
Рис. 8. Продолжительность обратного течения (черные точки) и относительный объем утечек (белые точки) для клапанов с разными модулями Юнга
Клапан полностью закрывался из рассмотренных случаев только при E = 0,2 МПа, время закрытия клапана Tзакр, полученное из анализа перемещения створки, составило 0,4 с – это в 1,5 раза меньше, чем продолжительность обратного течения. Данный результат объясняется тем, что после смыкания створки клапана выгибаются, увеличивая площадь соприкосновения (коапта- ция створок) и еще некоторое время проталкивая жидкость в направлении обратного течения.
Заключение
Впервые разработана вычислительная модель для исследования течения в венозном клапане подколенной вены при пробе Вальсальвы. Разработанная модель течения протестирована по длительности обратных токов с использованием результатов ультразвуковых доплеровских измерений скорости кровотока для здорового и несостоятельного клапана. Для модели здорового клапана длительность обратного тока была меньше 1 с, а для несостоятельного клапана – больше 1 с, что соответствует клиническим результатам. Для модели несостоятельных клапанов обнаружено два режима движения створок при проведении пробы Вальсальвы – постоянно открытое состояние и колебания с периодическим закрытием-открытием. В перспективе разработка трехмерной модели венозного клапана позволит уточнить обнаруженные эффекты и закономерности.
Vol. 35, no. 2. – P. 1–21.
Финансирование. Работа выполнена при финансовой поддержке Минобрнауки России в рамках госзадания «Изучение регуляторных механизмов сердечно-сосудистой, нервной и дыхательной систем для разработки новых подходов к выявлению ортостатических расстройств и вегетативной дисрегуляции при колебательных постуральных нагрузках» (№ 122020300239–8).
Результаты получены при использовании ресурсов СКЦ «Политехнический» СПБПУ.
Список литературы Численное моделирование течения жидкости в венозном клапане при пробе Вальсальвы
- Левтов В.А., Регирер С.А., Шадрина Н.Х. Реология крови. - М.: Медицина, 1982. - 270 с.
- Ariane M., Wen W., Vigolo D., Brill A., Nash F.G.B., Barigou M., Alexiadis A. Modelling and simulation of flow and agglomeration in deep veins valves using discrete multi physics // Computers in Biology and Medicine. - 2017. -Vol. 89. - P. 96-103.
- Ariane M., Vigolo D., Brill A., Nash F.G.B., Barigou M., Alexiadis A. Using discrete multi-physics for studying the dynamics of emboli in flexible venous valves // Computers and Fluids. - 2018. - Vol. 166. - P. 57-63.
- Benson, A.A., Huang H.-Y.S. Tissue level mechanical properties and extracellular matrix investigation of the bovine jugular venous valve tissue // Bioengineering. - 2019. -Vol. 6, iss. 2. - P. 1-15.
- Bertolotto M., Simon F., Richenberg J., Belfield J., Dogra V., et al. Ultrasound evaluation of varicoceles: systematic literature review and rationale of the ESUR-SPIWG Guidelines and Recommendations // Journal of Ultrasound. - 2020. - Vol. 23. - P. 487-507.
- Buxton G., Clarke N. Computational phlebology: the simulation of a vein valve // Journal of Biological Physics. -2006. - Vol.32. - P. 507-521.
- Calandrini S., Aulisa E. Fluid-structure interaction simulations of venous valves: A monolithic ALE method for large structural displacements // International Journal for Numerical Methods in Biomedical Engineering. - 2019. -Vol. 35, no. 2. - P. 1-21.
- Chen H., Berwick Z., Krieger J., Chambers S., Lurie F., Kassab G. Biomechanical comparison between mono-, bi-, and tricuspid valve architectures // Journal of Vascular Surgery: Venous and Lymphatic Disorders. - 2014. - Vol. 2. -P. 188-193.
- 9. Chen H.Y., Tien W-S., Chambers S.D., Dabiri D., Kassab G.S. Search for an optimal design of a bioprosthetic venous valve: in silico and in vitro studies // European Journal of Vascular and Endovascular Surgery. - 2019. - Vol. 58. - P. 112-119.
- 10. Caggiati A. The venous valves of the lower limb // Phlebo-lymphology. - 2013. - Vol. 20, no. 2. - P. 87-95.
- 11. De Maeseneer M., Pichot O., Cavezzi A. Duplex ultrasound investigation of the veins of the lower limbs after treatment for varicose veins e UIP Consensus Document // European Journal of Vascular and Endovascular Surgery. - 2011. -Vol. 42. - P. 89-102.
- 12. Garcia M.I.M., Cano A.G., Monrove J.C.D. Arterial pressure changes during the Valsalva maneuver to predict fluid responsiveness in spontaneously breathing patients // Intensive Care Medicine. - 2009. - Vol. 35. - P. 77-84.
- 13. Gataulin Y.A., Yukhnev A.D., Rosukhovskiy D.A. Numerical analysis of the flow in the model of a venous valve: normal and surgical correct // Journal of Physics: Conference Series. - 2021. - Vol. 2103. - P. 1-6.
- 14. Gataulin Y.A., Yukhnev A.D., Smirnov S.I., Rosukhovskiy D.A. Numerical analysis of the leaflet elasticity effect on the flow in the model of a venous valve // Journal of Physics: Conference Series. - 2019. - Vol. 1359. - P. 1-6.
- 15. Hemalatha K., Manivannan M. Valsalva Maneuver for the analysis of interaction hemodynamic - Model study // 2010 International Conference on Recent Trends in Information, Telecommunication and Computing. - 2010. - P. 28-32.
- 16. Jeanneret C., Aschwanden M., Labs K.H., Jager K. Duplex ultrasound for the assessment of venous reflux // Current Problems in Dermatology. - 1999. - Vol. 27. - P. 102-108.
- 17. Jeanneret C., Jäger K.A., Zaugg C.E., Hoffmann U. Venous reflux and venous distensibility in varicose and healthy veins // European Journal of Vascular and Endovascular Surgery. - 2007. - Vol. 34, no. 2. - P. 236-242.
- 18. Langevelde K., Sramek A., Rosendaal F.R. The effect of aging on venous valves // Arteriosclerosis, Thrombosis and Vascular Biology. - 2010. - Vol. 30. - P. 2075-2080.
- 19. Liang F., Liu H. Simulation of hemodynamic responses to the Valsalva maneuver: an integrative computational model of the cardiovascular system and the autonomic nervous system // The Journal of Physiological Sciences. - 2006. -Vol. 56. - P. 45-65.
- 20. Liu X., Liu L. Effect of valve lesion on venous valve cycle: a modified immersed finite element modeling // PLoS ONE. -2021. - Vol. 14, no. 3. - P. 1-26.
- 21. Lurie F., Kistner R.L., Eklof B., Kessler D. Mechanism of venous valve closure and role of the valve in circulation: a new concept // Journal of Vascular Surgery. - 2003. - Vol. 38. - P. 955-961.
- 22. Lu K., Clark J.W., Ghorbel F.H., Ware D.L., Bidani A. A human cardiopulmonary system model to the analysis of the Valsalva maneuver // The American Journal of Physiology -Heart and Circulatory Physiology. - 2001. - Vol. 281. -P. 2661-2679.
- 23. Moberg N. Hemodynamic model of the cardiovascular system during Valsalva maneuver and orthostatic changes. -Master's Thesis, Umea University Department of Engineering Physics, UMEA SWEDEN, 2011. - 89 p.
- 24. Moore H.M., Gohel M., Davies A.H. Number and location of venous valves within the popliteal and femoral veins – a review of the literature // Journal of Anatomy. - 2011. - Vol. 219, no. 4. - P.439-443.
- 25. Necas M. Duplex ultrasound in the assessment of lower extremity venous insufficiency // Australasian Journal of Ultrasound in Medicine. - 2010. - Vol. 13, no. 4. - P. 37-45.
- 26. Randall E.B., Billeschou A., Brinth L.S., Mehlsen J., Olufsen M.S. A model-based analysis of autonomic nervous function in response to the Valsalva maneuver // Journal of Applied Physiology. - 2019. - Vol. 127. - P. 1386-1402.
- 27. Ricci S., Moro L., Minotti G.C., Incalzi R.A., Maeseneer M.D. Valsalva maneuver in phlebologic practice // Phlebology. - 2017. - Vol. 38, no. 2. - P. 1-9.
- 28. Simao M., Ferreira J.M., Mora-rodriguez J., Ramos H.M. Identification of DVT diseases using numerical simulations // Medical and Biological Engineering and Computing. -2016. - Vol. 54. - P. 1591-1609.
- 29. Soifer E., Weiss D., Marom G., Einav S. The effect of pathologic venous valve on neighboring valves: fluid-structure interactions modeling // Medical and Biological Engineering and Computing. - 2017. - Vol. 55, no. 6. - P. 991-999.
- 30. Tikhomolova L.G., Gataulin Y.A., Yukhnev A.D., Rosukhovskiy D.A. Fluid-structure interaction modelling of the venous valve with elastic leaflets // Journal of Physics: Conference Series. - 2020. - Vol. 1697. - P. 1-6.
- 31. Zervides C., Giannoukas A.D. Computational phlebology: reviewing computer models of the venous system // Phlebology. - 2013. - Vol. 28. - P. 209-218.


