Чрескожные коронарные вмешательства у больных гемобластозами
Автор: Гительзон Е.А., Файбушевич А.Г., Гительзон Д.Г., Веретник Г.И.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Обзоры литературы
Статья в выпуске: 4 т.15, 2020 года.
Бесплатный доступ
Усовершенствование диагностических и лечебных схем для больных гемобластозами позволило повысить уровень выживаемо сти среди этих пациентов. Однако в клинической практике наблюдается тенденция к увеличению количества пациентов с сочетанием ИБС и гемобластоза. В большинстве случаев наличие конкурирующей ИБС у онкогематологических больных осложняет лечение основного заболе вания. Кардиотоксичность химиотерапии может стать потенциальной причиной прерывания или прекращения противоопухолевого лечения, потенциально ухудшая «общий» прогноз жизни. До сих пор нет ясности по проведению чрескожных коронарных вмешательств у больных гемо бластозами, так в литературе представлены лишь отдельные описания случаев.
Ишемическая болезнь сердца, гемобластоз, чрескожное коронарное вмешательство
Короткий адрес: https://sciup.org/140260064
IDR: 140260064 | DOI: 10.25881/BPNMSC.2020.97.92.015
Percutaneous coronary intervention in patients with blood malignancy
Improvement of diagnostic and treatment regimens for patients with blood malignancies allowed increasing the survival rate among these patients. However, there is a tendency to increase the number of patients with a combination of coronary artery disease and blood malignancy in clinical practice. In most cases, the presence of competing coronary artery disease in oncohematologic patients complicates the treatment of the underlying disease. Cardiotoxicity of chemotherapy can be a cause of interruption or termination of anti-tumor treatment, potentially worsening overall outcomes. Until now it is not clear about percutaneous coronary interventions in patients with blood malignancy.
Текст научной статьи Чрескожные коронарные вмешательства у больных гемобластозами
Усовершенствование схем лечения больных гемобластозами, появление новых лекарственных препаратов, прицельно поражающих опухолевые клетки, разработка и синтез факторов свертывания крови позволили увеличить продолжительность жизни онкогематологических пациентов и изменить ее качество. Это неизбежно сопровождается развитием характерных для их возрастных групп заболеваний, встречающихся в общей популяции и требующих хирургического вмешательства, в том числе становятся крайне актуальными кардиоваскулярные осложнения. В первую очередь речь идет об увеличении количества больных гемобластозами в сочетании с ИБС. В большинстве случаев наличие конкурирующей ИБС у онкогематологических больных осложняет лечение основного заболевания. В первое полугодие после верификации онкологического диагноза значительно увеличивается риск развития и прогрессирования ИБС.
В настоящее время проведено мало исследований, посвященных изучению эффективности чрескожного коронарного вмешательства (ЧКВ) у онкогематологиче-ских больных. Следует учитывать, что все исследования выполнены на недостаточно большом количестве пациентов, что не позволяет определить четкие рекомендации по выполнению ЧКВ у данной категории больных.
Во время проведения ЧКВ у онкогематологического больного перед доктором всегда возникает вопрос о выборе типа стента: с лекарственным покрытием или без него. Не решен также вопрос о безопасности и сроках назначения антиагрегантной терапии онкогематологиче-ским больным. Используемые в лечении цитостатические лекарственные препараты могут увеличивать время эн-дотелизации стента. Многие химиопрепараты повышают риск тромбообразования у этих больных. Это требует к каждому пациенту индивидуального подхода с учетом риска тромбоза стента и/или кровотечения.
Кардиотоксичность противоопухолевой химиотерапии, как фактор развития сердечно-сосудистых осложнений
Достижения последних лет в медицине определили основные направления исследований по созданию новых лекарственных средств для противоопухолевой терапии. Cпектр лекарств для лечения онкогематологических заболеваний значительно расширился благодаря активной разработке новых способов противоопухолевой терапии, которые обладают специфической направленностью, что позволяет избирательно поражать опухолевые клетки. Но следует учитывать, что при лечении онкогематоло-гических пациентов применяются многокомпонентные схемы химиотерапии и нередко в сочетании с лучевым

воздействием. В целом противоопухолевая терапия направлена на подавление пролиферации и индуцирование клеточного апоптоза, вследствие этого под колоссальное токсическое воздействие попадают не только опухолевые, но и здоровые ткани организма, в том числе и миокард.
Под кардиотоксичностью понимают развитие нежелательных сердечно-сосудистых проявлений как на фоне противоопухолевого лечения, так и после его окончания. В результате действия химиотерапевтических лекарственных средств могут развиваться различные виды повреждений сердца, такие как его дисфункция и сердечная недостаточность, артериальная гипертензия, тромбоэмболические и вазоспастические явления, аритмии сердца, ишемия и инфаркт миокарда [8]. Развитие кардиотоксических побочных эффектов от химиотерапии зависит от нескольких факторов, таких как выбор лекарственного средства, дозировка, интервал введения, совокупная доза, способ введения и связь с лучевой терапией [44; 63].
В литературе встречаются сообщения об острых коронарных событиях, вызванных применением различных химиотерапевтических лекарственных средств [68]. Описаны несколько механизмов развития этих событий: вазоспастические процессы, цитотоксическое воздействие на эндотелий и митохондрии, остановка клеточного цикла эндотелиальных клеток сердца и даже выброс цитокинов, приводящий к разрыву бляшки и активации тромбоцитов. Коронарный вазоспазм является одним из наиболее часто отмеченных побочных эффектов химиотерапии, который может привести к ишемии или инфаркту миокарда. Широко варьируется и временной интервал начала ишемического процесса. По данным Mandel E.M. и соавт., винкристин может вызывать это осложнение в течение нескольких часов после инфузии [45]. Ритуксимаб также провоцирует развитие постинфузионного инфаркта миокарда, начало которого варьируется от момента инфузии до нескольких суток после [11; 53; 54]. При этом описано, что он вызывает инфаркт миокарда у пациентов без предшествующего заболевания коронарных артерий [54]. Апоптоз эндотелиальных клеток, приводящий к вазоспастической стенокардии и инфаркту миокарда, является неблагоприятным эффектом применения таких препаратов как этопозид, блеомицин, бевацизумаб и винбластин [59]. Другие ингибиторы тирозинкиназы (сунитиниб, пазопаниб и сорафениб) имеют побочный эффект в виде артериальных тромботических осложнений [15]. Леналидомид является
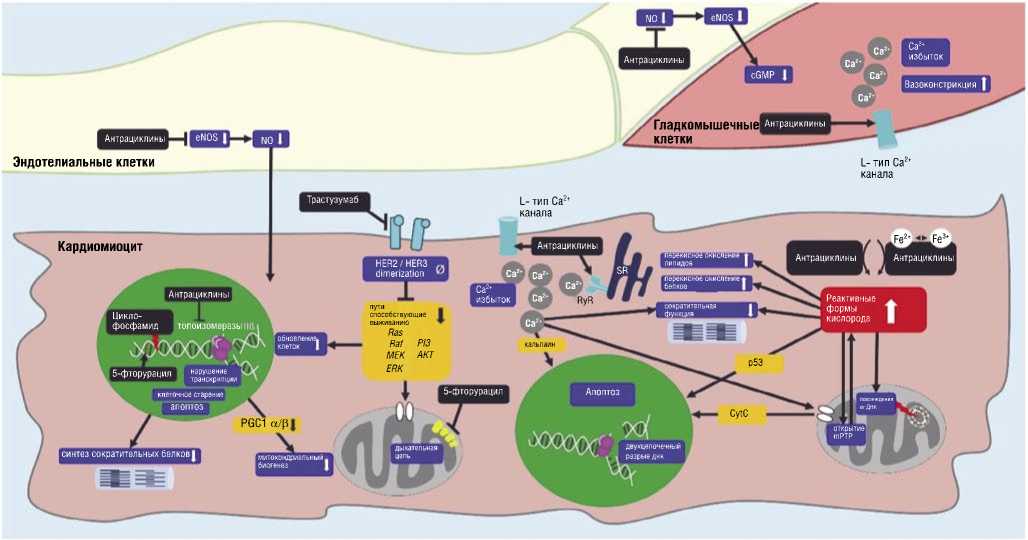
Рис. 1. Молекулярные/клеточные мишени для химиотерапевтических препаратов [65].
иммуномодулирующим средством, используемым при лечении множественной миеломы, также увеличивает риск возникновения артериальных и венозных тромбоэмболических осложнений, включая инфаркт миокарда и цереброваскулярные осложнения [14].
Лучевая терапия, как фактор развития сердечнососудистых осложнений
Лучевая терапия является одним из основных элементов противоопухолевого лечения и также, как и химиотерапия препятствует пролиферации и жизнеспособности клеток путем фрагментации клеточной ДНК, что в свою очередь может приводить к значительным нарушениям в работе сердечно-сосудистой системы. Однако, ее применение в лечении некоторых злокачественных новообразований грудной клетки таких как, рак молочной железы, легких, пищевода и лимфомы Ходжкина и неходжкинской лимфомы, приводит к значительному негативному воздействию на сердце, включающее в себя прогрессирование атеросклероза коронарных артерий, рестриктивную кардиомиопатию, констриктивный перикардит и пороки сердца [4; 7; 16; 17; 40; 42].
Прогрессирование атеросклероза хорошо документировано у онкогематологических больных, подвергшихся воздействию лучевой терапии. Эти пациенты имеют более высокий риск развития ИБС, напрямую зависящий от полученной дозы облучения. Не существует безопасного порога лучевого воздействия, ниже которого риск приближается к нулю [17]. Лучевая терапия является независимым фактором риска прогрессирования атеросклероза, который в свою очередь, может клинически не проявляться в первый год после лечения. Механизм инициации атеросклероза связан с радиационным воспалением стенки сосуда, приводящим к накоплению миофибробластов и пролиферации интимы с агрегацией богатых липидами макрофагов [60–62]. Повреждение также происходит и в микроциркуляторном русле, вызывая воспаление и образование тромбов, которые блокируют микроцирку-ляторное русло, что в итоге приводит к ишемии, фиброзу и гибели клеток миокарда [55]. При этом вероятность васкулопатии увеличивается и ускоряется при уже имеющихся сердечно-сосудистых факторах риска, особенно при гиперхолестеринемии [19; 27] (Рис. 2).
По данным Hancock S.L. и соавт., у пациентов с лимфомой Ходжкина проведение лучевой терапии сопровождалось троекратным повышением относительного риска смерти от острых сердечно-сосудистых осложнений, по сравнению с пациентами, не получавшими лучевую терапию. И авторы также отметили, что увеличение дозы облучения (>30 Гр) связано повышением риска смерти (ОШ 3,50; 95% ДИ 2,7–4,3) [26]. В литературе отмечено, что у пациентов с лимфомой Ходжкина высокой степени лучевого воздействия подвержены ствол левой коронарной артерии и правая коронарная артерия [28]. По данным Aleman B.M.P. и соавт., лучевая терапия средостения связана с 7-кратным увеличением риска ИБС [9].
Еще один важный аспект — развитие рестеноза в ранее имплантированном стенте вследствие лучевого воздействия. Однако имеющиеся литературные данные по этой проблеме противоречивы. Так, Liang J.J. и соавт. показали, что проведение лучевой терапии как до ЧКВ, так и после него никак не влияет на частоту рестенозирования. В группе пациентов, подвергшихся ЧКВ до лучевой терапии частота рестеноза оказалась сопоставимой с частотой в контрольной группе — 3,2 и 6,6%, соответственно (ОР 0,6; 95% ДИ 0,2–1,6; р = 0,31),
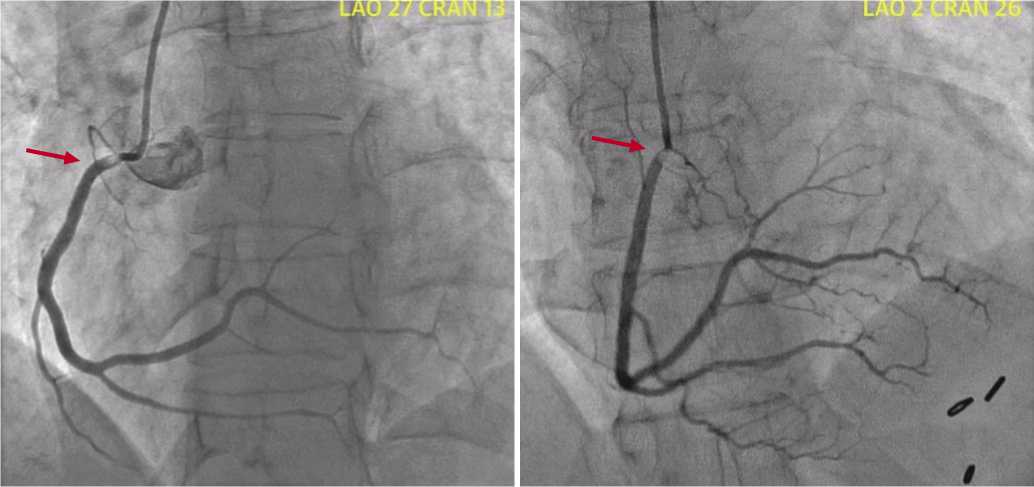
Рис. 2. Коронарограмма пациента после лучевой терапии лимфомы Ходжкина. Стрелками указано стенотическое поражение правой коронарной артерии [19].

а в группе пациентов, которым ЧКВ проводилось после лучевой терапии — 9,2 и 9,7%, соответственно (ОР 1,2; 95% ДИ 0,4–3,4; р = 0,79) [42]. Однако Schomig K. и со-авт. показали результаты десятилетнего наблюдения за пациентами с лимфомой, перенесших ЧКВ по поводу инфаркта миокарда. При этом лучевая терапия оказалась независимым предиктором развития рестеноза в ранее имплантиронном стенте (ОШ 21,7; 95% ДИ 4,7–100,9; р<0,001 [56]. Кроме того, облучение может вызвать фиброз артерий, что усложняет использование внутренних грудных (маммарных) артерий при необходимости проведения коронарного шунтирования.
ЧКВ у пациентов с гемобластозами
На сегодняшний день эндоваскулярная реваскуляризация миокарда в сочетании с оптимальной медикаментозной терапией является основным методом лечения больных с ИБС. Но до сих пор остается много вопросов по реваскуляризации миокарда у отдельных групп пациентов с высоким риском развития осложнений как во время, так и после вмешательства.
В литературе появляется все больше сообщений о связи онкологических и сердечно-сосудистых заболеваний. Несколько исследований показали, что ИБС и онкология имеют общие факторы риска, такие как курение, ожирение, пассивный образ жизни, гиперлипидемия, гипертония и сахарный диабет [24; 32; 34; 67]. Помимо общих факторов риска в патогенезе и прогрессировании как онкологических, так и сердечно-сосудистых заболеваний важную роль играет и воспаление [43]. Опухолевые клетки, продуцируя различные провоспалительные цитокины и хемокины, способствуют повышению проницаемости эндотелия сосудов и выходу прокоагулянтных факторов (факторов активации тромбоцитов и тканевого фактора) во внесосудистое пространство. При этом в сосудистую интиму начинают проникать частицы холестерина и липопротеинов низкой плотности, образуя атеросклеротические бляшки. Таким образом проатеросклеротический эффект воспаления в дополнение к протромботическому состоянию системы гемостаза увеличивает риск развития ИБС у онкологических пациентов [12; 18; 24].
ИБС может предшествовать развитию онкологического заболевания или может возникнуть в результате его лечения с использованием кардиотоксической химиотерапии и лучевой терапии [33; 65; 70]. Поэтому онкогематологические пациенты прежде всего нуждаются в индивидуальном подходе к лечению. Тщательная оценка индивидуального и семейного анамнеза пациента должна проводиться перед любой противоопухолевой терапией. В рамках «сердечной команды» при выставлении показаний к проведению эндоваскулярных вмешательств для больных гемобластозами необходимо учитывать заключение онкогематолога с целью оценки операционных рисков на фоне тяжелого коморбидного фона у этих пациентов. Кроме того, некоторые исследования показывают, что у онкологических пациентов острый инфаркт миокарда чаще сопровождается кардиогенным шоком и внутрибольничной смертностью по сравнению с пациентами без онкологии [66].
В большинстве случаев клинический фон злокачественных новообразований отягощен развитием анемического синдрома. По данным Mercadante S. и соавт. анемия встречается более чем у трети онкологических больных [46]. А частота встречаемости анемического синдрома у больных гемобластозами доходит до 70% [1]. Анемия у больных с сочетанием гемобластоза и ИБС может служить фактором прогрессирования ишемии, спровоцировать развитие сердечной недостаточности и повысить риск фатального исхода при остром инфаркте миокарда.
Развитие первичного анемического синдрома зависит от формы и стадии гемобластоза. Опухолевые клетки активируют иммунную систему организма и запускают воспалительные реакции, которые приводят к увеличению концентрации TNF (фактора некроза опухоли) и подавлению синтеза эритропоэтина. Вторичный анемический синдром обусловлен непосредственным токсическим действием химиотерапевтических лекарственных средств на эритроидные предшественники. Некоторые химиопрепараты могут оказывать прямое негативное воздействие на почечные канальцы, тем самым снижая выработку эритропоэтина [1].
Кроме того, у онкогематологических пациентов высок риск развития тромбогеморрагических событий. Нарушения свертывания крови при гемобластозах обусловлены самим неопластическим процессом. По мнению ряда авторов, механизм этих нарушений чаще всего бывает вызван развитием тромбоцитопении вследствие подавления нормального кроветворения. У онкологических больных повышен риск развития геморрагических осложнений. Кровотечение возникает примерно у 10% пациентов с солидными опухолями и еще чаще у пациентов с гематологическими злокачественными новообразованиями [21]. Другие исследователи нарушения гемостаза объясняют способностью бластных клеток продуцировать тканевой тромбопластин, активированные факторы свертывания, а также опухолевые прокоагулянты, которые являются прямыми активаторами II и Х факторов [2]. Проведенные исследования показали, что у больных злокачественными новообразованиями активация системы гемостаза осуществляется преимущественно по внешнему механизму процесса свертывания крови [25].
Считается, что существует циклическая связь, при которой опухолевые клетки способствуют тромбозу, а сгустки белков поддерживают опухолевый процесс. Опухолевые клетки могут влиять на экспрессию гемостатических белков, воспалительных цитокинов, проангиогенных факторов, прокоагулянтных микрочастиц и молекул адгезии, вызывая гиперкоагуляцию [21]. Также сам по себе неопластический процесс, оказывая влияние на тромбоцитарное звено системы гемостаза путем усиления метаболизма арахидоновой кислоты, образования тромбина и повышения уровня фактора Виллебранда, способствует повышению адгезии и агрегации тромбоцитов [13; 29].
Онкологические заболевания часто сопровождаются тромбоцитопенией и нарушениями функций тромбоцитов, примерно у 10–25% пациентов с солидными опухолями, а также у большинства больных острой лейкемией, лимфомой, миелодиспластическим синдромом и множественной миеломой [20; 44]. Тромбоцитопения, как известно, ассоциирована с повышенным риском развития тяжёлых сердечно-сосудистых осложнений при проведении ЧКВ и может приводить к летальным исходам [39; 40; 52]. Тромбоцитопения у этих больных с одной стороны развивается вследствие самого опухолевого процесса и обусловлена инфильтрацией костного мозга, спленомегалией, аутоиммунной реакцией и активацией системы свертывания крови, но может быть связана и с применяемыми химиотерапевтическими агентами, которые оказывают прямое миелосупрессивное воздействие [6]. В то же время клинические исследования показывают, что функция тромбоцитов важнее, чем их количество [37]. Независимо от уровня тромбоцитопении, пациенты могут быть предрасположены к коронарному тромбозу, потому что их тромбоциты больше по размеру и более адгезивны к поверхности сосудов. Описано, что у пациентов с острым инфарктом миокарда или инсультом средний объем тромбоцитов значительно увеличивается, несмотря на сопутствующее снижение их количества [51]. Так, в модели на грызунах крупные тромбоциты появляются в кровообращении в течение 12 часов после индукции тромбоцитопении, а через 18 часов почти половина всех тромбоцитов больше нормы [49; 69]. Проведенный эксперимент подтверждает идею о том, что крупные тромбоциты обладают более высоким тромботическим потенциалом. Поскольку производство тромбоцитов естественным образом регулируется для поддержания общей массы тромбоцитов, можно сделать вывод, что более крупные тромбоциты не только обеспечивают гемостатическую пробку и предотвращают кровотечение из-за высокой активности, но также могут быть связаны с коронарным тромбозом у пациентов с тромбоцитопенией.
Вышесказанное подчеркивает необходимость тщательной оценки риска тромбоза и кровотечения в этой популяционной группе. При планировании проведения ЧКВ у таких больных эта информация оказывает большое влияние на возможные варианты стентирования коронарных артерий. Большинство ЧКВ возможно безопасно выполнять пациентам с количеством тромбоцитов 40–50 000/ мкл.
В исследовании ZEUS показано, что у пациентов с высоким риском кровотечения применение зотароли-мус-покрытых стентов снижает частоту тромбоза стента, инфаркта миокарда и повторной реваскуляризации целевого сосуда, несмотря на более короткую продолжительность двойной антиагрегантной терапии (ДАТ) от 15 до 60 суток по сравнению с пациентами, которым были имплантированы ГМС. Важно отметить, что у некоторых из этих пациентов были множественные факторы риска кровотечения и тромбоза стента, включая рак (n = 84). Кроме того, случаи кровотечения не отличались между группами по типу стента [10].
Стремление к улучшению отдаленных результатов ЧКВ послужило поводом для разработки СЛП третьего поколения, представляющих собой стенты с биодегради-румемым полимером с лекарственным покрытием, нанесенным только со стороны, обращенной к стенке сосуда. По результатам исследования EVOLVE II при сравнении этих стентов со стентами с постоянным полимерным покрытием не было отмечено статистических различий по частоте повторных реваскуляризаций на целевых сосудах, 6,7% против 6,5% (р = 0,83) [47].
Недавно было продемонстировано, что при имплантации таких стентов продолжительность ДАТ может быть сокращена до 1 месяца. В исследовании LEADERS FREE было проанализировано применение бесполимер-ных стентов с лекарственным покрытием (BioFreedom Biolimus A9, Biosensors Europe SA, Моргес, Швейцария), которые в течение 1 месяца переносят биолимус A9 (высоколипофильный аналог сиролимуса) в стенку сосуда. Данные стенты сравнивали с ГМС у пациентов с высоким риском кровотечений после ЧКВ. Бесполимерные СЛП BioFreedom Biolimus A9 были имплантированы 1221 пациентам и ГМС Gazelle (Biosensors Interventional, Сингапур) — 1211 больным. Важно подчеркнуть, что в обеих группах исследования были пациенты с раком, верифицированным в предшествующие 3 года. Таким образом, в группе бесполимерных СЛП таких пациентов было 119 (9,7%), а в группе ГМС — 120 (9,9%). Результаты показали, что бесполимерные СЛП превосходят ГМС при сравнении риска инфаркта миокарда или тромбоза стента на фоне 1-месячного курса ДАТ у пациентов с высоким риском кровотечения после интервенции. Частота кровотечений (3–5 тип по BARC) статистически не различалась между группами и составляла 10% (Рис. 3) [22; 23].
Несмотря на активное развитие технологии производства стентов, а также получение хороших результатов при применении современных СЛП на фоне сокращенной ДАТ, нет конкретных рекомендаций по выбору типа стентов при ЧКВ у онкогематологических больных. Проблема заключается в том, что информация о ЧКВ у таких пациентов обычно не собирается в стандартных реестрах. Кроме того, онкогематологические больные часто исключаются из клинических испытаний по поводу ЧКВ. На данный момент имеются лишь единичные работы с малой выборкой пациентов и клинические примеры применения ЧКВ у онкогематологических больных. В связи с этим врачи по рентгенэндоваскулярным диагностике и лечению часто предпочитают применение ГМС у онкологических пациентов из-за опасений по поводу повышенного риска кровотечений и ожидаемой потребности в хирургии, направленной на лечение онкологии [66].
Kokolis S. и соавт. показали, что системная хими-отреапия снижает частоту рестенозов после стентирования коронарных артерий. Всего в исследовании были
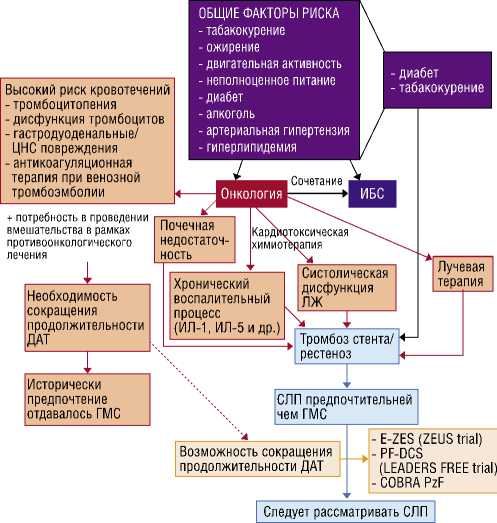
Рис. 3. Современные стенты для применения у пациентов с онкологическими заболеваниями [22].
включены 78 онкологических больных, разделенных на 2 группы: I (основная) группа — 40 пациентов, которым проводили курсы химиотерапии и II (контрольная) — 38 пациентов, не получавшие химиотерапию. Всем пациентам было проведено ЧКВ с имплантацией ГМС. Частота рестенозов была статистически ниже в I группе по сравнению со II группой, 5% и 26% соответственно (СР = 0,15, 95% ДИ 0,03–0,7, р<0,01) [5].
Mohanty B.D. и соавт. демонстируя клинический пример лечения инфаркта миокарда у пациента с раком мочевого пузыря, выдвинули гипотезу о влиянии химиотерапии на процесс развития неоинтимы, замедляя его и тем самым, повышая риск тромбообразования (Рис. 4) [48].
Jao G.T. и соавт. столкнулись с проблемой поиска литературных данных по лечению инфаркта миокарда у больных острым миелолейкозом (ОМЛ). В их обзоре представлены только 8 сообщений. Авторы отметили, что прогноз для пациентов с инфарктом миокарда с подъемом сегмента ST (ИМпST) на фоне ОМЛ явно хуже, чем для неонкологических пациентов c ИМпST. Также они считают, что ЧКВ с имплантацией ГМС является более безопасным методом лечения инфаркта миокарда у таких пациентов, объясняя это пожилым возрастом больных и необходимостью проведения кардиотоксиче-ской противоопухолевой терапии [31].
Еще один вопрос, требующий более детального изучения, это применение ДАТ, включающей в себя ингибитор ЦОГ-1 и ЦОГ-2 (ацетилсалициловая кислота) и один из ингибиторов P2Y12-рецепторов тромбоцитов (клопидогрел, прасугрел, тикагрелор) у данной категории пациентов. Как известно, ДАТ является «золотым стандартом» при ЧКВ [35; 42]. Но у 25–50% пациентов, принимающих клопидогрел, наблюдается недостаточный фармакологический ответ, приводящий к недостаточной защите от неблагоприятных сердечнососудистых осложнений [57; 64]. В метаанализе Sofi F. и соавторы выявлена связь между высокой остаточной реактивностью тромбоцитов на фоне приема клопи-догрела и развитием кардиальных осложнений [58]. Несмотря на то, что в литературе нет конкретных данных по назначению ДАТ онкологическим пациентам с тромбоцитопенией, отказ от использования ацетилсалициловой кислоты у таких больных при ОКС приводит к худшим результатам [30].
С целью достижения более эффективного применения антиагрегантов становится актуальной персонализированная антиагрегантная терапия [36]. На данной момент для этого в клинической практике используются лабораторные тесты, включающие генетический анализ и определение агрегационной способности тромбоцитов.
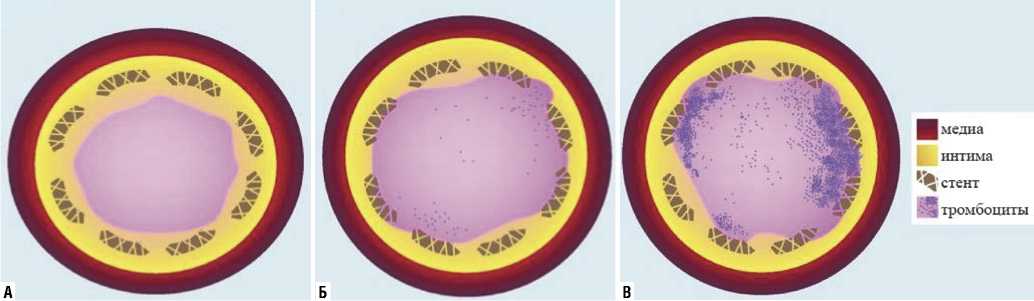
Рис. 4. Предполагемые схемы поперченых разрезов коронарных артерий, изображающие реэндотелизацию через 6 недель после имплантации стента в трех различных клинических сценариях. А — ГМС, нет химиотерапии, 4-недельный курс ДАТ, стент полность покрыт неоинтимой; Б — СЛП, нет химиотерапии, ДАТ, стент неполностью покрыт неоинтимой; В — ГМС, химиотерапия, 4-недельный курс ДАТ, неполная реэндоте-лизация из-за влияния химиотерапии [48].

Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Чрескожные коронарные вмешательства у больных гемобластозами
- Березин П.Г., Милованов В.В., Иванников А.А. Роль эритропоэтинов в лечении анемии у онкологических больных // Исследования и практика в медицине. — 2017. — Т.4. — №2. — С. 37-42. [Berezin PG, Milovanov VV, Ivannikov AA. The role of erythropoietin in treatment of anemia in cancer patients. Research and Practical Medicine Journal. 2017; 4(2): 37-42. (In Russ).] doi: 10.17709/2409-2231-2017-4-2-5.
- Владимирова С.Г., Тарасова Л.Н., Скольская О.Ю. Показатели гемостаза у больных острым миелоидным лейкозом в период манифестации заболевания // Онкогематология. — 2012. — Т.7. — №2. — С. 36-41. [Vladimirova SG, Tarasova LN, Skolskaya OYu. Hemostasis in acute myeloid leukemia patients during disease manifestation. Oncohematology. 2012; 7(2): 36-41. (In Russ).] doi: 10.17650/1818-8346-2012-7-2-36-41.
- Голубцов О.Ю., Тыренко В.В., Лютов В.В. и др. Кардиоваскулярные осложнения противоопухолевой терапии // Современные проблемы науки и образования. — 2017. — №2. — С. 1-15. [Golubcov OYu, Tirenko VV, Lutov VV, et al. Cardiovascular complications of chemotherapy. 2017; 2: 1-15. (In Russ).] Доступно по: http://www.science-education.ru/ru/article/ view?id=26380.
- Емелина Е.И., Шуйкова К.В., Гендлин Г.Е. и др. Поражение сердца при лечении современными противоопухолевыми препаратами и лучевые повреждения сердца у больных с лимфомами // Клиническая онкогематология. — 2009. — Т.2. — №2. — С. 152-160. [Emelina EI, Shuyko-va KV, Gendlin GE. Cardiac damage after modern chemo- and radiotherapy in patients with lymphomas. Klinicheskaya onkogematologiya. 2009; 2(2): 152-160. (In Russ).] Доступно по: http://www.hematology.ru/journals/cli-nical_oncohaematology/2009/2/gematolog_0209.pdf.
- Коколис С., Тарко Д.Б., Меран Р. и др. Системная химиотерапия сопутствующих раковых образований снижает частоту рестенозов после стентиро-вания коронарных артерий // Международный журнал интервенционной кардиоангиологии. — 2003. — №3. — С. 26-29. [Kokolis S, Tarko DB, Me-hran R, et al. Chemotherapy reduces the incidence of restenosis after coronary artery stenting. Mezhdunarodnyj zhurnal intervencionnoj kardioangiologii. 2004; 3: 26-29. (In Russ).]
- Кольцова Е.М., Баландина А.Н., Серегина Е.А., и др. Аспекты методологии лабораторных исследований гемостаза в детской гематологии-онкологии и общие подходы в патологии гемостаза при лейкозах // Российский журнал детской гематологии и онкологии. — 2018. — Т.5. — №3. — С. 74-88. [Koltsova EM, Balandina AN, Seregina EA, et al. Aspects of the methodology of laboratory studies of hemostasis in pediatric hematology-oncology and general approaches in the pathology of hemos-tasis in leukemia. Russian Journal of Pediatric Hematology and Oncology. 2018; 5(3): 74-88. (In Russ).] doi:10.17650/2311-1267-2018-5-3-74-88.
- Прус Ю.А., Сергиенко И.В., Кухарчук В.В. и др. Кардиотоксичность, индуцированная химиотерапией и лучевой терапией // Атеросклероз и дислипидемии. — 2017. — Т.3. — №28. — С. 56-72. [Prus YuA, Se-rgienko IV, Kukharchuk VV. Cardiotoxicity induced by chemotherapy and radiotherapy. Ateroskleroz i dislipidemii. 2017; 3(28): 56-72. (In Russ).]
- Селиверстова Д.В., Евсина О.В. Кардиотоксичность химиотерапии // Сердце: журнал для практикующих врачей. — 2016. — Т.15. — №1. — С. 50-57. [Seliverstova DV, Evsina OV. Cardiotoxicity of chemotherapy. Russian Heart Journal. 2016; 15(1): 50-57. (In Russ).] doi: 10.18087/rhj. 2016.1.2115.
- Aleman BMP, Belt-Dusebout AWVD, Bruin MLD, et al. Late cardiotoxicity after treatment for Hodgkin lymphoma. Blood. 2007; 109(5): 1878-1886. doi: 10.1182/blood-2006-07-034405.
- Ariotti S, Adamo M, Costa F, et al. Is bare-metal stent implantation still justifiable in high bleeding risk patients undergoing percutaneous coronary intervention? J Am Coll Cardiol Intv. 2016; 9(5): 426-436. doi: 10.1016/ j.jcin.2015.11.015.
- Arunprasath P, Gobu P, Dubashi B, et al. Rituximab induced myocardial infarction: a fatal drug reaction J. Cancer Res. Ther. 2011; 7(3): 346-348. doi: 10.4103/0973-1482.87003.
- Blann AD, Dunmore S. Arterial and venous thrombosis in cancer patients. Cardiol Res Pract. 2011; 11: 394740. doi: 10.4061/2011/394740.
- Bromberg ME, Cappello M. Cancer and blood coagulation: molecular aspects. Cancer J. Sci. Am. 1999; 5(3): 132-138. Available at: https://pubmed. ncbi.nlm.nih.gov/10367166.
- Cesarman-Maus G, Braggio E, Fonseca R. Thrombosis in multiple myeloma (MM). Hematology. 2012; 17(1): 177-180. doi: 10.1179/102453312X133-36169156933.
- Cheng H, Feldman T, Butt Y, et al. T-cell prolymphocytic leukemia with extensive cardiovascular infiltrate leading to multiple myocardial infarctions and cardiac death. Tex. Heart Inst. J. 2014; 41(6): 626-630. doi: 10.14503/ THIJ-13-3581.
- Curigliano G, Cardinale D, Suter T, et al. Cardiovascular toxicity induced by chemotherapy, targeted agents and radiotherapy: ESMO Clinical Practice Guidelines. Ann Oncol. 2012; 23(7): 155-66. doi: 10.1093/annonc/mds293.
- Darby SC, Ewertz M, McGalle P, et al. Risk of ischemic heart disease in women after radiotherapy for breast cancer. N Engl J Med. 2013; 368(11): 987-998. doi: 10.1056/NEJMoa1209825.
- Demers M, Krause DS, Schatzberg D, et al. Cancers predispose neutrophils to release extracellular DNA traps that contribute to cancer-associated thrombosis. Proc Natl Acad Sci U S A. 2012; 109(32): 13076-13081. doi: 10.1073/pnas.1200419109.
- Desai MY, Jellis CL, Kotecha R, et al. Radiation-Associated Cardiac Disease: A Practical Approach to Diagnosis and Management. JACC: Cardiovascular Imaging. 2018; 11(8): 1132-1149. doi: 10.1016/j.jcmg.2018.04.028.
- Elting LS, Rubenstein EB, Martin CG, et al. Incidence, cost, and outcomes of bleeding and chemotherapy dose modification among solid tumor patients with chemotherapy-induced thrombocytopenia. J Clin Oncol. 2001 ; 19(4): 1137-1146. doi: 10.1200/Jœ.2001.19.4.1137.
- Falanga A, Russo L, Milesi V. The coagulopathy of cancer. Curr Opin Hemat-ol. 2014; 21(5): 423-429. doi: 10.1097/MOH.0000000000000072.
- Ganatra S, Sharma A, Levy MS. Re-evaluating the safety of drug-eluting st-ents in cancer patients. JACC Cardiovasc Interv. 2017; 10(22): 2334-2337. doi:10.1016/j .jcin.2017.06.068.
- Garot P, Morice MC, Tresukosol D, et al. 2-year outcomes of high bleeding risk patients after polymer-free drug-coated stents. J Am Coll Cardiol. 2017; 69(2) : 162-171. doi: 10.1016/j.jacc.2016.10.009.
- Giza DE, Iliescu G, Hassan S, et al. Cancer as a risk factor for cardiovascular disease. Curr Oncol Rep. 2017; 19(6): 39. doi: 10.1007/s11912-017-0601 -x.
- Goad KE, Gralnick HR. Coagulation disorders in cancer. Hematol Oncol Clin North Am. 1996; 10(2): 457-484. doi: 10.1016/s0889-8588(05) 70347-6.
- Hancock SL, Tucker MA, Hoppe RT. Factors Affecting Late Mortality from Heart Disease after Treatment of Hodgkin's Disease. JAMA. 1993; 270(16): 1949-1955. Доступно по: https://pubmed.ncbi.nlm.nih.gov/8411552.
- Hendry JH. Threshold doses and circulatory disease risks. Ann ICRP. 2015; 44 (Suppl 1): 69-75. doi: 10.1177/0146645314560688.
- Herrmann J, Lerman A, Sandhu NP, et al. Evaluation and management of patients with heart disease and cancer: cardio-oncology. Mayo Clin Proc. 2014; 89(9): 1287-1306. doi:10.1016/j.mayocp.2014.05.013.
- Hillen HF. Thrombosis in cancer patients. Ann. Oncol. 2000; 11(3): 273-276. doi: 10.1093/annonc/11 .suppl_3.273.
- Iliescu CA, Grines CL, Herrmann J, et al. SCAI Expert Consensus Statement: Evaluation, Managment, and Special Considerations of Cardio-Oncology Patients in the Cardiac Catheterization Laboratory (Endorsed by the Cardiological Society of India, and Sociedad Latino Americana de Cardiolog a Intervencionista). Catheter Cardiovasc Interv. 2016; 87(5): 202-223. doi: 10.1002/ccd.26379.
- Jao GT. ST-elevation myocardial infarction and myelodysplastic syndrome with acute myeloid leukemia transformation. Tex Heart Inst J. 2014; 41(2): 234-237. Published 2014 Apr 1. doi:10.14503/THIJ-12-2905.
- Johnson CB, Davis MK, Law A, et al. Shared risk factors for cardiovascular disease and cancer: implications for preventive health and clinical care in oncology patients. Can J Cardiol. 2016; 32(7): 900-907. doi: 10.1016/ j.cjca.2016.04.008.
- Khosrow-Khavar F, Filion KB, Al-Qurashi S, et al. Cardiotoxicity of aromatase inhibitors and tamoxifen in postmenopausal women with breast cancer: a systematic review and meta-analysis of randomized controlled trials. Ann Oncol. 2017; 28(3): 487-496. doi: 10.1093/annonc/mdw673.
- Koene RJ, Prizment AE, Blaes A, et al. Shared risk factors in cardiovascular disease and cancer. Circulation. 2016; 133(11): 1104-1114. doi: 10.1161/ CIRCULATIONAHA.115.020406.
- Kolh P, Windecker S, Alfonso F, et al. 2014 ESC/EACTS Guidelines on myocardial revascularization: the Task Force on Myocardial Revascularization of the European Society of Cardiology (ESC) and the European Association for Car-dio-Thoracic Surgery (EACTS). Developed with the special contribution of the European Association of Percutaneous Cardiovascular Interventions (EAPCI). Eur J Cardiothorac Surg. 2014; 46(4): 517-592. doi: 10.1093/ ejcts/ezu366.
- Koltowski L, Tomaniak M, Aradi D, et al. Optimal aNtiplate-let pharmacotherapy guided by bedSIDE genetic or functional TESTing in elective PCI patients: A pilot study: ONSIDE TEST pilot. Cardiol J. 2017; 24(3): 284-292. doi: 10.5603/CJ.a2017.0026.
- Kroll MH, Feng S. Targeting shear stress-induced platelet activation: is lesion-specific antiplatelet therapy a realistic clinical goal? Expert Rev Cardiov-asc Ther. 2005; 3(5): 941-951. doi: 10.1586/14779072.3.5.941.
- Kwok CS, Khan MA, Rao CV, et al. Access and non-access site bleeding after percutaneous coronary intervention and risk of subsequent mortality and major adverse cardiovascular events: systematic review and meta-analysis. Circ Cardiovasc Interv. 2015; 8(4): 001645. doi: 10.1161/CIRCINTERVENTI-ONS. 114.001645.
- Kwok CS, Rao SV, Myint PK, et al. Major bleeding after percutaneous coronary intervention and risk of subsequent mortality: a systematic review and meta-analysis. Open Heart. 2014; 1(1): 000021. doi: 10.1136/openhrt-2013-000021.
- Lancellotti P, Nkomo VT, Badano LP, et al. Expert Consensus for Multi-Modality Imaging Evaluation of Cardiovascular Complications of Radiotherapy in Adults: A Report from the European Association of Cardiovascular Imaging and the American Society of Echocardiography. Journal of the American Society of Echocardiography. 2013; 28(9): 1013-1032. doi: 10.1016/j. echo.2013.07.005.
- Levine GN, Bates ER, Bittl JA, et al. 2016 ACC/AHA Guideline Focused Update on Duration of Dual Antiplatelet Therapy in Patients With Coronary Artery Disease: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines: An Update of the 2011 ACCF/AHA/ /SCAI Guideline for Percutaneous Coronary Intervention, 2011 ACCF/ AHA Guideline for Coronary Artery Bypass Graft Surgery, 2012 ACC/ AHA/ACP/AATS/PCNA/SCAI/STS Guideline for the Diagnosis and Management of Patients With Stable Ischemic Heart Disease, 2013 ACCF/AHA Guideline for the Management of ST-Elevation Myocardial Infarction, 2014 AHA/ACC Guideline for the Management of Patients With Non-ST-Elevation Acute Coronary Syndromes, and 2014 ACC/AHA Guideline on Perioperative Car-diovascular Evaluation and Management of Patients Undergoing Noncardiac Surgery. Circulation. 2016; 134(10): 123-155. doi: 10.1161/CIR.0000000000000404.
- Liang JJ, Sio TT, Slusser JP, et al. Outcomes after percutaneous coronary intervention with stents in patients treated with thoracic external beam radiation for cancer. J Am Coll Cardiol Intv. 2014; 7(12): 1412-1420. doi: 10.1016/j .jcin.2014.05.035.
- Libby P. Inflammation in atherosclerosis. Nature. 2002; 420(6917): 868-874. doi: 10.1038/nature01323.
- Liu VY, Agha AM, Lopez-Mattei J, et al. Interventional Cardio-Oncology: Adding a New Dimension to the Cardio-Oncology Field. Front Cardiovasc Med. 2018; 5: 48. doi: 10.3389/fcvm.2018.00048.
- Mandel EM, Lewinski U, Djaldetti M. Vincristine-induced myocardial infarction. Cancer. 1975; 36(6): 1979-1982. doi: 10.1002/cncr.2820360908.
- Mercadante S, Gebbia V, Marrazzo A, et al. Anemia in cancer: pathophysio-logy and treatment. Cancer Treat Rev. 2000; 26(4): 303-311. doi: 10.1053/ ctrv.2000.0181.
- Meredith IT, Verheye S, Dubois C, et al. Final five-year clinical outcomes in the EVOLVE trial: a randomized evaluation of a novel bioabsorbable polymer-coated, everolimus-eluting stent. Eurointervention. 2018; 13(17): 2047-2050. doi: 10.4244/EIJ-D-17-00529.
- Mohanty BD, Mohanty S, Hussain Y, et al. Management of ischemic coronary disease in patients receiving chemotherapy: an uncharted clinical challenge. Future Cardio. 2017; 13(3): 247-257. doi:10.2217/fca-2017-0002.
- Odell TT, Murphy JR, Jackson CW. Stimulation of megakaryocytopoiesis by acute thrombocytopenia in rats. Blood. 1976; 48(5): 765-775. Available at: https://pubmed.ncbi.nlm.nih.gov/974268.
- Plana JC, Galderisi M, Barac A, et al. Expert consensus for multimodality imaging evaluation of adult patients during and after cancer therapy: a report from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. Am Soc Echocardiogr. 2014; 27(9): 911-939. doi: 10.1016/j.echo.2014.07.012.
- Polk A, Vistisen K, Vaage-Nilsen M, et al. A systematic review of the pathophysiology of 5-fluorouracil-induced cardiotoxicity. BMC Pharmacol Toxicol. 2014; 15: 47. doi: 10.1186/2050-6511-15-47.
- Potts J, Mohamed MO, Lopez Mattei JC, et al. Percutaneous coronary intervention and in-hospital outcomes in patients with leukemia: a nationwide analysis. Catheter Cardiovasc Interv. 2020; 96(1): 53-63. doi: 10.1002/ ccd.28432.
- Renard D, Cornillet L, Castelnovo G. Myocardial infarction after rituximab infusion. Neuromuscul Disord. 2013; 23(7): 599-601. doi: 10.1016/j.nmd. 2013.03.014.
- Roy A, Khanna N, Senguttuvan NB. Rituximab-vincristine chemotherapy-induced acute anterior wall myocardial infarction with cardiogenic shock. Tex Heart Inst J. 2014; 41(1): 80-82. doi: 10.14503/THIJ-12-2853.
- Saiki H, Petersen IA, Scott CG, et al. Risk of heart failure with preserved ejection fraction in older women after contemporary radiotherapy for breast cancer. Circulation. 2017; 135(15): 1388-1396. doi: 10.1161/CIRCULATI0-NAHA.116.025434
- Schomig K, Ndrepepa G, Mehilli J, et al. Thoracic radiotherapy in patients with lymphoma and restenosis after coronary stent placement. Catheter Cardiovasc Interv. 2007; 70(3): 359-365. doi: 10.1002/ccd.21109.
- Siller-Matula JM, Trenk D, Schrôr K, et al. Response variability to P2Y12 receptor inhibitors: expectations and reality. JACC Cardiovasc Interv. 2013; 6(11): 1111-1128. doi: 10.1016/j.jcin.2013.06.011.
- Sofi F, Giusti B, Marcucci R, et al. Cytochrome P450 2C19*2 polymorphism and cardiovascular recurrences in patients taking clopidogrel: a meta-analy-sis. Pharmacogenomics J. 2011; 11(3): 199-206. doi: 10.1038/tpj.2010.21.
- Stefenelli T, Kuzmits R, Ulrich W, et al. Acute vascular toxicity after combination chemotherapy with cisplatin, vinblastine, and bleomycin for testicular cancer. Eur Heart J. 1988; 9(5): 552-556. doi: 10.1093/oxfordjournals. eurheartj.a062542.
- Stewart FA. Mechanisms and dose-response relationships for radiation-induced cardiovascular disease. Ann ICRP. 2012; 41(3-4): 72-79. doi: 10.1016/j.icrp.2012.06.031.
- Stewart FA, Seemann I, Hoving S, et al. Understanding radiation-induced cardiovascular damage and strategies for intervention. Clin Oncol. 2013; 25(10): 617-624. doi: 10.1016/j.clon.2013.06.012.
- Stewart FA, Hoving S, Russell NS. Vascular damage as an underlying mechanism of cardiac and cerebral toxicity in irradiated cancer patients. Radiat Res. 2010; 174(6): 865-869. doi: 10.1667/RR1862.1.
- Suter TM, Ewer MS. Cancer drugs and the heart: importance and management. Eur Heart Jn. 2013; 34(15): 1102-1111. doi:10.1093/eurheartj/ehs181.
- Tantry US, Bonello L, Aradi D, et al. Consensus and update on the definition of on-treatment platelet reactivity to adenosine diphosphate associated with ischemia and bleeding. J Am Coll Cardiol. 2013; 62(24): 2261-2273.doi: 10.1016/j.jacc.2013.07.101.
- Totzeck M, Schuler M, Stuschke M, et al. Cardio-oncology — strategies for management of cancer-therapy related cardiovascular disease. International Journal of Cardiology. 2019; 280: 163-175. doi: 10.1016/j.ijcard. 2019.01.038.
- Wang F, Gulati R, Lennon RG, et al. Cancer history portends worse acute and long-term noncardia (but not cardiac) mortality after primary percutaneous coronary intervention for acute ST-segment elevation myocardial infarction. Mayo Clin Proc. 2016; 91(12): 1680-1692. doi: 10.1016/j.mayo-cp.2016.06.029.
- Weaver KE, Foraker RE, Alfano CM, et al. Cardiovascular risk factors among long-term survivors of breast, prostate, colorectal, and gynecologic cancers: a gap in survivorship care? J Cancer Surviv. 2013; 7(2): 253-261. doi: 10.1007/s11764-013-0267-9.
- Yeh ET, Bickford CL. Cardiovascular complications of cancer therapy: incidence, pathogenesis, diagnosis, and management. J Am Coll Cardiol. 2009; 53(24): 2231-2247. doi: 10.1016/j.jacc.2009.02.050.
- Yusuf SW, Iliescu C, Bathina JD, et al. Antiplatelet therapy and percutaneous coronary intervention in patients with acute coronary syndrome and thrombocytopenia. Tex Heart Inst J. 2010; 37(3): 336-340. Available at: https:// pubmed.ncbi.nlm.nih.gov/20548817/
- Zamorano JL, Lancellotti P, Munoz DR, et al. ESC position paper on cancer treatments and cardiovascular toxicity developed under the auspices of the ESC Committee for Practice Guidelines: the task force for cancer treatments and cardiovascular toxicity of the European Society of Cardiology (ESC). Eur Heart J. 2016; 37(36): 2768-2801. doi: 10.1093/eurheartj/ehw211.


