Циркулярная резекция левого главного и верхнедолевого бронхов с бронхопластикой у пациента с центральным раком нижней доли левого легкого (клинический случай)
Автор: Гатьятов Р.Р., Шаназаров Н.А., Зинченко С.В.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Хирургия
Статья в выпуске: 3 т.21, 2025 года.
Бесплатный доступ
Представленный клинический случай акцентирует внимание на сложностях хирургического лечения пациента с центральным немелкоклеточным раком левого легкого. Минимальный стандартный объем хирургического лечения такого больного – это пневмонэктомия слева с систематической медиастинальной лимфодиссекцией из-за распространения опухоли на дистальную часть левого главного бронха. С учетом молодого возраста (47 лет) пациента для улучшения качества жизни выполнена органосохранная операция: нижняя лобэктомия слева с систематической медиастинальной лимфодиссекцией, циркулярная резекция левого главного и левого верхнедолевого бронхов, бронхопластика с формированием циркулярного анастомоза между левым верхнедолевым и левым главным бронхами. Для профилактики возникновения бронхоплеврального свища использовали свободный неваскуляризированный плеврально-жировой лоскут с перикардиальной области. Послеоперационный период протекал без осложнений. Через 30 мес после операции пациент продолжает наблюдаться у онколога без признаков рецидива и генерализации. Таким образом, бронхопластические операции дают возможность сохранить больному больше паренхимы легкого и улучшить качество жизни по сравнению с пневмони билобэктомиями, при этом оставаясь радикальным методом лечения рака легкого без ухудшения показателей безрецидивной выживаемости.
Бронхопластическая лобэктомия, циркулярный бронхиальный анастомоз, свободный плеврально-жировой лоскут, рак легкого
Короткий адрес: https://sciup.org/149149426
IDR: 149149426 | УДК: 616.233-089.85 | DOI: 10.15275/ssmj2103280
Circular resection of the left main and upper lobe bronchi with bronchoplasty in a patient with central cancer of the lower lobe of the left lung (clinical case)
This clinical case focuses on the complexity of surgical treatment of patient with central non-small cell carcinoma of the left lung. The minimum standard amount of surgical treatment for our patient is a left pneumonectomy with systematic mediastinal lymph dissection due to the spread of the tumor to the distal part of the left main bronchus. Taking into account the young age (47 years old) of patient, in order to improve the quality of life, we performed organpreserving surgery: lower lobectomy on the left lung with systematic mediastinal lymph dissection, circular resection of the left main bronchus, the left upper lobular bronchus, bronchoplasty with the formation of a circular anastomosis between the left upper lobular and left main bronchus. To prevent the occurrence of bronchopleural fistula, we used a free, unvascularized pleural fat flap from the pericardial part. The postoperative period was uneventful. 30 months after the operation, the patient is observed without tumor recurrence and generalization. Thus, bronchoplastic surgeries make it possible to save the patient more lung parenchyma and improve the quality of life compared to pneumon- and bilobectomies, while remaining a radical method of treating lung cancer, without worsening disease-free survival.
Текст научной статьи Циркулярная резекция левого главного и верхнедолевого бронхов с бронхопластикой у пациента с центральным раком нижней доли левого легкого (клинический случай)
EDN: ITGIYC
Введение. Проблема лечения злокачественных новообразований (ЗНО) органов грудной полости (ОГП) была и остается актуальной в силу того, что данная патология имеет широкое распространение и тенденцию к росту заболеваемости. В течение последних десятилетий рак легкого (РЛ) устойчиво занимает 1-е место в структуре заболеваемости и смертности от ЗНО [1]. Стандартизированный показатель заболеваемости РЛ в Челябинской области в 2021 г. составил 25,3 случая на 100 тыс. жителей, в то время как в Российской Федерации он был 20,8 случая на 100 тыс. жителей [1].
Хирургическое лечение остается одним из основных методов терапии РЛ наряду с химио- и лучевой терапией. Основные операции при РЛ – анатомические резекции: лоб- и пневмонэктомия с систематической лимфодиссекцией. Пневмонэктомия – это удаление целого легкого (правого или левого), поэтому данная операция переносится больными тяжело и сопровождается различными осложнениями в послеоперационный период и высокой летальностью (до 20% случаев – по данным различных источников) [2–4]. Бронхопластическая лобэктомия является альтернативой пневмонэктомии при центральном немелкоклеточном РЛ. В многочисленных публикациях представлены благоприятные результаты бронхопластических лобэктомий, которые характеризуются отдаленными результатами, сравнимыми с пневмонэктомией и низкой послеоперационной смертностью. Бронхопластические операции также связаны с лучшим качеством жизни пациентов по сравнению с пневмонэктомией за счет сохранения паренхимы легкого [5–9].
Для профилактики возникновения бронхоплеврального свища применяются различные васкуляризированные лоскуты. В нашем клиническом примере мы использовали свободный неваскуляризированный плеврально-жировой лоскут, полученный из перикардиальной зоны. Следует отметить, что трансплантация собственной жировой ткани в реконструктивной хирургии активно применяется уже более 20 лет, и жизнеспособность аутологичной жировой ткани основана на свойствах адипоцитов [10].
Цель – на примере клинического случая показать результаты хирургического лечения пациента с центральным немелкоклеточным (плоскоклеточным) раком нижней доли левого легкого и распространением на левый главный бронх.
Информированное согласие пациента на публикацию своих данных получено.
Описание клинического случая. Пациент С. 47 лет находился в отделении торакальной онкологии ГАУЗ «Челябинский областной клинический центр онкологии и ядерной медицины» в мае 2022 г. с диагнозом «Центральный плоскоклеточный рак нижнедолевого бронха левого легкого с распространением на дистальную часть левого главного бронха» (рис. 1).
В феврале 2022 г. после повышения температуры тела до 39ºС направлен по месту жительства на компьютерную томографию ОГП без контрастного исследования для исключения вирусной пневмонии.
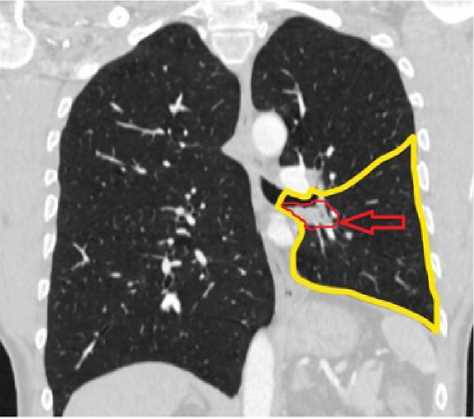
Рис. 1. Центральный рак нижнедолевого бронха левого легкого с распространением на левый главный бронх (желтым очерчены границы резекции легкого и бронхов, красным – опухоль)
На этом исследовании выявлен центральный рак нижней доли левого легкого.
В марте 2023 г. пациенту выполнена бронхоскопия: слева просвет нижнедолевого бронха в области устья обтурирован за счет инфильтративного новообразования бледно-розового цвета, выполнена биопсия опухоли, верифицирован умеренно дифференцированный плоскоклеточный РЛ. Согласно клиническим стандартам выполнены следующие обследования: магнитно-резонансная томография головного мозга с контрастным усилением, компьютерная томография органов брюшной полости и забрюшинного пространства с контрастным усилением, остеосцинтиграфия костей скелета, ультразвуковое исследование шейных и надключичных лимфатических узлов, оценена функция дыхания. Признаков генерализации опухолевого процесса не обнаружено. Функциональных противопоказаний к операции также не выявлено. Проведен консилиум врачей: онколога, химио- и радиотерапевта, решено выполнить хирургическое лечение данного ЗНО.
Минимальный стандартный объем хирургического лечения в данной ситуации – это пневмонэктомия слева с систематической медиастинальной лимфо-диссекцией. С учетом молодого возраста пациента для улучшения качества жизни мы выполнили органосохранную операцию: нижнюю лобэктомию слева с систематической медиастинальной лимфодиссек-цией, циркулярную резекцию левого главного бронха, левого верхнедолевого бронха, бронхопластику с формированием циркулярного анастомоза между левым верхнедолевым и левым главным бронхами. Схема резекции бронхов продемонстрирована на рис. 2.
Для профилактики возникновения бронхоплеврального свища мы использовали свободный неваскуляризированный плеврально-жировой лоскут с перикардиальной области.
После боковой торакотомии слева в 4-м межреберье выполнена ревизия, отдаленных метастазов не выявлено.
Выполнена систематическая лимфодиссекция: удалены лимфатические узлы бифуркации трахеи, субаортальной группы, легочной связки, корня легкого.
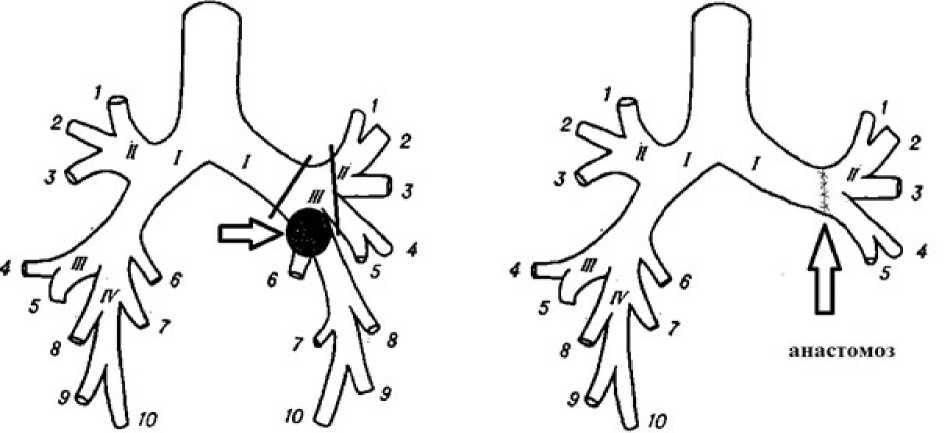
Рис. 2. Схема резекции бронхов и сформированного бронхиального анастомоза (на схеме стрелки указывают на опухоли и анастомоз между бронхами)
Нижняя легочная вена и нисходящий ствол легочной артерии выделены, перевязаны с прошиванием.
Выделены левый главный и левый верхнедолевой бронхи, выполнены циркулярные резекции данных бронхов с отступом от опухоли до 1 см (см. рис. 2).
После резекции бронхов выполнили гистологический контроль всех краев резекции и, убедившись в отсутствии атипичных клеток по краям резекции, сформировали циркулярный анастомоз бронхов непрерывным швом нерассасывающейся нитью пролен 3/0 между левым главным и верхнедолевым бронхами (рис. 3).
Выполнен контроль герметичности бронхиальных швов: герметичность достигнута.
Для дополнительного укрытия межбронхиального анастомоза из области перикарда переднего средостения сформирован свободный (без ножки) плеврально-жировой лоскут размерами 10×5×0,5 см. Данным лоскутом укрыт межбронхиальный анасто-
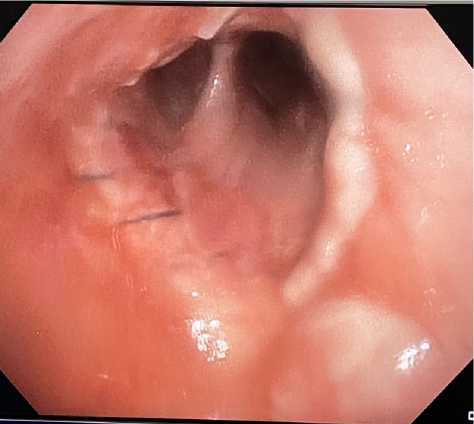
Рис. 3. Эндоскопическая картина анастомоза через 7 дней после операции моз, лоскут фиксирован за края 3 узловыми швами викрил 3/0.
Длительность операции – 135 мин. Объем кровопотери составил 200 мл.
Послеоперационный период протекал без осложнений. Удаление дренажей выполнено на 4-е сутки после операции. На 7-е сутки после вмешательства выполнен эндоскопический контроль (см. рис. 3), на котором зафиксирован герметичный межбронхиальный анастомоз, в некоторых местах анастомоза видна нить – пролен 3/0.
На 8-е сутки после хирургического лечения пациент выписан из стационара.
Окончательное гистологическое заключение: «Плоскоклеточная неороговевающая карцинома ткани легкого, умеренной степени дифференцировки, образование размером 3,0×2,0×1,0 см. Края резекции – роста атипичных клеток не обнаружено. Опухоль отстоит от края резекции по бронху на 1,0 см. В 22 исследованных лимфатических узлах опухолевого роста не выявлено, в них кониофиброз, липоматоз».
Окончательный клинический диагноз: «Центральный плоскоклеточный рак нижней доли левого легкого рT1cN0M0 R0G2 IA3-степени». С учетом радикального хирургического лечения и I стадии заболевания адъювантное лечение не назначено по решению консилиума врачей.
Через 30 мес после операции пациент продолжает наблюдаться у онколога по месту жительства без признаков рецидива и генерализации ЗНО. На рис. 4 представлены данные мультиспиральной компьютерной томографии ОГП с контрастным усилением через 18 мес после операции.
Обсуждение. Быстрому развитию бронхопластической хирургии РЛ способствовало стремление к органосохранным вмешательствам при центральных новообразованиях легкого. Реконструктивно-пластические операции при ЗНО применяют относительно редко, хотя многие авторы отмечают их высокую эффективность [7, 8].
Бронхопластическая резекция легкого дает возможность сохранить полноценный хирургический контроль над первичной опухолью с гораздо меньшими
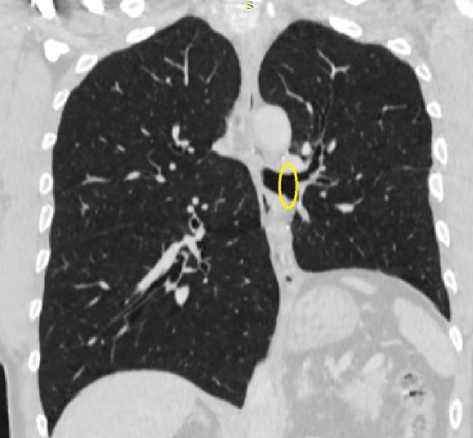
Рис. 4. Мультиспиральная компьютерная томография органов грудной полости с контрастным усилением (анастомоз указан желтым овалом) через 18 мес после хирургического лечения – признаков рецидива не выявлено последующими функциональными потерями. Целесообразность выполнения данного вида операции определяется в каждом отдельном случае индивидуально, стандартизованные подходы пока не разработаны.
Циркулярные бронхопластические операции в крупных лечебных центрах выполняются рутинно [2, 3]. Однако стоит указать, что рутинно выполняются верхние бронхопластические лобэктомии (справа или слева) с анастомозом главного и промежуточно-го/нижнедолевого бронха, когда оба бронха лежат на одной линии/плоскости, распределение натяжения нити – равномерное на протяжении всего бронхиального шва. При выполнении бронхопластической нижней лобэктомии необходимо создать анастомоз между главным и верхнедолевым бронхами, а они расположены друг к другу под углом, близким к 900 (см. рис. 2), поэтому распределение натяжения нити в шве циркулярного анастомоза неравномерное, что может приводить к прорезыванию нити и возникновению бронхоплеврального свища. Вследствие этого подобные операции выполняются редко, и поэтому необходимо дополнительное укрытие межбронхиального шва пластическим материалом для профилактики возникновения бронхоплеврального свища.
Чтобы минимизировать риск несостоятельности бронхиальных швов, хирурги предложили новую стратегию – дополнительное интраоперационное укрытие швов бронха. Для этого применяют различные пластические материалы, способные улучшить кровоснабжение тканей в зоне шва: мышечные лоскуты, париетальную плевру, диафрагмальный лоскут, непарную вену, перикардиальный лоскут и тимус. Особое значение укрытие бронхиальных швов приобретает при выполнении комбинированных резекций и в ситуации, когда перед операцией проводилось предоперационное лечение [9].
Несмотря на разнообразие существующих методик, специалисты не пришли к единому мнению о способах профилактики несостоятельности швов культи бронха. При этом данные, полученные в ходе исследований, имеют ограниченное применение при решении вопроса о дополнительном укрытии межбронхиальных анастомозов. В частности, использование мышечных лоскутов для укрытия межбронхиальных анастомозов сопряжено с риском стеноза в области анастомоза или тромбоза питающего лоскут сосуда и его некрозом, что ограничивает возможность применения данного метода [9].
При выборе лоскута для укрытия бронхиального шва рекомендуется руководствоваться определенными морфометрическими параметрами: длина лоскута должна соответствовать протяженности зоны герметизации, тогда как ширина должна находиться в минимально допустимых пределах, обеспечивающих сохранение функциональности соседних анатомических структур. Однако такая конфигурация создает риск нарушения кровоснабжения в дистальных участках трансплантата вследствие сужения сосудистого ложа. Именно поэтому в данном клиническом случае мы использовали свободный перикардиальный плеврально-жировой лоскут. Данный лоскут выкраивается из париетальной плевры с жировой клетчаткой в области перикарда переднего средостения. Технически такой стебель формируется без особых трудностей с времязатратностью не более 15 мин оперативного вмешательства.
Данным свободным лоскутом можно укрыть как бронхиальные швы культи бронха, так и швы межбронхиальных анастомозов после различных бронхопластических операций. Свободный лоскут дает возможность перемещать его в любое место, которое необходимо дополнительно укрыть, в то время как лоскуты на ножке ограничены в перемещении.
Выживаемость неваскуляризированного плеврально-жирового лоскута обусловлена характеристиками жировых клеток (адипоцитов) [10], обладающих способностью к пролиферации, дифференцировке и синтезу биологически активных веществ, обеспечивающих регенеративную активность тканей.
Заключение. Проведение бронхопластических операций позволяет обеспечить сохранение большего объема легочной паренхимы у пациентов и способствует улучшению качества их жизни по сравнению с пневмон- и билобэктомиями, при этом оставаясь радикальным методом лечения РЛ и не оказывая существенного негативного влияния на показатели без-рецидивной выживаемости больных.


