Циторедуктивные технологии лечения рака предстательной железы
Автор: Виланд В.Ф.
Журнал: Экспериментальная и клиническая урология @ecuro
Рубрика: Рак предстательной железы, рак почки
Статья в выпуске: 2-3, 2011 года.
Бесплатный доступ
Рак предстательной железы, циторедуктивные технологии
Короткий адрес: https://sciup.org/142187844
IDR: 142187844
Cytoreductive methods of prostate cancer treatment
Текст статьи Циторедуктивные технологии лечения рака предстательной железы
Университетская урологическая клиника г. Регенсбург, Германия
Рисунок 1. Сцинтиграфия скелета (метастазы в седалищную кость и позвоночник).
информированное согласие. Нужно быть готовым к тому, что если планируется циторедуктивная операция, то большинство пациентов будут искать второго мнения, или пожелают получить его уже после выполнения лечения.
При рассмотрении проблем циторедуктивного лечения очень важным является вопрос взаимоотношений «доктор-пациент». Самой распространенной моделью является «патриархальная». В этой модели врач думает: «Я знаю, что для вас лучше». Такая модель должна остаться в прошлом. Сегодня многим специалистам трудно принять решение пациента о получении второго мнения. Это вызывает негативные эмоции и негодование у докторов.
Современные права пациентов гласят: «Вы можете получить второе мнение:
-
• когда вы чувствуете, что на вас оказывается давление в принятии решения, и вы хотите получить больше информации;
-
• когда вы хотите узнать о других методах лечения;
-
• когда вам проведено лечение, и оно не увенчалось успехом;
-
• если у вас сложное, редкое заболевание и выбор лечения может существенно повлиять на вашу дальнейшую жизнь, трудоспособность, семейную жизнь;
-
• когда рекомендованное лечение, включающее открытую хирургию, опасно, имеет риск побочных явлений или необычно высокую цену;
Cytoreductive methods of prostate cancer treatment
W.F. Wieland
-
• когда ваши лечащие доктора не могут поставить диагноз».
Так, например, получение «второго мнения» European Consensus Group в 2006 г. при раке яичка дало неожиданные результаты, заключающиеся в том, что в 30% случаев не соблюдались рекомендации EAU по ведению и лечению таких пациентов. Результат применения системы «второго мнения»: в 40% случаев лечебная тактика была изменена (Schrader M., 2009).
Ситуация в государственной системе здравоохранения: каждый вид лечения оплачивается для каждого пациента. Но во многих медицинских областях, особенно в онкологии, пациенты, по крайней мере, частично оплачивают свое лечение после самостоятельного принятия решения о виде лечения совместно с лечащим врачом. Получение второго мнения стимулирует к заметным изменениям в лечении системного и местно-распространенного РПЖ.
Обычная ситуация при диагностированном РПЖ:
-
• хирургическое лечение резервируется для случаев локализованного РПЖ с неблагоприятным прогнозом при T3/4, N+, М+ (Swanson G., 2006).
-
• системное лечение распространенного заболевания с гор- a
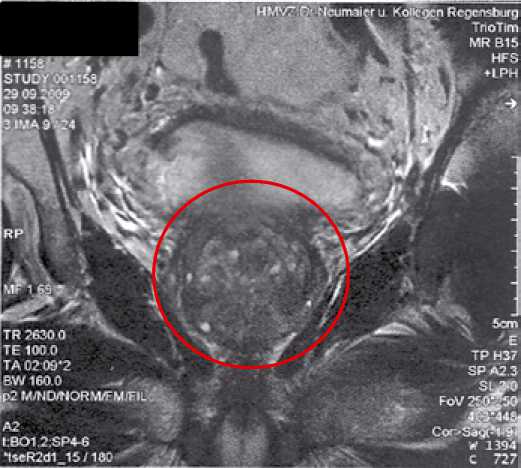
Рисунок 2. Местно-распространенный РПЖ на МРТ.
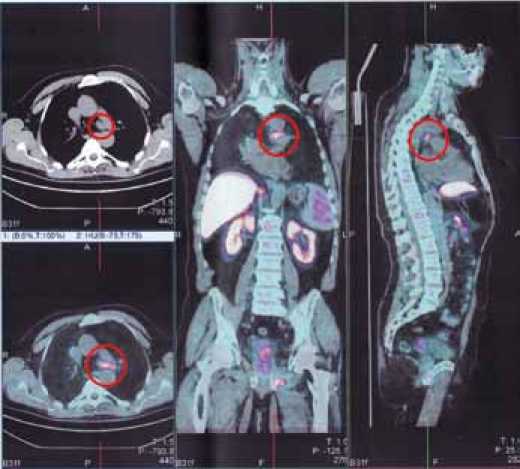
Рисунок 3. Метастазы в лимфоузлы средостения.
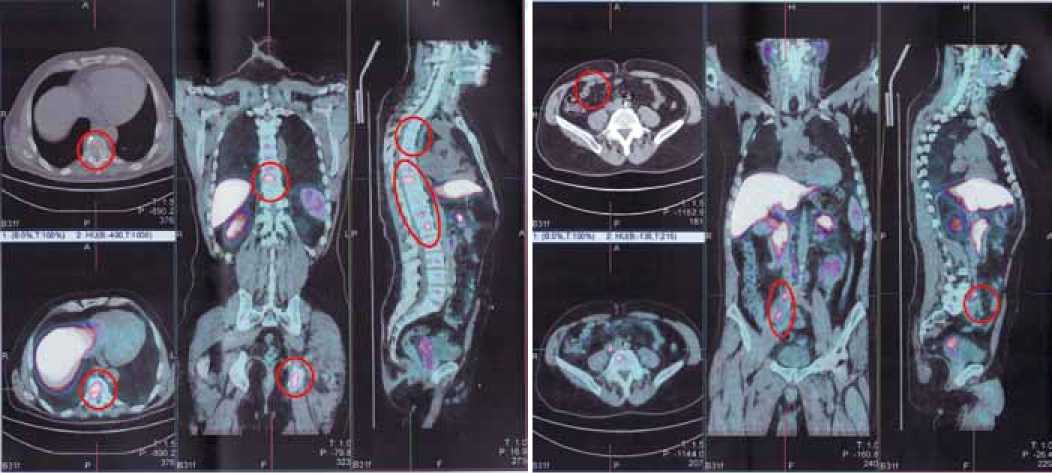
Рисунок 4. Метастазы в позвоночник и кости таза.
Рисунок 5. Метастазы в подвздошные лимфоузлы.
мональной или лучевой терапией – всегда ли необходимо и выполнимо?
Что делать в такой ситуации? Перенимать подходы из других областей онкологии, например, лечения генитального рака у женщин или почечно-клеточного рака. Это обеспечивает лучшую выживаемость у пациентов после полной резекции опухоли даже при метастатическом заболевании, а также прогностическое преимущество пациентов после идеальной резекции отдаленных метастазов в легком, печени и мозге.
На основании данных G. Swanson и др. стало известно, что специфическая выживаемость при РПЖ с метастазами в лимфоузлах увеличивается до 70% после простатэктомии и гормональной абляции в сравнении с 30%-ой выживаемостью без циторедуктивной хирургии. Местно-распространенный РПЖ (≥ pT3) показал лучшие показатели выживаемости у больных после радикальной простатэктомии и андрогенной блокады.
В случае инвазии опухоли предстательной железы в шейку мочевого пузыря, радикальная цисто-простатэктомия, сопровождаемая адъювантной гормональной терапией, может привести к хорошему местному онкологическому контролю, так же как и к лучшей РПЖ- специфической выживаемости: до 92% даже в случае метастазов в лимфатических узлах (Kumazawa T., 2009).
В случае РПЖ с метастазами в кости скелета экспериментальная циторедуктивная хирургия у определенной части пациентов (хорошее общее состояние, ПСА менее 100 нг/мл, небольшое число метастазов) могла бы привести к более длительному ответу при системном лечении (Swanson G., 2006).
КЛИНИЧЕСКИЙ СЛУЧАЙ
Мужчина, 63 лет, в отличной физической форме без боли и особого беспокойства по поводу своей бо-
ЭКСПЕРИМЕНТАЛЬНАЯ И КЛИНИЧЕСКАЯ УРОЛОГИЯ №2-3 2011

лезни. В 2009 г. установлен диагноз распространенного РПЖ на основании:
-
• повышения уровня ПСА до 60,3 нг/мл;
-
• показателя Глисона 9;
-
• данных сцинтиграфии (метастазы в Th9 и L4/5) (рисунок 1);
-
• данных МРТ (инфильтрация в семенные пузырьки, седалищную кость, лимфатические узлы) (рисунок 2).
Результаты были подтверждены с помощью ПЭТ-КТ с холином (рисунки 3, 4, 5): метастазы в Th8 и L1, L5 инфильтрация в семенные пузырьки, в левую седалищную кость, правую подвздошную кость, легкое и брюшную полость, лимфатические узлы средостения (2,3/2,6 см) и подвздошные лимфоузлы с двух сторон (1,4/1,6/1,1 см).
Был проведен международный консилиум в составе:
-
• профессор Per-Anders Abrahamson, Lund (Швеция);
-
• профессор Олег Иванович Апо-лихин, Москва (Россия)
-
• профессор Jelle Barentsz, Nijmegen (Нидерланды)
-
• профессор Christian Chaussy, Munich (Германия)
-
• профессор Manfred Herbst, Munich (Германия)
-
• профессор Wolf F. Wieland, Regensburg (Германия)
После презентации рекомендаций EAU, предлагающих гормональную терапию с применением аналогов ЛГРГ и антиандрогенов, пациенту было рекомендовано соответствующее лечение. Однако пациент отказался от данной тактики с просьбой проведения радикального лечения. Он хотел работать в следующем году с той же интенсивностью и мотивацией, и считал, что побочные эффекты гормонального лечения и местные симптомы распространения опухоли нарушат его образ жизни. Следуя пожеланиям пациента, мы начали неоадъювантную системную терапию бикалу-тамидом 150 мг и доцетакселом 75 мг/м2 внутривенно (3 цикла) с пер- спективой проведения циторедуктивной операции после повторного стадирования вслед за окончанием 3-го цикла доцетаксела. Результаты повторного стадирования в феврале 2010 г. (профессор Barentsz, Nijmegen, NL):
-
• местно-распространенный РПЖ с инвазией в правый семенной пузырек и треугольник Льето;
-
• различная по степени инфильтрация лимфоузлов таза, некоторые из них с активными клетками на Т3-МРТ;
-
• несколько костных метастазов, 2 из них – с опасностью перелома (Th9, и правая тазовая кость).
После проведения повторного ста-дирования консилиум специалистов предложил следующий вариант лечения: сальважная радикальная про-статвезикулэктомия с расширенной лимфодиссекцией и местной лучевой терапией метастазов позвоночника.
2 марта 2010 г. после снижения уровня ПСА до 0,57 нг/мл на фоне проведения неоадъювантной терапии в университете Регенсбурга была проведена позадилонная радикальная простатвезикулэктомия с расширенной лимфодиссекцией. Во время операции были стентированы оба мочеточника, мочеточниковые катетеры удалены на 4-е сутки, уретральный катетер удален на 10-е сутки после радиологического подтверждения состоятельности анастомоза. Длительность госпитализации составила 14 дней. Результаты гистологического исследования макропрепаратов: pT4, pN1 (4/22), L1, V1, R2 (скелетные), cM1.
Была сформулирована стратегия последующего лечения:
-
• продолжение лечения аналогами ЛГРГ;
-
• дополнительное назначение тамоксифена 20 мг/сут. для уменьшения побочных эффектов гормональной терапии;
-
• адъювантная лучевая терапия малого таза;
-
• поддерживающая терапия бисфосфонатами в/в каждые 4 недели.
В последующем:
-
• максимальная андрогенная блокада тренантоном (Leuprolide) каждые 3 месяца и бикалутами-дом 150 мг per os ежедневно;
-
• хорошее клиническое состояние;
-
• ПСА (0,70 нг/мл, на февраль