Действие криопреципитата на функцию печеночных клеток и признаки портальной гипертензии у больных циррозом печени
Автор: Карпова Радмила Владимировна, Черноусов А.Ф., Хоробрых Т.В., Яковенко А.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4 т.7, 2012 года.
Бесплатный доступ
Представлены результаты лечения 20 больных с циррозом печени, большинство из которых с декомпенсированным циррозом класса С по Child-Pugh. Всем больным пункционно под контролем УЗИ был введен криопреципитат в ткань печени. Результаты действия криопреципитата были изучены через 3 и 12 месяцев после введения. Положительная динамика отмечена у 85% больных с циррозом печени, которым был введен криопреципитат в цирротическую ткань. Из них 50% больных класса С по Child-Pugh перешли в класс В и А, 20% из класса В перешли в класс А. У 15% больных с функциональным классом А повышение количества баллов (более 6) не отмечено. Снижение портальной гипертензии через 12месяцев, отмечено у 66% больных, повышение - у 15%. Криопреципитат, веденный пункционно в ткань печени под контролем УЗИ, снижает параметры портальной гипертензии, улучшает функцию печеночных клеток.
Цирроз печени, криопреципитат, ультразвук
Короткий адрес: https://sciup.org/140188137
IDR: 140188137 | УДК: 616.153.96:616.149-008.341.1:616.36-004
Regeneration of cirrhotic liver under the influence of cryoprecipitate
Treatment results or 20 patients with severe liver cirrhosis were analyzed. All patients received cryoprecipitate intrahepatically. The results were analyzed after 6 and 12 months after the cryoprecipitate introduction. Improvement of the liver function was registered in 85% patients. Of them 50% changed the C stage cirrhosis by Child-Pugh on stage В and А, and 20% changed the B stage cirrhosis by Child-Pugh on stage A. Portal hypertension reduction was registered in 66% of the treated patients. The study vividly demonstrated, that the intrahepatic introduction of cryoprecipitate allows the stimulation of liver reparative regeneration, improves protein-synthetic liver function, decreases encephalopathy rate.
Текст научной статьи Действие криопреципитата на функцию печеночных клеток и признаки портальной гипертензии у больных циррозом печени
В отечественной и зарубежной литературе накоплен значительный опыт диагностики и лечения больных циррозом печени [5, 14, 17, 23, 24]. Однако существуют проблемы излечения таких больных. Несмотря на применение современных гепатопротекторов и противовирусных препаратов для лечения больных циррозом печени, ежегодно в мире от этого заболевания погибает 300 000 больных [5, 14, 17]. Известны различные способы хирургической стимуляции регенерации, в частности: лазерная, посегментарная резекция печени, интраоперационная лазерная и электрокоагуляция поверхности печени, криодеструкция печени, а также введение различных препаратов (стволовые клетки, гормоны и.т.д) [4, 12, 13, 22, 23, 24]. К сожалению, большинство из вышеуказанных способов является достаточно травматичным для цирротически измененной печени, а их стимулирующий эффект кратковременен. Считается, что стимуляторами регенерации печени являются вещества, образующиеся в момент гибели печеночных клеток на месте нанесения одного из видов хирургического или термического воздействия [13, 15, 17, 19, 24]. Наиболее эффективным методом является трансплантация печени, до которой большинство больных не доживает [3].
Для стимуляции регенерации цирротически измененной ткани печени нами применен высококонцентрированный раствор фибриногена (криопреципитат). В состав криопреципитата входят фибриноген, фибринста-билизирующий фактор FXIII, фибронектин, плазминоген, альбумин и глобулярные фракции, а так же иммунорегулирующий комплекс. Криопреципитат активизирует местные репаративные процессы за счет уникальных биологических свойств фибриногена, являющегося природной матрицей регенерации [15].
При динамическом исследовании в экспериментах на кроликах нами доказано, что высококонцентрированный раствор фибриногена, введенный пункционным методом в цирротически измененную ткань печени, является стимулятором ее регенерации, что улучшает клиническую и морфологическую картину заболевания. Основываясь на данные эксперимента, о положительном влиянии криопреципитата на течение цирроза печени, мы применили его в лечении больных циррозом печени токсической и вирусной этиологии (гепатит С и В) [15].
Материалы и методы исследования
На кафедре факультетской хирургии № 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, с апреля 2010 г. по сентябрь 2011 г. под наблюдением находилось 20 пациентов с циррозом печени. Мужчин было 11, женщин — 9. У 9 (45%) пациентов цирроз был токсической этиологии, у 9 (45%) смешанной: вирусной (гепатит С или В) и токсической, у 2(10%) вирусной этиологии (гепатит С и В). У всех больных был диагностирован цирроз печени на основании клинико-лабораторных данных. У 12 (60%) больных диагноз был подтвержден морфологическим исследованием пункционного материала из печени. У 8 (40%) больных диагностическую пункцию не выполняли из-за выраженной коагулопатии и тромбоцитопении. Всем 20 исследуемым был введен криопреципитат (по 2 мл) в каждый сегмент печени, кроме первого, чрескожно под контролем УЗИ. У больных

Карпова Р.В., Черноусов А.Ф., Хоробрых Т.В., Яковенко А.В.
ДЕЙСТВИЕ КРИОПРЕЦИПИТАТА НА ФУНКЦИЮ ПЕЧЕНОЧНЫХ КЛЕТОК И ПРИЗНАКИ ПОРТАЛЬНОЙ ГИПЕРТЕНЗИИ У БОЛЬНЫХ ЦИРРОЗОМ ПЕЧЕНИ с выраженной коагулопатией и тромбоцитопенией, после введения криопреципитата в печень, на выходе иглы из пункционного канала вводили тромбин 600–800 МЕ, растворенный в 2–3 мл 10% хлористого кальция. Таким образом, мы препятствовали развитию кровотечения из места пункции. Криопреципетат в печень вводили через иглу 25 G для спинномозговой пункции по 2 мл в каждый сегмент органа. Действие криопреципитата на регенерацию печени оценивали по клинико-лабораторным данным через 3 и 12 месяцев. Осложнений во время проведения операции введения криопреципитата не отмечено.
Признаки портальной гипертензии, структуру и размеры печени мы оценивали на основании данных УЗИ брюшной полости, которое позволяло измерять: диаметр и линейную скорость кровотока (ЛСК) в воротной и селезеночной венах, размеры и плотность печени, размеры селезенки, наличие асцита (рис. 1, рис. 2). Для определения степени компенсации функций печени применяли классификацию Child-Pugh. Класс А — от 5 до 6 баллов, класс В от 7 до 9 баллов, класс С от 10 до15 баллов. Баллы оценивали по наличию асцита, энцефалопатии, уровню билирубина, альбумина и протромбиновому времени [17].
Результаты и их обсуждение
До введения криопреципитата в ткань печени цирроз класса В по Child-Pugh был диагностирован у 6 (30%) пациентов, класс А — у 3(15%) из 20, класс С — у 11(55%).
После введение криопреципитата в ткань печени мы выявили положительную динамику клинико-лабораторных данных по классу Child-Pugh у 19 (95%) больных, у одного (5%) больного с циррозом класса С динамики выявлено не было из-за выраженного фиброза стромы печени и массивной гибели гепатоцитов. После лечения большинство 9 из 11 (81,8%) больных циррозом класса С по Child-Pugh перешли в группу класса В. Количество баллов с 10–15 снизилось до 7–9 по наличию асцита, альбумина, и протромбинового индекса (см. табл. 2). У одного (из 11) пациента с циррозом класса С изменений клинико-лабораторных данных не было как до, так и после введения криопреципитата, у другого цирроз из класса С перешел в класс А. При исследовании 6 больных с циррозом класса В мы отметили: что у 4 из них цирроз перешел в класс А, у двоих изменений отмечено не было. Ухудшения клинико-лабораторных данных у больных циррозом класса А, мы не отметили. Таким образом, через 12 месяцев после введения криопреципитата в ткань печени под контролем УЗИ, мы отметили статистически значимое (р < 0,01) улучшение клинико-лабораторных показателей у всех 20 больных (табл. 1, табл. 2).
По данным УЗИ брюшной полости через 3 и 12 месяца после введения криопреципитата отмечено уменьшение размеров печени и признаков воспаления у 11(55%) больных с циррозом класса В и С в равной
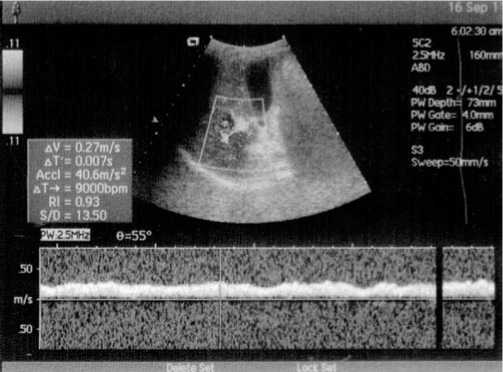
Рис. 1. Линейная скорость кровотока в воротной вене
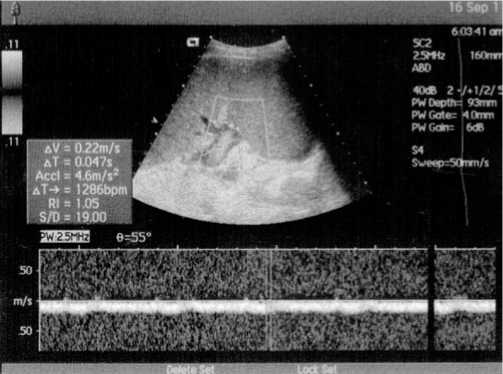
Рис. 2. Линейная скорость кровотока в селезеночной вене
Табл. 1. Действие криопреципитата на функциональный класс по классификации Child-Pugh у больных цирроза печени
|
Функциональный класс цирроза печени по Child-Pugh |
До введения криопреципитата (n = 20) |
После введения криопреципитата (n = 20) |
|
Класс А |
3 (15%) |
8 (40%) |
|
Класс В |
6 (30%) |
11(55%) |
|
Класс С |
11(55%) |
1 (5%) |
Табл. 2. Количество баллов по шкале Child-Pugh до и после введения криопреципитата в ткань печени (средние величины)
|
Лечение |
Асцит |
Энцефалопатия |
Билли-рубин |
Альбумин |
Протромбиновый индекс |
|
до |
12 ± 3 |
5 ± 1,25 |
7 ± 1,75 |
12 ± 3 |
11 ± 2,75 |
|
Через 3 месяца |
7 ± 1,75 |
3 ± 0,75 |
3 ± 0,75 |
7 ± 1,75 |
9 ± 2,25 |
|
Через 12 месяцев |
2 ± 0,5 |
0 |
1 ± 0.25 |
2 ± 0,5 |
7 ± 1,75 |
|
Р |
Р < 0,05 |
Р < 0,05 |
Р < 0,05 |
Р < 0,05 |
Р < 0,05 |

Карпова Р.В., Черноусов А.Ф., Хоробрых Т.В., Яковенко А.В.
ДЕЙСТВИЕ КРИОПРЕЦИПИТАТА НА ФУНКЦИЮ ПЕЧЕНОЧНЫХ КЛЕТОК И ПРИЗНАКИ ПОРТАЛЬНОЙ ГИПЕРТЕНЗИИ У БОЛЬНЫХ ЦИРРОЗОМ ПЕЧЕНИ степени (р < 0,05). Данная положительная динамика связано с перенесенным острым гепатитом в активной фазе цирроза печени, это соответствует данным литературных источников [6, 9, 10, 11, 14, 17].
Сохранение размеров печени, без увеличения очагов некроза, диагностировано у 4(20%) больных с циррозом класса В вирусной этиологии (гепатит НСV — ПЦР исследование). Сохранение размеров печени у больных с выраженным фиброзом печени (класса В и С по Child-Pugh) очень важно, так как гибель гепатоцитов и разрастание соединительной ткани ведет к уменьшению размеров печени [10, 11, 14, 17].
У 5(25%) больных класса А и В имело место увеличение размеров печени при нормальных показателях трансаминаз и билирубина. Данное увеличение связано с регенерацией печени, так у данных больных изменилась структура печени: появились участки, соответствующие нормальной структуре печени, плотность печени и зоны фиброза были меньше чем до лечения [14, 17].
Сопоставляя вышеописанные данные УЗИ с лабораторными показателями крови исследуемых, мы выявили снижение билирубина, уменьшение трансаминаз, увеличение альбумина, уменьшение или отсутствие асцита, особенно у 11(55%) больных (классом В и С) после снижения активности цирроза печени (табл. 2).
Линейную скорость кровотока (ЛСК) мы измеряли в воротной и селезёночной венах. В среднем, этот показатель по нашим данным составлял: в воротной вене — 13,9 ± 4,3 см/с; в селезёночной вене — 17,3 ± 6,0 см /с. При этом у здоровых лиц ЛСК в воротной вене была 17,2 ± 2,5 см/с, а в селезёночной вене — 15,2 ± 2,4 см/с. По литературным данным нормальный уровень ЛСК в воротной вене варьируется в широких пределах от 12–16 см/с до 23 см/с и более [7, 8]. Различия могут быть обусловлены субъективными факторами: различные аппараты, специалисты, исследование на вдохе и выдохе, локализация измерения. Большинство публикаций свидетельствуют о том, что ЛСК при ЦП может как уменьшаться, так и оставаться в нормальных пределах [7, 8, 19].
Изменение диаметра воротной вены в сторону уменьшения, через 3 и 12 месяцев после введения криопреципитата в печень, мы наблюдали у 11(55%) больных (рис. 4), что было обусловлено снижением ЛСК в портальной системе без перераспределения кровотока в селезеночную вену. По данным УЗИ прогрессирование перипортального фиброза не было. Это означает, что криопреципитат, стимулируя регенерацию печени, возможно уменьшает перипортальный фиброз, улучшает микроциркулярное кровообращение в печени, снижая при этом портальную гипертензию[1, 8, 11, 16, 21]. У 9(45%) больных диаметр воротной вены существенно не изменился.
Уменьшение скорости кровотока, через 3 и 12 месяцев после введения криопреципитата в печень, на 6–8 см/с в воротной вене было у 10(50%) больных с циррозом
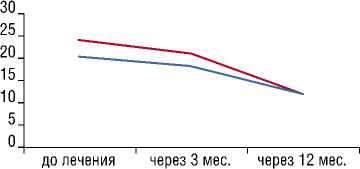
---- скорость кровотока в селезеночной вене
----скорость кровотока в портальной вене
Рис. 3. Скорость кровотока в воротной и селезеночной венах до и после лечения больных циррозом печени криопреципитатом (средние величины см/с)
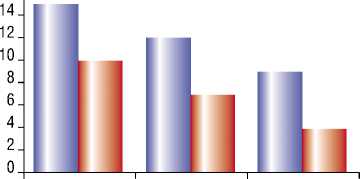
I ■ диаметр воротной вены
I ■ диаметр селезеночной вены
Рис. 4. Диаметр воротной и селезеночной вен до и после лечения больных криопреципитатом (средние величины в мм)
преимущественно класса В и С по Child-Pugh (р < 0,01) (рис. 3). У 5(25%) больных скорость кровотока не изменилась как через 3, так и через 12 месяцев, в основном это были пациенты с декомпенсированным циррозом класса С. Снижение скорости кровотока в воротной и селезеночной венах на фоне сохранения или уменьшения их диаметра, доказывает отсутствие прогрессирования портальной гипертензии [6, 7, 13, 14, 17]. У 5(25%) больных скорость кровотока в воротной вене увеличилась на 2–4 см/с, у 4 за счет снижения скорости кровотока и диаметра селезеночной вены. Таким образом, кровоток устремился в сторону воротной вены, что не наблюдают авторы литературных источников, при прогрессировании цирроза печени [7, 8, 16]. У 1 (из 5) больного с декомпенсированным циррозом класса С (15 баллов), увеличение ЛСК в воротной вене было за счет уменьшения ее диаметра, на фоне развития перипортального фиброза.
У 8(40%) больных (с циррозом класса В и С по Child-Pugh), мы выявили уменьшение размеров селезенки на 2–4 см, за счет снижения портальной гипертензии и снижения скорости кровотока на 4–8 см/с по селезеночной вене. Сохранение размеров селезенки отмечено у 12(60%) больных циррозом класса В (1 больной) и С (11 больных) по Child-Pugh.
Увеличение диаметра селезеночной вены мы не наблюдали, как через 3 так и через 12 месяцев. Это
Карпова Р.В., Черноусов А.Ф., Хоробрых Т.В., Яковенко А.В.
ДЕЙСТВИЕ КРИОПРЕЦИПИТАТА НА ФУНКЦИЮ ПЕЧЕНОЧНЫХ КЛЕТОК И ПРИЗНАКИ ПОРТАЛЬНОЙ ГИПЕРТЕНЗИИ У БОЛЬНЫХ ЦИРРОЗОМ ПЕЧЕНИ свидетельствует об отсутствии нарастания портальной гипертензии, на фоне регенерации печени [2, 3, 8, 16, 20]. Сохранение диаметра селезеночной вены констатировали у 9(45%) пациентов с циррозом класса С по Child-Pugh, у 11(55%) с циррозом печени класса В было отмечено уменьшение селезеночной вены на 3–4 мм (рис. 4).
Скорость кровотока в селезеночной вене у большинства больных по данным УЗИ либо сохранялась, либо уменьшалась. У 8(40%) исследуемых она сохранила свои показатели, у других 8(40%) уменьшилась на 8–10 см/с (р < 0,05)(рис. 3). Следовательно, сохранение и уменьшение скорости кровотока и диаметра селезеночной вены подтверждает регенерирующее действие криопреципитата на ткань печени [4, 13]. Регенерация печени вероятно снижает давление в портальной и в селезеночной вене [13]. У 4(20%) больных было отмечено увеличение скорости кровотока в селезеночной вене на 5–7 см/с, за счет уменьшения диаметра селезеночной вены (р > 0,05).
Таким образом, анализируя ультразвуковое исследование размеров селезенки, портальной системы, можно утверждать, что криопреципитат введенный в ткань печени под контролем УЗИ снижает показатели портальной гипертензии у 66% больных. У 19% больных изменения параметров портальной гипертензии не было. У 15% больных скорость кровотока в селезеночной вене возрасла без статистически достоверной вероятности (р > 0,05), т.е данное незначительное изменение было не существенным для возникновения кровотечения. Повышение портальной гипертензии было за счет уменьшения диаметра воротной и селезеночной вен. Криопреципитат, введенный в ткань печени, улучшает ее микроциркуляцию, снижает скорость кровотока в воротной и селезеночной венах, тем самым улучшая регенерацию печени у большинства больных
Следовательно, положительная динамика как через 3 так и через 12 месяцев, отмечена у 85% больных с циррозом печени, из них 50% больных из класса С по Child-Pugh перешли в класс В и А, 20% из класса В перешли в класс А. У 15% больных циррозом печени классом А мы отметили снижение от 2 до 4 баллов по всем параметрам шкалы Child-Pugh (табл. 2). Снижение портальной гипертензии отмечено у 66% больных. Незначительное повышение портальной гипертензии у 15% больных было обусловлено уменьшением диаметра воротной и селезеночной вен.
Анализируя данные УЗИ печени, ее структуру, размеры, измеряя параметры портальной гипертензии, и коррелируя это с морфологическим исследованием пунктатов печени можно предположить, что криопреципитат вызывает регенерацию печени. У 10 (50%) пациентов (которым была выполнена биопсия печени) с выраженным фиброзом 4 стадии по Knodell, после введения криопреципитата, отмечено снижение степени гистологической активности и появление признаков регенерации (двуядерные, гипертрофированные гепатоциты с правильным балочным строением) (рис. 5, рис. 6).
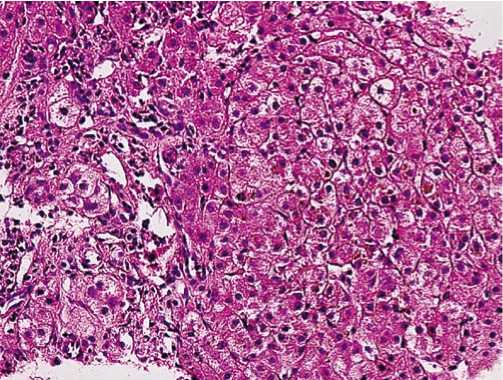
Рис. 5. Ложная долька печени: пролиферирующие гепатоциты, с нарушенным балочным строением. В просветах синусоидов увеличено количество лейкоцитов. Окр. гематоксилин-эозин. х 200
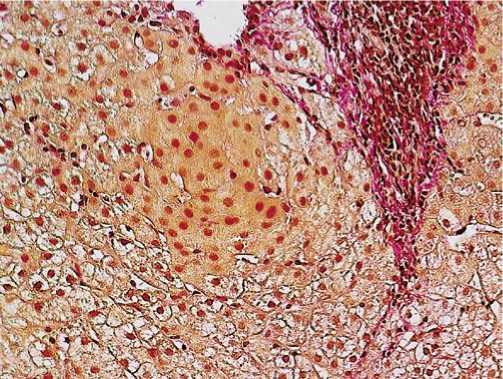
Рис. 6. Участок регенерации (двуядерные, пролиферирующие гепатоциты с правильным балочным строением), оттесняющий фиброзную ткань. Окр. пикрофуксин. х 200
Выводы
Таким образом, криопреципитат, веденный посег-ментарно в ткань печени под контролем УЗИ, улучшает функциональный класс (А, В, С) цирроза печени по классификации Child-Pugh: повышая альбумин и протромбиновый индекс, уменьшая асцит, энцефалопатию, уровень билирубина. На основании данных УЗИ, а именно диаметра и ЛСК воротной и селезеночной вен, криопреципитат либо снижает либо сохраняет признаки портальной гипертензии. Положительное воздействие криопреципитата на структуру печеночной ткани, подтверждено морфологическим исследованием пунктата ткани органа до и после введения препарата.
Карпова Р.В., Черноусов А.Ф., Хоробрых Т.В., Яковенко А.В.
ДЕЙСТВИЕ КРИОПРЕЦИПИТАТА НА ФУНКЦИЮ ПЕЧЕНОЧНЫХ КЛЕТОК И ПРИЗНАКИ ПОРТАЛЬНОЙ ГИПЕРТЕНЗИИ У БОЛЬНЫХ ЦИРРОЗОМ ПЕЧЕНИ
Список литературы Действие криопреципитата на функцию печеночных клеток и признаки портальной гипертензии у больных циррозом печени
- Афукова О.А. Сравнительная оценка ультразвукового и компьютерно-томографического методов исследования в диагностике цирроза печени: автореф. дис.. канд. мед. наук/О.А. Афукова. -Москва, 2006. -31с.
- Борисов А.Е. Оценка эффективности доплерографии у больных с диффузными заболеваниями печени с синдромом портальной гипертензии/А.Е. Борисов, В.А. Кащенко//Вестник хирургии. -2002. № 2. -С. 26-31.
- Готье С.В. Ортотопическая трансплантация печени в лечении ее диффузных и очаговых заболеваний/С.В. Готье, А.К. Ерамишанцев, О.М. Цирульникова//Анналы хирургической гепатологии. -1996. -Т 1, № 2. -С. 38-51.
- Ишенин Ю.М. Хирургия цирроза печени/Ишенин Ю.М., Потапов А.В., Чесновский В.М. -Нижнекамск, 2005. -104 с.
- Ивашкин В.Т. Клиническая гепатология сегодня и завтра/В.Т.Ивашкин, A.О. Буеверов//Российский журнал гастрэнтерологии, гепатологии, колопроктологии. -2002. -Т. 12, № 1. -С. 4-9.
- Ивашкин В.Т. Фиброз печени/В.Т.Ивашкин, Ч.С. Павлов-М.: Видар, 2011. -168 с.
- Камалов Ю.Р. Значение ультразвукового исследования при хронических диффузных заболеваниях печен: автореф. дис.. канд. мед. Наук/Ю. Р. Камалов, -Москва,1987. -42 с.
- Мардарьева С.В. Портальная гипертензионная гастропатия как проявление портальной гипертензии при циррозе печени (клинико-лабораторные и инструментальные корреляции и особенности терапии): автореф. дис. канд.мед. наук/С.В. Мардарьева. -Москва, 2006. -35 с.
- Митьков В.В. Оценка портального кровотока при циррозе печени/В.В. Митьков, М.Д. Митькова, И.Г. Федотов//Ультразвуковая диагностика. -2000, № 4. -С. 10-17.
- Митьков В.В. Допплерография в диагностике заболеваний печени, желчного пузыря, поджелудочной железы и их сосудов/В.В.Митьков. -М.: Видар. 2000. -152 с.
- Митьков В.В. Практическое руководство по ультразвуковой диагностике/B.В.Митьков. -М: Видар. 2005. -С. 31-32.
- Муслимов С.А. Морфологические аспекты регенеративной хирургии/С.А. Муслимов. -Уфа: Башкортостан, 2000. -165 с.
- Нартайлаков М.А. Регенеративная хирургия хронических гепатитов и циррозов печени/М.А. Нартайлаков, С.А. Пышкин, С.Б. Цирятьевой. -Уфа: Башкортостан, 2008. -283 с.
- Павлов Ч.С. Фиброз печени при хронических вирусных гепатитах В и С: автореф. дис.. док. мед. Наук/Ч.С. Павлов. -Москва, 2008. -31с.
- Хоробрых Т.В. Фибриновый клей в неотложной абдоминальной хирургии: автореф. дисс. д-ра. мед. наук./Т.В. Хоробрых. -Москва, 2005. -36 с.
- Хоробрых Т.В., Мардарьева С.В., Карпова Р.В. Коррекция портальной гипертензии как профилактика кровотечения у больных циррозом печени/Т.В.Хоробрых, С.В. Мардарьева, Р.В. Карпова//Вестник хирургической гастрэнтерологии. -2011. № 2. -С. 14-18.
- Шерлок Ш. Заболевания печени и желчных путей/Шерлок Ш. -М.: ГЭОТАР, 1999. -860 с.
- Шумаков В.И. -Транспланталогия/В.И. Шумаков. -Тула: Медицина,1995. -С. 275-280.
- Черноусов А.Ф. Малоинвазивные хирургические вмешательства под контролем УЗИ в лечении диффузных заболеваний печени/А.Ф.Черноусов Т.В. Хоробрых, Р.В. Карпова//Вестник хирургической гастроэнтерологии. -2011. № 4. -С. 4-9.
- Adrian К.Р. Can Doppler Sonography Grade the Severity of Hepatitis Celated Liver Disease/К.Р. Adrian. AJR, 2005: Vol. 184. -P. 1848-1853.
- O’Donohue J Ng C, Diagnostic value of Doppler ssessment of the hepatic and portal vessels and ultrasound of the spleen in liver disease/Ng C O’Donohue, S. Catnach, R. Williams//European journal of gastroenterology & hepatology. -2004. -Vol. 1, № 2. -P. 147-155.
- Malouf N.N. Adult-derived stem cells from the liver become myocytes in the heart in vivo/N.N. Malouf, W.B. Coleman, J.W. Grisham, R.A.[et al]//Am. J. Pathol. -2001. -Vol. 158. -P. 1929-1935.
- Hirokazu Nagai. Differentiation of liver epithelial (stem-like) cells into hepatocytes induced by coculture with hepatic stellate cells/Nagai Hirokazu. Kunihiko Terada//Biochemical and Biophysical Research Communications.-2002. -Vol. 293. -Р. 1420-1425.
- Theise N.D. Liver from bone marrow in humans/N.D.Theise, M. Nimmakayalu, R. Gardner//Hepatology. -2000. Vol. 32. -Р. 11-16.


