Денситометрическое определение эфедрина в судебно-химической практике
Автор: Кормишин Василий Алексеевич, Воронин Александр Васильевич, Шаталаев Иван Федорович
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Коррекция экологического неблагополучия
Статья в выпуске: 5-3 т.14, 2012 года.
Бесплатный доступ
Определены аналитические характеристики методики анализа эфедрина методом тонкослойной хроматографии с применением денситометрии. Предел обнаружения эфедрина составляет 1,0 мкг в пробе. Показана возможность количественного определения эфедрина в модельных образцах в диапазоне концентраций 10,0-250,0 мкг/мл.
Эфедрин, денситометрия, тонкослойная хроматография
Короткий адрес: https://sciup.org/148201588
IDR: 148201588 | УДК: 340.67:615.214.2.099.074:543.544
Densitometric ephedrine'S definition in judicial and chemical practice
Analytical characteristics of a technique for the ephedrine analysis by a method of thin layer chromatography with densitometry application are defined. The detection limit of ephedrine makes 1,0 mkg in test. Possibility of quantitative ephedrine definition in modeling samples in a range of concentration of 10,0-250,0 mkg/ml is shown.
Текст научной статьи Денситометрическое определение эфедрина в судебно-химической практике
(версия 3.12, разработчик Плахотний И.Н., г. Днепропетровск). Принцип обработки графических файлов данной программой аналогичен работе двухлучевого денситометра [8].
Цель работы: определение некоторых аналитических характеристик и возможностей количественного определения методики судебно-химического исследования биологических жидкостей на эфедрин методом ТСХ с применением компьютерной денситометрии.
Материалы и методы. Материалы исследования: стандартный раствор эфедрина в метаноле концентрации 1,0 мг/мл (фирма «ABBOTT»), модельные образцы мочи, содержащие определенные концентрации эфедрина, образцы мочи, не содержащие наркотических средств и психотропных веществ. Для приготовления растворов стандартных образцов использовали метанольный раствор эфедрина концентрации 1,0 мг/мл. Модельные образцы мочи готовили путем добавления расчетного количества вышеуказанного раствора в образцы мочи, не содержащие наркотических средств, психотропных и лекарственных веществ. В работе были использованы методы ТСХ, денситометрии (с использованием компьютерной программы для обработки изображений «ТСХ-менеджер»), регрессионный статистический анализ.
Условия хроматографического анализа: пластины для ТСХ «Сорбфил ПТСХ-П-А», системы растворителей для ТСХ – этилацетат-мета-нол-25% раствор аммиака (17:2:1) [1]; метанол-25% раствор аммиака (100:1,5) [3]. Объем пробы, наносимой на пластинку – 100 мкл; проявление – обработка 0,5% раствором нингидрина в ацетоне с последующим нагреванием в токе воздуха при 800С в течение 15 мин [7].
Пробоподготовку модельных проб мочи осуществляли методом жидкость-жидкостной экстракции: к 2 мл мочи добавляли 25% раствор аммиака до рН 10-11, затем проводили экстракцию 5 мл смеси хлороформ-н-бутанол (9:1) в течение 5 мин, операцию повторяли дважды [2, 5]. Водный раствор отбрасывали, органическую фазу упаривали в токе воздуха при комнатной температуре. Сухой остаток растворяли в 0,5 мл хлороформа. 100 мкл полученного раствора наносили на линию старта хроматографической пластины, хроматографировали и денситомет-рировали.
Результаты и их обсуждение. Для исследования была выбрана методика анализа эфедрина методом ТСХ, используемая в практике судебно-химического отделения Ульяновского областного бюро судебно-медицинской экспертизы [7]. Основной проблемой ТСХ-анализа эфедрина с визуальной регистрацией является невозможность сохранения результатов - «пятна» (зоны на хроматограмме, соответствующие эфедрину) после проявления теряют интенсивность окраски в течение 15-20 мин; и как следствие невозможность выполнения повторных измерений величины Rf и оценки количественного параметра - площади «пятна». Кроме того, фоновая составляющая хроматограммы выступает в роли значимого фактора, способствующего повышению величины предела обнаружения эфедрина, т.е. снижению чувствительности анализа.
Пластинки после хроматографирования, проявления и высушивания сканировали на планшетном сканере и фотографировали с помощью цифрового фотоаппарата, полученные файлы формата .jpeg обрабатывали с помощью программы «ГСХ-менеджер». Таким образом, сама хроматографическая пластинка утрачивала значение носителя аналитической информации, ее замещал электронный образ. При исследовании растворов стандартного образца эфедрина в диапазоне концентраций 10,0-250,0 мкг/мл проводили по 10 параллельных определений. Полученные результаты представлены в табл. 1.
Таблица 1. Аналитические характеристики методики определения эфедрина методом тонкослойной хроматографии
|
Хроматографическая система |
Эффективность растровых манипуляций |
Предел обнаруже ния, мкг |
Величина Rf |
|
этилацетат-метанол-25% раствор аммиака (17:2:1) |
+ |
1,0 |
0,21 ±0,05 |
|
метанол-25% раствор аммиака (100:1,5) |
++ |
1,0 |
0,36 ±0,03 |
Примечание: «+» - просмотр изображения в негативе; «++» - просмотр изображения в негативе с увеличением резкости изображения
На основании вышеуказанных результатов, интервал поиска Rf для эфедрина в компьютерной программе был задан на уровне 0,1, т.е. в диапазоне ± 0,05 от среднего значения Rf. Значение предела обнаружения составило 1,0 мкг эфедрина в пробе. При исследовании модельных образцов мочи также удалось достичь предела обнаружения около 1,0 мкг в пробе за счет применения растровых манипуляций с электронным образом хроматограммы - изменения резкости, интенсивности изображения, изменения параметров яркости и контрастности, возможности просмотра хроматограммы в негативе. Данные манипуляции позволяют сделать почти незаметное для человеческого глаза «пятно» анализируемого вещества четко детектируемым. На рис. 1 приведены хроматограммы модельных образцов мочи с концентрациями эфедрина 10,0, 50,0,200,0,250,0 мкг/мл.
Градуировочная зависимость «площадь пятна (Y) - количество эфедрина, мкг (X)», построенная в диапазоне концентраций 10,0-250,0 мкг/мл, описывается уравнением полиномиальной (квадратичной) регрессии. Однако для установления данной зависимости необходимо использовать более трех растворов стандартного образца вещества различных концентраций (градуировочных образцов), что в условиях повседневной аналитической практики приведет к снижению производительности анализа. Для упрощения аналитической задачи нами было предложено применение линейной регрессии, количество градуировочных образцов было уменьшено до двух, при этом относительная ошибка определения не превышала 35%, что приемлемо для предварительного этапа анализа. Вышеуказанные зависимости были определены для вариантов анализа с применением в качестве источника электронного образа хроматограммы планшетного сканера и цифрового фотоаппарата (табл. 2).
Результаты контроля правильности методики определения эфедрина с применением его контрольных растворов (приготовленных независимо от градуировочных образцов) при использовании различных комбинаций пар градуировочных образцов представлены в табл. 3.

б)
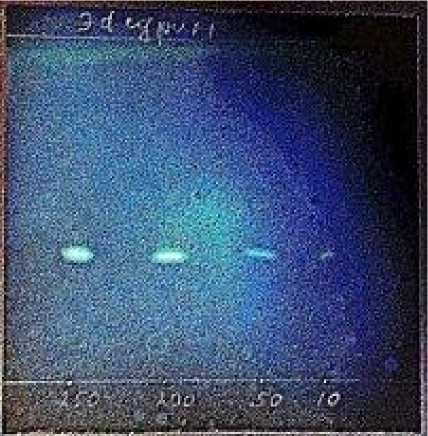
в)
Рис.1. Хроматограммы модельных образцов мочи с концентрацией эфедрина 10,0, 50,0, 200,0, 250,0 мкг/мл:
а – после обработки 0,5% раствором нингидрина в ацетоне без растровых манипуляций; б – просмотр в негативе; в – просмотр в негативе с увеличением резкости изображения
Относительная ошибка определения среднего значения содержания эфедрина в пробе в диапазоне концентраций 10,0-250,0 мкг/мл не превышает соответственно 35% при использовании для получения электронного образа хроматограммы цифрового фотоаппарата, и 7,8% – в случае сканирования хроматографических пластинок, последний вариант является наиболее предпочтительным. Наименьшая величина ошибки достигается при концентрации эфедрина в пробе 100,0 мкг/мл.
Таблица 2. Градуировочные характеристики количественного денситометрического определения эфедрина
|
Источник электронного образа |
Полиномиальная регрессия |
Линейная регрессия |
|
сканер |
Y=0,009∙X2+73,9∙X+274,4 |
Y=76,9∙X-46,3 |
|
фотоаппарат |
Y= 0,025∙X2+66,5∙X-569,7 |
Y=61,4∙X+477,2 |
Таблица 3. Результаты контроля правильности количественного денситометрического определения эфедрина
|
Градуировочные образцы, мкг/мл |
Контрольный раствор, мкг/мл |
Относительная ошибка |
|
|
фотоаппарат |
сканер |
||
|
250,0; 100,0 |
10,0* |
35,00 |
7,80 |
|
100,0; 10,0* |
250,0 |
13,00 |
3,10 |
|
250,0; 10,0* |
100,0 |
14,00 |
0,30 |
Примечание: * – концентрация стандартного метанольного раствора эфедрина 10,0 мкг/мл при объеме, наносимой на пластинку пробы 100 мкл соответствует пределу обнаружения
Выводы: вышеописанный методический подход в настоящее время внедряется в практику судебно-химического отделения Ульяновского областного бюро судебно-медицинской экспертизы, поскольку является экспрессным, технически доступным и экономически приемлемым вариантом предварительного исследования эфедрина в биологических жидкостях. Анализ проводится сериями с использованием градуировочных образцов – метанольных растворов эфедрина с концентрацией 10,0 и 250,0 мкг/мл. Данная методика может быть применена в клинико-токсикологическом анализе и при процедуре медицинского освидетельствования живых лиц.
Список литературы Денситометрическое определение эфедрина в судебно-химической практике
- Еремин, С.К. Анализ наркотических средств. Под ред. Б.Н. Изотова/С.К. Еремин, Б.Н. Изотов, Н.В. Веселовская. -М.: Мысль, 1993. 270 с.
- Бабаханян, Р.В. Наркотические средства, психотропные и сильнодействующие вещества/Р.В. Бабаханян и др. -СПБ; Реноме, 2008. 276 с.
- Калетина, Н.И. Токсикологическая химия. Метаболизм и анализ токсикантов: учебное пособие. -М.:ГЭОТАР-Медиа, 2008. 1016 с.
- Симонов, Е.А. Наркотики: методы анализа на коже, в ее придатках и выделениях/Е.А. Симонов, Б.Н. Изотов, А.В. Фесенко. -М.: Анахарсис, 2000. 130 с.
- CLARKE`S Isolation and identification of drugs in pharmaceutical body fluids, and post-mortem material. -London. The pharmaceutical press. 1986. 1023 p.
- Постановление Правительства РФ N 681 «Об утверждении перечня наркотических средств, психотропных веществ и их прекурсоров, подлежащих контролю в Российской Федерации» от 30 июня 1998 г. 34 с.
- Методические указания. Химико-токсикологический анализ веществ, вызывающих одурманивание. -М., 1987. 122 с.
- электронный ресурс: http://www.garryc2008.narod.ru/WEB страница Плахотного И.Н. (дата обращения 09. 09 2011)


