Диагностическая значимость расчета F-shunt для оценки вентиляционно-перфузионных нарушений в лёгких при аортокоронарном шунтировании
Автор: Киладзе Иракли Зурабович, Гончарова А.В., Дементьева И.И., Морозов Ю.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Статья в выпуске: 1 т.9, 2014 года.
Бесплатный доступ
Короткий адрес: https://sciup.org/140188270
IDR: 140188270
Текст статьи Диагностическая значимость расчета F-shunt для оценки вентиляционно-перфузионных нарушений в лёгких при аортокоронарном шунтировании
Газообмен в лёгких закономерно нарушается во время искусственной вентиляции лёгких (ИВЛ), что проявляется в изменении параметров оксигенации крови. Основной причиной таких нарушений является развитие микроателектазов, которые, по данным некоторых авторов, регистрируются до 90% пациентов, подвергшихся общей анестезии с ИВЛ [4]. Возникновению микроателектазов способствуют пожилой возраст, наличие у пациента хронической обструктивной болезни легких (ХОБЛ), морбидного ожирения.
Считается, что в среднем микроателектазы могут занимать до 15–20% лёгочной ткани вблизи диафрагмы или до 10% об общего объёма лёгочной ткани [10]. При кардиохирургических операциях в условиях искусственного кровообращения (ИК) развитие ателектазов и их объём значительно выше, чем при других хирургических вмешательствах [12]. Ателектазы развиваются уже через 1 час после начала ИК и сохраняются в среднем в течение двух суток после операции у лиц без сопутствующего ожирения [2].
Микроателектазы как правило не видны на обычной рентгенограмме грудной клетки, если они не становятся массивными и сливными, а для их визуализации используется компьютерная томография. Однако существует достаточно простой и информативный метод оценки внутрилёгочного компонента гипоксемии во время ИВЛ – это определение F-shunt.
Данный показатель вычисляется как соотношение между артериоальвео-лярной и артериовенозной разницами к общей концентрации кислорода. Если используется только образец артериальной крови, то F-shunt вычисляется исходя из артериовенозной разницы в 2,3 ммоль/л. Физиологический смысл данного параметра заключается в том, что он показывает долю венозного возврата в лёгочных капиллярах без оксигенации крови. В норме величина F-shunt составляет 4–8% [14]. Увеличение значений F-shunt указывает на патологическое лёгочное несоответствие между вентиляцией и перфузией, например, связанное с перфузией невентилируемых участков лёгкого, то есть развитие микроателектазов.
Цель работы: оценить диагностическую ценность определения F-shunt у пациентов с хронической обструктивной болезнью легких при операциях аортокоронарного шунтирования.
Материалы и методы
Обследовано 256 пациентов с ХОБЛ, которым выполнена операция аортокоронарного шунтирования в условиях ИК (группа 1, n = 135) и на работающем сердце без ИК (группа 2, n = 121). Характеристика больных приведена в таблице 1.
Аортокоронарное шунтирование выполнялось в условиях многокомпонентной сбалансированной анестезии по принятой в Федеральном государственном бюджетном учреждении «Российский научный центр имени академика Б.В. Петровского»
Табл. 1. Характеристика групп больных (M ± m)
|
Группа 1 (n = 135) |
Группа 2 (n = 21) |
|
|
Средний возраст, лет |
60,3 ± 8,9 |
63,9 ± 8,3 |
|
Длительность операции, мин |
268,7 ± 53,6 |
219,6 ± 46,3 |
|
Длительность ИК, мин |
83,8 ± 30,6 |
- |
|
Длительность пережатия аорты, мин |
51,5 ± 16,6 |
- |
|
Средний койко-день |
26,4 ± 3,4 |
23,9 ± 3,8 |
|
Средний койко-день в ОРИТ |
2,4 ± 0,8 |
2,2 ± 0,4 |
|
Средняя продолжительность ИВЛ в ОРИТ, час |
10,7 ± 4,0 |
9,7 ± 3,8 |
Примечание : ОРИТ – отделение реанимации и интенсивной терапии.
РАМН методике. Вводная анестезия осуществлялась болюсным введением мидазолама (0,05–0,08 мг/кг), кетамина (0,5–0,7 мг/кг), пропофола (0,5–0,7 мг/кг), фентанила (2,5–3,5 мкг/кг) и пипекуро-ниума бромида 0,1 мг/кг. Поддержание анестезии обеспечивалось инфузией пропофола (2-4 мг/кгхчас), фентанила (3-5 мкг/кгхчас) и ингаляцией изо-флюрана в концентрации 0,8–1,3 МАК с поправкой на возраст. Поддержание миорелаксации проводилось с помощью болюсного введения пипекурониума бромида. На наиболее травматичные этапы операции дробно добавляли фентанил по 0,2–0,3 мг.
Операции с ИК проводились в условиях нормотермии и фармакохолодовой кардиоплегии раствором «Консол» в непульсирующем режиме с перфузионным индексом 2,5 л/мин х м 2 .
После интубации пациента, до начала и после окончания основного этапа, а также в конце операции и у больных с продолжающейся ИВЛ в послеоперационном периоде на приборе «Radiometer 800 Flex» (Дания) в пробах артериальной и венозной крови определяли рO 2 (мм рт. ст.), pCO 2 (мм рт. ст.), концентрацию гемоглобина (Hb, г/л). Рассчитывали F-shunt (%) как соотношение:
Qs 0,03 х (А - a)pOi
Fshunt, % =--- = --------;----------:------
Qt 1,36 х Hb х (SaOi- SvO^ )
где: (A-a)pO 2 – артериоальвеоляр-ная разница по кислороду, мм рт. ст., Hb – концентрация гемоглобина в артериальной крови, г/л, SaO 2 -SvO 2 – артериовенозная разница по кислороду, мм рт. ст.
Результаты исследования обработаны параметрическими и непараметрическими методами статистического анализа с использованием критериев Стьюдента и Манна-Уитни. Достоверность различий считали при р < 0,05. Данные представлены как M ± о.

Киладзе И.З., Гончарова А.В., Дементьева И.И., Морозов Ю.А. ДИАГНОСТИЧЕСКАЯ ЗНАЧИМОСТЬ РАСЧЕТА F-SHUNT ДЛЯ ОЦЕНКИ ВЕНТИЛЯЦИОННОПЕРФУЗИОННЫХ НАРУШЕНИЙ В ЛЁГКИХ ПРИ АОРТОКОРОНАРНОМ ШУНТИРОВАНИИ
Результаты
Данные об изменении параметров оксигенации на этапах исследования представлены в таблице 2.
Как видно из приведенных в таблице 2 данных, достоверные различия выявлены только в концентрации гемоглобина до и после основного этапа, что связано с гемодилюцией во время ИК, а также в конце операции, и рО 2 в артериальной крови на этих же этапах.
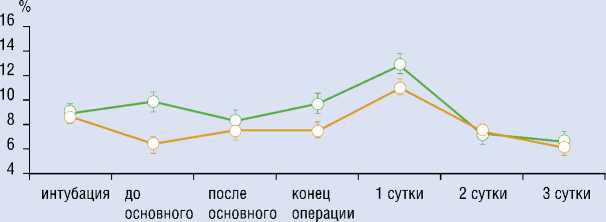
Изменения величины F-shunt представлено на рисунке 1.
После интубации значения F-shu-nt не отличались у пациентов групп 1 и 2 и были несколько выше нормальных значений, что может быть связано с наличием у всех больных ХОБЛ. Переход на ИК характеризовался возрастанием F-shunt, тогда как в группе 2 показатель F-shunt в начале основного этапа уменьшался (р < 0,05 между группами). По завершении основного этапа регистрировалось уменьшение F-shunt в группе 1 и возрастание F-shunt в группе 2, что может быть обусловлено включением собственных лёгких у пациентов группы 1 после окончания ИК. К концу операции в группе 1 величина F-shunt несколько возрастала, в то время как в группе 2 не изменялась, но в целом разница по F-shunt между группами была достоверной.
На 1 сутки после операции отмечалось увеличение F-shunt в обеих группах по сравнению с концом операции, причем между ними сохранялись значимые различия. 8,4 и 7,6% больных соответственно для групп 1 и 2 находились на продленной ИВЛ более одних суток после хирургического вмешательства. На 2 и 3 сутки значения F-shunt резко уменьшались и были ниже дооперационных величин. На этих этапах не установлено различий в величинах F-shunt между группам 1 и 2.
Обсуждение
Нарушение оксигенирующей функции лёгких является одним из наиболее частых осложнений после коронарного шунтирования, особенно выполняемого в условиях ИК, даже в отсутствии исходной лёгочной патологии. Распространенность и выраженность послеоперационных респираторных осложнений после такого типа операций колеблется от субклинических функциональных изменений у большинства пациентов до развития острого лёгочного дистресс-синдрома, который встречается в 2% случаев [1].
Табл. 2. Показатели параметров оксигенации на этапах исследования (M ± σ )
|
Показатель |
Этап |
Группа 1 |
Группа 2 |
|
Гемоглобин, г/л |
Интубация |
12,2 ± 1,8 |
12,1 ± 1,2 |
|
До основного этапа |
9,9 ± 1,6 |
12,3 ± 1,3* |
|
|
После основного этапа |
9,7 ± 1,7 |
12,4 ± 1,3* |
|
|
Конец операции |
10,1 ± 1,0 |
11,3 ± 1,6* |
|
|
1 сутки |
11,1 ± 1,1 |
10,7 ± 0,9 |
|
|
2 сутки |
11,3 ± 1,4 |
11,3 ± 1,0 |
|
|
3 сутки |
11,2 ± 1,3 |
11,0 ± 0,9 |
|
|
рО2 в артерии, мм рт. ст. |
Интубация |
273,0 ± 81,1 |
293,6 ± 43,6 |
|
До основного этапа |
250,0 ± 39,6 |
304,4 ± 40,5* |
|
|
После основного этапа |
246,0 ± 54,7 |
300,1 ± 38,6* |
|
|
Конец операции |
245,0 ± 63,1 |
281,1 ± 53,8* |
|
|
1 сутки |
262,0 ± 62,7 |
289,7 ± 71,8 |
|
|
2 сутки |
174,1 ± 63,0 |
165,9 ± 32,0 |
|
|
3 сутки |
178,5 ± 63,4 |
207,3 ± 71,0 |
|
|
рСО2 в артерии, мм рт. ст. |
Интубация |
39,8 ± 5,6 |
37,4 ± 4,3 |
|
До основного этапа |
40,3 ± 5,0 |
39,5 ± 4,1 |
|
|
После основного этапа |
40,7 ± 5,0 |
39,5 ± 4,0 |
|
|
Конец операции |
39,3 ± 6,0 |
39,5 ± 5,2 |
|
|
1 сутки |
35,4 ± 5,1 |
33,5 ± 3,5 |
|
|
2 сутки |
35,6 ± 4,0 |
35,1 ± 5,1 |
|
|
3 сутки |
37,7 ± 5,6 |
36,5 ± 3,9 |
|
|
рО2 в вене, мм рт. ст. |
Интубация |
46,9 ± 6,8 |
43,5 ± 5,4 |
|
До основного этапа |
46,3 ± 4,9 |
46,1 ± 5,6 |
|
|
После основного этапа |
46,9 ± 5,1 |
46,1 ± 5,7 |
|
|
Конец операции |
48,7 ± 6,8 |
47,3 ± 8,8 |
|
|
1 сутки |
42,1 ± 6,0 |
39,7 ± 7,1 |
|
|
2 сутки |
39,9 ± 6,2 |
40,9 ± 5,8 |
|
|
3 сутки |
42,8 ± 8,6 |
43,2 ± 6,8 |
|
|
рСО2 в артерии, мм рт. ст. |
Интубация |
46,7 ± 5,0 |
46,9 ± 4,6 |
|
До основного этапа |
48,0 ± 5,1 |
47,7 ± 4,7 |
|
|
После основного этапа |
47,8 ± 4,9 |
47,7 ± 4,5 |
|
|
Конец операции |
46,8 ± 5,9 |
48,4 ± 4,9 |
|
|
1 сутки |
45,3 ± 5,9 |
44,3 ± 4,0 |
|
|
2 сутки |
43,6 ± 6,1 |
44,9 ± 4,9 |
|
|
3 сутки |
44,9 ± 6,9 |
44,8 ± 4,8 |
Примечание: * – достоверность различий между группами р < 0,05.
этапа этапа
группа 1
группа 2
Рис. 1.
Изменения величины F-shunt
Киладзе И.З., Гончарова А.В., Дементьева И.И., Морозов Ю.А.
ДИАГНОСТИЧЕСКАЯ ЗНАЧИМОСТЬ РАСЧЕТА F-SHUNT ДЛЯ ОЦЕНКИ ВЕНТИЛЯЦИОННОПЕРФУЗИОННЫХ НАРУШЕНИЙ В ЛЁГКИХ ПРИ АОРТОКОРОНАРНОМ ШУНТИРОВАНИИ
Возникновение микроателектазов приводит к вентиляционно-перфузионным нарушениям в лёгких, и этот механизм считается основным в развитии послеоперационной гипоксемии. Проведение операций на сердце в условиях ИК увеличивает в 2 раза риск нарушений функции лёгких по сравнению с пациентами, оперированными без ИК, а также тяжесть гипоксии коррелирует с продолжительностью послеоперационной ИВЛ [8].
В экспериментах на животных L. Magnusson и др. (1997) установили, что после ИК микроателектазы занимали до 35% от общей площади легких и наиболее часто встречаются в околодиафраг-мальных отделах лёгких, в то время как до начала ИК площадь микроателектазов составляла не более 4% [6]. Выявлена выраженная корреляционная связь между количеством ателектазов в лёгких и величиной F-shunt (r 2 = 0,67). Такую же зависимость между размером пульмонарных уплотнений по данным компьютерной томографии у пациентов с нарушением функции лёгких после коронарного шунтирования и значениями F-shunt нашли и T. Hachenberg и др. (1992) [3].
В исследовании P.R. Rodrigues и др. (2011) было показано, что при операции реваскуляризации миокарда наибольшие значения F-shunt регистрировались в конце ИК и на 1 сутки после операции с динамическим снижением через 48 часов, что согласуется с полученными нами данными [11].
Важным механизмом развития микроателектазов во время ИК является секвестрация в сосудах лёгких активированных на чужеродной поверхности экс-тракорпоральнтого контура лейкоцитов [13]. Впервые данный феномен был описан у пациентов на хроническом гемодиализе в 1968 году L.S. Kaplow и J.A. Goffinet [5]. Это согласуется с неопубликованными данными Ю.А. Морозова и М.А. Чар-ной, что при аортокоронарном шунтировании в условиях ИК за время перфузии происходит уменьшение количества лейкоцитов в периферической крови на 2–35%. Острая интраперфузионная лейкопения свыше 10% ассоциировалась с увеличением частоты послеоперационной лёгочной дисфункции.
Высвобождение биологически активных веществ (провоспалительных цитокинов, интерлейкинов, катехоламинов и проч.) с развитием асептического местного воспаления в лёгких усугубляет ишемические и перфузионные нарушения в пульмонарных сосудах, что сопровождается увеличением величины F-shunt [7]. Близкие данные были получены и в исследовании B.S. Rasmussen и др. (2007), которые показали, что проведение коронарного шунтирования в условиях ИК сопровождалось достоверно более высокими значениями F-shunt (р = 0,047) без существенной разницы в других показателях оксигенации (р = 0,47) по сравнению с аналогичной операцией без ИК [9]. При этом выявлены значимые различия между уровнем провоспалительных интерлейкинов в лёгких.
Заключение
Таким образом, наше исследование и анализ литературы показали, что расчет F-shunt является простым неинвазивным и информативным методом оценки вентиляционно-перфузионных изменений в лёгких в периоперационном периоде при операциях аортокоронарного шунтирования. Максимальные значения F-shunt регистрируются за период с конца операции до 1 суток после хирургического вмешательства. Коронарное шунтирование проводимое в условиях ИК, характеризуется достоверно более выраженными вентиляционно-перфузионными нарушениями в интраоперационном периоде.
Список литературы Диагностическая значимость расчета F-shunt для оценки вентиляционно-перфузионных нарушений в лёгких при аортокоронарном шунтировании
- Asimakopoulos G., Smith P.L., Ratnatunga CP., Taylor K.M. Lung injury and acute respiratory distress syndrome after cardiopulmonary bypass.//Ann. Thorac. Surg. -1999. -Vol. 68. -Р. 1107-1115.
- Eichenberger A.S., Proietti S., Wicky S. et al. Morbid obesity and postoperative pulmonary atelectasis: an underestimated problem.//Anesth. Analg. -2000. -Vol. 95. -P. 1788-1792.
- Hachenberg T., Brussel T., Roos N. et al. Gas exchange impairment and pulmonary densities after cardiac surgery.//Acta Anaesthesiol. Scand. -1992. -Vol. 36. -P. 800-805.
- Hedenstierna G., Rothern H.U. Atelectasis formation during anesthesia: causes and measures to prevent it.//J. Clin. Monit. Comput. -2000. -Vol. 16(5-6). -P. 329-335.
- Kaplow L.S., Goffinet J.A. Profound neutropenia during the early phase of hemodialysis.//JAMA. -1968. -Vol. 203(13). -P. 1135-1137.
- Magnusson L., Zemgulis V., Wicky S. et al. Atelectasis is a major cause of hypoxemia and shunt after cardiopulmonary bypass: an experimental study.//Anesthesiology. -1997. -Vol. 87. -P. 1153-1163.
- Massoudy P., Zahler S., Becker B.F. et al. Evidence for inflammatory responses of the lungs during coronary artery bypass grafting with cardiopulmonary bypass.//Chest. -2001. -Vol. 119. -P. 31-36.
- Nozawa E., Kobayashi E., Matsumoto M.E. et al. Assessment of factors that influence weaning from long-term mechanical ventilation after cardiac surgery.//Arq. Bras. Cardiol. -2003. -Vol. 80. -P. 301-310.
- Rasmussen B.S., Laugesen H., Sollid J. et al. Oxygenation and release of inflammatory mediators after off-pump compared with after on-pump coronary artery bypass surgery.//Acta Anaesthesiol. Scand. -2007. -Vol. 51(9). -P. 1202-1210.
- Reber A., Engberg G., Sporre B. et al. Volumetric analysis of aeration in the lungs during general anaesthesia.//Br. J. Anaesth. -1996. -Vol. 1996. -P. 760-766.
- Rodrigues P.R., Sawada A.Y., Rouby J.J. et al. Computed tomography assessment of lung structure in patients undergoing cardiac surgery with cardiopulmonary bypass.//Braz. J. Med. Biol. Res. -2011. -Vol. 44(6). -P. 598-605.
- Tenling A., Hachenberg T., Tyden H. et al. Atelectasis and gas exchange after cardiac surgery.//Anesthesiology. -1998. -Vol. 89. -P. 371-378.
- Vroege R., Rutten P.M., Kalkman C. et al. Biocompatibility of three different membrane oxygenators: effects on complement, neutrophil and monocyte activation.//Perfusion. -1997. -Vol. 12. -P. 369-375.
- Wandrup J.H. Quantifying pulmonary oxygen transfer deficits in critically ill patients.//Acta Anaesth. Scand. -1995. -Vol. 39(107). -P. 37-44.


