Динамическая оценка волемического статуса с помощью шкалы Vexus у пациентов после хирургической коррекции клапанных пороков сердца, осложненных острым повреждением почек: серия клинических случаев
Автор: Зозуля М.В., Сотников А.В., Ленькин А.И.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Случаи из клинической практики
Статья в выпуске: 3 т.27, 2023 года.
Бесплатный доступ
Актуальность. Перегрузка жидкостью - независимый фактор риска развития острого повреждения почек после кардиохирургических операций. Объективная оценка волемического статуса является не решенной клинической задачей. Цель. Проанализировать взаимосвязь между динамикой паттернов кровотока в спланхнических венах (портальной, печеночных и междолевых почечных), отображающих степень венозного застоя, и выраженностью почечной дисфункции у представленных пациентов. Методы. С февраля по май 2023 г. у троих пациентов после вмешательства на открытом сердце послеоперационный период осложнился острым повреждением почек, у двоих потребовалась заместительная почечная терапия. Всем больным в периоперационном периоде проводили допплерографию кровотока в спланхнических венах согласно шкале VExUS (англ. Venous Excess Ultrasound, ультразвуковая оценка венозного застоя). Результаты. Наиболее характерные изменения паттернов кровотока выявили в портальной и междолевых почечных венах. У двоих пациентов с анурией, которым потребовалась заместительная почечная терапия, отмечали пульсирующий кровоток в портальной вене с систолическим реверсом, что отображало выраженный венозный застой, а также бифазный кровоток в почечных венах. После восстановления диуреза у одного больного нормализовался паттерн кровотока в портальной вене, у другого кровоток оставался пульсирующим, что проявлялось сохранением клинических признаков гипергидратации. У третьего пациента портальный кровоток также имел пульсирующий характер, но без систолического реверса. Кровоток в почках был бифазным, хотя исходно являлся непрерывным. После восстановления диуреза и разрешения гипергидратации паттерн кровотока восстановился до дооперационного. Заключение. У представленных пациентов динамическая оценка кровотока в спланхнических венах по шкале VExUS позволила объективно оценить степень венозного застоя и послужила дополнительным критерием для начала заместительной почечной терапии при прогрессировании острого повреждения почек. Однако интерпретация шкалы требует комплексной оценки в связи с умеренной специфичностью. Необходимы дальнейшие исследования для валидации этого вида мониторинга.
Венозный застой, волемический статус, клинический случай, острое повреждение почек, шкала vexus
Короткий адрес: https://sciup.org/142239091
IDR: 142239091 | DOI: 10.21688/1681-3472-2023-3-89-98
Dynamic volume status assessment with the Vexus score after heart valve surgery complicated by acute kidney injury: a case series
Background: Fluid overload is an independent risk factor for acute kidney injury after cardiac surgery. An objective volume status assessment remains an unsolved clinical problem. Objective: To analyze the relationship between the dynamic changes in splanchnic blood flow patterns (portal, hepatic, and interlobar renal veins), reflecting the venous congestion severity, and severity of renal dysfunction in the studied patients. Methods: From February to May 2023, 3 patients after open heart surgery developed acute kidney injury in the postoperative period: 2 of them required renal replacement therapy. In the perioperative period, all patients underwent Doppler ultrasonographic assessment of the splanchnic blood flow according to the venous excess ultrasound (VExUS) score. Results: The most distinct changes in blood flow patterns were observed in portal and interlobar renal veins. Two anuric patients requiring renal replacement therapy had a pulsatile portal venous flow with systolic flow reversal that indicated severe venous congestion and biphasic renal venous flow. After restoration of urine output in 1 patient, the blood flow pattern in the portal vein returned to the normal pattern. In another patient, the blood flow remained pulsatile, which manifested itself by persisting clinical signs of overhydration. In the third patient, the portal blood flow also was pulsatile but had no systolic flow reversal. The renal blood flow was biphasic, although it was initially continuous. After restoration of urine output and overhydration improvement, the blood flow pattern returned to the preoperative pattern. Conclusion: In the studied patients, the dynamic assessment of splanchnic blood flow using the VExUS score allowed to objectively assess the venous congestion severity and served as an additional criterion for initiating renal replacement therapy in case of acute kidney injury progression. Further research could validate this type of monitoring because its interpretation requires a comprehensive assessment due to moderate specificity.
Текст научной статьи Динамическая оценка волемического статуса с помощью шкалы Vexus у пациентов после хирургической коррекции клапанных пороков сердца, осложненных острым повреждением почек: серия клинических случаев
Цитировать: Зозуля М.В., Сотников А.В., Ленькин А.И. Динамическая оценка волемического статуса с помощью шкалы VExUS у пациентов после хирургической коррекции клапанных пороков сердца, осложненных острым повреждением почек: серия клинических случаев. Патология кровообращения и кардиохирургия. 2023;27(3):89-98. https://
Острое повреждение почек (ОПП), ассоциированное с кардиохирургическим вмешательством, является одним из наиболее распространенных послеоперационных осложнений с частотой развития от 5 до 42 % в зависимости от определения ОПП и типа хирургического вмешательства [1]. Тяжелое ОПП приводит к 3–8-кратному увеличению периоперационной летальности [1]. Поэтому крайне важна своевременная диагностика этого грозного осложнения. Положительный гидробаланс после кардиохирургических операций ассоциирован с риском как возникновения, так и прогрессирования ОПП [2]. Оценка волемического статуса и в особенности выявление перегрузки жидкостью остается нерешенной клинической задачей. В 2020 г. была представлена шкала VExUS (англ. Venous Excess Ultrasound, ультразвуковая оценка венозного застоя) — оценка паттернов кровотока в спланхни-ческих венах (диаметр нижней полой вены (НПВ), кровоток в печеночных, портальной и почечных венах), — которая, за исключением некоторых клинических ситуаций, достаточно точно отображает волемический статус пациента, в особенности при наличии венозного застоя [3].
Цель — проанализировать взаимосвязь между динамикой паттернов кровотока в спланхнических венах (портальной, печеночных и междолевых почечных), отображающих степень венозного застоя, и выраженностью почечной дисфункции у представленных пациентов.
Методы
Работа выполнена в рамках проспективного обсервационного исследования «Оценка гиперволемии с помощью ультразвуковых методик у пациентов после хирургической коррекции клапанных пороков сердца», которое проводится на кафедре анестезиологии и реаниматологии им. В.Л. Ванев-ского СЗГМУ им. И.И. Мечникова (протокол заседания локального этического комитета от 12.04.2023 г. № 4). С февраля по май 2023 г. у 3 пациентов после выполнения открытой операции на сердце в условиях искусственного кровообращения (ИК) по поводу приобретенных клапанных пороков послеоперационный период осложнился ОПП: двоим потребовалась заместительная почечная терапия (ЗПТ), у одного больного отмечались редукция диуреза (менее 0,5 мл/кг за 12 ч) и практически 2-кратное повышение уровня креатинина сыворотки крови.
Всем пациентам в периоперационном периоде (до операции, при поступлении в отделение реанимации и интенсивной терапии (ОРИТ), через 8, 16, 24 ч и в дальнейшем один раз в сутки при нахождении в ОРИТ) проводили ультразвуковой мониторинг кровотока в спланхнических венах по шкале VExUS. В ее основе — диаметр и респираторная вариабельность НПВ и паттерны кровотока в печеночных венах, портальной и междолевых почечных венах. В норме диаметр НПВ составляет менее 2,1 см, а респираторная вариабельность (измеряемая при быстром глубоком вдохе) — более 50 % [3]. Чем более выражен венозный застой, тем более расширена в покое вена и снижена ее респираторная вариабельность. Следующий паттерн — это кровоток в печеночных венах, который меняется при дальнейшем прогрессировании венозного застоя, когда достигается предел эластичности НПВ. Венозный кровоток в печеночных венах имеет фазовый характер, во многом повторяя кривую давления в правом предсердии (центрального венозного давления). Волна S в печеночных венах соответствует нисходящей волне Х на кривой центрального венозного давления. Далее антеградная волна D соответствует волне Y на кривой центрального венозного давления — время диастолы, пассивного наполнения правого желудочка (ПЖ) кровью. Волна S в норме превосходит волну D. В конце диастолы при синусовом ритме определяется ретроградная волна A — сокращение предсердия [3]. При гипергидратации происходит уменьшение амплитуды волны S, она становится меньше амплитуды волны D, а при выраженной гипергидратации происходит реверс кровотока в систолу.
Кровоток в портальной вене подвержен влиянию давления в правом предсердии в меньшей степени, так как она отграничена от печеночных вен сетью синусоидных капилляров. Поэтому в норме кровоток в портальной вене монофазный и направлен к печени, имеет скорость около 20–40 см/с. Чем более выражен венозный застой, тем более пульсирующим становится портальный кровоток, при тяжелой гипергидратации происходит систолический реверс кровотока. Количественным показателем, отображающим степень венозного застоя, может служить пульсационный индекс (ПИ) — соотношение разницы между максимальной и минимальной скоростью в воротной вене, деленное на максимальную скорость.
Наиболее технически трудным является исследование кровотока в почечных венах ввиду их малого диаметра и смещения почек при дыхании. В норме отток венозной крови от почки происходит как в систолу, так и в диастолу, он непрерывный [3]. При увеличении сопротивления оттоку характер кровотока становится пульсирующим, затем бифазным: отдельно в систолу и в диастолу, — затем монофаз-ным. В систолу происходит реверс кровотока, который не виден, так как накладывается на кровоток в почечной артерии.
Результаты
Клинико-демографические данные пациентов и основные показатели послеоперационного периода представлены в табл. 1. Периоперационную инфузионную терапию проводили согласно последним клиническим рекомендациям [4]. Диагностику и подтверждение перегрузки жидкостью осуществляли с помощью инвазивного гемодинамического мониторинга (катетера Свана – Ганца и методики препульмональной термодилюции), а именно оценки динамики показателей центрального венозного давления и давления заклинивания легочной артерии, сердечного выброса/сердечного индекса (табл. 2), результатов эхокардиографии. Также учитывали данные послеоперационного и кумулятивного (на утро следующего дня) гидробаланса.
У представленных пациентов послеоперационный период осложнился развитием ОПП: у двоих — до стадии 3 по классификации KDIGO (англ. Kidney Disease: Improving Global Outcomes, Инициатива по улучшению глобальных исходов заболеваний почек), что потребовало применения ЗПТ, у одного — до стадии 2 по KDIGO (повышение креатинина в первые 24 ч после операции и редукция диуреза менее 0,5 мл/кг более 12 ч). В послеоперационном периоде у первого больного была минимальная потребность в инотропах (8 ч) и вазопрессорах (3 ч). После вмешательства развилась анурия. По данным мониторинга центральной гемодинамики, нарастали явления перегрузки жидкостью (росли значения давления заклинивания в легочных капиллярах и центрального венозного давления) при сохранном сердечном выбросе. При выполнении эхокардиографии отметили расширение правых отделов сердца при сохранной систолической функции ПЖ. В связи с нарастанием явлений гипергидратации, сохранением анурии, появлением ажитации, усилением дыхательной недостаточности со вторых суток начали продленный сеанс ЗПТ. На фоне гемодиафильтрации не потребовался повторный перевод пациента на инвазивную вентиляцию легких, произошла нормализация когнитивного статуса, че- рез 48 ч ЗПТ завершили. В течение последующих суток восстановился адекватный темп диуреза.
Послеоперационный период у второго пациента осложнился сердечно-сосудистой недостаточностью (добутамин 5 мкг/кг ⋅ мин, норадреналин 0,8 мкг/кг ⋅ мин), которая стабилизировалась в течение первых 12 ч после вмешательства, и ОПП (стадия 3 по KDIGO), основной причиной которого, вероятнее всего, послужил гемолиз, так как его признаки (макрогематурия/гемоглобинурия) появились еще во время ИК; также повлияла сердечно-сосудистая недостаточность в послеоперационном периоде. Спустя 24 ч после вмешательства сохранялась анурия. При этом не отметили клинических признаков гипергидратации (периферических отеков, ортопноэ, набухания шейных вен). По данным эхокардиографии, правые камеры погранично расширены, сократительная функция ПЖ снижена. С учетом данных ультразвукового исследования, лабораторных показателей и появления симптомов системного воспалительного ответа (гипертермия, повышение уровня С-реактивного белка) начали сеанс ЗПТ совместно с цитокиновой сорбцией с помощью картриджа HA330 (Jafron BioMedical Co, Чжухай, Китай). Восстановление диуреза произошло спустя 12 ч после окончания сеанса ЗПТ. У первых двоих пациентов до начала ЗПТ проводили агрессивную диуретическую терапию (инфузия фуросемида 20–40 мг/ч). После окончания ЗПТ диуретическую терапию (фуросемид 20 мг/ч) возобновили и продолжали до восстановления адекватного темпа диуреза.
У третьего пациента в анамнезе была тяжелая артериальная гипертензия с привычным артериальным давлением 160–170/60–65 мм рт. ст. Во время ИК среднее артериальное давление поддерживали в пределах 60 мм рт. ст. Послеоперационный период протекал без инотропной и вазопрессорной поддержки, продолжительность послеоперационной респираторной поддержки составила 4 ч. Через 12 ч после операции отмечали редукцию диуреза (менее 0,5 мл/кг за 12 ч), практически 2-кратное увеличение концентрации сывороточного креатинина. По данным эхокардиографии не отметили выраженного расширения правых камер сердца, сократительная функция ПЖ была нормальной. После оценки состояния пациента приняли решение о консервативной ренопротективной тактике ведения: поддержание целевого артериального давления 140–150/80–90 мм рт. ст., коррекция волемического статуса, отмена нефротоксических препаратов, коррекция гипергликемии. На 3-и сут. после операции отметили восстановление адекватного темпа
|
Табл. 1. Клинико-демографические данные пациентов с острым повреждением почек и основные показатели послеоперационного периода |
|||
|
Показатель |
Пациент № 1 |
Пациент № 2 |
Пациент № 3 |
|
Пол |
Мужской |
Мужской |
Мужской |
|
Возраст, лет |
43 |
66 |
68 |
|
Вес, кг |
75 |
65 |
63 |
|
Индекс массы тела, кг/м2 |
23 |
23 |
22 |
|
Расчетная прогностическая летальность по шкале EuroSCORE II, % |
13,6 |
1,6 |
1,1 |
|
Основной диагноз |
Инфекционный эндокардит МК и АоК. Недостаточность МК и АоК тяжелой степени |
ИБС. Постоянная форма ФП. Недостаточность ТкК тяжелой степени |
Комбинированный порок АоК: недостаточность тяжелой степени и умеренный стеноз |
|
ХБП, стадия (СКФ по CKD-EPI, мл/мин/1,73 м2) |
С3б (42) |
С1 (103,1) |
C2 (64) |
|
Сахарный диабет |
Да |
Нет |
Нет |
|
Операция |
Протезирование МК и АоК |
Пластика ТкК, повторное АКШ, эпикардиальная РЧА устьев легочных вен, резекция ушка ЛП |
Протезирование АоК |
|
Фракция выброса левого желудочка до операции, % |
67 |
63 |
60 |
|
Длительность операции, мин |
630 |
410 |
175 |
|
Пережатие аорты, мин |
118 |
Нет |
53 |
|
Длительность ИК, мин |
145 |
135 |
74 |
|
ИВЛ п/о, ч |
12 |
20 |
4 |
|
Послеоперационный гидробаланс, мл |
50 |
3 215 |
1 400 |
|
Гидробаланс в 1-е сут. п/о, мл |
3 150 |
4 165 |
2 100 |
|
Длительность инотропной/вазопрес-сорной поддержки п/о, ч |
8/3 |
20/23 |
0/0 |
|
Длительность нахождения в ОРИТ, сут. |
11 |
6 |
3 |
|
Повторное поступление в ОРИТ |
Неоднократно (тампонада сердца, пароксизмы ФП с гемодинамической нестабильностью, судорожный синдром) |
Нет |
Однократно (пароксизм ФП с гемодинамической нестабильностью) |
|
Длительность госпитализации, сут. |
54 |
23 |
23 |
|
SOFA в 1-е сут. п/о, баллы |
8 |
11 |
3 |
|
Этиология острого повреждения почек |
ССВР, длительное ИК, исходная гипергидратация, ХБП |
Гемолиз, ишемия почек, длительное ИК, ХБП |
Ишемически-реперфу-зионное повреждение почек, ХБП |
|
Заместительная почечная терапия |
Продленная вено-венозная гемодиафильтрация, 47 ч |
Продленная вено-венозная гемодиафильтрация, 19 ч |
Нет |
|
Экстракорпоральная гемокоррекция |
Нет |
Селективная гемосорбция цитокинов |
Нет |
|
Делирий |
Да |
Да |
Нет |
|
Тропонин T в 1-е сут. п/о, пг/мл |
1 069 |
3 981 |
787 |
|
Креатинин до операции/ в 1-е сут. п/о, мкмоль/л |
176/227 |
59/203 |
109/188 |
Примечание. МК — митральный клапан; АоК — аортальный клапан; ТкК — трикуспидальный клапан; ИБС — ишемическая болезнь сердца; ФП — фибрилляция предсердий; ХБП — хроническая болезнь почек; СКФ — скорость клубочковой фильтрации; АКШ — аортокоронарное шунтирование; РЧА — радиочастотная абляция; ЛП — левое предсердие; ИК — искусственное кровообращение; ИВЛ — искусственная вентиляция легких; п/о — после операции; ОРИТ — отделение реанимации и интенсивной терапии; SOFA — англ. Sequential Organ Failure Assessment, динамическая оценка органной недостаточности; ССВР — синдром системной воспалительной реакции.
Табл. 2. Данные гемодинамического мониторинга в раннем послеоперационном периоде (№ — номер пациента)
|
Этап |
СВ, л/мин / СИ, л/мин/м2 |
ДЗЛА, мм рт. ст. |
ЦВД, мм рт. ст. |
ДЛАср, мм рт. ст. |
||||||||
|
№ 1 |
№ 2 |
№ 3 |
№ 1 |
№ 2 |
№ 3 |
№ 1 |
№ 2 |
№ 3 |
№ 1 |
№ 2 |
№ 3 |
|
|
После интубации трахеи |
3,5/1,8 |
3/1,8 |
2,6/1,5 |
16 |
7 |
13 |
11 |
5 |
10 |
35 |
21 |
16 |
|
После сведения грудины |
4,3/2,2 |
2,7/1,5 |
3,2/1,8 |
9 |
13 |
6 |
8 |
6 |
2 |
25 |
27 |
8 |
|
При поступлении в ОРИТ |
4,9/2,5 |
2,1/3,6 |
3,3/1,9 |
11 |
13 |
8 |
11 |
6 |
7 |
31 |
24 |
13 |
|
Через 8 ч после операции |
7,5/3,8 |
2,9/1,7 |
5,1/2,9 |
11 |
12 |
8 |
12 |
9 |
6 |
21 |
36 |
15 |
|
Через 16 ч после операции |
5,2/2,7 |
5,2/3,0 |
20 |
9 |
14 |
10 |
4 |
38 |
15 |
|||
|
Через 24 ч после операции |
5,7/2,9 |
5,6/3,3 |
19 |
5 |
16 |
12 |
6 |
40 |
17 |
|||
Примечание. СВ — сердечный выброс; СИ — сердечный индекс; ДЗЛА — давление заклинивания легочной артерии; ЦВД — центральное венозное давление; ДЛАср — среднее давление в легочной артерии; ОРИТ — отделение реанимации и интенсивной терапии.
диуреза на фоне внутривенной инфузии фуросемида в дозе 20 мг/ч и снижение уровня сывороточного креатинина.
По данным ультразвукового исследования по шкале VExUS отметили перегрузку жидкостью до операции у первого пациента (дилатированная НПВ с респираторной вариацией менее 50 %, S < D в печеночных венах, ПИ в воротной вене более 50 % и бифазный кровоток в почечных венах), что соотносилось с данными клинического осмотра (ортопноэ, периферические отеки, асцит). У второго больного изменения по шкале VExUS также соответствовали перегрузке большого круга кровообращения (выраженная пульсация кровотока в воротной вене, S < D в печеночных венах, пульсирующий кровоток в почечных венах), но они были обусловлены изначальной тяжелой трикуспидальной недостаточностью, клинические признаки гипергидратации отсутствовали. У третьего пациента не было признаков гипергидратации, показатели по шкале VExUS находились в пределах нормы (незначительная пульсация кровотока в воротной вене, ПИ менее 30 %, постоянный кровоток в почечных венах, S > D в печеночных венах, диаметр НПВ < 2,1 см). Выраженная перегрузка жидкостью у пер- вого и второго пациентов в послеоперационном периоде сопровождалась делирием, длительной ИВЛ (12 и 20 ч соответственно), множественной органной дисфункцией (показатели по шкале SOFA (англ. Sequential Organ Failure Assessment — динамическая оценка органной недостаточности) составили 8 и 11 баллов соответственно), необходимостью в длительной интенсивной терапии (пребывание в ОРИТ 11 и 6 сут. соответственно). После восстановления диуреза у второго больного нормализовался паттерн кровотока в портальной вене, и его дальнейший послеоперационный период протекал без особенностей. У первого пациента кровоток в портальной вене оставался пульсирующим все время госпитализации, что проявлялось сохранением клинических признаков гипергидратации и более тяжелым течением послеоперационного периода: неоднократными переводами в ОРИТ, присоединением вторичной инфекции. Стоит отметить, что некоторые из этих переводов были обусловлены потребностью в экстренном хирургическом вмешательстве (рестернотомия по поводу тампонады сердца). У третьего пациента при поступлении в ОРИТ не было ультразвуковых признаков перегрузки жидкостью (пульсирующий непрерывный
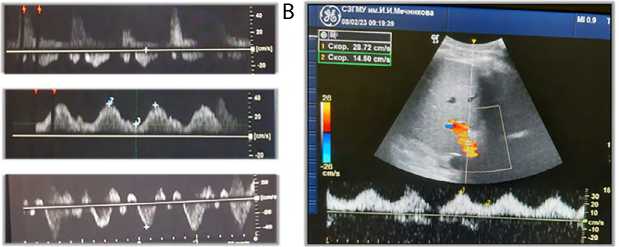
Рис. 1. Динамика паттернов кровотока в воротной вене у пациента № 1: до операции (A); на 2-й день после операции (B); на 21-й день после операции (C)
А
B
C
дцшз
D
E
F
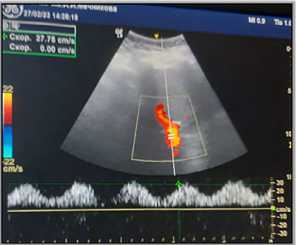
Рис. 2. Динамика паттернов кровотока в портальной вене у пациента № 2: 2-е сут. после операции, до ЗПТ, ЦВД +10 мм рт. ст. (A); 2-е сут. после операции, начало ЗПТ, ЦВД +16 мм рт. ст. (B); 3-е сут. после операции, ЗПТ, ЦВД +14 мм рт. ст. (C); 4-е сут. после операции, завершена ЗПТ, делирий, ЦВД +11 мм рт. ст. (D); 5-е сут. после операции, восстановлен диурез (4 л), делирий, ЦВД +6 мм рт. ст. (E); 7-е сут. после операции, в профильном отделении (F)
Примечание. ЗПТ — заместительная почечная терапия; ЦВД — центральное венозное давление.
кровоток в почках, ПИ в воротной вене менее 30 %), однако спустя 12 ч на фоне редукции диуреза венозный кровоток в почках приобрел бифазный характер, ПИ в воротной вене составлял более 50 %. После восстановления диуреза и разрешения гипергидратации паттерн кровотоков восстановился до дооперационного. Наглядно динамика кровотоков в спланхнических венах у троих пациентов представлена на рис. 1–4.
Обсуждение
Шкала VExUS изначально была валидирована для прогнозирования венозного застоя после кардиохирургических операций, который, в свою очередь, ассоциирован с ОПП [5]. Мы использовали определение ОПП согласно критериям KDIGO, так как считается, что эта классификация более чувствительна, чем AKIN (англ. Acute Kidney Injury Network — Группа по изучению острого повреждения почек) и RIFLE
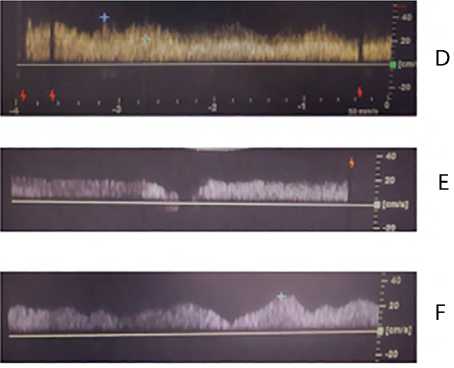
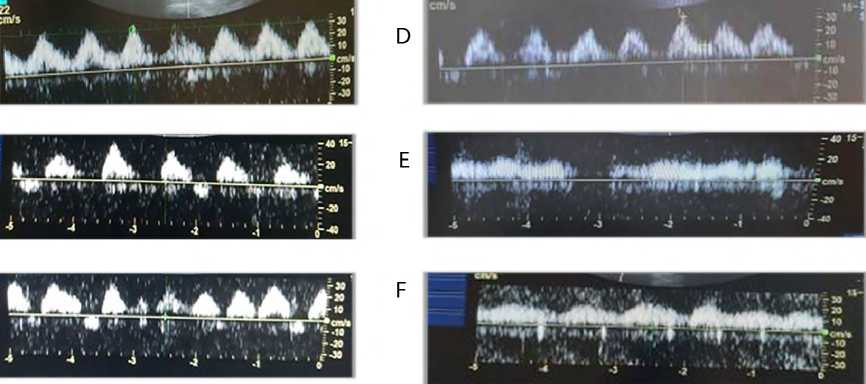
Рис. 3. Динамика паттернов кровотока в портальной вене у пациента № 3: до операции (A); при поступлении в ОРИТ, ЦВД +6 мм рт. ст. (B); 2-е сут. после операции, в профильном отделении, снижена фракция выброса до 39 % (C); повторное поступление в ОРИТ на 3-е сут., снижена фракция выброса до 35 %, ЦВД +9 мм рт. ст. (D); 4-е сут. после операции, в ОРИТ, ЦВД +8 мм рт. ст. (E); 7-е сут. после операции, в отделении (F)
Примечание. ОРИТ — отделение реанимации и интенсивной терапии; ЦВД — центральное венозное давление.



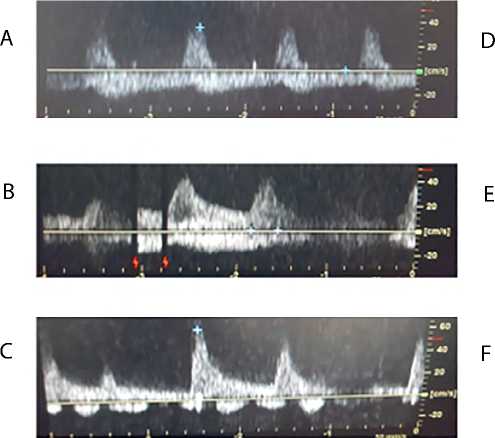
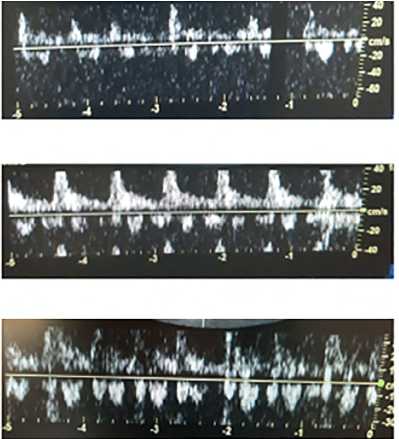
Рис. 4. Динамика паттернов кровотока в почечных венах у пациента № 3: до операции (A); при поступлении в ОРИТ, ЦВД +6 мм рт. ст. (B); 2-е сут. после операции, в отделении, снижена фракция выброса до 35 % (C); 3-е сут. после операции, повторное поступление в ОРИТ, ЦВД +9 мм рт. ст. (D); 4-е сут. после операции, ЦВД +8 мм рт. ст. (E);
7-е сут. после операции, в отделении (F)
Примечание . ОРИТ — отделение реанимации и интенсивной терапии; ЦВД — центральное венозное давление.
(англ. Risk, Injury, Failure, Loss of kidney function, and End-stage kidney disease — Риск, повреждение, недостаточность, потеря функции и терминальная стадия или хроническая болезнь почек) [6]. Этиология и патофизиология ОПП, связанного с кардиохирургическим вмешательством, многофакторны: перегрузка жидкостью, ишемически-реперфузионные повреждения почек, гипоперфузия, гемолиз, системное воспаление, оксидативный стресс и нефро-токсины — все эти факторы в большей или меньшей степени присутствуют в периоперационном периоде кардиохирургических вмешательств, выполняемых в условиях ИК [7]. В нашей серии наблюдений причиной ОПП у первого пациента послужили исходно выраженная гипергидратация, хронический системный воспалительный процесс и длительное ИК; у второго больного вероятными причинами ОПП были гемолиз и длительное ИК; у третьего — ишемически-реперфузионное повреждение почек на фоне гипоперфузии во время ИК. Помимо этого, у всех троих пациентов изначально была хроническая болезнь почек различных стадий, что является значимым немодифицируемым фактором риска развития ОПП после операции [7]. До вмешательства у первого больного были признаки гипергидратации как клинически, так и по шкале VExUS, у второго клинические проявления отсутствовали, а характерные изменения по шкале VExUS были обусловлены тяжелой недостаточностью ТкК. В третьем случае изначально ни клинически, ни по шкале VExUS не было признаков гипергидратации. Однако к моменту диагностики ОПП и решения вопроса о начале ЗПТ у всех троих больных были характерные изменения по шкале VExUS. У пациентов, которым потребовалась ЗПТ, кровоток в воротной вене был реверсирован, что отражало тяжелую степень перегрузки жидкостью, которая не развилась у третьего больного.
Стоит отметить, что кровоток в печеночных венах не столь однозначно отражает волемический статус: при тяжелой недостаточности трикуспидального клапана, легочной гипертензии, систолической дисфункции ПЖ (когда нет активного движения кольца трикуспидального клапана во время систолы) возможен паттерн S < D или реверс кровотока в систолу без венозного застоя. При фибрилляции предсердий возможен паттерн S < D даже без перегрузки жидкостью (подобное отмечалось во втором наблюдении: сохранение паттерна S < D уже после ЗПТ на фоне полиурии, когда кровоток в воротной вене нормализовался). Согласно концепции R.O.S.E. (англ. Resuscitation, Optimization, Stabilization, Evacuation — Реанимация, оптимизация, стабилизация, эвакуация; фазы инфузионной терапии при шоке) триггером удаления жидкости помимо показателей центральной гемодинамики может служить
Табл. 3. Ограничения и недостатки шкалы VExUS
|
НПВ не дилатирована, но есть гиперволемия |
Дилатация НПВ без гиперволемии |
S < D в печеночных венах без гиперволемии |
Пульсирующий кровоток в воротной вене без гиперволемии |
Непульсирующий кровоток в воротной вене при гиперволемии |
|
Внутрибрюш-ная гипертензия |
Атлеты |
Тяжелая недостаточность ТкК* и тяжелая дисфункция правого желудочка (нет систолического движения ТкК) |
Худые здоровые люди; правожелудочковая недостаточность, тяжелая недостаточность ТкК |
Неалкогольная жировая болезнь печени, цирроз печени |
|
Тяжелая недостаточность ТкК |
Хроническая легочная гипертензия |
Артериовенозные мальформации, печеночнопортальные фистулы |
||
|
Хроническая легочная гипертензия, ОРДС |
Фибрилляция предсердий |
Цирроз печени**, портальная гипертензия |
||
|
Систолическая дисфункция правого желудочка |
Цирроз печени и жировая болезнь печени |
Синдром Бадда – Киари |
Примечание. НПВ — нижняя полая вена; ТкК — трикуспидальный клапан; ОРДС — острый респираторный дистресс-синдром;
* — при хорошей растяжимости правого предсердия кровоток в печеночных венах может быть не нарушен; ** — при циррозе печени возможны несколько вариантов кровотока в портальной вене (гепатопетальный пульсирующий и непульсирующий, гепатофугальный, отсутствие кровотока при тромбозе портальной вены).
высокая градация по шкале VExUS [8]. Более того, проводится исследование применения комбинации шкал VExUS и LUS (англ. Lung Ultrasound score — Шкала ультразвуковой оценки легких) среди пациентов с сепсисом, что говорит о высокой степени доверия к этому виду мониторинга [9]. Преимуществами исследования являются его неинвазивность, простота интерпретации и доступность. У второго пациента не было клинических признаков гипергидратации на момент решения вопроса о начале ЗПТ, однако по шкале VExUS отмечали прогрессирование перегрузки жидкостью (увеличение ПИ, появление прерывистого бифазного кровотока в почечных венах). Это послужило дополнительным критерием при определении показаний к ЗПТ, что в дальнейшем благотворно повлияло на течение послеоперационного периода.
Несмотря на свои преимущества, шкала VExUS имеет ряд ограничений, ее интерпретация может быть как ложноположительной, так и ложноотрицательной при выявлении венозного застоя [10; 11]. Эти ограничения представлены в табл. 3.
Заключение
У представленных пациентов динамическая оценка кровотока в спланхнических венах по шкале VExUS позволила объективно оценить степень венозного застоя и послужила дополнительным критерием для начала ЗПТ при прогрессировании ОПП. Однако ее интерпретация требует комплексной оценки в связи с умеренной специфичностью. Необходимы дальнейшие исследования для валидации этого вида мониторинга.
Список литературы Динамическая оценка волемического статуса с помощью шкалы Vexus у пациентов после хирургической коррекции клапанных пороков сердца, осложненных острым повреждением почек: серия клинических случаев
- Peng K., McIlroy D.R., Bollen B.A., Billings F.T. 4th, Zarbock A., Popescu W.M., Fox A.A., Shore-Lesserson L., Zhou S., Geube M.A., Ji F., Bhatia M., Schwann N.M., Shaw A.D., Liu H. Society of Cardiovascular Anesthesiologists clinical practice update for management of acute kidney injury associated with cardiac surgery. Anesth Analg. 2022;135(4):744-756. PMID: 35544772. https://doi.org/10.1213/ANE.0000000000006068
- Chen X., Xu J., Li Y., Shen B., Jiang W., Luo Z., Wang C., Teng J., Ding X., Lv W. The effect of postoperative fluid balance on the occurrence and progression of acute kidney injury after cardiac surgery. J Cardiothorac Vasc Anesth. 2021;35(9):2700-2706. PMID: 33158712. https://doi.org/10.1053/Uvca.2020.10.007
- Soliman-Aboumarie H., Denault A.Y. How to assess systemic venous congestion with point of care ultrasound. Eur Heart J Cardiovasc Imaging. 2023;24(2):177-180. PMID: 36464836. https://doi.org/10.1093/ehici/ieac239
- Бобовник С.В., Горобец Е.С., Заболотских И.Б., Киров М.Ю., Кохно В.Н., Кузьков В.В., Лебединский К.М., Ломиворо-тов В.В., Лубнин А.Ю., Мороз Г.Б., Мусаева Т.С., Неймарк М.И., Щеголев А.В. Периоперационная инфузионная терапия у взрослых. Анестезиология и реаниматология. 2021;(4):17-33. https://doi.org/10.17116/anaesthesiology20210417 Bobovnik S.V., Gorobets E.S., Zabolotskikh I.B., Kirov M.Yu., Kokhno V.N., Kuzkov V.V., Lebedinskii K.M., Lomivorotov V.V., Lubnin A.Yu., Moroz G.B., Musaeva T.S., Neimark M.I., Shchegolev A.V. Perioperative fluid therapy in adults. Anesteziologiya i reanimatologiya = Russian Journal of Anaesthesiology andReanimatology. 2021;(4):17-33. (In Russ.) https://doi.org/10.17116/anaesthesiologv20210417
- Malbrain M.L.N.G., Martin G., Ostermann M. Everything you need to know about deresuscitation. Intensive Care Med. 2022;48(12):1781-1786. PMID: 35932335; PMCID: PMC9362613. https://doi.org/10.1007/s00134-022-06761-7
- Beaubien-Souligny W., Rola P., Haycock K., Bouchard J., Lamarche Y., Spiegel R., Denault A.Y. Quantifying systemic congestion with Point-Of-Care ultrasound: development of the venous excess ultrasound grading system. Ultrasound J. 2020;12(1):16. PMID: 32270297; PMCID: PMC7142196. https:// doi.org/10.1186/s13089-020-00163-w
- Romano M., Viana E., Martins J.D., Corga Da Silva R. Evaluation of congestion levels in septic patients admitted to critical care units with a combined Venous Excess-Lung Ultrasound Score (VExLUS) — a research protocol. POCUS J. 2023;8(1):93-98. PMID: 37152345; PMCID: PMC10155730. https://doi. org/10.24908/pocus.v8i1.16188
- Luo X., Jiang L., Du B., Wen Y., Wang M., Xi X.; Beijing Acute Kidney Injury Trial (BAKIT) workgroup. A comparison of different diagnostic criteria of acute kidney injury in critically ill patients. Crit Care. 2014;18(4):R144. PMID: 25005361; PMCID: PMC4227114. https://doi.org/10.1186/cc13977
- Iranpour P., Lall C., Houshyar R., Helmy M., Yang A., Choi J.-I., Ward G., Goodwin S.C. Altered Doppler flow patterns in cirrhosis patients: an overview. Ultrasonography. 2016;35( 1 ):3-12. PMID: 26169079; PMCID: PMC4701371. https://doi.org/10.14366/usg.15020
- Wang Y., Bellomo R. Cardiac surgery-associated acute kidney injury: risk factors, pathophysiology and treatment. Nat Rev Nephrol. 2017;13(11):697-711. PMID: 28869251. https://doi. org/10.1038/nrneph.2017.119
- Argaiz E.R. VExUS Nexus: bedside assessment of venous congestion. Adv Chronic Kidney Dis. 2021;28(3):252-261. PMID: 34906310. https://doi.org/10.1053Aackd.2021.03.004


