Динамика показателей стабильности дентальных имплантатов (ISQ) при использовании низкоинтенсивного лазерного излучения в лечебно-профилактическом режиме
Автор: О.С. Гилева, М.А. Чупраков, Т.В. Либик, Е.С. Сюткина, Ф.З. Мирсаева
Журнал: Российский журнал биомеханики @journal-biomech
Статья в выпуске: 4 (82) т.22, 2018 года.
Бесплатный доступ
Целью настоящей работы явилось исследование первичной и вторичной стабильности дентальных имплантатов, установленных с помощью пред- и послеоперационной лазеротерапии аппаратом B-CureLaserDentalPro методом частотно-резонансного анализа. Фотобиостимулирующие эффекты низкоинтенсивного лазерного излучения аппаратом B-CureLaserDentalPro продемонстрированы на примере гармонизации формирования костно- имплантационного комплекса. В слепом рандомизированном сравнительном плацебоконтролируемом проспективном исследовании определено, что профессиональное и индивидуальное использование диодного лазера 5-го поколения с длиной волны 808 нм, мощностью 250 мВт, частотой импульсов 14 кГц, расфокусированным лучом 4,5 1,0 см, плотностью потока энергии 14,4 Дж/мин на пике (3,2 Дж/см2 в мин) на этапах предоперационной подготовки и послеоперационного сопровождения дентальной имплантации обеспечивает полноценную остеоинтеграцию имплантатов по показателям вторичной стабильности, ISQ2, определяемым частотно-резонансным методом (OsstellISQ), своевременное функциональное нагружение имплантата постоянной ортопедической конструкцией с долгосрочным благоприятным прогнозом лечения. По результатам исследования внутригрупповые, а также индивидуальные показатели вторичной стабильности имплантатов при включении в комплекс дентальной имплантации лазеротерапии в профилактическом и лечебно- реабилитационном режимах соответствовали критерию «превосходные» и превышали показатели первичной стабильности в среднем на 14,6%. В группе сравнения полноценная остеоинтеграция отмечена у 96,5% пациентов и с достоверно (p < 0,001) меньшим (на 5,9%) приростом значения ISQ; неуспех лечения фиксировали в 3,5% наблюдений (дезинтеграция и утрата имплантата).
Дентальная имлантация, остеоинтеграция, стабильность имплантата, низкоинтенсивное лазерное излучение, лазеротерапия
Короткий адрес: https://sciup.org/146282110
IDR: 146282110 | УДК: 531/534: | DOI: 10.15593/RZhBiomeh/2018.4.07
Dynamics of dental implant stability indicators (ISQ) using low-level laser therapy in treatment and prevention modes
The aim of this work was to study the primary and secondary stability of dental implants, installed with the use of pre- and postoperative laser therapy by special device B-CureLaserDentalPro , using the method of frequency-resonance analysis. Photobiostimulation effects of low-level laser therapy device B-CureLaserDentalPro is demonstrated on the example of harmonization of the formation of the bone-implant complex. The blind randomized comparative placebo controlled prospective study determined that the professional and individual use of a 5th generation diode laser with a wavelength of 808 nm, a power of 250 mW, a pulse frequency of 14 kHz, a defocused beam of 4.5 1.0 cm, a power flux density of 14.4 J/min at peak (3.2 J/cm2 per min) at the stages of preoperative preparation and postoperative follow-up of dental implantation provides full-fledged osseointegration of implants with secondary stability indicators ( ISQ 2), determined by the frequency-resonance method (Osstell ISQ ), ensuring timely functional loading of the implant with a permanent orthopedic design with a long-term favorable prognosis of treatment. Intragroup and all individual indicators of secondary stability of implants in the combination of dental implants with pre-and postoperative irradiation of periimplant tissues with a defocused beam B-CureLaserDentalPro met the criterion of excellent, exceeding the initial stability by 14.6%, whereas in control observations full-fledged osseointegration with significantly ( p 2 was noted in 96.5%, and patients with failure of loss of implant in 3.5% of cases.
Текст научной статьи Динамика показателей стабильности дентальных имплантатов (ISQ) при использовании низкоинтенсивного лазерного излучения в лечебно-профилактическом режиме
В последние десятилетия для стоматологической реабилитации пациентов с отсутствием зубов широко используется протезирование (съемное, несъемное, комбинированное) с опорой на дентальные имплантаты [8, 14, 18, 33]. У лиц с сохранным или компенсированным системным статусом, при наличии в полости рта благоприятных условий для установки имплантатов (достаточное количество костной ткани, тип костной ткани и др.), при успешно проведенной операции и рациональном протезировании возможен предсказуемо положительный и долгосрочный результат комплексного лечения с полным восстановлением эстетики лица, жевательных и речевых функций и, как следствие, с улучшением качества жизни стоматологического пациента [4, 12].
Однако нередко констатируется, что протетическое лечение с использованием дентальных имплантатов в качестве опоры не всегда завершается положительным результатом и сохраняет его в отдаленные сроки в силу многих труднопрогнозируемых факторов (индивидуальные общие реакции организма, изменения системного здоровья пациента, местные реакции тканей в зоне имплантации и др.) [6, 7, 15, 29]. Эффективность имплантационного лечения зависит от сроков выявления и адекватной коррекции воспалительных изменений в зоне имплантации и связанных с ними нарушений стабильности имплантата [1, 24].
Известно, что организация тканей на поверхности «имплантат ‒ кость» может происходить как костная интеграция (остеоинтеграция), фиброзно-костная интеграция (фиброостеоинтеграция) или соединительнотканная интеграция. Именно остеоинтеграция признается единственным условием долгосрочного успеха протезирования с опорой на дентальные имплантаты [1, 17]. Для прогнозирования исходов дентальной имплантации предложен ряд методов, косвенно оценивающих степень остеоинтеграции, в том числе по показателям (признакам) стабильности имплантатов: клиническим (перкутирование, мануальный контроль устойчивости); рентгенологическим; торк-тесту; периотестометрии; частотно- (или магнито-) резонансному анализу. К числу надежных и точных методов оценки стабильности дентальных имплантатов относится метод частотно-резонансного анализа ( Resonance Frequency Analysis , RFA ) [2, 20, 49]. В настоящее время RFA -метод активно используется в клинической имплантологии для прогнозирования исходов дентальной имплантации [9, 31, 55], определения показаний к началу ортопедического этапа лечения. Так, конкретные значения (<50 ед.) коэффициента стабильности имплантата ( Implant Stability Quotient , ISQ ) считаются критерием исключения из протокола немедленной нагрузки имплантата [47]. Динамическая оценка коэффициентов ISQ на этапах имплантационного лечения с последующей фиксацией данных в амбулаторной карте конкретного пациента созвучна идее персонифицированной терапии и оправдана с юридической точки зрения [30].
Специалисты сходятся во мнении, что в сравнении с другими методами оценки степени остеоинтеграции имплантатов метод RFA отличается эргономичностью (простотой воспроизведения, скоростью получения результатов, компактностью прибора и др.), безопасностью, валидностью получаемых результатов, их высокой прогностической и диагностической ценностью [21, 26, 34‒36, 47]. Метод RFA успешно используется в исследованиях in vivo и in vitro для: оценки качества остеоинтеграции имплантатов при определенных анатомо-физиологических условиях [25, 40, 45]; поиска наиболее эффективных фармакологических [27], в том числе клеточных, технологий [42, 50]; определения наиболее перспективных физиотерапевтических [10, 16] и инструментально-технологических [19, 41, 46, 51, 53] подходов к оптимизации остеоинтеграции при дентальной имплантации.
Признано, что одним из перспективных направлений улучшения и гармонизации репаративных процессов в мягких тканях (ранозаживления) и костных структурах челюстей (остеоинтеграции) после установки дентальных имплантатов является использование низкоинтенсивного лазерного излучения (НИЛИ) [13, 22, 23, 28, 37, 38, 43, 48, 52, 54]. Аппараты последнего поколения, генерирующие НИЛИ необходимой плотности и мощности, могут быть использованы врачом-стоматологом в профессиональных условиях и пациентом в качестве домашнего лечения, причем последнее весьма актуально с позиций повышения комплаентности пациента к проводимому стоматологическому лечению и поддержания полученных результатов. Спектр применения в стоматологической практике портативного диодного лазерного аппарата на основе Ga-Al-As с инфракрасным диапазоном излучения расфокусированным лучом (длина волны – 808 нм, мощность – 250 мВт)
B-CureLaserDentalPro ( GoodEnergies ®, Israel ) на сегодняшний день до конца не определен. Пилотные исследования обосновывают целесообразность его использования в комплексе стоматологического лечения с дентальной имплантацией [5, 29]. Однако клиническая эффективность лазеротерапии аппаратом
B-CureLaserDentalPro не подтверждена динамикой объективных показателей стабильности дентальных имплантатов, отражающей эволюцию и состоятельность процессов остеоинтеграции.
Цель – методом частотно-резонансного анализа исследовать первичную и вторичную стабильность дентальных имплантатов, установленных с использованием пред- и послеоперационной лазеротерапии аппаратом B-CureLaserDentalPro .
Материалы и методы исследования
Клинико-функциональные и биомеханические исследования проведены на кафедре терапевтической стоматологии и пропедевтики стоматологических заболеваний Пермского государственного медицинского университета им. академика Е.А. Вагнера Минздрава России (г. Пермь), кафедре хирургической стоматологии Башкирского государственного медицинского университета Минздрава России (г. Уфа), в хирургическом и ортопедическом отделении Городской стоматологической поликлиники № 2 (г. Пермь) с июня 2016 по февраль 2017 г. План, структура и методология исследования утверждены локальным этическим комитетом Пермского государственного медицинского университета им. академика Е.А. Вагнера.
В простом слепом рандомизированном проспективном многоцентровом сравнительном плацебоконтролируемом исследовании приняли участие 30 пациентов с частичным отсутствием зубов, комплексное стоматологическое лечение которых включало в себя следующие этапы: подготовительный (санация полости рта); традиционная предоперационная подготовка пациента с дополнительным облучением зоны планируемой имплантации аппаратом B-CureLaserDentalPro ; операция дентальной имплантации в соответствии с традиционным протоколом; послеоперационное ведение пациента с использованием лазеротерапии B-CureLaserDentalPro в лечебно-реабилитационном режиме; ортопедический этап с нагружением дентальных имплантатов.
Критерии включения пациентов с исследование: возраст – 25‒60 лет;
санированная полость рта и удовлетворительная гигиена полости рта; отсутствие системных противопоказаний к дентальной имплантации и лазеротерапии; наличие достаточного объема и необходимого качества челюстной кости в месте имплантации; наличие дефектов зубных рядов (частичное отсутствие зубов; К.08.1 по МКБ-10); наличие информированного согласия на лечение, а также на участие в исследовании.
Критерии исключения: наличие системных, местных или иных противопоказаний к используемым методам лечения; возраст – моложе 25 и старше 60 лет; отсутствие согласия на протезирование с опорой на имплантаты и на участие в настоящем исследовании.
Предмет исследования – первичная и вторичная стабильность имплантата по показателям ISQ , получаемым по результатам RFA .
Единица наблюдения – дентальный имплантат (136 шт.), установленный в кость верхней/нижней челюсти в соответствии с протоколом дентальной имплантации (с использованием / без использования лазеротерапии в лечебно-профилактическом режиме).
Объекты исследования – 30 пациентов (13 мужчин и 17 женщин в возрасте от 28 до 57 лет) с частичным отсутствием зубов, имеющих показания и намерения к лечению с использованием дентальной имплантации, не имеющие противопоказаний к лазеротерапии. Для оценки роли НИЛИ как фактора оптимизации дентальной имплантации методом ограниченной рандомизации были сформированы две группы наблюдения: основная ‒ 7 мужчин и 8 женщин в возрасте от 31 до 54 лет, которые в комплексе мероприятий по дентальной имплантации получали лазеротерапию активным, генерирующим инфракрасное лазерное излучение аппаратом B-CureLaserDentalPro , и группа сравнения ‒ 6 мужчин и 9 женщин в возрасте от 28 до 57 лет, которые для лечения получали неактивный плацебоаппарат B-CureLaserDentalPro , имитирующий генерацию НИЛИ, имеющий идентичный внешний дизайн.
При планировании дентальной имплантации, проводимой хирургом-стоматологом и врачом-ортопедом, использовали стандартные методы клиникофункционального обследования пациентов. Состояние костной ткани челюстей оценивали по данным конусно-лучевой компьютерной томографии ( PlanmecaProMax 3 D, PLANMECA, Finland ) с оценкой качества, архитектоники, плотности (методом динамической денситометрии) и атрофии костной ткани челюстей (I‒II тип кости по Lekholm U . и Zarb G ., D 2- D 3 по Misch C.E. et al .) По итогам комплексного обследования формулировали диагноз частичного отсутствия зубов по МКБ-10 и классификации Kennedy E . (1923).
По итогам первичного обследования пациенты сравниваемых групп в целом были сопоставимы по возрастно-половым характеристикам, уровням сохранности системного и стоматологического здоровья, структуре и клинико-топографическим характеристикам дефектов зубных рядов, качеству костной ткани, что обусловило сопоставимые подходы к выбору методики дентальной имплантации и проведенных реконструктивно-пластических операций, а также режимов лазеротерапии.
Оптимизированный протокол операции дентальной имплантации с пред- и послеоперационным проведением лазеротерапии
Операцию дентальной имплантации у пациентов обеих групп проводили по стандартной двухэтапной методике, включающей этап установки внутрикостных винтовых имплантатов и через 3 (на нижнюю челюсть) или 4‒6 (на верхнюю челюсть) месяцев – этап открытия имплантата с установкой формирователя десны.
Перед оперативным вмешательством проводили стандартную медикаментозную подготовку. Кроме того, за 2‒3 дня до оперативного вмешательства пациентам проводилась лазеротерапия в профилактическом режиме. В качестве источника НИЛИ использовали аппарат B-CureLaserDentalPro – лазер 5-го поколения с матрицами, состоящими из импульсных полупроводниковых (Ga Al As) лазерных диодов, с длиной волны – 808 нм, мощностью – 250 мВт, частотой импульсов – 14 кГц, расфокусированным лучом - 4,5 х 1,0 см, плотностью потока энергии - 14,4 Дж/мин на пике (3,2 Дж/см2 в мин); допущен к применению в качестве медицинского изделия (№ РЗН 2014/2167) приказом Росздравнадзора РФ от 10.03.2015 № 914. Процедуры проводил врач-стоматолог в условиях поликлинического приема по контактной стабильной методике, транскутанно, в проекции челюстного секстанта с планируемым местом установки имплантата(ов). Курс лазеротерапии – 2‒3 ежедневные процедуры, продолжительность процедуры – 8 мин. Планиметрические характеристики широкого когерентного лазерного пучка (площадь 4,5 см2, 4,5 см в длину и 1 см в ширину), генерируемого аппаратом B-CureLaserDentalPro, оптимальны для облучения соответствующего челюстного сегмента с планируемой зоной имплантации. Непосредственно перед операцией полость рта обрабатывали антисептическими средствами. Операцию дентальной имплантации проводили соответственно протоколу с использованием многофункционального имплант-центра ImplantCenter™ 2 (Acteon, France).
По завершении оперативного вмешательства пациентам назначали лазеротерапию в лечебно-реабилитационном режиме. Процедуры проводились обученным пациентом в домашних условиях с первого дня после установки дентальных имплантатов. Методика: контактная, стабильная, с аналогичными параметрами длины волны и мощности, частотой импульсов и площадью облучения кожи лица в проекции зубочелюстного сегмента(ов), соответствующего дентальной имплантации. Лечебные сеансы лазеротерапии проводили ежедневно, утром и вечером, до приема пищи, продолжительностью по 8 мин (суммарная экспозиция – 16 мин), курсом 7‒10 дней, при необходимости курс лазеротерапии повторяли до момента открытия имплантата.
Всего пациентам было установлено 136 (79 – у лиц основной и 57 – у лиц группы сравнения) дентальных имплантатов Alpha-Bio с поверхностью NanoTec™ ( Alpha-BioTech , Израиль) диаметром 3,5‒5,0 мм, длиной 10,0‒13,0 мм. Всего на верхнюю челюсть было установлено 93 имплантата (54 – пациентам основной и 39 – пациентам группы сравнения), на нижнюю челюсть – 43 имплантата (25 ‒ в основной и 18 – в группе сравнения).
Аппаратная лазеротерапия проводилась пациентам также на этапе установки формирователя(ей) десны по контактной стабильной методике, транскутанно в проекции установленного формирователя; ежедневно, продолжительностью 8 мин, курсом 3‒5 процедур в зависимости от клинической ситуации.
Методика оценки остеоинтеграции дентальных имплантатов методом RFA
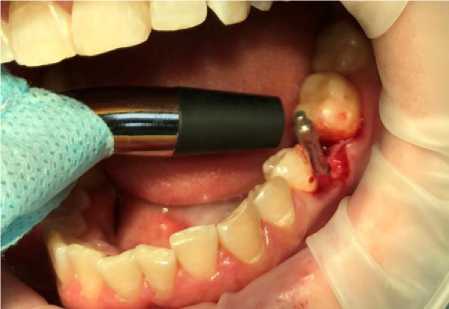
Для клинической оценки степени остеоинтеграции имплантатов методом частотно-резонансного анализа был использован прибор Osstell ISQ (рис. 1, а ), принцип действия которого основан на определении жесткости крепления имплантата в челюстной кости на основе анализа вынужденных колебаний, возбуждаемых в имплантате с помощью переменного магнитного поля излучателя.
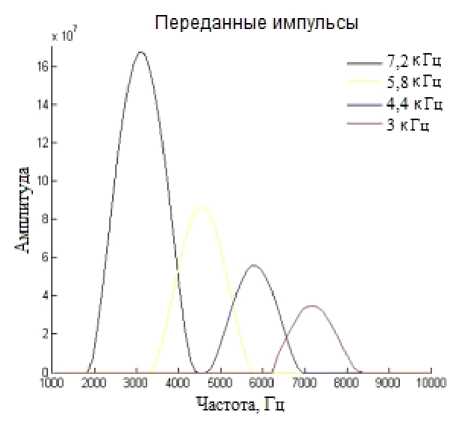
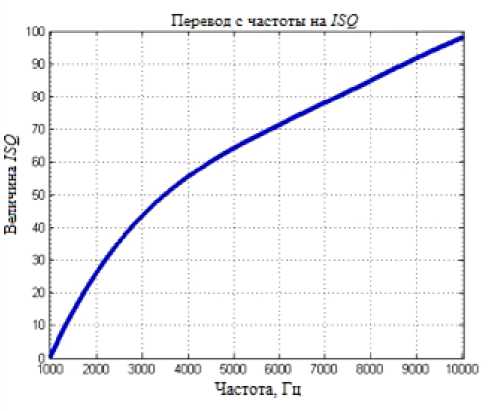
В примененной нами системе оценки остеоинтеграции Osstell ISQ используется специальный магнитный штифт Smartpeg, который фиксировали к дентальному имплантату или абатменту посредством винтового соединения. Известно, что штифт возбуждается магнитным импульсом от измерительного зонда прибора, и на основе ответного сигнала прибор рассчитывал резонансную частоту, являющуюся мерой жесткости крепления дентального имплантата в костной ткани челюсти. Импульсы прибора поступают на штифт в диапазоне частот 2‒8 кГц (4 импульса – 3; 4,4; 5,8 и 7,2 кГц) с различной амплитудой (рис. 1, в), каждый импульс посылается четыре раза, таким образом, измерительный цикл включает 16 импульсов прибора, на которые поступает 16 ответных сигналов, анализируемых с помощью программного комплекса с расчетом среднего значения, выводимого на экране аппарата (перевод частоты сигнала в показатель ISQ представлен на рис. 2, б), в диапазоне от 1 до 100 [32]. Исходили из того, что чем выше значение ISQ, тем выше жесткость крепления имплантата. Измерение проводил подготовленный хирург-стоматолог в условиях операционной хирургического отделения. Во время проведения измерения зонд удерживали неподвижно в мезиодистальном/вестибулооральном направлении на расстоянии 3‒7 мм от штифта Smartpeg (см. рис. 1, б). При измерении прибор подавал звуковой сигнал и на дисплее отображалось итоговое значение ISQ.

в г
Рис. 1. Прибор Osstell ISQ для частотно-резонансного анализа, установленный в операционной хирургического стоматологического отделения ( а ); процедура измерения первичной стабильности имплантата методом резонансно-частотного анализа прибором Osstell ISQ : штифт Smartpeg зафиксирован на имплантате, зонд установлен в вестибулооральном направлении в проекции штифта ( б ); излучаемые прибором Osstell ISQ разночастотные сигналы ( в ); трансляция получаемого от штифта Smartpeg сигнала в значение ISQ ( г )
Регистрацию показателей первичной стабильности имплантатов ( ISQ 1 ) проводили сразу после установки дентальных имплантатов ( T 1 ) для выявления ранних признаков их низкой стабильности и прогноза потери. Оценка вторичной стабильности имплантатов проводилась на этапе их открытия, через 3-6 месяцев, ( Т 90 - на нижней челюсти и T iso — на верхней челюсти).
Всего в динамике наблюдений у 30 пациентов со 136 установленными дентальными имплантатами проанализировано 544 показателя ISQ (на двух точках наблюдения, в двух проекциях), полученные данные определяли последующую врачебную тактику. Так, в случаях фиксации исходно (на Т i ) низких или снижающихся в отдаленные сроки ( Т 90 - Т iso ) показателей ISQ (соответственно ISQ i и ISQ 2 ) пациентам проводили дополнительное рентгенологическое обследование, вносили коррекцию в тактику лечения и протезирования.
Оценку первичной стабильности дентальных имплантатов непосредственно после их установки определяли в соответствии с рекомендациями A.P. Saadoun и соавт. (2004): ISQ < 50 - недостаточная стабильность; 50 < ISQ < 60 - адекватная стабильность; 60 < ISQ < 75 - превосходная стабильность; ISQ > 75 - ишемия, риск развития некроза кости.
Статистическая обработка результатов исследования
Достоверность различий между сравниваемыми величинами стабильности дентальных имплантатов в динамике наблюдения и в сравнении показателей сформированных групп оценивали методами параметрической ( t -критерия для независимых выборок (1) и t -критерия для парных выборок (2) при нормальности распределения данных) и непараметрической ( U- критерий Манна‒Уитни для независимых выборок (3), критерий Вилкоксона для парных выборок (4) при ненормальности распределения данных) статистики с определением значений среднего, среднеквадратичного отклонения, максимума и минимума, нормальности распределения. Статистическую оценку данных проводили с использованием программного обеспечения Statistica 13.
t = —1 1 2 : ~ t( s ^ 1 / n +1/ n2
Zn t = ~ tn-1, sz
n x ( n x + 1)
2 ’
T n' ( n' + 1)
T
- 0,5
n ( n + 1)(2 n' + 1) *
Результаты и их обсуждение
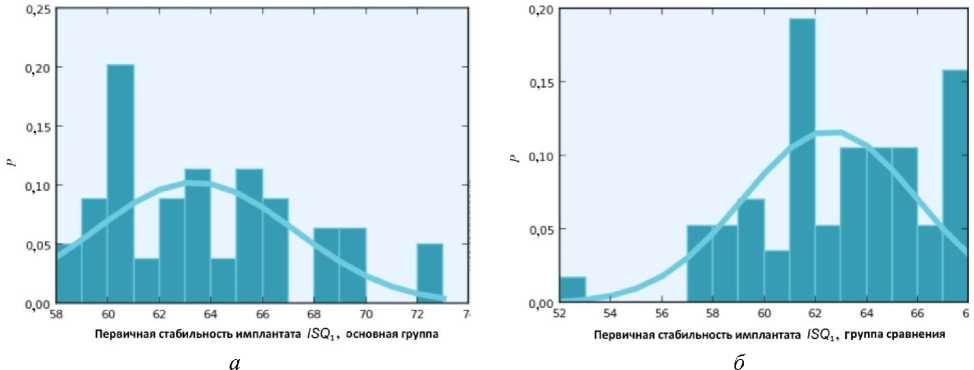
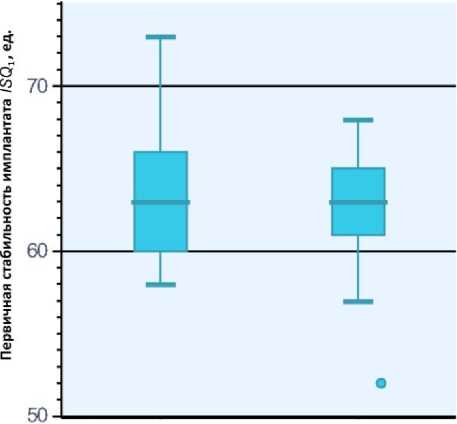
При оценке показателей первичной стабильности имплантатов их распределение у пациентов обеих групп оказалось нормальным (рис. 2, а, б) (показатели нормальности распределения: в основной группе - 0,03091, в группе сравнения - 0,2754), что позволило использовать методы параметрической статистики. Показатели ISQ на исходной точке отсчета (Т1) у пациентов основной группы, у которых стандартный протокол дентальной имплантации был дополнен пред- и послеоперационной лазеротерапией, составили 63,354 ± 3,876 ед. и достоверно (p = 0,2181) не отличались от средних значений ISQ1 (62,561 ± 3,407 ед.) у лиц группы сравнения, использующих неактивный плацебоаппарат B-CureLaserDentalPro, что отражало высокую степень стабильности всех установленных в ходе операции имплантатов (табл. 1; рис. 2, в).
Основная группа Группа сравнения
в
Рис. 2. Диаграммы распределения показателей ISQ 1 в основной группе
( p abnormal = 0,03091) ( а ) и группе сравнения ( p abnormal = 0,2754) ( б );
сравнительная диаграмма показателей первичной стабильности имплантатов ( ISQ 1 ) в группах сравнения ( в )
Таблица 1
Показатели первичной стабильности имплантатов ( ISQ 1 ) в группах наблюдения
|
Группа |
N |
Среднее |
Стандартное отклонение |
Min |
Max |
|
Основная |
79 |
63,354 |
3,876 |
58,0 |
73,0 |
|
Сравнения |
57 |
62,561 |
3,407 |
52,0 |
68,0 |
Фиксируемые исходно показатели первичной стабильности имплантатов укладывались в диапазон «адекватной» или «превосходной» стабильности по A.P. Saadoun . Ни у одного из пациентов первичный коэффициент ISQ 1 не был ниже 50 ед., прогнозируя благоприятные исходы имплантационного лечения.
Учитывая ( Meredith H.N ., 1996), что средненормативные показатели ISQ при установке дентальных имплантатов на верхней и нижней челюстях, как правило, отличаются (58 ед. в среднем на верхней и 66 ед. – на нижней челюсти), у пациентов сравниваемых групп проводили сравнительный анализ первичной стабильности имплантатов в зависимости от установки на верхнюю или нижнюю челюсть. Так, у пациентов основной группы первичная стабильность имплантатов, установленных на нижнюю челюсть, составила 68,781 ± 2,342, тогда как показатели верхнечелюстных имплантатов были достоверно ( p < 0,05) ниже 61,498 ± 1,908. Сходные различия ISQ на разных челюстях отмечены и у лиц группы сравнения, у которых показатель первичной устойчивости нижнечелюстных имплантатов составил 66,231 ± 1,244, а на верхней челюсти – 59,890 ± 2,986. При сравнительной оценке показателей первичной стабильности имплантатов, установленных на разных челюстях у пациентов сравниваемых групп, выявлено отсутствие достоверных межгрупповых различий в показателях (нижняя челюсть: 68,781 ± 2,342 – основная группа, 66,231 ± 1,244 – группа сравнения, p > 0,05; верхняя челюсть: 61,498 ± 1,908 – основная группа, 59,890 ± ± 2,986 – группа сравнения, p > 0,05).
Высокие показатели первичной стабильности имплантатов, отмечаемые у пациентов обеих групп наблюдения, не связывали с прямыми эффектами сочетанной лазеротерапии, а объясняли четким следованием протоколу оперативного вмешательства, исключением противопоказаний, связанных с недостаточным качеством костной ткани челюстей, использованием современного инструментальноаппаратурного обеспечения дентальной имплантации. Вместе с тем проведенные ранее клинико-функциональные исследования по использованию B-CureLaserDentalPro в пред- и ранний постоперационный период [3, 5, 29] свидетельствовали об эффективном купировании отечно-болевого и сенсорно-парестетического симптомов в периимплантационной зоне, достоверном (в 3,5 раза) снижении частоты развития, степени выраженности и длительности сохранения симптомов постимплантационного мукозита, профилактике периимплантита. Вклад лазеротерапии в профилактику осложнений раннего и позднего послеоперационного периода создавал необходимые условия для полноценной регенерации мягкотканных и костных структур, последующей полноценной остеоинтеграции дентальных имплантатов. Исходили из того, что вторичная стабильность имплантатов, определяемая после их открытия, во многом зависела от исходных показателей ISQ и отражала характер ремоделирования костной ткани вокруг имплантата.
На этапе открытия все имплантаты, установленные пациентам основной группы, были клинически стабильны, что коррелировало с показателями вторичной стабильности. Оценка нормальности распределения данных по показателю вторичной стабильности имплантатов (рис. 3, а , б ) обусловила необходимость использования непараметрических статистических методов, так как полученные значения у лиц группы сравнения отличались ненормальным распределением (см. рис. 3, б ).
По данным RFA, у пациентов основной группы, в комплексе лечения которых использовалась пред- и послеоперационная лазеротерапия, показатели вторичной стабильности имплантатов (T90, T180) составили в среднем 72,608 ± 1,353 ед., что соответствовало показателям полностью остеоинтегрированных имплантатов, а в сравнении с отдельными данными [11, 27] ‒ даже превышало их (табл. 2, рис. 3). Прирост показателей вторичной стабильности имплантатов ISQ2 на фоне лазеротерапии составил 9,254 ед. (прирост на 14,6%). Данные RFA, прямо коррелируемые с клинико- рентгенологическими показателями, определили показания к функциональному нагружению имплантатов у всех пациентов основной группы.
У большинства пациентов группы сравнения значения вторичной стабильности имплантатов (в среднем 66,281 ± 7,126 ед.) превышали показатели первичной стабильности, что указывало на успешную остеоинтеграцию имплантатов и возможность фиксации на них протетических конструкций. Однако в 3,5% случаев (два имплантата на верхней челюсти) показатель ISQ 2 после раскрытия имплантата составил 30,5 ± 1,5 ед. (падение ISQ 1 на 24,0 ± 1,0 ед.), а после рентгенологического исследования по периферии имплантата определяли зону просветления до 2 мм, с резорбцией костной ткани в цервикальном участке (рентгенологическая картина дезинтеграции имплантата и клиническое заключение «неуспех дентальной имплантации»). Прирост показателей вторичной стабильности имплантатов ISQ 2 у лиц группы сравнения составил 3,72 ед. (прирост на 5,9%).
По данным теста Манна‒Уитни, показатели вторичной стабильности имплантатов у лиц основной и группы сравнения имели достоверные различия ( p < 0,001; U = 44,5) и были выше у лиц, получавших лазеротерапию активным аппаратом B-CureLaserDentalPro .
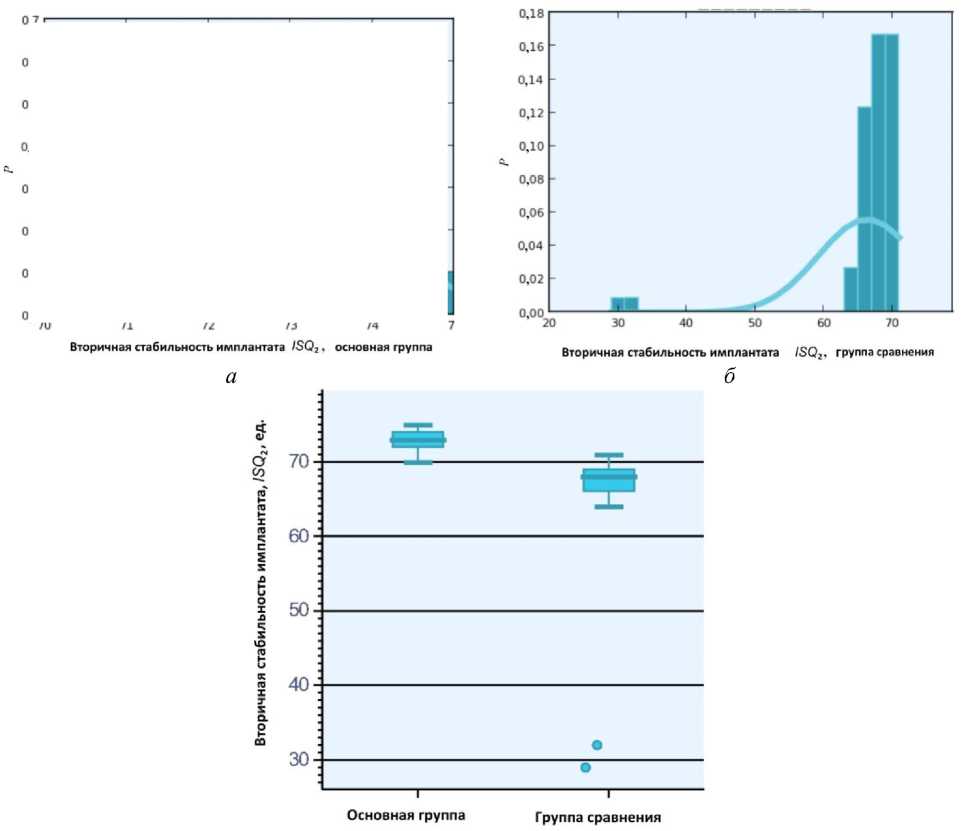
в
Рис. 3. Диаграммы распределения показателей ISQ 2 в основной группе ( p abnormal = 0,1500) ( а ) и группе сравнения ( p abnormal < 0,001) ( б ); сравнительная диаграмма показателей вторичной стабильности имплантатов ( ISQ 2 ) в группах сравнения
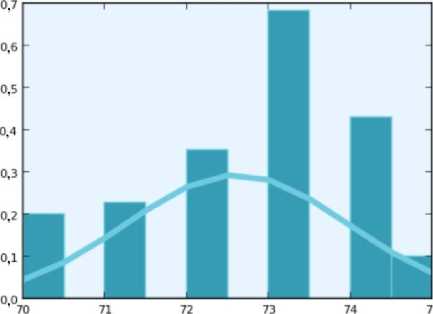
Таблица 2
Показатели вторичной стабильности имплантатов (ISQ 2 ) в группах наблюдения
|
Группа |
N |
Среднее |
Стандартное отклонение |
Min |
Max |
|
Основная |
79 |
72,608 |
1,353 |
70,0 |
75,0 |
|
Сравнения |
57 |
66,281 |
7,126 |
29,0 |
71,0 |
Сравнительная внутригрупповая оценка показателей первичной и вторичной стабильности имплантатов показала достоверный прирост значений ISQ у лиц основной группы ( p < 0,001 по показателю t -критерия для парных выборок) и лиц группы сравнения ( p < 0,01 по показателю критерия Вилкоксона), однако фиксируемые в динамике изменения показателей устойчивости имплантатов, отражающие степень их остеоинтеграции, оказались достоверно более значимыми у лиц, получавших до- и послеоперационную лазеротерапию с использованием активного аппарата.
Заключение
Фотобиостимулирующие эффекты низкоинтенсивного лазерного излучения аппаратом B-CureLaserDentalPro продемонстрированы на примере гармонизации формирования костно-имплантационного комплекса. В слепом рандомизированном сравнительном плацебоконтролируемом проспективном исследовании определено, что профессиональное и индивидуальное использование диодного лазера 5-го поколения с длиной волны 808 нм, мощностью 250 мВт, частотой импульсов 14 кГц, расфокусированным лучом 4,5 х 1,0 см, плотностью потока энергии 14,4 Дж/мин на пике (3,2 Дж/см2 в мин) на этапах предоперационной подготовки и послеоперационного сопровождения дентальной имплантации обеспечивает полноценную остеоинтеграцию имплантатов по показателям вторичной стабильности ISQ 2 , определяемым частотно-резонансным методом ( OsstellISQ ), своевременное функциональное нагружение имплантата постоянной ортопедической конструкцией с долгосрочным благоприятным прогнозом лечения.
Внутригрупповой и все индивидуальные показатели вторичной стабильности имплантатов при комбинировании дентальной имплантации с пред- и послеоперационным облучением периимплантатных тканей расфокусированным лучом B-CureLaserDentalPro соответствовали критерию «превосходные», превышая показатели первичной стабильности на 14,6%, тогда как в контрольных наблюдениях полноценная остеоинтеграция с достоверно ( p < 0,001) меньшим (на 5,9%) относительно исходного уровня приростом значения ISQ была отмечена у 96,5% пациентов, а неуспех лечения с дезинтеграцией и утратой имплантата – в 3,5% наблюдений.
имплантация: состояние вопроса на сегодняшний день (обзор литературы) // Клиническая стоматология. – 2017. – № 2 (82). – С. 32‒34.
DOI: 10.26717/BJSTR.2017.01.000477
Список литературы Динамика показателей стабильности дентальных имплантатов (ISQ) при использовании низкоинтенсивного лазерного излучения в лечебно-профилактическом режиме
- Бениашвили Р.М., Кулаков А.А., Гурин А.Н., Григорьянц Л.А., Комлев В.С., Семкин В.А. Десневая и костная пластика в дентальной имплантологии. - М.: ГЭОТАР-Медиа, 2017. - 240 с.
- Воробьев А.А., Шемонаев В.И., Михальченко Д.В., Величко А.С. Взгляд на проблему дентальной имплантации в свете современных научных представлений // Волгоградский научно-медицинский журнал. - 2009. - № 2(22). - С. 19-24.
- Гилева О.С., Задорина И.И., Исламова А.Ф., Пленкина В.А., Синтюрина А.А., Чупраков М.А. Оценка болевого симптома у пациентов с воспалительными заболеваниями слизистой оболочки рта, паро- и эндодонта [ЭР] // Современные проблемы науки и образования. - 2017. - № 4. - URL: http://science-education.ru/ru/article/view?id=26577 (дата обращения 01.06.2018).
- Гилева О.С., Либик Т.В., Назукин Е.Д., Яков А.Ю., Городилова Е.А. Сравнительная оценка эффективности различных методик лечения пациентов с частичными и полным дефектами зубных рядов по стоматологическим паказателям качества жизни (Профиль влияния стоматологического здоровья, OHIP-49-RU) // Стоматология для всех. - 2015. - № 2. - С. 14-18.
- Гилева О.С., Подгорный Р.В., Чупраков М.А., Яков А.Ю., Либик Т.В., Задорина И.И. Эффективность применения лазеротерапии по технологии B-CureLaserDentalPro при дентальной имплантации // Проблемы стоматологии. - 2017. - Т. 13, № 1. - С. 94-102.


