Диссеминированный перитонеальный лейомиоматоз у пациентки с анамнезом лапароскопической миомэктомии: клиническое наблюдение
Автор: Сидакова З.А., Баранова А.А., Чернавина К.М., Алдушкина Ю.В., Грицай А.Н., Любченко Л.Н.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Случай из клинической практики
Статья в выпуске: 3 т.24, 2025 года.
Бесплатный доступ
Актуальность. Диссеминированный перитонеальный лейомиоматоз (ДПЛ) – редкое заболевание мезенхимального происхождения, характеризующееся наличием множества доброкачественных миоматозных опухолевых узлов, рассеянных по поверхности брюшины, сальнику и другим мягким тканям брюшной полости и/или малого таза. Несмотря на доброкачественные морфологические характеристики, ДПЛ отличается склонностью к рецидивированию, а также возможным риском злокачественной трансформации. Кроме того, клинические проявления опухоли напоминают канцероматоз брюшины, что требует проведения тщательного дифференциально-диагностического поиска для постановки верного диагноза и обеспечения надлежащего лечения пациентов. В настоящее время вследствие редкости ДПЛ отсутствуют стандарты диагностики и лечения данного заболевания. Цель исследования – описание клинического наблюдения пациентки с гормонально-чувствительным рецидивирующим ДПЛ и анамнезом лапароскопической миомэктомии для совершенствования алгоритмов ведения подобных пациентов. Материал и методы. Материалом для статьи послужили данные НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиала ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, где пациентка проходила лечение по поводу ДПЛ. Для определения тактики лечения пациентки в описанном клиническом наблюдении выполнен развернутый дифференциально-диагностический поиск, включающий различные визуализирующие техники для оценки распространенности опухолевого процесса, а также методики забора опухолевого материала для его морфологической оценки, в частности, была проведена диагностическая лапароскопия со срочным морфологическим исследованием, позволившим окончательно определить объем оперативного вмешательства и достичь максимально возможной циторедукции. При последующем плановом морфологическом исследовании в опухоли выявлена экспрессия рецепторов эстрогена и прогестерона, что послужило поводом для назначения гормональной терапии совместно с тщательным динамическим наблюдением с целью улучшения возможности контроля заболевания. Заключение. Изучение и демонстрация редких клинических случаев расширяют кругозор и понимание природы заболевания. Клиническое наблюдение и проведенный обзор литературы продемонстрировали, что клетки лейомиомы склонны к имплантационной диссеминации.
Диссеминированный перитонеальный лейомиоматоз, миома матки, лейомиома, морцелляция, мезенхимальные опухоли, гинекология, малоинвазивные вмешательства
Короткий адрес: https://sciup.org/140310585
IDR: 140310585 | УДК: 616-006.363.03 | DOI: 10.21294/1814-4861-2025-24-3-180-189
Disseminated peritoneal leiomyomatosis following laparoscopic myomectomy: a case report
Background. Disseminated peritoneal leiomyomatosis (DPL) is a rare disease of mesenchymal origin that is characterized by the presence of multiple benign myomatous tumors proliferated along the surface of the peritoneum, omentum and other soft tissues of the abdominal cavity and / or pelvis. Despite the benign morphological characteristics, DPL is known for its tendency for recurrence or malignancy. In addition, clinical manifestations of these tumors resemble peritoneal carcinomatosis, therefore, imaging investigations are important to accurately diagnose and treat lesions Currently, due to the rarity of DPL, there are no conventional guidelines for the diagnosis and treatment of this disease. The purpose of this study was to present a case report of a female patient with hormonally sensitive recurrent DPL following laparoscopic myomectomy to improve the algorithms for managing this disease. Material and Methods. The patient with DPL was treated at N.A. Lopatkin Research Institute of Urology and Interventional Radiology, a branch of the National Medical Research Center of Radiology of the Russian Ministry of Health, DPL. To determine the extent of the tumor and the appropriate treatment tactics for the patient, an extensive differential diagnostic search involving various imaging techniques was performed. The patient underwent diagnostic laparoscopy with urgent morphological examination to finally determine the extent of surgery and achieve the maximum cytoreduction. A subsequent planned morphological examination revealed the presence of estrogen and progesterone receptors within the tumor cells, that was the reason for prescribing hormonal therapy and careful follow-up for the patient. Conclusion. Study and demonstration of rare clinical cases expands the horizons and understanding of the nature of the disease. Our case report and literature review demonstrated that leiomyoma cells are prone to implantation dissemination.
Текст научной статьи Диссеминированный перитонеальный лейомиоматоз у пациентки с анамнезом лапароскопической миомэктомии: клиническое наблюдение
Диссеминированный перитонеальный лейомио-матоз (ДПЛ) – редкое заболевание мезенхимального происхождения, характеризующееся наличием множества миоматозных опухолевых узлов, рассеянных по поверхности брюшины, сальнику и другим мягким тканям брюшной полости и/или малого таза [1, 2]. При патоморфологическом и иммуногистохимическом исследовании опухолевые узлы при ДПЛ демонстрируют классические признаки типичной доброкачественной лейомиомы, представленной переплетающимися пучками веретеновидных клеток со слабовыраженной атипией или без нее, с низкой митотической активностью и положительной экспрессией виментина, гладкомышечного актина, десмина и кальдесмона [1, 3, 4]. Впервые диссеминация миоматозных опухолевых узлов по брюшине описана в 1952 г. Wilson et Peale, а термин «ДПЛ» введен Taubert et al. в 1965 г. [1].
Этиопатогенетические основы ДПЛ до конца не изучены. Выдвинуты гормональная, ятрогенная и генетическая теории развития и прогрессирования ДПЛ. Согласно гормональной теории, ведущим фактором в развитии ДПЛ является повышенный уровень женских половых гормонов. В исследованиях на животных установлено, что гиперэстроге-ния в течение длительного времени может вызывать метаплазию мезенхимальных стволовых клеток в фибробласты, лейомиоциты или эндометриальную строму. В подобных случаях у животных развивались узелковые опухолевые образования из клеток мезенхимы, сходные с таковыми у людей при ДПЛ. Кроме того, по данным иммуногистохимического окрашивания опухолевые клетки при ДПЛ в большинстве описанных случаев экспрессируют высокие уровни рецепторов эстрогена и прогестерона [1]. Гормональная теория также подтверждается опубликованными клиническими наблюдениями, где ДПЛ преимущественно обнаруживается у женщин в пременопаузе с нарушением гормонального статуса (например, с анамнезом длительной заместительной гормональной терапии, наличием гормон-продуцирующей опухоли и др.).
Согласно ятрогенной теории, развитие ДПЛ обусловлено диссеминацией или имплантацией опухолевых клеток при миомэктомии или гистерэктомии с морцелляцией [5, 6]. В зарубежной литературе опубликовано 28 статей, описывающих 41 случай ятрогенного ДПЛ [4]. Доказательством ятрогенной теории являются исследования, установившие, что у одного и того же пациента клетки опухолевых узлов при ДПЛ и лейомиоме матки имеют идентичные хромосомные аберрации. Цитогенетические анализы также демонстрируют, что опухолевые образования при ДПЛ могут быть продуктами клонального развития или потенциальными метастатическими отложениями уни-центрического заболевания и следовать сходным патогенетическим путям [7, 8].
Однако до сих пор отсутствует четкая корреляционная связь между ДПЛ и миомой матки, поскольку также описаны клинические случаи ДПЛ без ее наличия в анамнезе, в частности у мужчин. Кроме того, описаны ДПЛ, при которых отсутствует экспрессия опухолевыми клетками рецепторов к эстрогену и прогестерону [1, 3, 5]. Согласно генетической теории, ДПЛ возникает вследствие наследственной предрасположенности к независимой метаплазии подбрюшинных мезенхимальных клеток. Данная теория доказывается наличием ряда случаев диагностирования ДПЛ у родственников. Так, N. Halama et al. [1] описана семья с ДПЛ как у женщин, так и у мужчин. Экспериментальный анализ R. Vaishnavi et al. [9] обнаружил потенциальную связь между генетической предрасположенностью, гормональным дисбалансом и ятрогенными факторами в патогенезе развития ДПЛ. Однако следует учитывать, что в патогенезе ДПЛ могут участвовать не только герминальные изменения, но и спонтанные генетические поломки, возникающие в течение жизни. На основании вышеописанного к факторам риска ДПЛ можно отнести: женский пол (особенно репродуктивного возраста, чаще 30–40 лет), нарушения гормонального статуса (наличие гормон-продуцирующей опухоли, беременность, длительный прием оральных контрацептивов и др.), наличие миомы матки, лапароскопическую миоэктомию по поводу миомы матки с использованием морцелляции в анамнезе, а также семейный анамнез [10–12].
В настоящее время в мировой литературе описано около 200 случаев ДПЛ, большинство из которых приходится на женщин пременопаузального возраста с анамнезом длительной гиперэстрогении и/или лейомиомой матки, реже ДПЛ регистрировался у мужчин или женщин в постменопаузе [1–5]. ДПЛ, вероятно, имеет большую распространенность вследствие часто бессимптомного течения заболевания, а также все большего использования малоинвазивных хирургических техник лечения лейомиом [10]. Так, лейомиомы матки являются наиболее распространенными доброкачественными гинекологическими опухолями, склонными к рецидивированию у женщин в пременопаузе: к 50-летнему возрасту они диагностируются у 70 % женщин. Согласно эпидемиологическому исследованию, в России заболеваемость миомой матки высокая: в 2019 г. глобальный стандартизи- рованный по возрасту показатель заболеваемости лейомиомой составил 586,64 на 100 тыс., уступив место только Латвии, а общемировая заболеваемость лейомиомой оценена авторами в 0,25 на 100 тыс. женщин [13].
Несмотря на относительную редкость, ДПЛ представляет большой интерес с практической точки зрения. Так, согласно классификации ВОЗ (2020), ДПЛ, как и паразитарная лейомиома, внутривенный лейомиоматоз, доброкачественная метастазирующая лейомиома, относится к гладкомышечным опухолям неопределенного злокачественного потенциала (smooth muscle tumors of uncertain malignant potential, STUMP), т. е. к опухолям, которые не могут быть однозначно отнесены к доброкачественным или злокачественным из-за особенностей своих поведенческих характеристик, в частности, из-за высокой частоты рецидивов и риска злокачественной малигнизации [14].
Согласно критическому обзору 62 случаев рецидивирующей или метастатической лейомиомы матки S. Sanada et al. [15], лапароскопическая операция с использованием неограниченной морцел-ляции выполнена в 23 (37,0 %) случаях, при этом исходно злокачественный потенциал опухоли был недооценен у 14 (24,2 %) пациенток, а истинная злокачественная трансформация наблюдалась в 7 (11,3 %) случаях. По мнению авторов, рецидиви-рование лейомиом наблюдалось преимущественно в областях, прилежащих к интраоперационному полю, а медиана времени до рецидива составляла в среднем 51,5 мес.
Злокачественная трансформация ДПЛ чаще наблюдается у мужчин, женщин в постменопаузе, у лиц без анамнеза лапароскопической хирургии с морцелляцией, а также в случаях отсутствия экспрессии опухолевыми клетками гормональных рецепторов [3]. Время между инициальной диагностикой ДПЛ и злокачественной трансформацией, по данным ряда авторов, может варьировать от 1 мес до 8 лет [1, 3, 4, 6]. Знания клиницистов о ДПЛ необходимы для постановки верного диагноза и обеспечения надлежащего лечения.
Целью исследования является изложение клинического наблюдения пациентки с гормональночувствительным рецидивирующим ДПЛ и анамнезом лапароскопической консервативной миомэктомии.
Материалом для статьи послужили данные НИИ урологии и интервенционной радиологии им. Н.В. Лопаткина – филиала ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, где пациентка проходила лечение по поводу ДПЛ.
Клиническое наблюдение
Пациентка, 40 лет, обратилась к онкогинекологу в НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина в октябре 2022 г. с жалобами на пальпируемое образование в правой подвздошной области. Из анамнеза установлено, что в 2015 г. по поводу множественных миом матки выполнена лапароскопическая консервативная миомэктомия с морцелляцией узлов. В 2020 г. при динамическом наблюдении, по данным УЗИ, в правой подвздошной области выявлено опухолевое образование, размерами до 2,5 см. В течение 2 мес опухолевое образование в правой подвздошной области стало пальпироваться, по поводу чего в октябре 2022 г. пациентка самостоятельно обратилась в НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина Из гинекологического анамнеза: реализованная репродуктивная функция: в анамнезе 2 родов, менструации регулярные, по 6–7 дней через 28 дней. Семейный анамнез отягощен миомами матки.
В НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина пациентке рекомендовано комплексное обследование. По данным МРТ с контрастным усилением от октября 2022 г.: в полости малого таза выявлены множественные узловые образования по брюшине, асцит, кистозно-солидное образование в проекции левого яичника, эндометриоз.
С целью морфологической верификации диагноза в октябре 2022 г. выполнена чрескожная трепан-биопсия опухолевого образования правой подвздошной области под ультразвуковой навигацией. По данным гистологического исследования от ноября 2022 г.: столбики опухолевого узла представлены разнонаправленными пучками гладкомышечных клеток без признаков ядер-ной атипии, с очаговым гиалинозом стромы и многочисленными сосудистыми полостями без митозов и некрозов. При иммуногистохимическом исследовании в клетках опухоли отмечена диффузная экспрессия гладкомышечного актина и кальдесмона, без экспрессии CD34 и десмина. На основании вышеописанного морфологическая картина и иммунофенотип полученного биопсионного материала соответствовали лейомиоме. Также произведена пункция заднего свода влагалища для забора асцитической жидкости. По данным цитологического исследования от октября 2022 г.: в асцитической жидкости отсутствовали клетки с опухолевой атипией. По данным неинвазивных визуализирующих методик исследования в других органах и системах признаков опухолевого роста не выявлено.
В отделении реконструктивно-пластической гинекологии и онкологии НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина в декабре 2022 г. выполнено раздельно-диагностическое выскабливание полости матки и цервикального канала. По данным гистологического заключения полученного материала выявлены железистофиброзный полип эндометрия и субмукозная лейомиома тела матки.
Для оценки распространенности опухолевого процесса и уточнения диагноза в январе 2023 г. выполнена диагностическая лапароскопия с целью срочного интраоперационного исследования левого придатка матки и пораженных участков брюшины. При интраоперационной ревизии в полости малого таза имелась асцитическая жидкость, до 1 л, в области правого яичника – опухолевый узел, размером до 3,5 см, а также множественные опухолевые узлы по париетальной брюшине (2 опухолевых узла с четкими ровными контурами в левой подвздошной области; единичный опухолевый узел в правом боковом фланге живота; множественные мелкие опухолевые узлы по париетальной брюшине малого таза слева; опухолевый узел, размером до 5 см, по париетальной брюшине передней брюшной стенки по срединной линии) (рис. 1). Произведен забор асцитической жидкости для цитологического исследования (признаки клеточной атипии не выявлены). Выполнены удаление левого придатка матки и биопсия патологических участков брюшины. Полученный материал отправлен на срочное гистологическое исследование, по данным которого опухолевый материал из левого яичника и узловых образований брюшины соответствовал лейомиоме. Интраоперационно установлен диагноз ДПЛ. Произведена конверсия и дополнительно выполнена экстирпация матки с левым придатком и правой маточной трубой, парциальная перитонэктомия пораженных участков брюшины малого таза.
По данным планового патоморфологического исследования от января 2023 г.: макроскопически в срезах тела матки выявлены участки множественных субсерозных и интрамуральных лейомиом с вторичными дегенеративными изменениями и признаками расстройства кровообращения в виде некроза, кровоизлияний в ткань узлов. Шейка матки обычного строения, с очагами гипер-, паракератоза многослойного плоского эпителия покрова экзоцервикса, фокусами плоскоклеточной метаплазии желез, ретенционными кистами. Маточные трубы с очаговым фиброзом складок эндосаль-пинкса. В срезах ткани левого яичника определялся прилежащий опухолевый узел, имеющий строение лейомиомы. Морфологическая картина узловых образований брюшины также соответствовала лейомиоме (рис. 2). При иммуногистохимическом исследовании наблюдалась позитивная реакция опухолевых клеток с гладкомышечным актином и кальдесмоном, а также с рецепторами эстрогенов и прогестерона (рис. 3). Реакция с CD34 и десмином была отрицательная.
В послеоперационном периоде рекомендована длительная терапия синтетическим агонистом гонадотропин-рилизинг-гормона – бусерелином 3,75 мг каждые 28 дней длительно. Пациентка не придерживалась назначенного лечения. Через 6 мес, в июне 2023 г., при контрольной МРТ ор-
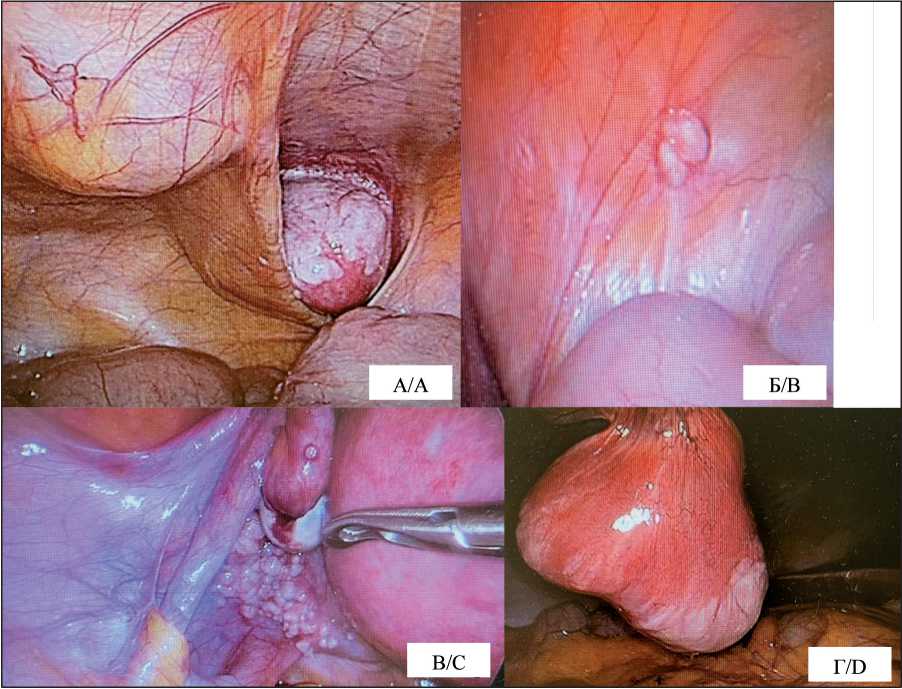
Рис. 1. Диагностическая лапароскопия от января 2023 г.: А – опухолевый узел, размером до 3,5 см, исходящий из левого яичника; Б – опухолевый узел в правом боковом фланге живота; В – множественные мелкие опухолевые узлы по париетальной брюшине малого таза слева;
Г – опухолевый узел, размером до 5 см, по париетальной брюшине передней брюшной стенки, по срединной линии. Примечание: рисунок выполнен авторами
Fig. 1. Diagnostic laparoscopy (January 2023): A – tumor originating from the left ovary of up to 3.5 cm in size; B – tumor in the right lateral flank of the abdomen; C – multiple small tumors along the parietal peritoneum of the pelvis on the left;
D – tumor of up to 5 cm in size along the parietal peritoneum of the anterior abdominal wall along the midline.
Note: created by the authors
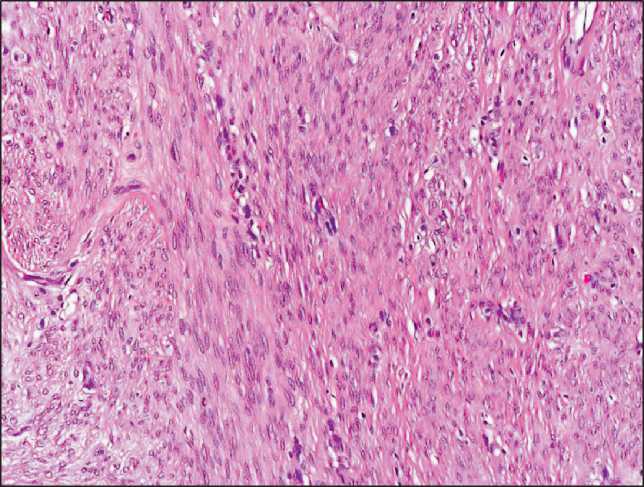
Рис. 2. Микрофото. Типичная лейомиома: разнонаправленные переплетающиеся пучки опухолевых клеток без признаков ядерной, клеточной атипии и выраженной митотической активности, окраска гематоксилином и эозином, ×20. Примечание: рисунок выполнен авторами
Fig. 2. Microphoto. Typical leiomyoma: interlacing bundles of smooth muscle cells without signs of nuclear, cellular atypia and pronounced mitotic activity, hematoxylin and eosin staining, ×20. Note: created by the authors
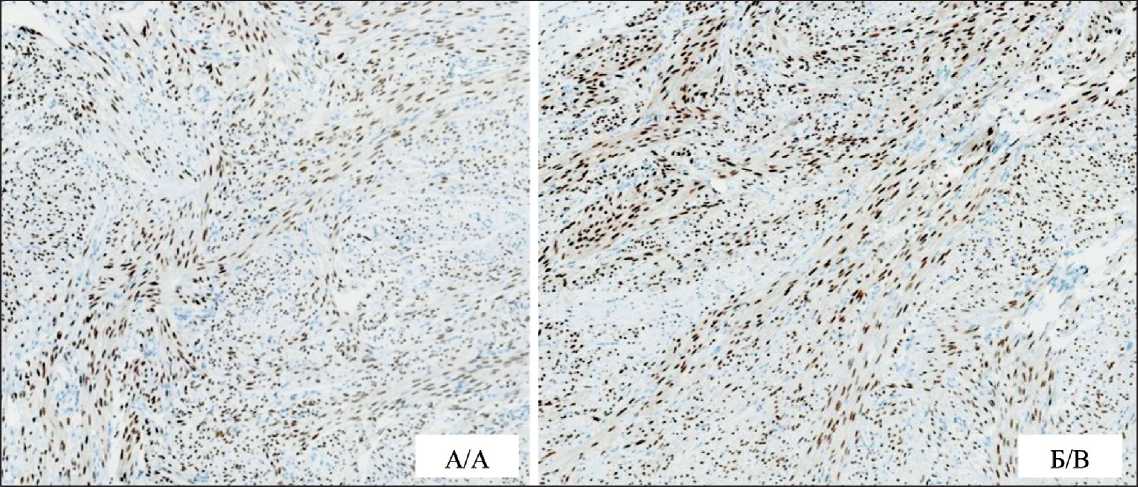
Рис. 3. Микрофото. Иммуногистохимическое исследование:
А – положительная реакция с антителами к рецепторам эстрогенов, ×20;
Б – положительная реакция с антителами к рецепторам прогестерона, ×20. Примечание: рисунок выполнен авторами Fig. 3. Microphoto. Immunohistochemistry: A – positive reaction with antibodies to estrogen receptors, ×20; B – positive reaction with antibodies to progesterone receptors, ×20. Note: created by the authors
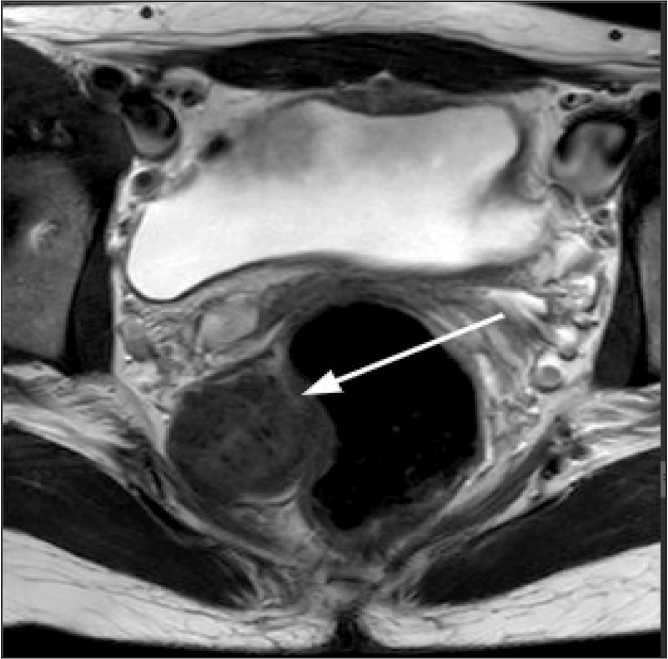
Рис. 4. МРТ органов малого таза: стрелкой указан опухолевый узел с ровными контурами, размерами 4,0×2,4 см, находящийся в параректальной клетчатке справа, деформирующий контур прямой кишки, без признаков инвазии в ее стенку. Примечание: рисунок выполнен авторами Fig. 4. MRI of the pelvic organs: the arrow indicates a tumor with smooth contours measuring 4.0×2.4 cm in the pararectal tissue to the right of the rectum, deforming the contour of the intestine, without signs of invasion into its wall. Note: created by the authors ганов малого таза с контрастным усилением: в параректальной клетчатке справа от прямой кишки, деформируя ее контур, без признаков инвазии в стенку, выявлено мягкотканое опухолевое образование с четкими ровными контурами, размерами 4,0×2,4 см, с ограничением диффузии и равномерным активным накоплением контрастного препарата (рис. 4). Также при МРТ выявлено опухолевое образование в большом сальнике, до 4 см в диаметре.
В августе 2023 г. по поводу рецидива опухолевого процесса выполнено повторное хирургическое вмешательство. При интраоперационной ревизии: в малом тазу 30 мл свободной жидкости, в пара-
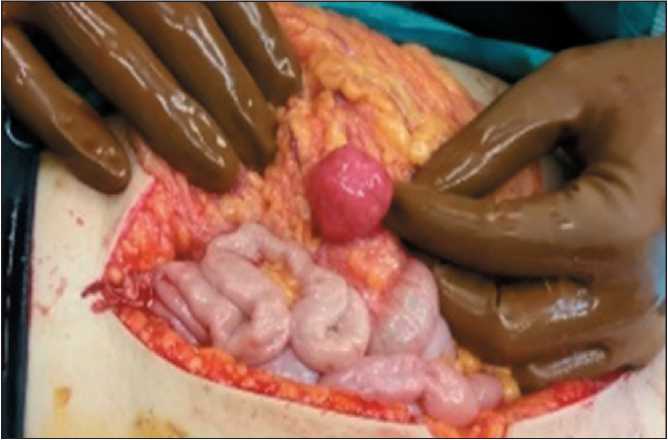
Рис. 5. Данные интраоперационной ревизии: опухолевое образование в большом сальнике, диаметром до 4 см. Примечание: рисунок выполнен авторами
Fig. 5. Intraoperative revision: tumor in the omentum up to 4 cm in diameter. Note: created by the authors ректальной клетчатке справа – миоматозный узел, размерами до 4 см, в большом сальнике опухолевый узел, также до 4 см в диаметре (рис. 5), по париетальной брюшине левого латерального канала 2 миоматозных узла, размерами до 0,5 см. Выполнены оментэктомия и удаление рецидивных опухолевых узлов. При цитологическом исследовании в асцитической жидкости клетки без признаков опухолевой атипии. По данным планового морфологического исследования удаленные опухолевые узлы соответствовали лейомиоме.
Пациентке настоятельно рекомендована гормональная терапия бусерелином. При динамическом наблюдении в январе 2024 г. по данным МРТ выявлен очередной рецидив опухоли по передней брюшной стенке живота справа, а также участок измененного контрастирования по нижнему краю послеоперационного рубца (рис. 6). Выполнена диагностическая биопсия опухолевого узла по передней брюшной стенке под ультразвуковой навигацией. По данным морфологического заключения – лейомиома. Учитывая молодой возраст манифестации заболевания и рецидивирующее течение опухолевого процесса, пациентка консультирована врачом-генетиком. Семейный анамнез отягощен миомой
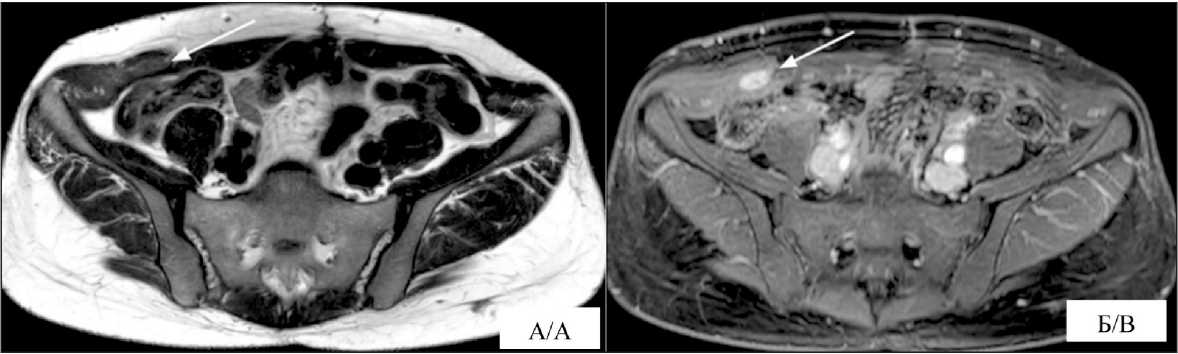
Рис. 6. МРТ органов малого таза от января 2024 г.: А – Т2-взвешенное изображение; Б – Т2-взвешенное изображение с жироподавлением (стрелкой указан опухолевый узел по передней брюшной стенке справа). Примечание: рисунок выполнен авторами Fig. 6. MRI of the pelvis (January 2024) (A – T2-weighted image; B – T2-weighted image with fat suppression): the arrow indicates a tumor on the anterior abdominal wall on the right. Note: created by the authors
матки. Рекомендовано выполнение молекулярногенетического исследования. При исследовании ДНК, выделенной из образца опухолевой ткани под контролем патоморфолога, мутаций в генах BRCA1/2, BRAF, PIK3CA, NRAS, KRAS не обнаружено. Фенотип опухоли со стабильной системой репарации неспаренных оснований ДНК (MSS-статус). Герминальных мутаций в гене CHEK2, ассоциированных с синдромом предрасположенности к раку 4 (ранее CHEK2-ассоциированный синдром Ли–Фраумени), не выявлено.
С учетом малых размеров рецидивного опухолевого узла пациентке рекомендованы строгое динамическое наблюдение, а также ранее назначенная гормональная терапия бусерелином. По данным МРТ от апреля 2024 г. опухолевые узлы в передней брюшной стенке, а также участок измененного контрастирования по нижнему краю рубца стабильны. Пациентка продолжает гормональную терапию и находится под строгим динамическим наблюдением по месту жительства, а также в НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина.
Обсуждение
Описанное клиническое наблюдение продемонстрировало, что клетки доброкачественной лейомиомы склонны к имплантационной диссе-минации, а морцелляция миоматозных узлов при консервативной миомэктомии может играть важную роль в патогенезе развития ДПЛ у пациенток репродуктивного возраста. Впервые морцеллятор для интракорпорального фрагментирования и возможности извлечения удаленных макропрепаратов через небольшие троакарные отверстия был предложен в 1977 г. K. Semm. С совершенствованием методики интракорпорального фрагментирования и широким внедрением морцелляции в хирургическую практику в литературе стали появляться работы, посвященные осложнениям и побочным эффектам данного метода [12]. В частности, в литературе описывались случаи перитонеальной диссеминации лейомиосаркомы, не диагностированной на предоперационном этапе, у пациенток, оперированных по поводу доброкачественных опухолей матки с использованием морцелляции [6]. В связи с чем, к примеру, в США, после долгих дискуссий и запретов, в настоящее время при малоинвазивных вмешательствах в гинекологической практике рекомендуется использовать технику «замкнутой» морцелляции – миому или матку перед непосредственным извлечением из полости малого таза следует помещать в специальный мешок и уже там морцеллировать [11, 16]. Согласно национальным клиническим рекомендациям (2024), при выполнении лапароскопической миомэктомии с целью исключения опухолевой диссеминации использование морцелляции также рекомендовано только в специальном контейнере [17].
В плане диагностики и лечения пациентов с ДПЛ отсутствуют установленные клинические стандарты ввиду редкости заболевания [1, 4]. Дифференциальная диагностика ДПЛ затруднена, поскольку клинические проявления заболевания напоминают карциноматоз брюшины [18]. Для определения тактики лечения пациентки в вышеописанном клиническом наблюдении выполнен развернутый дифференциально-диагностический поиск, включающий различные визуализирующие техники для оценки распространенности опухолевого процесса, а также методики извлечения опухолевого материала для его морфологической оценки (забор асцитической жидкости на цитологическое исследование, чрескожная трепан-биопсия новообразования с последующим гистологическим и иммуногистохимическим исследованием, а также диагностическая лапароскопия со срочным морфологическим исследованием).
Лечение ДПЛ, по данным авторов, проводится в основном в трех направлениях: динамический мониторинг, хирургическое вмешательство и гормональная терапия. При нераспространенных бессимптомных формах ДПЛ ряд экспертов предлагают ограничиться динамическим наблюдением с/без назначением гормональной терапии с целью снижения гиперэстрогении [6, 10, 12]. Данный подход считается особенно оправданным при наблюдаемой спонтанной регрессии ДПЛ, как и лейомиом матки, в послеродовом периоде, в период перименопаузы, а также после отмены гормональных контрацептивов и удаления гормон-продуцирующей опухоли [6]. Хирургическое лечение обоснованно при распространенных формах ДПЛ с выраженной симптоматикой. Оно должно преследовать цель обеспечения максимальной циторедукции и зависеть от желания пациентки сохранить фертильность и может включать гистерэктомию, двустороннюю аднексэктомию, оментэктомию, а также удаление всех видимых опухолевых узлов [10]. В послеоперационном периоде при гормон-позитивных опухолях для контроля заболевания, особенно при наличии остаточных опухолей, может быть рекомендована гормональная терапия. Также гормональная терапия показана пациентам с неоперабельной опухолью для повышения ее резектабельности в предоперационном периоде.
Необходимо учитывать, что больным ДПЛ рекомендуется долгосрочный мониторинг с целью ранней диагностики рецидива. В случае рециди-вирования заболевания перед выбором тактики лечения обязательно необходимо морфологическое подтверждение диагноза, в частности для исключения наличия злокачественного процесса. При рецидиве в зависимости от клинической ситуации пациенту также может быть рекомендовано динамическое наблюдение, хирургическое вмешательство и/или длительная гормональная терапия [19].
В представленном клиническом наблюдении срочное интраоперационное морфологическое исследование позволило окончательно определить объем оперативного вмешательства и достичь максимально возможной циторедукции. При последующем плановом морфологическом исследовании в опухоли выявлена экспрессия рецепторов эстрогена и прогестерона, что послужило поводом к назначению гормональной терапии совместно с тщательным динамическим наблюдением для улучшения возможности контроля заболевания. Ввиду особенностей течения ДПЛ и некомплаент-ности пациентки при последующем динамическом наблюдении был выявлен рецидив заболевания, потребовавший повторного оперативного вмешательства по причине наличия симптоматики. Последующее соблюдение гормональной терапии пациенткой позволило достичь стабилизации заболевания с учетом его местного рецидива.
Заключение
Диссеминированный перитонеальный лейо-миоматоз – редкое, сложно диагностируемое заболевание, зачастую протекающее бессимптомно. Несмотря на доброкачественные морфологические характеристики, ДПЛ отличается склонностью к рецидивированию, а также возможным риском


