Диссинхрония миокарда и ответ на сердечную ресинхронизирующую терапию
Автор: Лебедева Виктория Кимовна, Любимцева Тамара Алексеевна, Трукшина Мария Александровна, Лясникова Елена Александровна, Лебедев Дмитрий Сергеевич
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 1 т.30, 2015 года.
Бесплатный доступ
Цель исследования: дать сравнительную оценку зон максимальной внутрижелудочковой диссинхронии (ВЖД) миокарда и локализации желудочковых электродов у пациентов с различным ответом на сердечную ресинхронизирующую терапию (СРТ). Материал и методы. Ретроспективное исследование, включающее пациентов (n=40) с синусовым ритмом, полной блокадой левой ножки пучка Гиса (ПБЛНПГ), фракцией выброса левого желудочка (ФВ) 15%, относительный прирост ФВ ЛЖ ≥10%); 2-я группа, n=20 - недостаточный ответ на СРТ (отсутствие динамики размеров, объемов, ФВ ЛЖ). Для топической оценки зоны стимуляции желудочковых электродов использовался векторный анализ ЭКГ в начале и в конце периода наблюдения (разделение ЛЖ на 12 условных сегментов, ПЖ - на 3 сегмента). Межжелудочковая (МЖД) и внутрижелудочковая диссинхрония миокарда определялись при помощи эхокардиографии (ЭхоКГ) с тканевой допплерографией. Результаты. Исходно группы не различались по полу, возрасту и параметрам ЭхоКГ с тканевой допплерографией. Отсутствие исходной ВЖД наблюдалось у 7 пациентов 1-й группы и 8 пациентов 2-й группы, р=0,503; КМП ишемического генеза значимо превалировала во 2-й группе (75%, n=15, р=0,014). Дислокаций электродов за весь период наблюдения выявлено не было, имело место смещение ЛЖ электрода в пределах вены коронарного синуса в 3 случаях. Конечные размеры, объемы и ФВ ЛЖ между группами были различны (р
Сердечная ресинхронизирующая терапия, диссинхрония миокарда, анализ экг
Короткий адрес: https://sciup.org/14920012
IDR: 14920012
Myocardial dyssynchrony and response to cardiac resynchronization therapy
The aim of the study was to provide comparative analysis of the zones with maximum intraventricular myocardial dyssynchrony (IVD) and the localizations of ventricular electrodes in patients with differential responses to cardiac resynchronization therapy (CRT). Materials and Methods: Retrospective study comprised patients (n=40) who had sinus rhythm, complete left bundle branch block (LBBB), left ventricular (LV) ejection fraction (EF) 15%, relative increase of LV eF ≥10%), and group 2 (n=20) with insufficient response to CRT (the absence of dynamics in the sizes, volumes, and LV EF). For topical evaluation of the zone of stimulation with ventricular electrode, a vector analysis of ECG was performed in the beginning and the end of the follow up period (VL was divided in 12 segments, RV was divided in 3 segments). Intraventricular and interventricular dyssynchrony of the myocardium was detected by echocardiography with tissue Doppler sonography. Results: initially, the groups did not differ in regard to gender, age, and parameters of echocardiography with tissue Doppler sonography. The absence of initial IVD was observed in 7 patients of group 1 and in 8 patients of group 2, p = 0.503, cardiomyopathy of ischemic genesis significantly prevailed in group 2 (75%, n=15, р=0.014). Dislocation of the leads was not documented for the entire period of the study, displacement of LV electrodes within the vein of the coronary sinus occurred in three cases. The final sizes, volumes, and LV EF values differed between the groups (р
Текст научной статьи Диссинхрония миокарда и ответ на сердечную ресинхронизирующую терапию
На сегодняшний день СРТ вносит значительный вклад в комплексное лечение ХСН – улучшает функциональный статус и качество жизни пациентов, способствует обратному ремоделированию миокарда, а также снижает уровень смертности и госпитализаций вследствие ХСН [1, 2, 3]. СРТ направлена на снижение выраженности предсердно-желудочковой, меж- и внутрижелудочковой дис-синхронии миокарда. Однако около 30% пациентов не отвечают на данный вид терапии [4]. Рубцовые поля, отсутствие диссинхронии ЛЖ, неоптимальная позиция желудочковых электродов, а также неадекватно подобранные параметры программирования – факторы, связанные с низким ответом на СРТ [5, 6]. Итоговое расположение ЛЖ электрода зависит от анатомии вен коронарного синуса, наличия или отсутствия диафрагмальной стимуляции, а также свойств и стабильности положения самого электрода [7, 8].
При блокаде левой ножки пучка Гиса (БЛНПГ) имеет место достаточно обширная область поздней активации миокарда ЛЖ – свободная стенка, где анатомически располагаются боковая и заднебоковая вены коронарного синуса. Ответ на СРТ с позиционированием электродов в данные вены наблюдается в 90% случаев [9]. Однако зоны активации ЛЖ и, соответственно, механической диссин-хронии могут различаться, несмотря на одну и ту же ширину комплекса QRS [10]. Нередко степень ответа на СРТ сложно предсказуема из-за локальных свойств миокарда – местных функциональных блокад и рубцовых зон. Незначительные изменения позиции электродов и/или их взаимной ориентации могут серьезно влиять на ход возбуждения миокарда [11]. Влияние ПЖ стимуляции на распространение фронта возбуждения исследовано недостаточно; показано, что при стимуляции различных зон ПЖ изменяется пространственный ход волны возбуждения между ПЖ и ЛЖ электродами, что, в свою очередь, отражается на диссинхронии миокарда. Общепринятая практика имплантации ЛЖ электрода заключается в позиционировании его как можно дальше от кончика ПЖ электрода – в область латеральной или заднелатеральной стенки ЛЖ, однако выбор между целевой анатомической зоной, зоной наибольшей механической диссинхронии или зоной максимальной электрической задержки остается предметом научных споров [12].
Влияние межжелудочкового расстояния на ответ СРТ впервые было продемонстрировано в работах Heist et al., где, по данным рентгенограмм, в прямой и боковой проекциях больший отрезок между дистальными частями ПЖ и ЛЖ электродов коррелировал с более выраженным гемодинамическим ответом на ресинхронизирующую те- рапию [13]. Для стандартизации позиционирования ЛЖ электрода было предложено деление ЛЖ на сегменты [14]. В проспективном исследовании Merchant et al. было показано достоверное снижение выживаемости, менее выраженные степень обратного ремоделирования ЛЖ и снижение ФК ХСН в группе с апикальной позицией ЛЖ электрода по сравнению с группой базальной/срединной зоны имплантации за период наблюдения 15 мес. [8]. Сходные результаты были продемонстрированы в субанализе исследования MADIT-CRT [15].
Имплантация ЛЖ электрода относительно зон максимальной механической диссинхронии миокарда рассматривалась в работах Ypenburg et al. По данным тканевой допплерографии, самыми частыми зонами наибольшей внутрижелудочковой задержки являлись задняя (36%) и боковая (33%) стенки ЛЖ; стимуляция в зоне максимальной ВЖД ассоциировалась с большим эхокардиографическим ответом СРТ и лучшим прогнозом спустя 6 мес. наблюдения [16]. В исследовании Stankoviс et al. наличие ВЖД исходно, до имплантации СРТ, приводило к лучшему гемодинамическому ответу и выживаемости по сравнению с пациентами без ВЖД [17].
Цель работы: разработать предикторы ответа на СРТ путем сравнительной оценки зон максимальной внутрижелудочковой диссинхронии миокарда и локализации желудочковых электродов.
Материал и методы
Ретроспективное исследование, включающее 40 пациентов с синусовым ритмом, которым была имплантирована система СРТ по стандартным показаниям (полная БЛНПГ, комплекс QRS >120 мс, ФВ ЛЖ ≤ 35%, III и IV ФК ХСН на оптимальной медикаментозной терапии). Все пациенты были проинформированы и дали согласие на анализ данных в соответствии с целью настоящего исследования. Средний возраст составил 60,91±11,43 лет, 65% мужчин (n=26), 35% женщин (n=14), ишемический генез кардиомиопатии был выявлен в 48% случаев по результатам проведенной коронарографии и/или анамнезу документированного инфаркта миокарда. Пациенты, имеющие значимую патологию клапанного аппарата (клапанная регургитация >2-й степени, клапанный стеноз), а также легочную гипертензию выше 1-й степени не включались в исследование.
Пациенты были разделены на 2 группы: 1-я группа, n=20 – высокий ответ на СРТ. Критериями ответа на СРТ считалось уменьшение конечно-систолического объема ЛЖ (КСО) ≥15%, относительный прирост ФВ ЛЖ ≥10%, снижение ФК ХСН ≥1 [18, 19]. 2-я группа, n=20 – пациенты с недостаточным ответом на СРТ (отсутствие поло- жительной динамики размеров, объемов, ФВ ЛЖ, либо она была отрицательной). Общая характеристика пациентов представлена в таблице 1.
Имплантация системы СРТ проводилась под рентгеноскопическим контролем с применением стандартных рентгенологических проекций (прямая, левая косая, правая косая). Правопредсердный (ПП) электрод позиционировался в ушко ПП, ПЖ электрод – в область МЖП, ее базальный или срединный отделы, или верхушку ПЖ. ЛЖ электрод имплантировался в одну из ветвей коронарного синуса. Осложнений при имплантации системы СРТ в обеих группах выявлено не было. Период наблюдения составил 12,0±1,7 мес.
В рамках стандартного протокола программирования устройства СРТ проводилась регулярная оценка параметров детекции и стимуляции по схеме 0–3–6–12 мес. Атриовентрикулярная задержка (АВЗ) подбиралась на основании ЭКГ по продолжительности атриовентрикулярного интервала, форме детектированного/стимулиро-ванного зубца P, ширине бивентрикулярно-го комплекса QRS. За конечный результат АВЗ принимался интервал P-St (от начала зубца Р до спайка желудочкового стимула) в виде симметричного законченного зубца Р в выбранном отведении с наилучшей визуализацией. Параметры межжелудочковой задержки на протяжении данного периода наблюдения сохранялись на номинальных значениях. Выраженность сердечной недостаточности определялась по клиническим критериям 4 ФК ХСН (NYHA).
Электрокардиографический и эхокардиографический методы . Для анализа ЭКГ использовалась система для неинвазивных электрофизиологических исследований Astrocard (Медитек, Россия) со стандартными и усиленными однополюсными отведениями. Скорость записи 100 мм/с (максимум до 400 мм/с), амплитуда сигнала 10 мм/ 10 мВ, точность измерений 1 мс.
Трансторакальное ЭхоКГ-исследование на аппарате Vivid 7 с датчиком 2,5 MHz (GE, Vingmed Dimensions, Norway) осуществлялось по схеме 0 (до имплантации СРТ) – 6–12 мес. с оценкой параметров гемодинамики (КДД, КСД, КДО, КСО, ФВ ЛЖ) и диссинхронии миокарда в режиме тканевой допплерографии. Анализ МЖД и ВЖД проводился по методу C.M. Yu [20]. Межжелудочковую дис-синхронию оценивали по разнице во времени между началом систолических потоков в аорту и легочный ствол, измеряемых импульсно-волновым допплером, за норму МЖД принимали значение менее 40 мс. Внутрижелудочковую диссинхронию оценивали по двум показателям: индекс диссинхронии (Tsmax–Tsmin); стандартное отклонение по 12 сегментам ЛЖ (SD-12). Tsmax–Tsmin – показатель, отражающий максимальную временную разницу пиковых систолических скоростей между 12 сегментами ЛЖ, за норму принималось значение до 105 мс. Для опреде-
Таблица 1
Исходная характеристика пациентов
|
Параметры, единицы измерения |
Группа 1 |
Группа 2 |
p |
|
Возраст, годы |
59,8±10,4 |
62,1±8,2 |
0,264 |
|
Мужской пол, n (%) |
15 (75) |
18 (90) |
0,142 |
|
СРТ-Р/ СРТ-Д, n |
9/11 |
7/13 |
0,468 |
|
Ишемическая болезнь сердца, n (%) |
6 (30) |
15 (75) |
0,014 |
|
Анамнез инфаркта миокарда, n (%) |
2 (10) |
12 (60) |
0,009 |
|
Анамнез реваскуляризации миокарда, n (%) |
5 (25) |
10 (50) |
0,042 |
|
III ФК (NYHA), n (%) |
19 (95) |
19 (95) |
|
|
IV ФК (NYHA), n (%) |
1 (5) |
1 (5) |
|
|
Ширина QRS, мс |
158±21 |
154±33 |
0,307 |
|
Ширина QRS ≥ 150 мс, n (%) |
15 (75) |
17 (85) |
0,285 |
|
%) Эхокардиографические данные: |
|||
|
КДД ЛЖ, мм |
75,8±7,1 |
72,9±7,6 |
0,229 |
|
КСД ЛЖ, мм |
65,4±7,5 |
62,5±8,9 |
0,291 |
|
КДО ЛЖ, мл |
294,1±63,4 |
277,7±84,8 |
0,498 |
|
КСО ЛЖ, мл |
213,0±62,1 |
206,5±78,4 |
0,776 |
|
ФВ ЛЖ, % |
24,4±6,9 |
25,6±6,5 |
0,565 |
|
Межжелудочковая механическая задержка, мс |
49,2±23,7 |
51,5±19,8 |
0,346 |
|
Отсутствие внутрижелудочковой диссинхронии, n (%) |
7 (35) |
8 (40) |
0,503 |
|
Электроды: |
|||
|
ПЖ электрод – МЖП, базальный отдел, n (%) |
7 (35) |
5 (25) |
0,204 |
|
ПЖ электрод – МЖП срединный отдел, n (%) |
2 (10) |
2 (10) |
|
|
ПЖ электрод – верхушка ПЖ |
11 (55) |
13 (65) |
0,492 |
ления пиковых систолических скоростей использовали методику цветной тканевой допплерографии. SD-12 – статистический показатель, определяемый по значениям пиковых систолических скоростей 12 сегментов ЛЖ, значение SD-12 до 34 принималось за норму.
Совпадение зоны максимальной ВЖД с местом имплантации ЛЖ электрода оценивалось при помощи векторного анализа ЭКГ по 12 стандартным отведениям во время изолированной стимуляции ЛЖ с применением 12 условных сегментов: 3 задних, 3 заднебоковых, 3 боковых, 3 переднебоковых с разделением на базальный, срединный и апикальный уровни. Локализация ПЖ электрода определялась во время изолированной стимуляции ПЖ с применением 3 условных сегментов (базальный отдел МЖП, срединный отдел МЖП, верхушка ПЖ) [21, 22]. Анализ данных проводился дважды: после имплантации СРТ и в конце периода наблюдения.
Статистический анализ. Статистическая обработка данных осуществлялась при помощи пакета статистических программ Statistica 10 (StatSoft Inc., version 10.0.228.8, Oklahoma, USA) с использованием непараметрических математических критериев – U-критерия Манна–Уитни, двухвыборочного критерия Колмогорова–Смирнова – для независимых выборок, и критерия Вилкоксона парных сравнений, а также критерия хи-квадрат Макнемара (категориальные переменные) – для зависимых выборок. Для определения зависимости между переменными применялись критерии хи-квадрат и точный критерий Фишера. Ассоциации между несколькими переменными рассчитывалась при помощи коэффициента конкордации
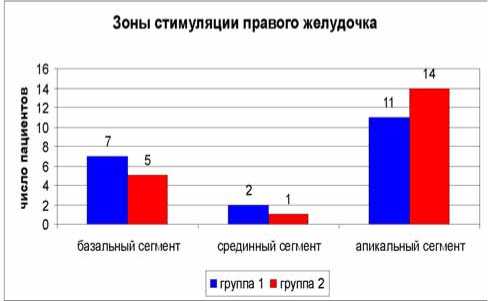
Зоны стимуляции левого желудочка
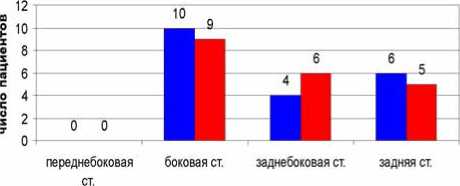
■ группа 1 ■группа 2
Рис. 1. Зоны стимуляции желудочковых электродов
Кендалла. Значения р менее 0,05 принимались статистически значимыми.
Результаты
Исходно группы не различались по полу, возрасту, параметрам ЭКГ и ЭхоКГ. Отсутствие ВЖД до имплантации СРТ было выявлено у 7 пациентов 1-й группы и 8 пациентов 2-й группы, р=0,503. У трети пациентов – 32,5% от общего количества – встречалось более 1 зоны ВЖД: в 1-й группе – у 8 человек, во 2-й – у 5 человек. Наиболее частыми зонами ВЖД являлись базальные и срединные сегменты боковой, задней и нижней стенок ЛЖ (табл. 2). Достоверных различий в локализациях и количестве исходных зон ВЖД между группами получено не было, однако в группе с высоким ответом на СРТ наблюдалась тенденция к большему преобладанию ВЖД, р=0,09.
Этиология КМП ишемического генеза значимо превалировала во 2-й группе, n=15, 75%, р=0,014. Анамнез перенесенного инфаркта миокарда (3 мес. и более до имплантации СРТ) и проведенная реваскуляризация миокарда также преобладали во 2-й группе (табл. 1). Дислокаций электродов за время наблюдения выявлено не было. По данным векторного анализа ЭКГ, имело место смещение ЛЖ электрода в пределах вены коронарного синуса в 3 случаях: 2 в 1-й группе, 1 – во 2-й. Смещение ЛЖ электрода в 1-й группе представляло собой изменение зоны стимуляции с базальных отделов на апикальные отделы боковой и заднебоковой стенок ЛЖ соответственно; во 2-й группе – с базальных отделов боковой стенки ЛЖ на ее срединные отделы. Доля бивентрикулярной стимуляции в обеих группах составляла 95% и более в течение всего периода наблюдения. Зоны стимуляции желудочковых электродов приведены в таблице 3, а также рисунке 1. Достоверных различий расположения ПЖ и ЛЖ электродов между группами получено не было.
Спустя 12 мес. наблюдения конечные размеры, объемы и ФВ ЛЖ значимо различались между группами ( ≤ 0,001); средняя ФВ ЛЖ в 1-й группе составила 44,9±5,9%, во 2-й группе – 26,9±6,4%. ФК ХСН был ниже в 1-й груп-
Таблица 2
Зоны внутрижелудочковой диссинхронии до имплантации СРТ
|
Группа |
Задняя стенка |
Передне-перегородочная |
Передняя стенка |
Нижняя стенка |
Перегородочная |
Боковая стенка |
Всего зон |
|
1 (n=13) |
5 |
0 |
0 |
6 |
1 |
11 |
23 |
|
2 (n=12) |
5 |
2 |
0 |
2 |
0 1 |
6 |
16 |
|
Всего зон |
10 |
2 |
0 |
8 |
2 |
17 |
Таблица 3
Зоны стимуляции желудочковых электродов
|
Группа |
Задняя стенка родочная |
Передне-перего- |
Передняя стенка |
Нижняя стенка |
Перегородочная |
Боковая стенка |
Всего зон |
|
1 (n=13) |
5 |
0 |
0 |
6 |
1 |
11 |
23 |
|
2 (n=12) |
5 |
2 |
0 |
2 |
1 |
6 |
16 |
|
Всего зон |
10 |
2 |
0 |
8 |
2 |
17 |
пе: n=15 против n=6 во 2-й группе с II ФК (NYHA), р=0,043 (табл. 4).
Конечные значения МЖД не различались между группами, и были в пределах нормальных значений: 36,2±16,1 мс, 39,2±11,8 мс соответственно, р=0,346. Отсутствие ВЖД спустя 12 мес. наблюдалось у 19 пациентов 1-й группы и 16 пациентов 2-й группы, р=0,493. Причем среди пациентов с исходной ВЖД (n=13 в 1-й группе, n=12 во 2-й) внутрижелудочковая диссинхрония спустя 12 мес. наблюдения была только у одного человека 1-й группы и у 4 человек 2-й группы. Таким образом, ВЖД нормализовалась в 91,7% случаев в 1-й группе и в 66,7% – во 2-й, р=0,068. Совпадение зоны максимальной ВЖД с зоной имплантации ЛЖ электрода, по данным ЭКГ, отмечено в большей степени в 1-й группе, р=0,028 (рис. 2).
Условный топический анализ взаимного расположения ПЖ и ЛЖ электродов представлен схемой межэлектродного соотношения (рис. 3). Максимальная дистанция – отрезок в виде 3 сегментов ЛЖ: а) ПЖ электрод в верхушке ПЖ, ЛЖ электрод – в базальном/срединном отделе боковой стенки ЛЖ, б) ПЖ электрод в базальном отделе МЖП, ЛЖ электрод в апикальной зоне боковой стенки ЛЖ. Минимальная дистанция характеризовалась нахож- дением электродов в соседних сегментах миокарда. Другие варианты взаимного расположения желудочковых электродов принимались за промежуточные дистанции. Сводная характеристика межэлектродных соотношений представлена в таблице 5 (передняя стенка ЛЖ не учитывалась ввиду отсутствия имплантации ЛЖ электродов в данную область).
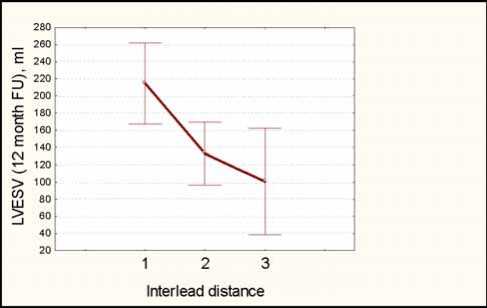
При сравнении 3 условных схем межэлектродного соотношения – минимальной (1), промежуточной (2), максимальной дистанции (3) – с динамикой размеров, объемов и ФВ ЛЖ была получена следующая зависимость: чем больше межэлектродное соотношение, тем меньше размеры, объемы ЛЖ и больше ФВ ЛЖ; коэффициент корреляции r=0,49 (ФВ/ди-станция), r=0,41 (КСО/дистанция), р<0,05, (рис. 4).
Обсуждение
В данном ретроспективном исследовании показано, что лучший ответ на СРТ связан как с совпадением зон ВЖД и места имплантации ЛЖ электрода, так и с отсутствием анамнеза ишемической болезни сердца. В исследовании C. Ypenburg et al. было отмечено, что лица с недостаточным ответом на СРТ помимо неоптимальной позиции ЛЖ электрода, расцененной как несовпадение с зоной ВЖД, имели достоверно чаще анамнез ишемической болезни сердца в сравнении с пациентами с высоким ответом на СРТ [16]. Тем не менее, однозначную связь между низким ответом на СРТ и ишемическим генезом КМП в рамках данной работы указать не представляется возможным. Нельзя исключить, что пациенты с ишемической болезнью сердца хуже отвечают на ресинхронизирующую терапию ввиду наличия обширных рубцовых зон миокарда; однако при КМП неишемического генеза наличие фиброзных полей также может влиять на степень ответа на данный вид терапии [23].
Существование исходной ВЖД может способствовать более выраженному улучшению гемодинамики в отдаленные сроки наблюдения. Подтверждение этому заключению было сделано в работе I. Stankovic et al., где ВЖД рассматривалась как независимый предиктор ответа на СРТ и была связана с большей выживаемостью пациентов в отдаленные сроки наблюдения [17]. В недавнем исследовании TARGET (Targeted Left Ventricular Lead Placement to Guide Cardiac Resynchronization Therapy
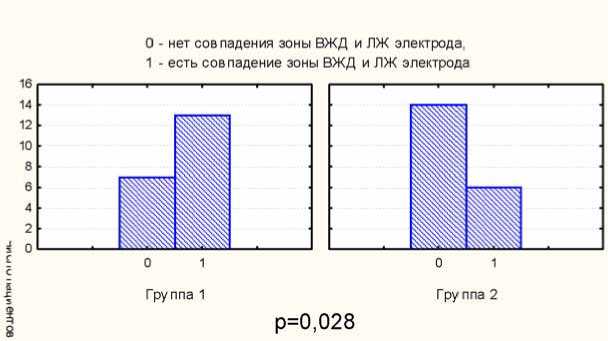
Рис. 2. Совпадение зон внутрижелудочковой диссинхронии и локализации ЛЖ электрода
Таблица 4
Характеристика пациентов спустя 12 мес. наблюдения
|
Параметры, единицы измерения |
Группа 1 |
Группа 2 |
p |
|
I ФК (NYHA), n (%) |
5 (25) |
||
|
II ФК (NYHA), n (%) |
15 (75) |
6 (30) |
0,043 |
|
III ФК (NYHA), n (%) |
14 (70) |
||
|
Ширина QRS, мс |
147±38 |
164±22 |
0,216 |
|
Эхокардиографические данные: |
|||
|
КДД ЛЖ, мм |
56,2±5,1 |
71,7±8,1 |
<0,001 |
|
КСД ЛЖ, мм |
42,9±4,4 |
60,8±8,6 |
<0,001 |
|
КДО ЛЖ, мл м |
153,4±70,4 |
292,1±84,9 |
<0,001 |
|
КСО ЛЖ, мл |
85,9±40,8 |
214,9±71,1 |
<0,001 |
|
ФВ ЛЖ, % |
44,9±5,9 |
26,9±6,4 |
<0,001 |
|
Межжелудочковая механическая задержка, мс |
36,2±16,1 |
39,2±11,8 |
0,346 |
|
Отсутствие внутрижелудочковой диссинхронии, n (%) |
19 (95) |
16 (80) |
0,493 |
|
Электроды: |
|||
|
Совпадение зоны ВЖД и ЛЖ электрода, n (%) |
12 |
6 |
0,028 |
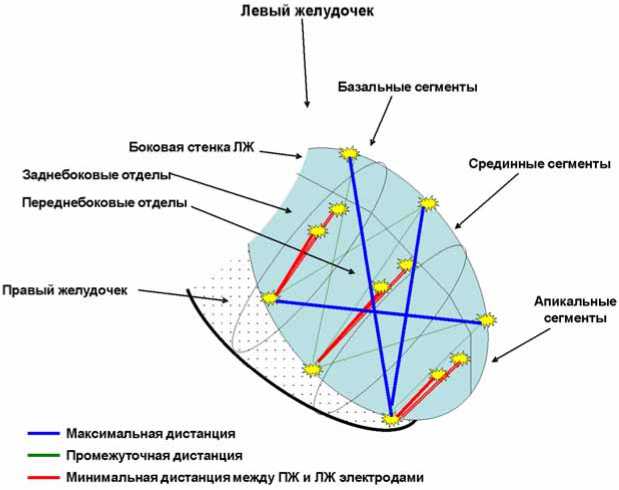
Рис. 3. Топический анализ взаимного расположения ПЖ и ЛЖ электродов
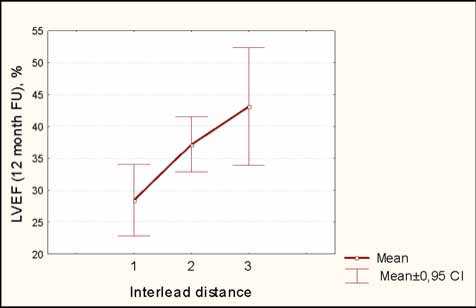
Рис. 4. Корреляция: а) между ФВ ЛЖ и условной межэлектродной дистанцией; б) между КСО ЛЖ и условной межэлектродной дистанцией
Study) было выявлено более значимое улучшение Таблица 5
клинических и гемодинамических параметров, а также снижение смертности и уровня госпитализаций вследствие ХСН у пациентов с СРТ, где имплантация ЛЖ электрода проводилась с учетом зоны максимальной ВЖД [24].
Выявленная зависимость между степенью ответа на СРТ и расчетным соотношением между желудочковыми электродами отражает патофизиологический принцип работы ресинхронизирующей системы в миокарде – необходимо достаточное расстояние между ПЖ и ЛЖ электродами для осуществления эффективной бивентрикулярной стимуляции с повышением насосной функции миокарда [25]. Расположение ПЖ электрода в верхушке ПЖ, а ЛЖ электрода в базальных или срединных отделах боковой стенки ЛЖ ассоциировалось с наилучшим гемодинамическим ответом в отдаленные сроки наблюдения [26].
В большинстве работ, посвященных данной теме, определение локализации желудочковых электродов осуществлялось прямым – рентгенологическим методом диагностики [27]. В настоящем исследовании с целью локализации зоны стимуляции применялся векторный анализ ЭКГ. При этом с учетом корректной интерпретации данных определяется зона стимуляции желудочкового электрода, а также ее изменение с течением времени. Полученные ЭКГ-данные в сравнении с зонами ВЖД представляются удобными инструментами для динамического наблюдения за пациентами с СРТ без привлечения дополнительных временных затрат.
Выводы
СРТ представляет собой сложный процесс, включающий правильный отбор пациентов, непосредственно процедуру имплантации устройства и электродов, а также послеоперационное долгосрочное наблюдение с коррекцией параметров СРТ и медикаментозной терапии. Предикторами лучшего ответа на СРТ можно считать наличие исходной ВЖД, совпадение зоны ВЖД с местом имплантации ЛЖ электрода и степень расстояния между желудочковыми электродами, что следует учитывать при
Характеристика межэлектродных условных дистанций: минимальной (1), промежуточной (2), максимальной (3)
|
Сегменты миокарда |
Базальный отдел МЖП |
Срединный отдел МЖП |
Апикальный отдел ПЖ |
|
Боковая ст. ЛЖ, базальный отдел |
2 |
2 |
3 |
|
Боковая ст. ЛЖ, срединный отдел |
2 |
2 |
3 |
|
Боковая ст. ЛЖ, апикальный отдел |
3 |
2 |
2 |
|
Заднебоковая ст. ЛЖ, базальный отдел |
1 |
2 |
2 |
|
Заднебоковая ст. ЛЖ, срединный отдел |
2 |
1 |
2 |
|
Заднебоковая ст. ЛЖ, апикальный отдел |
2 |
2 |
1 |
|
Задняя ст. ЛЖ, базальный отдела |
1 2 |
2 |
2 |
|
Задняя ст. ЛЖ, срединный отдел |
2 |
1 |
2 |
|
Задняя ст. ЛЖ, апикальный отдел |
2 |
2 |
1 |
|
Переднебоковая ст. ЛЖ, базальный отдел |
1 |
2 |
2 |
|
Переднебоковая ст. ЛЖ, срединный отдел |
2 |
1 |
2 |
|
Переднебоковая ст. ЛЖ, апикальный отдел |
2 |
2 |
1 |
имплантации. Совпадение зоны максимальной ВЖД с местом имплантации ЛЖ электрода ассоциировано со значимым улучшением гемодинамики пациентов с ресинхронизирующей терапией в отдаленные сроки наблюдения.
Список литературы Диссинхрония миокарда и ответ на сердечную ресинхронизирующую терапию
- Linde C., Leclercq C., Rex S. et al. Long-term benefits of biventricular pacing in congestive heart failure: results from the MUltisite STimulation in cardiomyopathy (MUSTIC) study//J. Am. Coll. of Cardiol. -2002. -Vol. 40. -P. 111-118.
- Chung E.S., Leon A.R., Tavazzi L. et al. Results of the Predictors of Response to CRT (PROSPECT) trial//Circulation. -2008. -Vol. 117(20). -P. 2608-2616.
- Moss A.J., Hall W.J., Cannom D.S. et al. Cardiac-resynchronization therapy for the prevention of heart-failure events//N. Engl. J. Med. -2009. -Vol. 361. -P. 1329-1338.
- Abraham W.T., Fisher W.G., Smith A.L. et al. Cardiac resynchronization in chronic heart failure//N. Engl. J. Med. -2002. -Vol. 346(24). -P. 1845-1853.
- Ypenburg C., Van De Veire N., Westenberg J.J. et al. Noninvasive imaging in cardiac resynchronization therapy. Part 2: Follow-up and optimization of settings//Pacing Clin. Electrophysiol. -2008. -Vol. 31(12). -P. 1628-1639.
- Bleeker G.B., Schalij M.J., Van der Wall E.E. et al. Postero-lateral scar tissue resulting in non-response to cardiac resynchronization therapy//J. Cardiovasc. Electrophysiol. -2006. -Vol. 17(8). -P. 899-901.
- Wilton S.B., Shibata M.A., Sondergaard R. et al. Relationship between left ventricular lead position using a simple radiographic classification scheme and long-term outcome with resynchronization therapy//J. Interv. Card. Electrophysiol. -2008. -Vol. 23(3). -P. 219-227.
- Merchant F.M., Heist E.K., McCarty D. et al. Impact of segmental left ventricle lead position on cardiac resynchronization therapy outcomes//Heart Rhythm. -2010. -Vol. 7(5). -P. 639-644.
- Fung J.W., Yu C.M., Yip G. et al. Variable left ventricular activation pattern in patients with Heart failure and left bundle branch block//Heart. -2004. -Vol. 90(1). -P. 17-19.
- Leclercq C., Faris O., Tunin R. et al. Systolic improvement and mechanical resynchronization does not require electrical synchrony in the dilated failing heart with left bundle-branch block//Circulation. -2002. -Vol. 106(14). -P. 1760-1763.
- Blendea D., Singh J.P. Lead positioning strategies to enhance response to cardiac resynchronization therapy//Heart Fail. Rev. -2011. -Vol. 16. -P. 291-303.
- Singh J.P., Heist E.K., Ruskin J.N. et al. “Dialing-in” cardiac resynchronization therapy: overcoming constraints of the coronary venous anatomy//J. Interv. Card. Electrophysiol. -2006. -Vol. 17(1). -P. 51-58.
- Heist E.K., Fan D., Mela T. et al. Radiographic left ventricular-right ventricular interlead distance predicts the acute hemodynamic response to cardiac resynchronization therapy//Am. J. Cardiol. -2005. -Vol. 96(5). -P. 685-690.
- Singh J.P., Houser S., Heist E.K. et al. The coronary venous anatomy: a segmental approach to aid cardiac resynchronization therapy//J. Am. Coll. Cardiol. -2005. -Vol. 46(1). -P. 68-74.
- Singh J.P. A sub-study of MADIT-CRT on left ventricular lead position/Heart Rhythm. Society Scientific Sessions. -2010.
- Ypenburg C., van Bommel R.J., Delgado V. et al. Optimal left ventricular lead position predicts reverse remodeling and survival after cardiac resynchronization therapy//J. Am. Coll. Cardiol. -2008. -Vol. 52(17). -P. 1402-1409.
- Stankovic I., Aarones M., Smith H.J. et al. Dynamic relationship of left-ventricular dyssynchrony and contractile reserve in patients undergoing cardiac resynchronization therapy//Eur. Heart J. -2014. -Vol. 35(1). -P. 48-55.
- Foley P.W., Leyva F., Frenneaux M.P. What is treatment success in cardiac resynchronization therapy?//Europace. -2009. -Vol. 11, Suppl. 5. -P. 58-65.
- Bleeker G.B., Bax J.J., Fung J.W. et al. Clinical versus echocardiographic parameters to assess response to cardiac resynchronization therapy//Am. J. Cardiol. -2006. -Vol. 97(2). -P. 260-263.
- Gorcsan J., Abraham T. et al. Echocardiograrhy for cardiac resynchronization therapy: recommendations for performance and reporting -a report from the American Society of Echocardiography Dyssynchrony Writing Group. ASE expert consensus statement//J. Am. Soc. Echocardiogr. -2008. -Vol. 21(3). -P. 191-213.
- Wellens H.J.J., Conover M. The ECG in emergency decision making. -2nd edition. -Saunders: Elsevier, 2006. -284 p.
- Barold S.S., Stroobandt R.X., Sinnaeve A.F. Cardiac pacemakers and resynchronization step by step: an illustrated guide. -2nd edition. -Oxford: Wiley-Blackwell, 2010. -452 p.
- Rahmouni H.W., Kirkpatrick J.N., St John Sutton M.G. Effects of cardiac resynchronization therapy on ventricular remodeling//Curr. Heart Fail. Rep. -2008. -Vol. 5(1). -P. 25-30.
- Khan F.Z., Virdee M.S., Palmer C.R. et al. Targeted left ventricular lead placement to guide cardiac resynchronization therapy: the TARGET study: a randomized, controlled trial//J. Am. Coll. Cardiol. -2012. -Vol. 59(17). -P. 1509-1518.
- Kirk J.A., Kass D.A. Electromechanical dyssynchrony and resynchronization of the failing heart//Circ. Res. -2001. -Vol. 113(6). -P. 765-776.
- Doring M., Braunschweig F., Eitel C. et al. Individually tailored left ventricular lead placement: lessons from multimodality integration between three-dimensional echocardiography and coronary sinus angiogram//Europace. -2013. -Vol. 15(5). -P. 718-727.
- Duckett S.G., Ginks M., Shetty A.K. et al. Invasive acute hemodynamic response to guide left ventricular lead implantation predicts chronic remodeling in patients undergoing cardiac resynchronization therapy//J. Am. Coll. Cardiol. -2011. -Vol. 58(11). -P. 1128-1136.


