Двадцатипятилетний опыт лечения постгипоксической энцефалопатии в кардиохирургии
Автор: Постнов В.Г., Караськов А.М., Ломиворотов В.Н., Ломиворотов В.В.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Анестезиология, реаниматология и перфузиология
Статья в выпуске: 1 т.12, 2008 года.
Бесплатный доступ
В публикации, основанной на 25-летнем опыте лечения постгипоксической энцефалопатии (ПГЭ) у кардиохирургических больных (более 1500 наблюдений), формируются четыре основных принципа интенсивной и восстановительной терапии при развитии клинической картины энцефалопатии.
Короткий адрес: https://sciup.org/142233187
IDR: 142233187
Текст научной статьи Двадцатипятилетний опыт лечения постгипоксической энцефалопатии в кардиохирургии
В.Г. Постнов, А.М. Караськов, В.Н. Ломиворотов, В.В. Ломиворотов
ФГУ «Новосибирский НИИ патологии кровообращения им. акад. Е.Н. Мешалкина Росмедтехнологий»
В публикации, основанной на 25-летнем опыте лечения постгипоксической энцефалопатии (ПГЭ) у кардиохирургических больных (более 1500 наблюдений), формируются четыре основных принципа интенсивной и восстановительной терапии при развитии клинической картины энцефалопатии.
Постгипоксическая энцефалопатия, развивающаяся впериоперационном или отсроченном (свыше 72 ч после операции) периодах у кардиохирургических больных, является самостоятельной клинической единицей или состоянием, развивающимся вследствие действия прямых или опосредованных факторов операционного периода. Таких, как длительное (свыше 2 ч) экстракорпоральное кровообращение, периоды неэффективной гемодинамики и «Stop-ИК», колебания осмолярности плазмы крови, ацидоз или алкалоз с недостаточно быстрой коррекцией. Кроме того, в отдаленном периоде свою негативную роль в формировании ПГЭ, вероятно, может играть фактор аутоиммунного конфликта, трудно достоверно верифицируемый в корреляции с клиническими проявлениями, а также нарушения тканевого дыхания, опосредованные почечной и печеночной недостаточностью, в том числе обусловленные септической или ИК - контактно опосредованной эндотоксемией [3]. Каждый из этих факторов, и прежде всего фактор неэффективной системной гемодинамики, является звеном в ишемическом каскаде.
Суммарный клинический эффект ПГЭ - в её комбинации сочетаний неврологических симптомов выпадения, недостаточности и раздражения. По рабочей классификации энцефалопатий, ПГЭ относится к рубрике II - 1.1, 1.2, 1.3, а также 11.10 [1]. До настоящего времени структурный неврологический и нейропсихологический анализ ПГЭ у кардиохирургических больных имеет далеко незавершенный характер, что в определенной мере затрудняет формирование универсальных схем и принципов проведения интенсивной и последующей восстановительной терапии при лечении ПГЭ [2, 3].
МАТЕРИАЛ И МЕТОДЫ
При оценке результатов лечения ПГЭ использованы неврологический и нейропсихоло гический методы. Клинико-неврологический метод проводился по схеме обследования, принятой в НИИ неврологии РАМН. Нейропсихологическое обследование - по схеме академика А.Р. Лурии (1969, 1973). Также в рамках лури-евской логики использовался ряд патопсихологических методик, направленных на углубленное изучение нейрокогнитивных процессов,со специальным акцентом на оценку состояния и протекания ментальных процессов в разных психических модальностях. Степень выраженности нарушений высших психических функций в процессе восстановительной терапии оценивалась по шкале балльных оценок, предложенной А.Р. Лурией. Использован 25-летний клинический опыт с анализом около 1 500 случаев развития ПГЭ и её интенсивной и восстановительной терапии в кардиохирургии взрослых и детей.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Нами сформулированы четыре принципа интенсивной и восстановительной терапии при развитии клинической картины ПГЭ. Первый принцип - протективного церебрального гипометаболизма, включающий в себя использование изолированной краниоцеребральной гипотермии, барбитуратов короткого действия, препаратов с выраженным общеанестезирующим действием, сочетающимся со снижением метаболизма и внутричерепного давления (пропофол, реланиум, седуксен, дормикум). Действие этого принципа реализуется в виде следующих алгоритмов. При развитии после эпизодов неэффективной гемодинамики или асистолий клиники ПГЭ в первые 6 часов используется комплекс стандартных мероприятий, включающий охлаждение головы пузырями со льдом, подъем головного конца кровати для обеспечения оптимального венозного оттока из полости черепа, перевод пациента на ИВЛ в режиме умеренной гипервентиляции (раСО2
30-35 мм рт. ст.), использование тиопентала натрия от 500 до 2000 мг/сутки в зависимости от массы тела внутримышечно или внутривенно, под контролем состояния системной гемодинамики. Этим достигается снижение церебрального метаболизма, а также внутричерепного давления, что в свою очередь способствует улучшению перфузии мозга.
Для этих же целей мы используем пропофол 1% р-р из расчета 2-4 мг/(кг- ч) внутривенно инфузионно, методом титрования, до появления клинических признаков поверхностной анестезии. Положительный протективный эффект мы отмечаем также при внутримышечном или внутривенном (медленно!) использовании мидазолама (дормикума) в дозе от 5 до 15 мг или 0,1-0,2 мг/(кг • ч), а также седуксена или реланиума (диазепама) от 10 до 60 мг в сутки, внутримышечно или внутривенно. Известный классический общетерапевтический принцип «покой больному органу» здесь соблюдается в полной мере. Оптимальная продолжительность использования барбитурата или бензодиазепина 48-96 ч. Возможно сочетание с фентанилом 0,005% раствором внутривенно 0,05-0,10 мг.
Второй принцип - поддержания адекватной общей и церебральной перфузионной гемодинамики, где в первую очередь осуществляется инотропная поддержка, в частности использование адреналина, допмина и поддержание нор-могликемии в виде отказа от инфузий глюкозосодержащих препаратов, т.е. поддержание эугликемии. Кроме того, важно соблюдение принципа «трипол-эйч»: гипертензия для улучшения мозгового кровотока, гиперволемия и гемодилюция для улучшения церебральной микроциркуляции.
Среди препаратов - протекторов церебрального перфузионного кровотока с комбинированным действием, т.е. сочетающих способность совместно, одномоментно и однонаправленно влиять на разные звенья патогенеза, - выделим инстенон. Его компоненты: а) этамиван -активатор лимбической системы и ретикулярной формации ствола мозга, гармонизирует корково-подкорковые процессы и вегетативную регуляцию; б) гексабендин - цереброваскулярный и коронарный вазодилататор, улучшает транспорт и утилизацию глюкозы и кислорода мозга; в) этофиллин - увеличивает минутный объем сердца, способствуя увеличению перфузионного давления в сосудах краевой зоны (пе-нумбры).
Инстенон нами используется в дозировке от 0,5 до 2,0 мл на 100,0-400,0 мл изотоничес кого раствора внутривенно капельно медленно (инфузия в течение 1,5-2,0 ч). Как правило, длительность курса от 5 до 7 суток.
Среди гемореологически активных средств при обеспечении второго принципа мы специально обращаем внимание на раннее использование пентоксифиллина (трентала) в комбинации с реополиглюкином внутривенно капельно. Дозировка для взрослого пациента составляет соответственно пентоксифиллин 2% от 5,0 до 10,0 мл и реополиглюкин от 100,0 до 200,0 мл однократно. Продолжительность курса - от пяти до десяти суток. Возможно последующее использование, особенно у лиц среднего и пожилого возраста, с антиагрегантной и реологической протекторной целью перорально клопи-догреля (плавикса) в дозе 75 мг в сутки в утренние часы. В кардиохирургии следует учитывать возможность повышенного кровотечения, что ограничивает в этот период использование пентоксифиллина.
Третий принцип - отсроченное (свыше 48 ч после операции) назначение препаратов, стимулирующих церебральный метаболизм: протекторов нейрометаболизма (актовегин, билобил, глицин, ноотропил, энцефабол, фенотропил); протекторов нейротрофики (кортексин, цереб-ролизин), комбинированных вариантов (фезам, инстенон); а также антигипоксантов (витамин Е или L-токоферол, мексидол).
Среди протекторов нейрометаболизма в остром периоде ПГЭ мы чаще используем актовегин в форме внутривенных капельных инфузий. Актовегин - гемодериват, активирующий обмен веществ в тканях мозга, в первую очередь, окислительный обмен глюкозы, повышающий утилизацию и потребление кислорода в тканях, повышая устойчивость тканей мозга к гипоксии, стимулирует трофику и регенерацию. Учитывая стимулирующий эффект актовегина, мы, следуя первому принципу, назначаем этот препарат через 48-72 ч после операции - от 400 до 800 мг внутривенно капельно на 100200 мл физиологического раствора у взрослых, половину или четверть такой дозы детям в зависимости от возраста и массы тела. Так как препарат не вызывает токсических реакций у человека даже в дозах, в 40 раз превышающих рекомендуемые среднетерапевтические дозы, использование актовегина в превышающих указанные дозы значениях мы считаем допустимым. При пилотных исследованиях мы получили достоверное (р<0,05; n=20) улучшение нейродинамических характеристик у пациентов в пробах на зрительный поиск Шульте и в свободном вербальном ассоциативном эксперименте
В подостром периоде ПГЭ (свыше 7-10 суток после операции) мы наиболее часто пользуемся энцефаболом (пиритинолом) в форме суспензии у детей и таблеток - у взрослых. Дозировка колеблется, в зависимости от возраста и веса пациента, от 100 до 600 мг в сутки. Длительность терапии от двух недель до трёх месяцев. Энцефабол - ноотропный препарат, стимулирующий повышение захвата и утилизацию глюкозы, стимулирует метаболизм нуклеиновых кислот и высвобождение ацетилхолина в синапсах, улучшает холинэргическую передачу. Улучшает кровообращение в ишемизированных участках мозга. Реализует своё действие через ингибирование лизосомальных ферментов, предотвращая этим образование свободных радикалов. Особенно эффективен при психастенических состояниях, сопровождающихся ослаблением памяти и мышления, ослаблением концентрации внимания с повышенной отвлекаемостью, утомляемостью, инактивностью, расстройствами аффектов.
Среди протекторов нейротрофики хотелось бы обратить внимание на положительный пробуждающий эффект кортексина - полипептида, получаемого путем экстракции из коры головного мозга телят или свиней. Обладает тканеспецифическим действием на кору головного мозга, оказывает церебропротективное, ноотропное, антиоксидантное и противосудорожное действие, снижает токсические эффекты нейротропных веществ, улучшает процессы обучения и памяти, стимулирует репаративные процессы в головном мозге. Мы использовали кортексин при постгипоксической энцефалопатии у оперированных взрослых и детей в официально рекомендуемых дозировках: взрослым - 10 мг/сутки внутримышечно однократно на изотоническом растворе курсом от пяти до 10 суток; детям с массой тела до 20 кг - в дозе 0,5 мг/кг, с массой тела более 20 кг - в дозе 10 мг/кг массы.
Во всех наблюдениях (n=15; 6 взрослых, 9 детей) удалось выявить наиболее заметное влияние кортексина на время восстановления речевого контакта (понимание и выполнение простых инструкций) при развитии клинической картины ПГЭ. У детей время сокращалось до 48-72 ч после операции при использовании кортексина, в то время как при отсутствии препарата время восстановления речевого контакта могло затягиваться до 5-7 суток после операции и более. Достаточно убедительный клинический эффект получен от использования мексидола. Мексидол обладает широким спектром фармакологической активности: антигипок-сант, нейропротектор, антиоксидант и антистрессор. В последние три года мы широко используем мексидол при развитии клинической картины острой постгипоксической энцефалопатии.
Наиболее отчетливый эффект нам удалось отметить среди пациентов с ПГЭ средней тяжести, для которой характерно снижение уровня бодрствования от сомноленции до сопора, при котором больного можно разбудить, добиться выполнения простых инструкций, составить короткую, в два-три предложения, беседу, после которой он истощается. В неврологическом плане здесь главным образом также страдает произвольность и спонтанность поведения, разной степени выраженности диспраксия (взора, регуляторная), а также речевая инактивность (динамическая дисфазия). Мы используем мексидол в стандартных рекомендуемых дозировках - от 5 до 10 мг/кг в сутки внутривенно капельно 40-60 капель/мин или внутримышечно по 200-400 мг 2 раза в сутки.
Наконец, четвертый принцип - это длительное, от 1 до 3 мес., использование средств, усиливающих когнитивные функции (ноотропов), воздействующих на специфические нейромедиаторные системы: холинергических (глиатилин), антиглутаматергических (акатинол-мемантин), ГАМК-ергических (фенибут), а также отдельных стабилизаторов настроения (нормотимиков и антидепрессантов).
Среди холинергических средств, используемых в подостром периоде лечения ПГЭ, хорошее впечатление сложилось от использования глиатилина. Это холиномиметик, расщепляющийся в организме на холин и глицерофосфат, обеспечивая синтез ацетилхолина и фосфатидилхо-лина нейрональных мембран. Стимулирует холинергическую передачу, улучшает пластичность нейрональных мембран. Мы используем у взрослых дозировку 800 мг утром и 400 мг вечером, а у детей от 7 до 12 лет половинную дозу для взрослых. На клиническом уровне отмечено ускорение выполнения инструкций и заданий при осмотре, ускорение «входа» в задания, связанные с движениями и действиями (динамический праксис, конструктивный праксис).
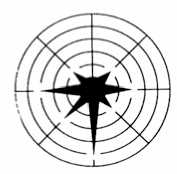
Среди ГАМК-ергических средств несомненную лидирующую роль занимает фенибут (рисунок, а). Он оказывает умеренное ноотропное и выраженное седативное, а также анксиолитическое действие. Кроме того, имеет отчет- а
психостимулирующее
ноо-мнемотропное
антиастеническое
антидискинетическое
антипаркинсоническое
противосудорожное
вегетостабилизирующее
транквилизирующее (седативное)
б
психостимулирующее (активирующее)
анксиолитическое
(транквилизирующее)
антифобическое миорелаксирующее
седативное
снотворное вегетостабилизирующее противосудорожное

психостимулирующее (усиливает тревогу и бессонницу)
тимоаналептическое вегетостабилизирующее гипотензивное
анксиолитическое антифобическое холинолитическое
седативное
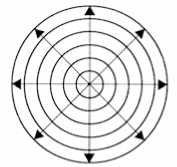
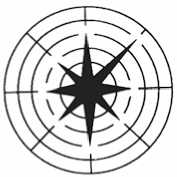
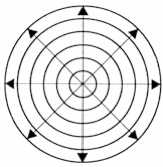
Спектры фармакологического действия: а - фенибута, б - тофизепама (грандаксина), в - мапротили-на (людиомила).
ливое вегетостабилизирующее действие. Назначается преимущественно в вечернее время. Особенно эффективен при ПГЭ, протекающей с гиперстеническими чертами, у ажитированных возбудимых пациентов. Дозирование - взрослым по 0,25-0,50 г 2-3 раза в сутки, детям до 8 лет - 0,05-0,01 г в сутки, 8-14 лет - по 0,25 2-3 раза в сутки. Отдельный аспект в терапии подострого и отдаленного периодов ПГЭ - это коррекция фона настроения. Два основных нарушения здесь - это тревожность и депрессия. Среди большого арсенала препаратов для лечения тревожности (анксиолитиков) мы выделяем тофизепам (грандаксин) рисунок, б .
Преобладающие и выгодные для лечения ПГЭ свойства грандаксина - способность устранять тревожность, не вызывая инактивнос-ти и сонливости, а также способность смягчать проявления вегето-сосудистой дистонии. Обычная дозировка от 25 до 75 мг/сутки (1-3 табл.), длительность использования 4-12 недель. Для лечения постоперационных депрессивных состояний в составе ПГЭ мы предпочитаем использовать четырехциклический антидепрессант сбалансированного действия мапротилин (людиомил) (рисунок, в ).
Мапротилин (людиомил) сочетает в себе сбалансированное действие на психику - тимо- аналептическое, психостимулирующее и седативное, вследствие чего у пациента не развивается сонливость и в то же время сохраняется длительно (до 24 ч при однократном приеме) ровный фон настроения. Мы используем людиомил по схеме, начиная с 10,0-12,5 мг в сутки, с постепенным увеличением дозы до 25-50 мг в сутки. Такая умеренная дозировка, наряду со своим тимоаналептическим эффектом, не обладает негативным влиянием на миокард, проводящую систему сердца и коронарный кровоток. Соблюдение указанных принципов позволяет снизить частоту остаточных неврологических и нейрокогнитивных нарушений у оперированных пациентов, в зависимости от выраженности энцефалопатии до 70-85% от общего числа анализируемых случаев.
ВЫВОДЫ
-
1. Использование протективного церебрального гипометаболизма в течение первых 48-72 часов после операции при развитии у пациентов клинической картины ПГЭ эффективно и целесообразно. 2. Поддержание адекватной общей и церебральной перфузионной ге
модинамики обеспечивает оптимальные для метаболизма мозга условия функционального восстановления. 3. Отсроченное свыше 48-72 ч назначение препаратов, стимулирующих церебральный метаболизм, позволяет гармонизировать во времени процессы восстановления, минуя ранний период развития энцефалопатий, которому свойственна активация накопления в мозге и спинномозговой жидкости катаболических продуктов. 4. Длительное, до трёх месяцев после операций, осложненных развитием ПГЭ, восстановительное лечение средствами, действующими на специфические нейромедиаторные системы, улучшает показатели нейрокогнитивных функций пациентов.
Список литературы Двадцатипятилетний опыт лечения постгипоксической энцефалопатии в кардиохирургии
- Классификация болезней нервной системы: пособие для врачей. М., 2002. 255 с.
- Неговский В.А., Гурвич А.М., Золотокрылина Е.С. Постреанимационная болезнь. М.: Медицина, 1987. 480 с.
- Шевченко Ю.Л., Михайленко А.А., Кузнецов А.Н., Ерофеев А.А. Кардиохирургическая агрессия и головной мозг. СПб.: Наука, 1997. 152 с.


