Двухэтапная циторедуктивная хирургия при осложнённом прогрессирующем раке тонкой кишки
Автор: Нгуен В.Т., Бромберг Б.Б., Новикова М.В., Просветов В.А., Коржук М.С., Демко А.Е., Еселевич Р.В., Суров Д.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Клинические наблюдения
Статья в выпуске: 3 т.17, 2022 года.
Бесплатный доступ
В статье представлено клиническое наблюдение больной агрессивной формой (индекс пролиферативной активности Ki67 - 70%) рака тонкой кишки (РТК). После установления диагноза в 2017 г. пациентке в онкологическом центре были выполнены радикальное (апрель 2017 г.) и циторедуктивное (февраль 2019 г.) оперативные вмешательства с послеоперационной внутрибрюшной нормотермической химиоперфузией, а также в течение 3 лет проводилась системная химиотерапия. Несмотря на комплексное лечение, в связи с неблагоприятными биологическими свойствами опухоли,констатировано прогрессирование онкологического процесса в виде перитонеальных метастазов. На фоне продолжающейся системной химиотерапии у больной развились жизнеугрожающие осложнения - нарушение тонкокишечной проходимости канцероматозного генеза и некроз рецидивных опухолевых узлов. Тяжесть клинической ситуации определила необходимость применения циторедуктивных технологий при оказании хирургической помощи больной в многопрофильном стационаре скорой помощи. В статье подробно описывается тактика комплексного лечения больной прогрессирующим осложнённым раком тонкой кишки, обсуждаются показания к хирургическому лечению, его объём и этапы, а также оцениваются непосредственные и отдалённые результаты.
Рак тонкой кишки, перитонеальный канцероматоз, перитонеальный индекс канцероматоза, некроз опухоли, кишечная непроходимость, циторедуктивная хирургия, гипертермическая внутрибрюшная химиоперфузия
Короткий адрес: https://sciup.org/140296581
IDR: 140296581 | DOI: 10.25881/20728255_2022_17_3_142
Using two-stage cytoreductive surgery in a patient with complicated progressive small intestinal cancer
The article presents a clinical observation of a patient with an aggressive (proliferative activity index Ki67 - 70%) form of small intestine cancer (SIC). After the diagnosis was established in 2017, the patient underwent radical (April 2017) and cytoreductive (February 2019) surgical interventions with postoperative intra-abdominal normothermic chemoperfusion at the oncology center, as well as systemic chemotherapy for 3 years. Despite the complex treatment, due to the unfavorable biological properties of the tumor, the progression of the oncological process in the form of peritoneal carcinomatosis was stated. Against the background of ongoing systemic chemotherapy, the patient developed life-threatening complications - a violation of the small intestine patency of carcinomatous genesis and necrosis of recurrent tumor nodes. The severity of the clinical situation determined the necessity of using cytoreductive technologies in the provision of surgical care in a multidisciplinary emergency hospital. The article describes in detail the tactics of complex treatment of a patient with advanced complicated small intestine cancer, discusses the indications for surgical treatment, its volume and stages, as well as evaluates immediate and long-term outcomes.
Текст научной статьи Двухэтапная циторедуктивная хирургия при осложнённом прогрессирующем раке тонкой кишки
Рак тонкой кишки (РТК) является редким видом опухоли, который составляет не более 4% от всех злокачественных новообразований органов желудочнокишечного тракта и встречается в 30–60 раз реже, чем рак толстой кишки [1; 2]. Средний возраст пациентов, в структуре которых несколько чаще встречаются женщины (1,3:1), составляет 60 лет. У больных, имеющих генетическую предрасположенность к возникновению РТК, заболевание манифестирует примерно на 10 лет раньше, чем в спорадических случаях. В настоящее время описано более
40 гистологических типов злокачественных новообразований тонкой кишки, среди которых наиболее часто встречаются карциноиды (37,4%), аденокарциномы (36,9%), лимфомы (17,3%) и стромальные опухоли (8,4%). Распределение гистологических вариантов РТК в различных отделах желудочно-кишечного тракта широко варьирует. Примерно 50% злокачественных опухолей возникает в двенадцатиперстной кишке, среди которых преобладает аденокарцинома, в 30% случаев поражаются тощая кишка и проксимальные отделы подвздошной кишки, где, как правило, встречаются лимфомы, тогда как карциноиды чаще локализуются в дистальных отделах подвздошной кишки. Также заслуживает внимания доказанная прямая зависимость рисков развития колоректального рака у больных РТК [2].
Диссеминированные формы РТК диагностируют у 30% больных, а в их структуре преобладают перитонеальные метастазы (25–30%), которые при РТК IV стадии чаще возникают при локализации опухоли в тощей или подвздошной кишке, чем в двенадцатиперстной кишке [3; 4]. Другие возможные варианты диссеми-нации РТК представлены метастазами в

печени (26,5%), в лимфатических узлах (11,8%), в лёгких (2,9%) и множественными метастазами (14,7%) [5; 6].
Низкая частота встречаемости РТК во многом обусловила длительное отсутствие официальных руководств по его диагностике и лечению. Только в 2018 г. французская международная группа опубликовала первые клинические рекомендации по диагностике и лечению больных данной категории, а в 2020 г. вышли в свет соответствующие рекомендации NCCN (National Comprehensive Cancer Network Guidelines) [7; 8].
Обращает на себя внимание тот факт, что отечественных клинических рекомендаций в настоящее время не существует. Таким образом, можно с уверенностью констатировать очевидную значимость данной проблемы для современной онкологии и в то же время отсутствие стандартизованных подходов к лечению больных РТК.
Необходимо подчеркнуть, что ранняя диагностика РТК крайне затруднена в связи с отсутствием специфических симптомов и эффективных скрининговых методов. По этой причине РТК, как правило, диагностируют на поздних стадиях, и зачастую манифестирует в виде жизнеугрожающих осложнений, в структуре которых преобладают различные формы нарушений кишечной проходимости и некроз опухоли.
Имеющиеся в настоящее время зарубежные рекомендации рассматривают хирургическое вмешательство в качестве основного метода лечения больных локализованными формами РТК [9]. В то же время отсутствие эффективной периоперационной системной терапии во многом определяет значительную частоту прогрессирования заболевания в виде местных рецидивов и/или отдалённых метастазов [9; 10].
Стандартным методом лечения пациентов с прогрессирующим РТК, в настоящее время, является системная химиотерапия, содержание которой, по своей сути, основано на принципах системной терапии больных колоректальным раком [11].
Данные обстоятельства обусловливают неблагоприятный прогноз у пациентов с РТК: 5-летняя выживаемость составляет не более 15–33%, а медиана общей выживаемости варьирует от 12 до 20 месяцев [12]. Необходимо отметить, что отдалённые результаты комплексного лечения больных РТК тесно коррелируют с уровнем экспрессии показателя пролиферативной активности Ki67, который является независимым прогностическим фактором выживаемости [13].
В то же время именно жизнеугрожающие осложнения, закономерно развивающиеся на фоне прогрессирования заболевания, оказывают существенное негативное влияние на выживаемость больных РТК [10; 14]. Выполняемые в подобных ситуациях симптоматические вмешательства в лучшем случае позволяют устранить осложнения опухоли тонкой кишки и не оказывают значимого влияния на динамику онкологического процесса. В связи с этим очевидный интерес представляет поиск путей одномоментного решения как общехирургических, так и онкологических задач при оказании хирургической помощи данной категории больных. Применение циторедуктивных технологий, как нам представляется, является наиболее перспективным направлением в решении этой проблемы.
Данное клиническое наблюдение демонстрирует успешную реализацию принципов циторедуктивной хирургии в лечении больной прогрессирующим РТК с исходно установленным неблагоприятным прогнозом (показатель пролиферативной активности Ki 67-70%) и развившимися на фоне комплексной терапии сочетанными жизнеугрожающими осложнениями.
Больная Л., 57 лет поступила в многопрофильный стационар 05.11.2020 г. с клинической картиной субкомпенси-рованных нарушений тонкокишечной проходимости. В 2017 г. пациентка была радикально оперирована по поводу рака тонкой кишки pT4N0M0G2. Результаты патоморфологического заключения — умереннодифференцированная аденокарцинома с инвазией всех слоёв стенки тонкой кишки, края резекции и регионарные лимфатические узлы без признаков опухолевого роста. Обращал на себя внимание высокий индекс пролиферативной активности (Ki67 — 70%). В ноябре 2018 г. отмечено прогрессирование заболевания в виде перитонеального канцероматоза, в связи с чем проводилась монохимиотерапия (капецитабин), а через 3 месяца в онкологическом центре выполнено циторедуктивное оперативное вмешательство с нормотермической послеоперационной химиоперфузией. Несмотря на комплексное лечение, в январе 2020 г. зарегистрировано повышение уровня онкологических маркеров и вновь отмечено прогрессирование заболевания в виде перитонеального канцероматоза, проводилась системная химиотерапия (оксали- платин, капецитабин). После очередного курса химиотерапии (03.11.2020 г.) у пациентки появились жалобы на интенсивные схваткообразные боли в животе, тошноту и рвоту, вздутие живота, задержку стула и газов, выраженную слабость и недомогание, в связи с чем больная была госпитализирована в многопрофильный стационар скорой помощи.
При поступлении состояние больной средней степени тяжести, сознание ясное. Предоперационная оценка общего состояния пациентки: индекс коморбид-ности Charlson — 8 баллов, ECOG 3, физический статус по шкале ASA — 4.
Объективно определялись клинические и рентгенологические признаки острых субкомпенсированных нарушений тонкокишечной проходимости, учитывая данные анамнеза, канцероматозно-го генеза (Рис. 1).
Учитывая эффективность комплексной консервативной терапии нарушений тонкокишечной проходимости, в целях дообследования больной были выполнены СКТ органов груди, живота и малого таза, МРТ малого таза с контрастированием эндоскопические исследования, а также функциональные исследования (эхокардиография, УЗИ сосудов нижних конечностей и шеи, спирометрия).
По данным СКТ с внутривенным контрастированием (от 08.11.2020 г.) определялись расширенные тонкая и толстая кишка с множественными горизонтальными уровнями жидкости. Кроме того, во всех отделах брюшной полости и в малом тазу визуализировались множественные опухолевые узлы на висцеральной брюшине между пет-
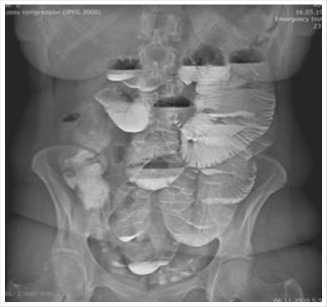
Рис. 1. Обзорная рентгенограмма живота. Рентгенологические признаки острой тонкокишечной непроходимости. В просвете пневматизированных петель тонкой кишки визуализируются множественные горизонтальные уровни жидкости (чаши Клойбера) и тонкокишечные арки.

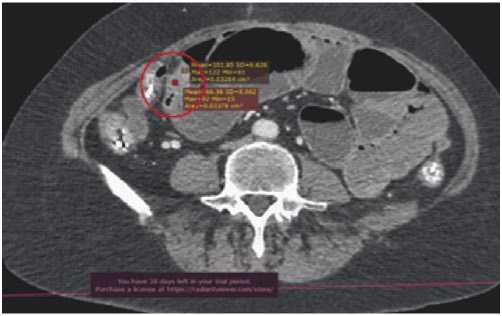
Рис. 2. Опухолевый инфильтрат в малом тазу.
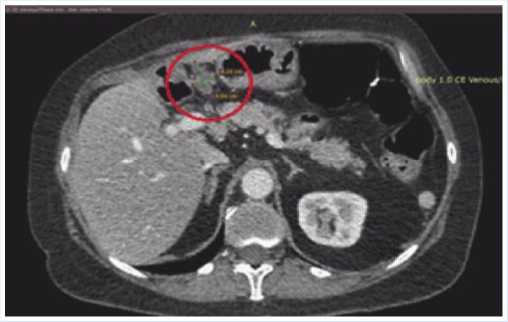
Рис. 3. Опухолевый инфильтрат в области печёночного изгиба ободочной кишки.
лями тонкой кишки, наиболее крупные из которых (24 x 27 x 30 мм, 10 x 24 x 1,0 мм и 12 x 11 x 15 мм) локализовались в передних и левых отделах таза (Рис. 2). В проекции печёночного изгиба ободочной кишки выявлено образование размерами 42,6 x 50,4 мм (Рис. 3), стенозирующее просвет кишки, с признаками некроза и инвазии в VI сегмент печени, в область культи круглой связки печени и в пилорический отдел желудка, а также в печеночно-двенадцатиперстную связку. Метастаз в лимфатическом узле, расположенном в области бифуркации аорты, размером 15 x 12 x 14 мм.
МРТ органов малого таза (от 10.11.2020 г.) выявила множественные опухолевые узлы (до 37,6 x 30,4 x 30,6 мм), расположенные в ректосигмоидном отделе толстой кишки и прорастающие её стенку с формированием опухолевого стеноза (Рис. 4, 5). Отмечалась инвазия всех слоёв стенки прямой кишки и мезоректальной клетчатки с вовлечением мезоректальной фасции и переходной складки брюшины, массивная инвазия опухолевых узлов в заднюю стенку матки и сигмовидную кишку с признаками их некроза. Достоверных данных за вовлечение мезорек-тальных ангионевральных структур выявлено не было (EMVI-).
На основании данных, полученных на предоперационном этапе, выполнена оценка индекса карциноматоза (PCI — СТ), который составил 20 баллов [15].
По данным фиброколоноскопии определялся местный рецидив в области сформированного в 2017 г. илеотранс-верзоанастомоза, а также прорастание опухоли в просвет кишки на уровне селезёночного изгиба ободочной кишки, проксимального отдела сигмовидной
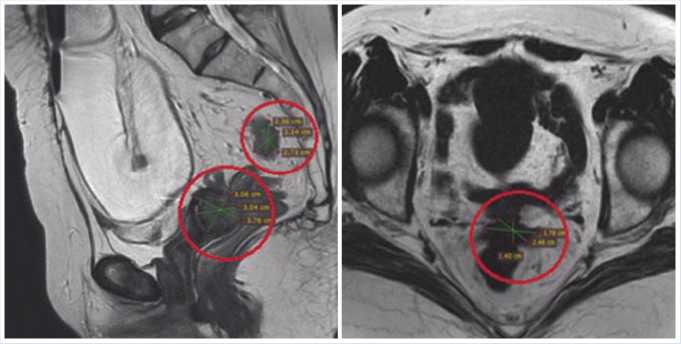
Рис. 4, 5. Опухолевый инфильтрат в малом тазу.
кишки и в прямой кишке с переходом на ректосигмоидный отдел с формированием стеноза её просвета.
Комплексная оценка преморбидного статуса больной выявила ИБС, атеросклеротический кардиосклероз, хроническую сердечную недостаточность 2 функционального класса по NYHA, хронические эрозивные эзофагит и гастрит вне обострения, а также варикозное расширение вен нижних конечностей.
Учитывая развитие у пациентки жизнеугожающих осложнений в виде декомпенсации многоуровневых нарушений кишечной проходимости и некроза рецидивных опухолевых узлов, 12.11.2020 г. больная была оперирована. В ходе ревизии были уточнены данные предоперационной лучевой диагностики — интраоперационный индекс PCI составил 22 балла [15]. Выявлены признаки некроза опухолевых узлов в малом тазу и в области ворот печени, явления многоуровнего декомпенсиро- ванного нарушения проходимости тонкой и толстой кишки (Рис. 6, 7). В связи с очевидным отсутствием перспектив применения симптоматического вмешательства в условиях сочетанных жизнеугрожающих осложнений прогрессирующей опухоли интраоперационным консилиумом, учитывая её потенциальную ре-зектабельность, было принято решение о попытке циторедуктивного вмешательства. Выполнены задняя супралева-торная эвисцерация таза, расширенная правосторонняя гемиколэктомия, резекция тонкой кишки, атипичная резекция VI сегмента печени (Рис. 8), тотальная перитонэктомия (Рис. 9–14). В результате выполненного оперативного вмешательства удалось достичь индекса полноты циторедукции ССR — 0 [15].
Учитывая тяжесть состояния больной, объём выполненного оперативного вмешательства, выраженность энтеральной недостаточности, высокие риски прогрессирования множественной органной
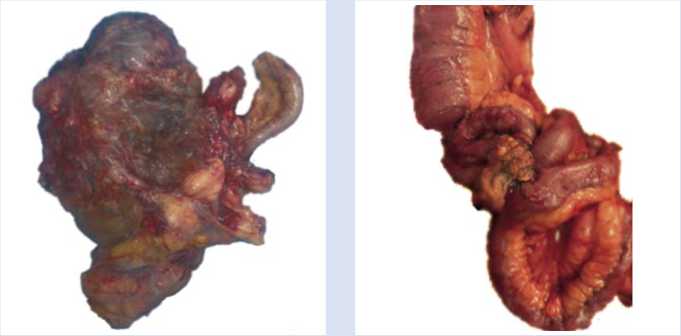
Рис. 6. Опухолевый конгломерат заднего Рис. 7. Многоуровневые нарушения тонкоки-компартмента малого таза с явлениями шечной проходимости канцероматоз- некроза. ного генеза.
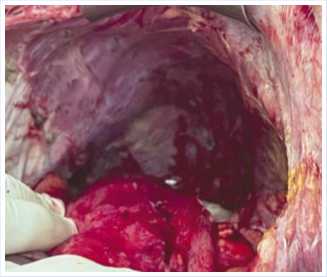
Рис.11. Вид операционной раны после пери-тонэктомии левого верхнего квадранта живота.
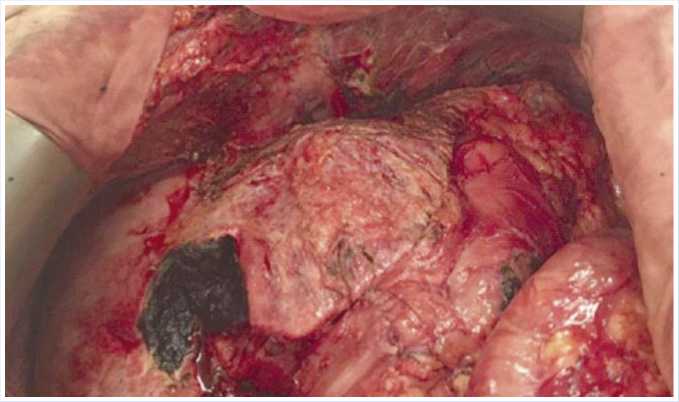
Рис. 8. Вид операционной раны после атипичной резекции IV сегмента печени, резекции круглой связки печени, глиссонэктомии и перитонэктомии верхнего левого квадранта живота.
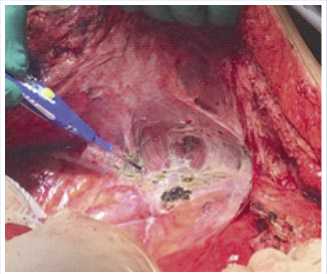
Рис. 9. Передне-боковая перитонэктомия.
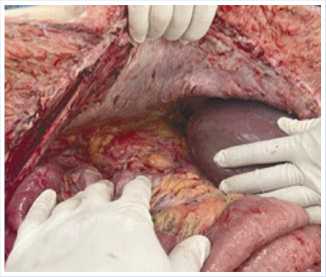
Рис. 10. Вид операционной раны после перито-нэктомии правого верхнего квадранта живота.
дисфункции в послеоперационном периоде, интраоперационным консилиумом было принято решение воздержаться от восстановления непрерывности желу- дочно-кишечного тракта. Реконструктивное вмешательство и гипертермическую внутрибрюшную химиоперфузию рекомендовано выполнить на втором
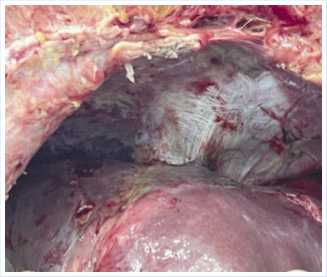
Рис. 12. Вид операционной раны после частичной глиссонэктомии и перитонэктомии сухожильного центра диафрагмы.
этапе хирургического лечения после стабилизации состояния больной через 7–10 суток. В завершении операции последовательно были сформированы илеостома и десцендостома, после контроля гемостаза брюшная полость санирована, дренирована и ушита. В результете гистологического исследования удалённых препаратов верифицированы yмеренно-дифферецированная аденокарцинома, перитонеальный канцероматоз, метастазы в печень, брыжейке тонкой кишки, малом сальнике и лимфатических узлах (pT4aN1cM1c Ro G2).
На 10 сутки послеоперационного периода на фоне многокомпонентной консервативной терапии состояние пациентки расценено как стабильное, средней степени тяжести. Клинико-лабораторные показатели в полной мере компенсированы, в связи с чем было принято решение о выполнении второго этапа хирургического лечения. 22.11.2020 г. выполнена релапаротомия, при последовательной ревизии брюшной полости видимых
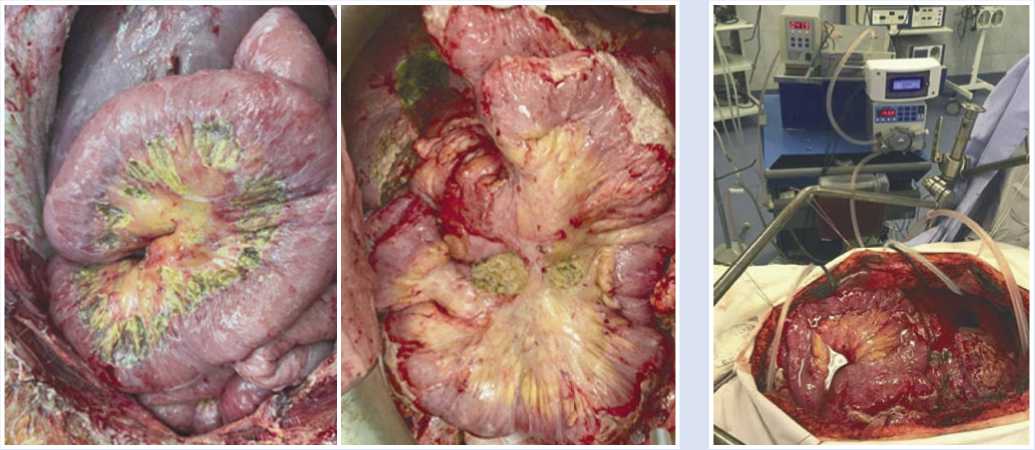
Рис. 13, 14 . Вид брыжейки тонкой кишки после мезентериальной перитонэктомии.
Рис. 15. Гипертермическая интраоперационная химиоперфузия брюшной полости, «coliseum technique».
опухолевых очагов не обнаружено, индекс PCI — 0, индекс полноты циторедукции ССR — 0 [15]
Выполнена гипертермическая интраоперационная внутрибрюшная химиоперфузия (Рис. 15) в режиме: цисплатин — 100 мг, митомицин — 40 мг; температура перфузата — 42 °С; время перфузии — 60 мин. [16]. Интраоперационных осложнений не было.
23.11.2020 г. больная переведена из отделения интенсивной терапии в хирургическое отделение. Послеоперационный период осложнился развитием острого энтерита и острого цистита, которые были успешно купированы консервативной терапией. Пациентка была выписана на 24 сутки после первой операции.
Динамическое наблюдение за состоянием больной включало оценку качества её жизни с помощью опросника SF-36 при поступлении, на 1, 3, 6, 9 и 12 месяцев после операции [17]. Результаты изучения качества жизни представлены на рис. 16.
Обращает на себя внимание, что восстановление показателей общего физиологического и психологического благополучия до исходного уровня произошло через 3 месяца после операции, а существенное улучшение данных показателей и качества жизни больной было зарегистрировано к началу 6 месяца послеоперационного периода. От предложений системной химиотерапии больная категорически отказалась. В ходе дальнейшего динамического наблюдения
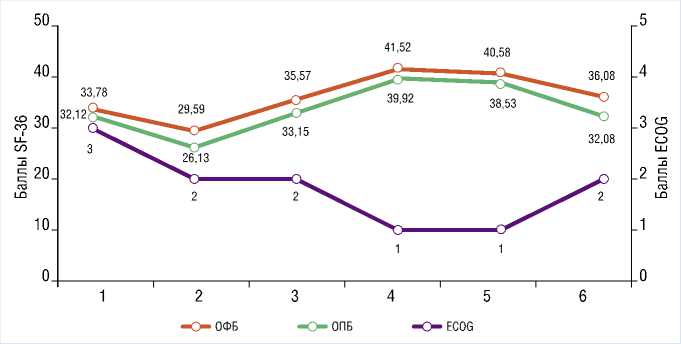
Рис.16. Динамика основных показателей качества жизни в послеоперационном периоде. ОФБ — общее физическое благополучие, ОПБ — общее психологическое благополучие, 1 — при поступлении, 2 — через 1 месяц после операции, 3 — через 3 месяца после операции, 4 — через 6 месяца после операции, 5 — через 9 месяцев после операции, 6 — через 12 месяцев после операции.
при контрольном обследовании в марте 2021 г., через 4 месяца после операции, данных за прогрессирование и рецидив РТК не получено. Однако, в июле 2021 г., через 8 месяцев после операции, были выявлены два метастаза в печени и перитонеальный канцероматоз с развитием гидронефроза вследствие вовлечения в патологический процесс левого мочеточника, в связи с чем было выполнено его стентирование. Прогрессирование РТК закономерно сопровождалось некоторым ухудшением качества жизни больной через 12 месяце после выписки из стационара.
На момент написания статьи общая выживаемость составила 59 месяцев, а безрецидивная выживаемость — 7 месяцев. При этом необходимо обратить внимание, что время до прогрессирования заболевания после циторедуктивной операции, выполняемой по поводу тяжелых сочетанных осложнений высокоагрессивного РТК, составило 8 месяцев.
Обсуждение
Прогрессирование злокачественных опухолей брюшной полости и малого таза в подавляющем большинстве случаев неизбежно сопровождается развитием

жизнеугрожающих осложнений, которые принципиальным образом изменяют динамику заболевания. Общепринятые хирургические подходы, заключающиеся в выполнении симптоматических операций, обладают ограниченным потенциалом в решении онкологических задач и не позволяют обоснованно рассчитывать на улучшение качества жизни и выживаемости пациентов.
В этой связи значительный интерес представляет возможность применения циторедуктивных технологий, которые не только позволяют ликвидировать развившиеся осложнения, но и обеспечивают достаточный уровень циторедукции, что убедительно демонстрирует данное клиническое наблюдение.
Очевидно, что одномоментное, в рамках одного оперативного вмешательства, решение изложенных задач неизбежно будет сопровождаться критическим увеличением периоперационных рисков и, как следствие, ухудшением непосредственных результатов в виде увеличения частоты послеоперационных осложнений и уровня летальности.
Обоснованным решением данной проблемы, по-видимому, является снижение хирургической агрессии за счёт применения тактики этапного хирургического лечения. При этом, основной задачей первого этапа у данной больной являлась ликвидация жизнеугрожающих осложнений, развившихся вследствие прогрессирования опухоли. В тоже время использование для её решения идеологии циторедуктивной хирургии позволило обеспечить полноценную элиминацию опухолевой ткани из организма. Выполнение на втором этапе внутрибрюшной гипертермической химиоперфузии завершило программу хирургического, в том числе циторедуктивного лечения. В конечном итоге, применение тактики этапной циторедуктивной хирургии у больной агрессивной формой прогрессирующего осложнённого РТК создало условия для пролонгации жизни и постепенного значимого улучшения основных показателей её качества.
Заключение
Таким образом, этапное применение циторедуктивных технологий в хирургическом лечении больных осложнёнными диссеминированными опухолями органов брюшной полости и малого таза позволяет не только устранить жизнеугрожающие осложнения, но и добиться полноценной циторедукции у больных с неблагоприятным преморбидным фоном и высокими периоперационными рисками.
Циторедуктивная хирургия обеспечивает улучшение показателей общего физиологического и психологического благополучия больных осложнёнными агрессивными формами РТК и потенциально способствует созданию предпосылок для проведения эффективной системной лекарственной терапии.
Согласие пациента . Пациентка добровольно подписала информированное согласие на публикацию персональной медицинской информации в обезличенной форме.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
55(9-10): 1183-1189. doi: 10.1080/0284186X. 2016.1182211.
Список литературы Двухэтапная циторедуктивная хирургия при осложнённом прогрессирующем раке тонкой кишки
- Howe JR, et al. Adenocarcinoma of the small bowel: Review of the National Cancer Data Base, 1985-1995. Cancer. 1999; 86(12): 26932706.
- DeVita VT, Lawrence TS, Rosenberg SA. DeVita, Hellman, and Rosenberg's cancer: principles & practice of oncology. 2019.
- Dabaja BS, et al. Adenocarcinoma of the small bowel: Presentation, prognostic factors, and outcome of 217 patients. Cancer. 2004; 101(3): 518-526. doi: 10.1002/cncr. 20404.
- Legué LM, et al. Trends in incidence, treatment and survival of small bowel adenocarcinomas between 1999 and 2013: a population-based study in The Netherlands. Acta Oncol. 2016; 55(9-10): 1183-1189. doi: 10.1080/0284186X. 2016.1182211.
- Frost DB, Mercado PD, Tyrell JS. Small bowel cancer: A 30-year review. Ann. Surg. Oncol. 1994; 1(4): 290-295. doi: 10.1007/BF02303567.
- Cordova-Delgado M, et al. Case Report: Molecular Features and Treatment Options for Small Bowel Adenocarcinoma. Front. Oncol. 2021; 11: 593561. doi: 10.3389/fonc.2021.593561.
- Locher C, et al. Small bowel adenocarcinoma: French intergroup clinical practice guidelines for diagnosis, treatments and follow-up (SNFGE, FFCD, GERCOR, UNICANCER, SFCD, SFED, SFRO). Dig. Liver Dis. 2018; 50(1): 15-19. doi: 10.1016/j .dld.2017.09.123.
- Benson AB, et al. Small Bowel Adenocarcin-oma, Version 1.2020, NCCN Clinical Practice Guidelines in Oncology. J. Natl. Compr. Canc. Netw. National Comprehensive Cancer Network. 2019; 17(9): 1109-1133. doi: 10.6004/ jnccn.2019.0043.
- Raghav K, Overman MJ. Small bowel adenocarcinomas — existing evidence and evolving paradigms. Nat. Rev. Clin. Oncol. 2013; 10(9): 534-544. doi: 10.1038/nrclinonc.2013.132.
- Гринев М.В. Циторедуктивная хирургия: (на модели лечения колоректального рака IV стадии). — СПБ: Гиппократ, 2003. — 92 с. [Grinev MV. Tsitoreduktivnaya khirurgiya: (na modeli lecheniya kolorektal'nogo raka IV stadii). St. Petersburg: Gippokrat; 2003. 92 p. (In Russ).]
- Aparicio T, et al. Small bowel adenocarcinoma: Epidemiology, risk factors, diagnosis and treatment. Dig. Liver Dis. 2014; 46(2): 97-104. doi: 10.1016/j.dld.2013.04.013.
- The BIG-RENAPE Group, et al. Cytoreductive Surgery Plus Hyperthermic Intraperitoneal Chemotherapy for Peritoneal Metastases From a Small Bowel Adenocarcinoma: Multi-Institutional Experience. Ann. Surg. Oncol. 2018; 25(5): 1184-1192. doi: 10.1245/s10434-018-6369-x.
- Li LT, et al. Ki67 is a promising molecular target in the diagnosis of cancer (Review). Mol. Med. Rep. 2015; 11(3): 1566-1572. doi: 10.3892/mmr.2014.2914.
- Беляев А.М. и др. Комплексное лечение кар-циноматоза брюшины при колоректальном раке // Medline. Российский Биомедицинский Журнал. — 2011. — Т.12. — С.185-201. [Belyaev AM, et al. Complex treatment of peritoneal carcinomatosis from colorectal cancer. Medlin. Rossiiskii Biomeditsinskii Zhurnal. 2011; 12: 185-201. (In Russ).]
- Беляев А.М. Циторедуктивные операции и гипертермическая внутрибрюшинная химиотерапия в комплексном лечении распространенных форм интраабдоминального рака: дис. на соиск. учен. степ. д-ра мед. наук. М., 2004. [Belyaev AM. Tsitoreduktivnye operatsii i gipertermicheskaya vnutribryushin-naya khimioterapiya v kompleksnom lechenii rasprostranennykh form intraabdominal'nogo raka. [dissertation] Moscow; 2004. (In Russ).]
- Беляева О.А. Химиоперфузионное лечение канцероматоза брюшной полости / О.А. Беляева [и др.]. — СПб., 2016. — 146 с. [Bely-aeva OA. Khimioperfuzionnoe lechenie kantse-romatoza bryushnoi polosti / O.A. Belyaeva [et al.]. St.-petersburg, 2016. 146 p. (In Russ).]
- Ионова Т.И. и др. Практические рекомендации по оценке качества жизни у онкологических больных // Злокачественные опухоли: Практические рекомендации RUSSCO^3s2. — 2017. — Т.7. — С.586-891. [Ionova TI, et al. Prakticheskie rekomendatsii po otsenke kachestva zhizni u onkologicheskikh bol'nykh. Zlokachestvennye opukholi: Prakticheskie rek-omendatsii RUSSCO^3s2. 2017.(7):586-891. (In Russ).] doi: 10.18027 / 2224-5057-2017-7-3s2-586-591.


