Двухэтапное лечение глубокой перипротезной инфекции тазобедренного сустава, осложненной забрюшинным дефектом мочевого пузыря
Автор: Иванян Сергей Тариэлович, Басов Станислав Владимирович, Грицук Николай Олегович, Пронин Владимир Александрович, Тихоненко Сергей Николаевич
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Случай из практики
Статья в выпуске: 5 т.27, 2021 года.
Бесплатный доступ
Цель. Продемонстрировать на конкретном клиническом примере необходимость мультидисциплинарного подхода к лечению пациентов с глубокой перипротезной инфекцией, подчеркнуть важность предоперационной подготовки и слаженной координированной работы смежных специалистов. Клинический случай. В статье представлен положительный пример двухэтапного лечения пациента с перипротезной инфекцией, осложненной дефектом мочевого пузыря. Пациент, 40 лет, находился на лечении в отделении гнойной хирургии ГБУ РО «Областная клиническая больница № 2» в январе 2019 г. с диагнозом при поступлении: глубокая перипротезная инфекция левого тазобедренного сустава 3 типа по Tsukayma. Тотальный эндопротез от 2008 г., миграция вертлужного компонента. При выполнении первого этапа оперативного лечения (удаление компонентов эндопротеза, санация, установка антибактериального спейсера) был выявлен забрюшинный дефект (пролежень) мочевого пузыря. В связи с техническими трудностями при удалении эндопротеза, с длительностью и травматичностью оперативного вмешательства, высокой кровопотерей, было принято решение отсрочить урологическую часть операции. По стабилизации состояния пациента была выполнена цистоскопия, чрескожная пункционная двусторонняя нефроуретеростомия под контролем ультразвукового исследования. Больной получал длительную этиотропную антибактериальную терапию. Через 6 месяцев после санации очага инфекции проведен второй этап хирургического лечения - имплантация ревизионной ортопедической конструкции с использованием индивидуального вертлужного компонента и стандартного ревизионного бедренного компонента. Результаты. Ближайшие и отдаленные результаты наблюдения - хорошие: достигнута стойкая ремиссия инфекционного процесса, пациент передвигается самостоятельно с дополнительной опорой на трость, объём движений в левом тазобедренном суставе удовлетворительный (HHS - 76,255 балла). Заключение. Лечение перипротезной инфекции должно выполняться мультидисциплинарной бригадой квалифицированных специалистов, координированность и слаженность работы которых становится ключом при лечении этой сложной патологии.
Эндопротезирование тазобедренного сустава, перипротезная инфекция, дефект мочевого пузыря, двухэтапное ревизионное эндопротезирование, 3d-технологии
Короткий адрес: https://sciup.org/142231586
IDR: 142231586 | УДК: 616.728.2-001.5-089.227.84-77-018.46-002.3:616.62-007.2 | DOI: 10.18019/1028-4427-2021-27-5-587-591
Two-stage treatment of hip periprosthetic joint infection complicated with retroperitoneal urinary bladder defect
Purpose To demonstrate the need for a multidisciplinary approach to the treatment of patients with deep periprosthetic joint infection (PJI) and emphasize the importance of preoperative preparation and well-coordinated work of related specialists using a specific clinical instance. Case report Reported is a successful experience of two-stage treatment of the patient with hip PJI complicated with urinary bladder defect. A 40-year old male patient diagnosed with left-sided deep hip PJI Tsukayama type 3 was treated at department of infection surgery, Rostov Regional Clinical Hospital No. 2 in January 2019. Total hip arthroplasty performed in 2008 was complicated by migration of acetabulum component. A retroperitoneal bladder defect (pressure ulcer) was detected during the first stage of resection arthroplasty and placement of an antibacterial spacer. Urological procedure was performed in a delayed manner due to technical difficulties of implant removal, prolonged and traumatic procedure, and high blood loss. With the patient's condition stabilized cystoscopy and bilateral ultrasound guided percutaneous nephroureterostomy were performed. Prolonged antibacterial aetiotropic treatment was administered. The second stage of surgical treatment included revision hip arthroplasty using a tailored acetabular component and a standard revision femoral component performed at 6 months of debridement. Results Short- and long-term results were good with sustained remission achieved. Patient could walk unassisted using a cane and had a satisfactory ROM in the left hip with HHS scored 76.255. Conclusion Multiple disciplinary teamwork is appropriate for treatment of deep PJI with much coherence, coordinated efforts and expertise from diverse professionals.
Текст научной статьи Двухэтапное лечение глубокой перипротезной инфекции тазобедренного сустава, осложненной забрюшинным дефектом мочевого пузыря
Число первичных артропластик тазобедренного сустава (ТБС) растет в геометрической прогрессии [1]. Аналогично возрастает количество осложнений и последующих ревизионных вмешательств. Именно перипротезная инфекция (ППИ) является третьей по частоте причиной ревизионного эндопротезирования, а по некоторым источникам – второй (27,6 %) [2]. При ревизионных вмешательствах риск возникновения инфекции колеблется от 4 до 10 %, а при ревизионных вмешательствах по поводу ППИ частота осложнений достигает 27–32,3 % [3–6]. Также необходимо отметить и высокие затраты на лечение, особенно при обширных дефектах костной ткани [7].
Двухэтапный метод является наиболее популярным вариантом лечения пациентов с ППИ. Процент успешного исхода, по данным различных авторов, при применении такой методики варьирует от 60 до 95 % [3, 8, 9].
Цель : продемонстрировать на конкретном клиническом примере необходимость мультидисциплинарного подхода к лечению пациентов с глубокой ППИ, подчеркнуть важность предоперационной подготовки и слаженной координированной работы смежных специалистов.
Клинический случай
Пациент, 40 лет, госпитализирован в отделение гнойной хирургии ГБУ РО «Областная клиническая больница № 2» в январе 2019 г. с диагнозом: глубокая перипротезная инфекция левого тазобедренного сустава 3 типа по Tsukayma. Тотальный эндопротез от 2008 г., миграция вертлужного компонента.
Из анамнеза: со слов пациента травма в 2008 г. – закрытый перелом шейки левой бедренной кости, оперирован после консолидации перелома с деформацией – тотальное эндопротезирование тазобедренного сустава (ТЭТС) слева. В 2016 г. повторная травма, после которой пациент отмечает укорочение левой нижней конечности, в 2017 г. открылся свищ с гнойным отделяемым в области послеоперационного (п/о) рубца левого тазобедренного сустава. Лечился амбулаторно. В декабре 2018 г. обратился за консультацией к травматологу отделения гнойной хирургии ГБУ РО ОКБ № 2, диагностирована ППИ, миграция компонентов эндопротеза. Пациент обследован в амбулаторном режиме. Госпитализирован в отделение гнойной хирургии и травматологии для оперативного лечения.
Локальный статус при поступлении: пациент передвигается с помощью средств дополнительной опоры, с ограниченной нагрузкой на левую нижнюю конечность. Относительное укорочение последней на 2,5 см. По боковой поверхности левого ТБС наличие п/о рубца, с признаками воспаления. В центре рубца – свищ с гнойно-серозным отделяемым. При ревизии зондом: наличие затека в проксимально-медиальном направлении. Движения в левом ТБС значительно ограничены, болезненны. При пальпации болезненность, незначительная флуктуация. Нейро-сосудистой патологии в дистальных отделах левой нижней конечности на момент осмотра не выявлено. До оперативного лечения функциональное состояние тазобедренного сустава по Harris Evaluation System of the Hip (HHS) было оценено на 29,825 балла.

Рис. 1. Пациент У., 40 лет, ППИ левого ТБС, миграция вертлужного компонента: а – рентгенограмма левого тазобедренного сустава в прямой проекции; б – фистулограмма левого тазобедренного сустава
На представленной рентгенограмме и фистуло-грамме левого ТБС от декабря 2018 г. (рис. 1): тотальный эндопротез тазобедренного сустава. Внутритазо- вая миграция вертлужного компонента. Контрастное вещество, введенное в свищевой ход, проникает в полость ТБС, окутывая головку и шейку эндопротеза.
Необходимо подчеркнуть, что амбулаторно до госпитализации пациент был консультирован различными специалистами, в том числе урологом.
16.01.2019 г. выполнено оперативное вмешательство – ревизия, удаление компонентов тотального эндопротеза левого тазобедренного сустава, секвестрне-крэктомия. Произведен пульс-лаваж и имплантация антибактериального блоковидного спейсера.
Через 20 минут после начала операции выявлено окрашивание мочи в мочеприемнике раствором бриллиантового зеленого, введенного в свищевой ход латеральной поверхности области левого ТБС. В операционную вызван уролог. Констатировано наличие забрюшинного дефекта мочевого пузыря (предположительно пролежня). Принято решение об урологическом оперативном пособии по окончании санации гнойного очага левого ТБС. Операция была продолжена. С техническими трудностями удалена ножка протеза проксимальной фиксации (отметим её стабильность) (рис. 2). Далее не удалось удалить вертлужный компонент протеза из выполненного передне-наружного доступа к тазобедренному суставу. Произведен забрюшинный доступ к вертлужной впадине. С техническими трудностями, после остеотомии частей тазовых костей, составляющих колонны вертлужной впадины, удалена чашка тотального эндопротеза. После тщательного дебридмента, остеонекрэктомии участка вертельной области бедренной кости с признаками остеомиелита и лаважа ран пульсирующей струёй установлен блоковидный антибактериальный спейсер (40 г костного цемента с 1 г гентамицина и 4 г ванкомицина) (рис. 3). Налажено низковакуумное активное дренирование ран, выполнен послойный шов раны. В связи с длительностью (5 часов) и травматичностью оперативного вмешательства, высокой кровопотерей (800 мл), было принято решение отсрочить урологическую часть операции. Пациент переведен в отделение реанимации.
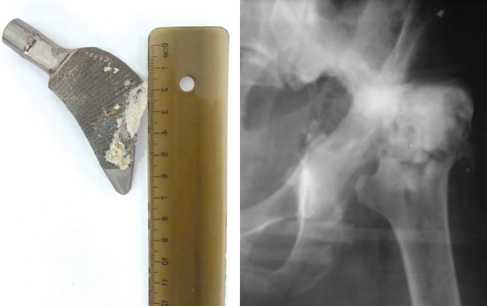
Рис. 3. Рентгенограмма левого ТБС в прямой проекции после первой операции – установки блоковидного спейсера
Рис. 2. Удаленный бедренный компонент эндопротеза бесцементной фиксации
После стабилизации состояния больного 17.01.2019 г. выполнена цистоскопия, чрескожная пункционная двусторонняя нефроуретеростомия под контролем ультразвукового исследования (рис. 4).
Мочевой катетер Фолея рекомендовано оставить на 3 недели, нефроуретеростомы на 4 недели.

Рис. 4. Урограмма: а, б – интраоперационный рентген-контроль нефроуретеростомии левой и правой почки электронно-оптическим преобразователем;
в – контрольная урограмма на следующий день после операции
Из тканевых интраоперационных биоптатов выделен MRSA. Системная антибактериальная терапия (АБТ) включала курс: ванкомицин 1г внутривенно капельно (в/в кап.) 2 раза в день (р/д) 10 дней, ципрофлоксацин 600 мг в/в кап. 2 р/д 10 дней, с переходом на пероральную супрессивную АБТ – левофлоксацин 500 мг 2 р/д, рифампицин 300 мг 2 р/д в течение 6 недель. Заживление раны первичным натяжением, пациент выписан на 17-е сутки. Иммобилизация левого тазобедренного сустава фабричным кокситным бандажом.
Заключительные диагнозы: а) основной – глубокая перипротезная инфекция левого тазобедренного сустава 3 типа по Tsukayma. Тотальный эндопротез от 2008 г., внутритазовая миграция вертлужного компонента. Хронический вторичный остеомиелит 2B (l, s) проксимального эпифиза левой бедренной кости. Дефект левой вертлужной впадины 3А типа по Paprosky, дефект проксимального отдела левой бедренной кости II типа по Mallory; б) осложнение основного – вне-брюшинный дефект стенки мочевого пузыря; в) сопутствующий – хронический вирусный гепатит "С". Хронический гайморит, стадия ремиссии.
11.02.2019 г. удален мочевой катетер, 18.02.2019 г. удалены нефростомы. Устья нефростом зажили первичным натяжением.
Через 2 недели после окончания приема антибиотиков выполнена 3-х кратная пункция левого ТБС с бак-терилогическим посевом пунктатов. Рост возбудителя не выявлен. Показатели крови в норме (L – 6,7 × 109/л; СОЭ – 29 мм/ч; СРБ – 3,2 мг/л).
После купирования инфекционного процесса пациенту запланировали второй этап реэндопротези- рования с использованием индивидуального вертлужного компонента, изготовленного с помощью аддитивных технологий. С целью выполнения данной задачи пациенту выполнена спиральная компьютерная томография (СКТ) таза с величиной среза до 0,5 мм и 3D-реконструкцией (рис. 5). Данные СКТ направлены по электронной почте инженерам-специалистам по 3D-печати. На основании имеющихся условий смоделирован вертлужный компонент с замещением дефектов, восстановлением центра вращения головки и возможностью фиксации ко всем 3 тазовым костям при помощи винтов (рис. 6).
Второй этап ревизионного эндопротезирования с использованием индивидуального вертлужного компонента и стандартной ревизионной ножки выполнен 21.06.2019 г. (рис. 7).

Рис. 5. СКТ костей таза пациента У., выполненная после первого этапа оперативного лечения и курса АБТ. 3D-реконструкция: а – косой передне-боковой вид левой вертлужной впадины; б – косой задне-боковой вид

Рис. 7. Рентгенограмма левого тазобедренного сустава в прямой проекции после второго этапа ревизионного эндопротезирования
Рис. 6. Вертлужный компонент тотального эндопротеза левого тазобедренного сустава, изготовленный с помощью 3D-печати: а, б – фото с разных ракурсов
В послеоперационном периоде проводилась антибактериальная терапия в объёме: ванкомицин 1 г в/в кап. 2 р/д 7 дней. Больной активизирован на 3 сутки после операции. Пациенту рекомендован режим передвижения с помощью средств дополнительной опоры с ограниченной нагрузкой на левую нижнюю конечность до 20 % массы тела в течение 4 недель, с последующим возрастанием – до полной нагрузки. Послеоперационная рана зажила первичным натяжением. Больной выписан на 14 сутки.
РЕЗУЛЬТАТЫ
Ближайшие и отдаленные результаты наблюдения – тазобедренном суставе – удовлетворительный: сгибание – хорошие: достигнута стойкая ремиссия инфекционного 90 0 , разгибание – 180 0 , отведение – 25 0 . Оценка функцио-процесса. Пациент передвигается самостоятельно с до- нального состояния тазобедренного сустава через год после полнительной опорой на трость. Объём движений в левом ревизионного эндопротезирования по HHS – 76,255 балла.
ОБСУЖДЕНИЕ
На сегодняшний день двухэтапную замену эндопротеза считают наиболее рациональным методом лечения ППИ [6]. Однако в доступных литературных источниках имеется ограниченное количество публикаций, посвященных возможности комплексного решения проблемы ППИ ТБС, осложненной повреждением органов малого таза.
В своей статье «Кто должен лечить перипротезную инфекцию: необходимость мультидисциплинарного подхода» Yacovelli S., Parvizi J. [10] предлагают междисциплинарный подход в качестве идеальной модели лечения ППИ. Отмечается важность лечения указанной патологии в клиниках с возможностью мультидис-циплинарной помощи под руководством хирурга-ортопеда с опытом лечения ППИ. В статье подчеркнута необходимость включения в бригаду следующих специалистов: рентгенологов, клинических фармакологов, микробиологов, эндокринологов, гематологов, нефрологов, анестезиологов, реабилитологов, физиотерапевтов. Важна помощь каждого от этапа диагностики ППИ до полной реабилитации пациента.
При обсуждении этого клинического случая необходимо отметить слабые стороны проведенных диагностических мероприятий и возникшие вопросы в ходе лечения.
Упущением была невыполненная компьютерная томография (КТ). КТ (ангиография) относится к дополнительным исследованиям, но может быть чрезвычайно важной при предоперационном планировании у пациентов с дефектами дна вертлужной впадины и миграцией вертлужного компонента эндопротеза в полость таза. Результаты таких исследований помогают избежать серьезных осложнений в ходе проведения оперативного вмешательства [11]. Выявила бы КТ внебрюшинный дефект мочевого пузыря? Урологи – соавторы данной статьи, а также литературные источники сообщают о высокой вероятности визуализации при выполнении обзорной КТ, однако ценным методом диагностики повреждения мочевого пузыря является ретроградная цистография, которая позволяет определить вид повреждения (внутри- или внебрюшинный) и, по расположению мочевых затеков, его приблизительную локализацию [12]. Как бы изменилась тактика лечения при выявлении дефекта мочевого пузыря до оперативного вмешательства? Вопрос дискутабельный. Литературных источников не найдено. Вероятнее всего, необходимо было бы первым этапом выполнить урологическое оперативное пособие и только после этого санацию очага ППИ. В доступных научных статьях указаны случаи интраоперационного повреждения мочевого пузыря. Так, в своих работах Konopitski A. et al. [13] и Grauer J.N. et al. [14] в лечение травмы мочевого пузыря, возникшей интероперационно, включают декомпрессию мочевого пузыря с помощью катетера Фолея, при необходимости ревизию и шов поврежденного участка, мониторинг гемодинамики и консультацию уролога с тщательным наблюдением. В статьях отмечается важность урологической предоперационной оценки анатомических изменений мочевого пузыря.
Стоит подчеркнуть, что при массивных дефектах вертлужной впадины выполнение второго этапа хирургического лечения может представлять очень сложную задачу, требующую тщательной предоперационной подготовки, конструктивного планирования хода операции и рационального подбора имплантатов [15]. Решить данную задачу позволяют 3D-технологии.
Представленный клинический случай демонстрирует возможный механизм лечения ППИ, осложненной забрюшинным дефектом мочевого пузыря. Особенностью является подробный анализ этапов лечения больного в многопрофильном стационаре, в том числе раскрытие допущенных ошибок и пути их решения.
ЗАКЛЮЧЕНИЕ
Проанализированные данные литературных источников, результаты клинического наблюдения свидетельствуют, что залогом успеха при лечении глубокой ППИ является тщательная предоперационная подготовка, мультидисциплинарный подход, при этом оперативное вмешательство должно выполняться ква- лифицированным, специально обученным травматологом – ортопедом в условиях лечебного учреждения, где имеется широкий профиль специалистов. Скоординированность, слаженность работы смежных специалистов становится ключом при лечении такой сложной патологии как перипротезная инфекция.
Список литературы Двухэтапное лечение глубокой перипротезной инфекции тазобедренного сустава, осложненной забрюшинным дефектом мочевого пузыря
- Травматизм, ортопедическая заболеваемость, состояние травматолого-ортопедической помощи населению России в 2018 году: сборник / Сост. Андреева Т.М., Огрызко Е.В., Попова М.М. Под ред. Н.А. Еськина. М.: ЦИТО им. Н.Н. Приорова, 2019. 166 с.
- Что изменилось в структуре ревизионного эндопротезирования тазобедренного сустава в последние годы? / И.И. Шубняков, Р.М. Тихилов, А.О. Денисов, М.А. Ахмедилов, А.Ж. Черный, З.А. Тотоев, А.А. Джавадов, А.С. Карпухин, Ю.В. Муравьёва // Травматология и ортопедия России. 2019. Т. 25, № 4. С. 9-27. DOI: 10.21823/2311-2905-2019-25-4-9-27.
- Анализ эффективности санирующих операций при параэндопротезной инфекции / Б. Лю, Р.М. Тихилов, И.И. Шубняков, С.А. Божкова, В.А. Артюх, А.О. Денисов // Травматология и ортопедия России. 2014. № 2. С. 22-29. DOI: 10.21823/2311-2905-2014-0-2-22-29.
- Прохоренко В.М., Павлов В.В. Инфекционные осложнения при эндопротезировании тазобедренного сустава. Новосибирск: Наука, 2010. 179 с.
- Successful antimicrobial therapy and implant retention for streptococcal infection of prosthetic joints / R.J. Everts, S.T. Chambers, D.R. Murdoch, A.G. Rothwell, J. McKie // ANZ. J. Surg. 2004. Vol. 74, No 4. P. 210-214. DOI: 10.1111/j.1445-2197.2004.02942.x.
- Two-stage revision total hip arthroplasty for periprosthetic infections using antibiotic-impregnated cement spacers of various types and materials / K. Uchiyama, N. Takahira, K. Fukushima, M. Moriya, T. Yamamoto, Y. Minegishi, R. Sakai, M. Itoman, M. Takaso // Scientific World Journal. 2013. P. 147248. DOI: 10.1155/2013/147248.
- Алгоритм первого этапа лечения поздней глубокой перипротезной инфекции тазобедренного сустава / В.Ю. Мурылев, Г.А. Куковенко, П.М. Елизаров, Л.Р. Иваненко, Г.Л. Сорокина, Я.А. Рукин, С.С. Алексеев, В.Г. Германов // Травматология и ортопедия России. 2018. Т. 24, № 4. С. 95-104. DOI: 10.21823/2311-2905-2018-24-4-95-104.
- Современные технологии лечения тяжелых костных дефектов в области вертлужной впадины: какие проблемы решают индивидуальные имплантаты? / А.Н. Коваленко, И.И. Шубняков, С.С. Билык, Р.М. Тихилов // Политравма. 2017. № 1. С. 72-81.
- Jaeblon T. Polymethylmethacrylate: properties and contemporary uses in orthopaedics // J. Am. Acad. Orthop. Surg. 2010. Vol. 18, No 5. P. 297-305. DOI: 10.5435/00124635-201005000-00006.
- Яковелли С., Парвизи Д. Кто должен лечить перипротезную инфекцию: необходимость мультидисциплинарного подхода // Травматология и ортопедия России. 2019. Том 25, № 4. С. 28-32. DOI: 10.21823/2311-2905-2019-25-4-28-32.
- Диагностика и лечение перипротезной инфекции тазобедренного сустава // Руководство по хирургии тазобедренного сустава : в 2 т. / В.А. Артюх, С.А. Божкова, А.Ю. Кочиш, О.В. Шнейдер, В.Л. Разоренов, И.С. Базаров. СПб: РНИИТО им. Р.Р. Вредена, 2015. Т. 2. С. 208-257.
- Давидов М.И., Гернер А.О., Никонов О.Е. Алгоритм диагностики и лечения внутрибрюшинного разрыва мочевого пузыря // Экспериментальная и клиническая урология. 2016. № 4. С. 116-121.
- Intraoperative bladder perforation during primary total hip arthroplasty / A. Konopitski, A. Boniello, P. Wang, M. Shah, A. Old, K. Gingrich // Arthroplast. Today. 2017. Vol. 4, No 1. P. 40-43. DOI: 10.1016/j.artd.2017.03.008.
- Grauer J.N., Halim A., Keggi K.J. Bladder tear during revision total hip arthroplasty // Am. J. Orthop. (Belle. Mead. N.J.). 2014. Vol. 43, No 8. P. E185-E188.
- Показания к ревизионному эндопротезированию тазобедренного сустава, планирование и техника ревизионной операции / Р.М. Тихилов, И.И. Шубняков, А.Н. Коваленко, А.О. Денисов, С.С. Билык // Руководство по хирургии тазобедренного сустава : в 2 т. СПб: РНИИТО им. Р.Р. Вредена, 2015. Т. 2. С. 258-355.


