Двухэтапное ревизионное эндопротезирование при перипротезной инфекции коленного сустава
Автор: Шпиняк С.П., Барабаш А.П., Гиркаао М.В.
Журнал: Кафедра травматологии и ортопедии @jkto
Рубрика: Клинические исследования
Статья в выпуске: 3 (19), 2016 года.
Бесплатный доступ
Эндопротез, коленный сустав, инфекция, спейсер
Короткий адрес: https://sciup.org/142211421
IDR: 142211421
Текст статьи Двухэтапное ревизионное эндопротезирование при перипротезной инфекции коленного сустава
В лечении пациентов с перипротезной инфекцией коленного сустава применяется комплексный подход, направленный на купирование воспалительного процесса, сохранение анатомо-функциональных свойств сустава и восстановление опороспособности конечности в короткие сроки. Более всего вышеуказанным условиям соответствуют операции двухэтапного ревизионного эндопротезирования с применением артикулирующих спейсеров, импрегнированных антимикробными химиопрепаратами [1; 2]. Это относительно новый метод хирургической реабилитации пациентов с рассматриваемой патологией. Первое упоминание об использовании спейсеров на основе «костного цемента», импрегнированных антибиотиками, для лечения глубокой перипротезной инфекции, датируется 1988-89 годами [3; 4], а первый промышленный артикулирующий спейсер был представлен в 1992 году – система для коленного сустава PROSTALAC® - Prosthesis with Antibiotic-Loaded Acrylic Cement (DePuy, США) [5; 6]. Отечественные разработки не имеют промышленного внедрения, их применение носит локальный характер и зависит от обеспечения лечебных учреждений, квалификации и, часто, энтузиазма оперирующих хирургов. [7; 8; 9]. Несмотря на указанные недостатки, выполнение данного вида оперативных вмешательств отечественными специалистами получает все большее «центробежное» распространение, как территориально, так и по уровню лечебных учреждений. Наблюдается «выход» первого этапа метода (имплантация спейсера) из крупных специализированных федеральных центров в больницы областного и городского звена, что окажет значительное влияние на качество и, что наиболее важно, сроки оказания медицинской помощи пациентам с пе-рипротезной инфекцией.
Цель исследования
Проанализировать результаты двухэтапного хирургического лечения пациентов с инфекционными осложнениями тотального эндопротезирования коленного сустава, проходивших лечение в отделении гнойной хирургии ФГБУ «СарНИИТО».
Материалы и методы
С 2011 по 2016 гг под наблюдением находился 131 пациент с перипротезной инфекцией коленного сустава (40 мужчин и 91 женщина – 30,5%/69,5%), которым проводилось или проводится лечение по методике двухэтапного реТЭП с длинным межоперационным интервалом. Средний возраст 62±10 лет. Сроки наблюдения – от 2 месяцев до 5 лет.
По срокам возникновения осложнений пациенты распределились следующим образом: до 3 месяцев – 40 больных (30,5%); 3-12 месяцев - 41 пациент (31,3%); позже 12 месяцев – 50 человек (38,2%). Важное значение в группе пациентов с осложнениями, возникшими в раннем послеоперационном периоде (n=40), имел срок обращения за специализированной медицинской помощью. Подавляющее большинство - 36 человек (90%), поступили в отделение гнойной хирургии СарНИИТО позже 3 месяцев после развития осложнений (средний срок -7 месяцев).
У всех больных наблюдалась глубокая перипротезная инфекция. Свищевая форма выявлена в 114 случаях (87%). Неста- бильность компонентов при первичном обращении диагностирована у 112 больных (85,5%).
Диагностический алгоритм при первичном обращении пациентов включал в себя определение характеристик инфекционного процесса с обязательным использованием клинических, лабораторных и инструментальных методов. У всех пациентов были выявлены изменения крови (лейкоцитарный сдвиг влево, увеличение скорости оседания эритроцитов и уровня С-реактивного белка), характерные для воспалительного процесса.
Выполнялся микробиологический анализ отделяемого свища, раны или, при их отсутствии, пунктата из сустава с идентификацией возбудителя и определением его чувствительности к антимикробным химиопрепаратам. В полученных образцах превалировали (68%) метициллин-резистентные штаммы золотистого стафилококка (MRSA).
Лучевая диагностика включала рентгенографию в стандартных проекциях и, при необходимости, проведение нагрузочных проб. Пациентам со свищевым ходом выполнялось зондирование фистулы. В случае возникновения технических трудностей (извитой свищевой ход) с целью выявления распространенности гнойных затеков и связи их с компонентами имплантата проводили тугое заполнение свища контрастным веществом (Омнипак, Урографин).
Интраоперационно всем больным осуществляли взятие материала непосредственно из сустава для повторного микробиологического и гистологического исследований.
При госпитализации больных для второго этапа оперативного лечения диагностические мероприятия включали клинические (осмотр), лабораторные (оперделение лейкоцитоза, скорости оседания эритроцитов, С-реактивного белка, микробиологическое и цитологическое исследования пунктата коленного сустава) и лучевые методы исследования.
Результаты и их обсуждение
Выполнение первого этапа. Всем пациентам (n=131) выполнено реэндопротезирование спейсерами различных модификаций (артикулирующие, неартикулирющие, металл-цементные, цемент-цементные) с использованием цемента с антимикробным химиопрепаратом (гентамицин, ванкомицин).
Устанавливали спейсеры различных модификаций:
-
1) по составу – цемент-цементные, металл-цементые;
-
2) по функциональной нагрузке – артикулирующие.
Во время оперативных вмешательств на коленном суставе использовали тибиальный компонент артикулирующего спей-сера коленного сустава и форму для его интраоперационного изготовления (патент РФ на полезную модель RU 127619 U1 A61F2/38 от 10.05.13).
В случае наличия у пациента обширных дефектов суставных поверхностей костей, составляющих коленный сустав и невозможности имплантации металлического бедренного компонента, выполняли установку цемент-цементного спейсера.
Особенностями ведения пациентов в послеоперационном периоде являлись:
установка отточного дренажа без возможности последующего орошения полости сустава антисептиками;
сроки удаления дренажа определяли индивидуально в зависимости от количества отделяемого и составляли в среднем 3-6 суток;
при выявлении других возбудителей внутривенную и пероральную терапию проводили в соответствии с результатами антибиотикограммы;
разработку движений в суставе разрешали осуществлять после удаления дренажа;
иммобилизация сустава тутором проводилась больным с цемент-цементными спейсерами только во время осуществления нагрузки на конечность для обеспечения стабильности сустава;
индивидуально (в зависимости от состояния костей и связочного аппарата сустава) разрешалось дозированное увеличение нагрузки с доведением до полной через 3 месяца после операции.
Рецидив воспаления был отмечен у 14 пациентов (10,7%), четверым из них выполнено артродезирование сустава аппаратами внешней фиксации. В десяти случаях повторно реимплан-тирован спейсер. Воспаление купировано у шести больных. Один пациент погиб в результате несчастного случая. Трое пациентов от предложенного артродезирования отказались, связь с ними потеряна.
Выполнение второго этапа. Не ранее чем через 3 месяца после установки спейсера 64 больным (48,8%) проведена имплантация ревизионного эндопротеза. За весь период наблюдения – от 4 месяцев до 4,5 лет, рецидив воспаления у этих пациентов выявлен в 4 случаях (6,2%), после чего им выполнено артроде-зирование коленного сустава.
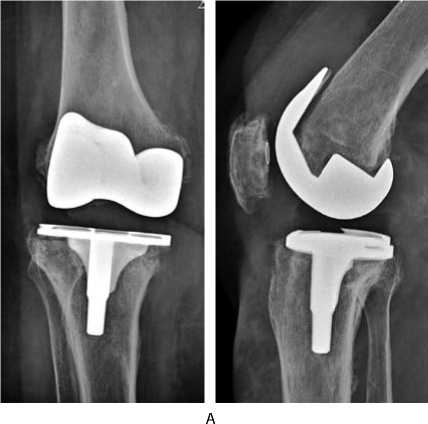
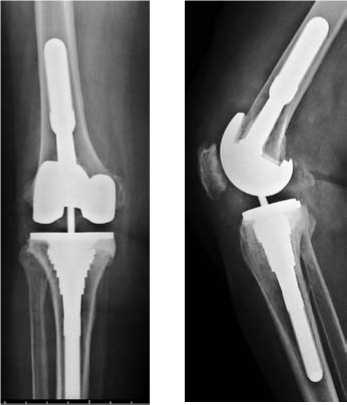
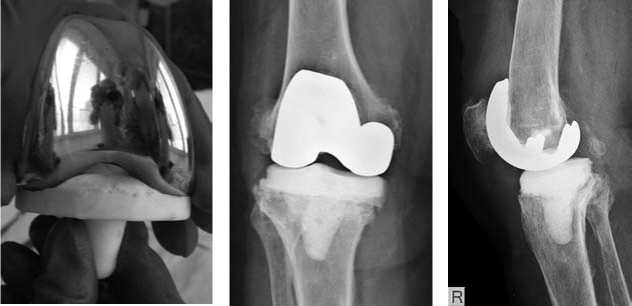
Клинический пример (рис.1)
Пациентка Г., 76 лет, лечилась в отделении гнойной хирургии СарНИИТО в 2014-2015 гг. с диагнозом: Т. 84.5. Инфекция и воспалительная реакция, обусловленная эндопротезированием. Глубокая перипротезная инфекция правого коленного сустава (свищевая форма). Состояние после ТЭП правого коленного сустава (2009 год). Нестабильность эндопротеза.
При поступлении предъявляла жалобы на боль, отек, гиперемию свищ с гнойным отделяемым в области правого коленного сустава, повышение температуры до 37,5 С°, деформацию и нарушение опороспособности правой нижней конечности.
В июне 2013 года по поводу первичного гонартроза III степени выполнено ТЭП правого коленного сустава. Через 15 месяцев возникла боль в области сустава, отмечена деформация конечности. За медицинской помощью не обращалась. В сентябре 2014 года возникли признаки перипротезной инфекции.
Б
В
Рис.1 Клинический пример (больная Г.): А) рентгенограммы через 1,5 года после ТЭП коленного сустава; Б) установка спейсера и рентгенограммы коленного сустава; В) рентгенограмма после реТЭП через 6 месяцев
При осмотре: ходит с опорой на костыли без опоры на правую нижнюю конечность. Движения в правом коленном суставе ограничены болевым синдромом сгибание/разгибание - 60º/0º/5º. Ткани правого коленного сустава отечны +2,5 см, гиперемированы, определяется послеоперационный рубец по передней поверхности сустава 15 см, в нижней трети которого свищ 5х5 мм с обильным гнойным отделяемым. Пальпация коленного сустава болезненная. Иннервация и кровообращение в дистальных отделах конечности не нарушены. Рентгенологически диагностирована нестабильность компонентов эндопротеза. При микробиологическом исследовании выявлен метициллин-резистентный золотистый стафилококк.
В сентябре 2014 года выполнено удаление эндопротеза правого коленного сустава, реТЭП артикулирующим металл-цементным спейсером. Пациентке разрешена дозированная нагрузка на конечность, разработка движений в суставе. Воспаление купировано. В марте 2015 года выполнено реэндопротезирование правого коленного сустава. Опороспособность конечности восстановлена. При осмотре через 9 месяцев: пациентка передвигается самостоятельно без дополнительной опоры. Рецидива воспаления за весь период наблюдения не было.
Заключение
Имплантация антимикробного спейсера позволила эффективно купировать воспаление в 89,3 % случаев, а также сохранить анатомо-функциональные взаимоотношения в оперированном суставе (во многих случаях обеспечить полную опороспособность конечности), а затем осуществить второй этап реэндопротезирования (n=64).
Использование системного подхода к обследованию пациентов с перипротезной инфекцией, планированию оперативного вмешательства и ведению больных в послеоперационном периоде в стационаре, а также обеспечение преемственности на амбулаторном этапе, обеспечило 93,8 % удовлетворительных результатов лечения при использовании рассматриваемой методики.
В случае рецидива инфекции возможно выполнение повторной установки спейсера или артродезирования сустава. При выборе объема вмешательства необходимо учитывать возраст и состоянии здоровья пациента, сохранность анатомических структур сустава, характеристику инфекционного процесса. Предпочтение следует отдавать реимплантации.
Список литературы Двухэтапное ревизионное эндопротезирование при перипротезной инфекции коленного сустава
- Прохоренко В.М., Павлов В.В. Инфекционные осложнения при эндопротезировании тазобедренного сустава. Новосибирск: Наука, 2010. 179 с.
- Куропаткин Г.В., Ахтямов И.Ф. Костный цемент в травматологии и ортопедии: 2-е изд. доп. и перераб. Казань: Издательство «ТаГраф», 2014. 188 с.
- Wilde A.H., Ruth J.T. Two-stage reimplantation in infected total knee arthroplasty//Clin. Orthop. Relat. Res. 1988. Vol. (236). Р.23-35.
- Booth R.E.Jr., Lotke P.A. The results of spacer block technique in revision of infected total knee arthroplasty//Clin. Orthop. Relat. Res. 1989. Vol. 248. Р.57-60.
- Duncan C.P., Beauchamp C.P., Masri B. The antibiotic loaded joint replacement system: A novel approach to the management of the infected knee replacement. J. Bone Joint Surg. (Br). (suppl III). 1992. Vol. 74. Р.296.
- The PROSTALAC functional spacer in two-stage revision for infected knee replacements/Haddad F.S., Masri B.A., Campbell D. //J. Bone Joint Surg. (Br). 2000. Vol.82. Р.807-812.
- Резник Л.Б., Дзюба Г.Г., Зинкин И.А. Артикулирующий спейсер коленного сустава/Патент РФ №88532. 2009. Бюл. №32.
- Тибиальный компонент артикулирующего спейсера коленного сустава и форма для его интраоперационного изготовления/Гиркало М.В., Норкин И.А., Клочков М.А., Шпиняк С.П., Помошников С.Н.//Патент РФ №127619. 2013. Бюл. №13.
- Спейсер коленного сустава/Ахтямов И.Ф., Кудрявцев А.И., Гильмутдинов И.Ш., Загидуллин М.В.//Патент РФ №136702. 2014. Бюл. №2.


