Двусторонняя полисегментарная пневмония, вызванная SARS-COV-2, у реципиента трансплантированной печени
Автор: Ищенко Роман Викторович, Головинский Сергей Владимирович, Ахмедьянов Артур Робертович, Восканян Сергей Эдуардович, Колышев Илья Юрьевич
Журнал: Клиническая практика @clinpractice
Рубрика: Описание клинических случаев
Статья в выпуске: 2 т.11, 2020 года.
Бесплатный доступ
Обоснование. В декабре 2019 года человечество встретилось с ранее неизвестным инфекционным заболеванием (COVID-19), вызванным новым коронавирусом - SARS-CoV-2, клиническая картина которого проявляется полисегментарной пневмонией и часто осложняется острым респираторным дистресс-синдромом. Важная роль в лечении COVID-19 принадлежит препаратам противовоспалительного и иммуносупрессивного действия. В этой связи особый интерес представляют случаи заболевания пациентов, находящихся на длительной иммуносупрессивной терапии, например реципиентов трансплантированных органов. Приводим собственное клиническое наблюдение COVID-19 у пациента-реципиента печени, которое, по-видимому, является первым в Российской Федерации. Описание клинического случая. Мужчина, 54 года; десять лет назад в ФМБЦ им. А.И. Бурназяна получил родственную трансплантацию правой доли печени по поводу гепатоцеллюлярной карциномы, T2N0M0; цирроза печени в исходе вирусного гепатита С. На момент госпитализации постоянно получал иммуносупрессивную монотерапию препаратом эверолимус. В инфекционный стационар переведен после обнаружения РНК SARS-CoV-2. При поступлении состояние удовлетворительное, признаков дыхательной недостаточности не выявлено. В дальнейшем наблюдалась легкая форма течения COVID-19 без признаков острой воспалительной реакции с нормальными значениями С-реактивного белка и незначительным повышением ферритина. Спустя 7 дней после проведенного лечения пациент выписан под амбулаторное наблюдение. Заключение. Данное клиническое наблюдение представляет интерес не только достигнутым успехом в лечении COVID-19 у иммунокомпрометированного пациента-реципиента трансплантированной печени, но также дебютом заболевания с транзиторного увеличения печеночных аминотрансфераз, что можно отнести к гастроинтестинальным проявлениям COVID-19.
Реципиенты трансплантированных органов, пересадка печени
Короткий адрес: https://sciup.org/143172649
IDR: 143172649 | DOI: 10.17816/clinpract35121
Bilateral polysegmentary pneumonia caused by SARS-COV-2 in a transplanted liver recipient
Background. In December 2019, the humanity met a previously unknown infectious disease (COVID-19) caused by a new coronavirus called SARS-CoV-2. An important role in the treatment of COVID-19 belongs to anti-inflammatory and immunosuppressive drugs. In this regard, the cases of the disease in patients undergoing long-term immunosuppressive therapy, for example, organ transplant recipients, are of particular interest. We present our clinical observation of COVID-19 in a liver recipient patient, which, apparently, is the first in the Russian Federation. Clinical case description A 54-year-old man, 10 years ago at the A.I. Burnazyan Center underwent transplantation of the right lobe of the liver after resection of hepatocellular carcinoma, T2N0M0, and due to liver cirrhosis as a result of НСV hepatitis. At the time of hospitalization, he had been constantly receiving immunosuppressive monotherapy with everolimus. The patient was transferred to an infectious disease hospital due to a positive PCR test for SARS-CoV-2 RNA. No signs of respiratory failure were found upon admission. Subsequently, a mild course of COVID-19 was observed, without signs of an acute inflammatory reaction, with normal CRP values and a slight increase of ferritin. 7 days after the treatment, the patient was discharged for outpatient observation. Conclusion. This clinical case is of interest not only by the success of the treatment of the new coronavirus infection COVID-19 in an immunocompromised patient - a recipient of a liver transplant, but also by the fact that the disease manifested itself primarily as a transient increase in hepatic aminotransferases, which can be attributed to the gastrointestinal manifestations of COVID-19.
Текст научной статьи Двусторонняя полисегментарная пневмония, вызванная SARS-COV-2, у реципиента трансплантированной печени
сердца), безусловно, был Китай [8]. В международной научной медицинской литературе, по данным на 14 мая 2020 года, нами обнаружены одна публикация серии наблюдений COVID-19 у реципиентов органов из США [9] и не более 10 клинических наблюдений из других стран. Приводим собственное клиническое наблюдение COVID-19 у пациента с пересаженной печенью, которое, по-видимому, является первым в Российской Федерации.
КЛИНИЧЕСКИЙ СЛУЧАЙ
О пациенте
Мужчина, 54 года, в экстренном порядке переведен из ФГБУ ГНЦ «ФМБЦ им. А.И. Бурназяна» ФМБА России в наш Центр (ФГБУ ФНКЦ ФМБА России) с жалобами на сухой кашель, повышение температуры до 38,5°С, общую слабость.
Из анамнеза известно, что в 2010 г. в ФМБЦ им. А.И. Бурназяна пациенту выполнена родственная трансплантация правой доли печени после удаления гепатоцеллюлярной карциномы T2N0M0 на фоне цирроза печени в исходе вирусного гепатита С. На момент госпитализации пациент постоянно получал иммуносупрессивную монотерапию препаратом эверолимус в дозировке 4 мг/сут. Контроль С0-концентрации эверолимуса в крови перед переводом — 6 нг/мл. Терапия ингибитором mTOR-рецепторов была выбрана еще в раннем посттрансплантационном периоде в связи с выраженной нефротоксичностью и развитием хронической болезни почек II стадии (скорость клубочковой фильтрации по формуле CKD-EPI — 62 мл/мин/м2) на фоне приема ингибиторов кальциневрина (та-кролимус, циклоспорин).
В конце марта 2020 г. при плановом обследовании по поводу трансплантированного органа по данным биохимического анализа крови выявлены высокие уровни печеночных трансаминаз, в связи с чем 06.04.2020 пациент был госпитализирован в Центр хирургии и трансплантологии ФГБУ ГНЦ
<линическая’2п20 п эакти ка Том 11 №2
«ФМБЦ им. А.И. Бурназяна» ФМБА России с предварительным диагнозом дисфункции печеночного трансплантата.
На обзорной рентгенограмме органов грудной клетки от 07.04.2020 выявлены инфильтративные изменения в проекции С4–5 слева. 08.04.2020 выполнена трепан-биопсия трансплантата печени. По данным гистологического исследования: фиброз F1 по Metavir, активность А0–1, слабовыраженный венулит, признаков отторжения трансплантата не выявлено. По результатам компьютерной томографии (КТ) органов брюшной полости и грудной клетки от 14.04.2020 в 3, 6, 10-м сегментах левого легкого и в 6, 7, 10-м сегментах правого легкого выявлены участки инфильтрации по типу «матового стекла» различной степени интенсивности и консолидации легочной ткани, участки тяжисто-го уплотнения, мелкие ретикулярные изменения (рис. 1).
Клинический диагноз: Двусторонняя полисег-ментарная вирусная пневмония.
Учитывая данные КТ-исследования, пациент был изолирован в боксированную палату, после чего ему выполнили анализ назофарингеального мазка на наличие РНК SARS-CoV-2 методом полимеразной цепной реакции (ПЦР). 16.04.2020 отмечалось появление сухого кашля и повышение температуры тела до 38,0°С. 17.04.2020 получен положительный результат ПЦР на наличие РНК SARS-CoV-2. Пациент переведен в специализированный стационар для продолжения лечения.
При поступлении состояние пациента удовлетворительное, температура тела 38,4°С; пальцевая пульсоксиметрия 96% на атмосферном воздухе. Повторное исследование мазка со слизистой оболочки ротоглотки методом ПЦР в момент поступ- ления пациента подтвердило наличие РНК вируса SARS-CoV-2.
Инструментальнаяи лабораторная диагностика
По данным лабораторных анализов крови выявлена лимфопения на фоне умеренно повышенного ферритина и нормального С-реактивного белка, а также повышение уровней гамма-глута-милтрансферазы, щелочной фосфатазы на фоне нормальных показателей билирубина и печеночных трансаминаз (табл. 1).
Лечение
Назначена лекарственная терапия в соответствии с рекомендациями Министерства здравоохранения Российской Федерации: гидроксихлорохин в дозе 200 мг 1 раз/сут внутрь (дозировка снижена относительно протокольной — 400 мг 2 раза/сут — в связи с анамнезом лекарственного поражения почек и высокого уровня печеночных трансаминаз); азитромицин по 500 мг 1 раз/сут внутрь, цефоперазон/сульбактам по 2,0 мг 1 раз/сут внутривенно, клексан 0,4 мл подкожно 1 раз/сут, инфузионная внутривенная терапия растворами кристаллоидов в объеме 1000 мл/сут. Кроме этого, пациент продолжил прием иммуносупрессивного препарата (эверо-лимус) в прежней дозировке — 4 мг/сут внутрь, а также индивидуально подобранную ранее антигипертензивную и базовую противоязвенную терапию.
Динамика и исходы
Со вторых суток стационарного лечения наблюдалась нормализация температуры тела. При контрольном лабораторном исследовании отмечено
Рис. 1. Пациент, 54 года: данные компьютерной томографии органов грудной клетки от 14 апреля
2020 г. при плановом обследовании
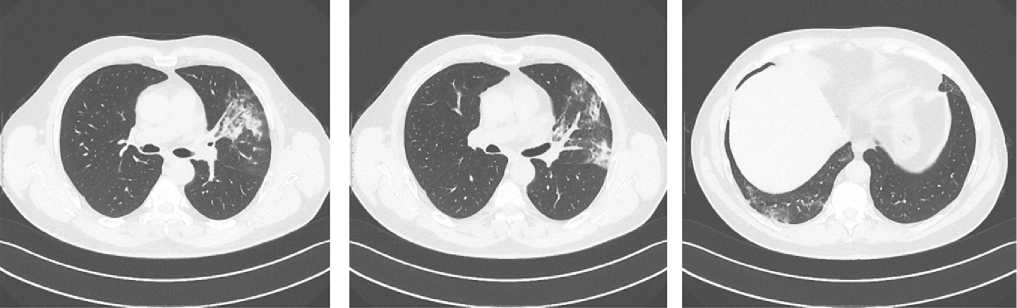
Таблица 1
Динамика лабораторных показателей (биохимическое исследование крови)
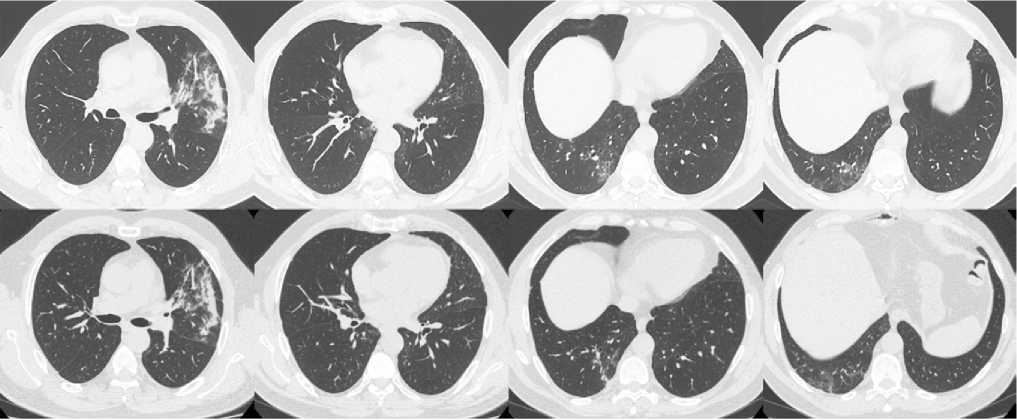
Контрольные исследования на 5-е и 7-е сут стационарного лечения мазка со слизистой оболочки ротоглотки методом ПЦР не выявили наличие РНК вируса SARS-CoV-2. Результаты КТ органов грудной клетки от 24.04.2020 продемонстрировали положительную динамику, уменьшение очагов «матового стекла» (рис. 2). Учитывая стабильное состояние пациента, отсутствие лихорадки и лабораторные маркеры острой воспалительной реакции, а также двукратный отрицательный результат ПЦР на РНК SARS-CoV-2, на 10-е сут стационарного лечения пациент был выписан на амбулаторное долечивание с рекомендациями продолжить иммуносупрессивную терапию под контролем концентрации препарата.
ОБСУЖДЕНИЕ
Данное наблюдение демонстрирует необходимость индивидуального подхода к каждому пациенту, поступающему в инфекционный стационар,
Рис. 2. Пациент, 54 года: данные компьютерной томографии органов грудной клетки от 24 апреля
2020 г. на фоне лечения
<линическая’2п20 п эакти ка Том 11 №2
особенно после перенесенной трансплантации органов. Представленный случай интересен тем, что у пациента, принимающего иммуносупрессивную терапию по поводу трансплантации печени, была обнаружена подтвержденная новая коронавирусная инфекция; клинические, рентгенологические и лабораторные симптомы вполне соответствовали диагнозу COVID-19.
В настоящее время влияние предшествующей иммуносупрессивной терапии на течение COVID-19 изучено недостаточно, и рекомендации по SARS/ MERS не подтверждены из-за короткой продолжительности эпидемии с ограниченными случаями. Необходимость приема глюкокортикостероидов при мягком течении COVID-19 является спорной. Также существует опасение, что снижение или прекращение иммуносупрессивной терапии может вызвать острое отторжение трансплантата. Позиционный документ европейских ассоциаций по изучению печени (EASL) и клинической микробиологии и инфекционным заболеваниям (ESCMID) рекомендует не снижать иммуносупрессивную терапию при COVID-19 [10].
Оптимальное управление трансплантационной иммуносупрессией в условиях COVID-19 также является предметом постоянных дискуссий. Аналогично другим вирусным инфекциям, было рекомендовано снижение или прекращение приема микофенолата мофетила [11]. Исследование 2012 г. показало, что репликация коронавирусов человека зависит от интактных иммунофилиновых путей и может быть ингибирована такролимусом. Наша многопрофильная команда рекомендовала пациенту продолжить прием эверолимуса как для защиты функции трансплантата, так и с целью предотвращения обострения воспалительной реакции на вирусную инфекцию.
В одной из работ описано более длительное выявление вируса у пациентов с легкой формой инфекции COVID-19 без значительного ухудшения по основному заболеванию [12]. На сегодняшний день очевидно, что наш пациент не прогрессировал до тяжелой формы болезни, связанной с гипериммунными реакциями, вероятно, вследствие его иммунокомпрометированного статуса.
Дальнейшие рандомизированные контролируемые клинические испытания особенностей течения и вирусологического клиренса при COVID-19 у реципиентов трансплантированных органов на фоне иммуносупрессии будут ценными для оптимизации подходов к лечению.
ЗАКЛЮЧЕНИЕ
Данный клинический случай демонстрирует успешное выздоровление реципиента трансплантата печени с пневмонией COVID-19 на фоне иммуносупрессивной терапии эверолимусом. Этот случай представляет интерес не только успехом лечения иммунокомпрометированного пациента-реципиента трансплантированной печени, но также тем, что дебют заболевания проявился в первую очередь транзиторным увеличением печеночных аминотрансфераз, что можно отнести к гастроинтестинальным симптомам новой коронавирусной инфекции COVID-19.
ИНФОРМИРОВАННОЕ СОГЛАСИЕ
От пациента получено письменное добровольное информированное согласие на публикацию описания клинического случая (дата подписания 06.06.2020).
Список литературы Двусторонняя полисегментарная пневмония, вызванная SARS-COV-2, у реципиента трансплантированной печени
- Huang C, Wang Y, Li X, et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet. 2020;395(10223):497-506. DOI: 10.1016/S0140-6736(20)30183-5
- Rothe C, Schunk M, Sothmann P, et al. Transmission of 2019-nCoV infection from an asymptomatic contact in Germany. N Engl J Med. 2020;382(10):970-971. DOI: 10.1056/NEJMc2001468
- Holshue ML, De Bolt C, Lindquist S, et al. First case of 2019 novel coronavirus in the United States. N Engl J Med. 2020;382(10):929-936. DOI: 10.1056/NEJMoa2001191
- Wang M, Cao R, Zhang L, et al. Remdesivir and chloroquine effectively inhibit the recently emerged novel coronavirus (2019-nCoV) in vitro. Cell Res. 2020;30(3):269-271. DOI: 10.1038/s41422-020-0282-0
- Cao B, Wang Y, Wen D, et al. A trial of lopinavir-ritonavir in adults hospitalized with severe Covid-19. N Engl J Med. DOI: 10.1056/NEJMoa2001282
- Qin C, Zhou L, Hu Z, et al. Dysregulation of immune response in patients with COVID-19 in Wuhan, China [e-pub ahead of print]. Clin Infect Dis. 2020.
- DOI: 10.1093/cid/ciaa248
- Siddiqi HK, Mehra MR. COVID-19 illness in native and immunosuppressed states: A clinical-therapeutic staging proposal. J Heart Lung Transplant. 2020;39(5):405-407.
- DOI: 10.1016/j.healun.2020.03.012
- Li F, Cai J, Dong N. First Cases of COVID-19 in heart transplantation from China. J Heart Lung Transplant. 2020;39(5):496-497.
- DOI: 10.1016/j.healun.2020.03.006
- Pereira MR, Mohan S, Cohen DJ, et al. COVID-19 in solid organ transplant recipients: Initial report from the US epicenter. Am J Transplant. 2020.
- DOI: 10.1111/ajt.15941
- Liu H, He X, Wang Y, et al. Management of COVID-19 in patients after liver transplantation: Beijing working party for liver transplantation [published online ahead of print, 2020 Apr 10]. Hepatol Int. 2020;1-5.
- DOI: 10.1007/s12072-020-10043-z
- Chen D, Yang B, Zhang Y, et al. Withdrawing mycophenolate mofetil in treating a young kidney transplant recipient with COVID-19: A case report. Medicine (Baltimore). 2020;99(24):e20481.
- DOI: 10.1097/MD.0000000000020481
- Hoehl S, Rabenau H, Berger A, et al. Evidence of SARS-CoV-2 infection in returning travelers from wuhan, China. N Engl J Med. 2020;382(13):1278-1280.
- DOI: 10.1056/NEJMc2001899


