Фактор полиморбидности в развитии контраст- индуцированной нефропатии у пациентов с острым инфарктом миокарда, перенесших коронароангиографию и чрескожное коронарное вмешательство
Автор: Урста А. А., Котиков А. Р., Урста О. В., Харьков Е. И., Петрова М. М.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 1 т.35, 2020 года.
Бесплатный доступ
Цель: оценить значимость фактора полиморбидности в развитии контраст-индуцированной нефропатии (КИН) у пациентов с острым инфарктом миокарда, перенесших коронароангиографию (КАГ) и чрескожное коронарное вмешательство (ЧКВ).Материал и методы. Проведен ретроспективный анализ историй болезни пациентов за 2015 г., проходивших лечение в отделении интенсивной терапии № 3 КГБУЗ «КМКБСМП» им. Н.С. Карповича с острым инфарктом миокарда, перенесших КАГ и ЧКВ. Была сформирована выборка из 33 пациентов с клинически верифицированной КИН. Статистический анализ полученных данных проводили при помощи комплекса пакетных программ и языка программирования R и программного обеспечения G*Power. В работе использовали непараметрические критерии: дисперсионный анализ повторных измерений и U-критерий Манна - Уитни, а также параметрический двухфакторный дисперсионный анализ после логарифмического преобразования непрерывных переменных.Результаты. Из 33 отобранных в выборку человек с диагностированной КИН было 15 женщин и 18 мужчин, средний возраст исследованных пациентов составил 70,9 + 11,5 лет. Представленную выборку разбили на две подкатегории: пациенты с наличием и отсутствием фактора полиморбидности соответственно. В среднем уровень креатинина у полиморбидных пациентов имел показатель 127 мкмоль/л (95; 179), у неполиморбидных - 130 мкмоль/л (91; 179). Двухфакторный дисперсионный анализ продемонстрировал отсутствие значимого влияния фактора полиморбидности на временные изменения показателей уровня креатинина плазмы крови у пациентов с КИН. Парные сравнения, которые были проведены как с логарифмически преобразованными значениями при помощи Т-теста, так и с непреобразованными значениями при помощи критерия Манна - Уитни, не выявили значимых различий между показателями креатинина у полиморбидных и неполиморбидных пациентов. Отсутствие выраженных корреляционных связей между значениями креатинина в выбранных временных отрезках при значимо увеличивающихся показателях можно объяснить влиянием другого фактора, в данном случае, воздействием на фильтрационную способность почек рентгеноконтрастного вещества. Асимметричный характер распределения полученных показателей креатинина как в целой выборке, так и в выделенных подгруппах объясняется его высокой вариативностью. В отношении пациентов с острым инфарктом миокарда, требующих проведения экстренной КАК и ЧКВ по жизненным показаниям, не следует акцентировать внимание на фактор полиморбидности.Заключение. Фактор полиморбидности не имеет значимого влияния на развитие КИН у пациентов с острым инфарктом миокарда, перенесших КАГ и ЧКВ.
Полиморбидность, острый инфаркт миокарда, чрескожное коронарное вмешательство, контраст-индуцированная нефропатия
Короткий адрес: https://sciup.org/149126169
IDR: 149126169 | УДК: 616.127-005.8-06:616.61 | DOI: 10.29001/2073-8552-2020-35-1-93-99
Polymorbidity factor in the development of contrastinduced nephropathy in patients with acute myocardial infarction who underwent coronary angiography and percutaneous coronary intervention
Aim. To estimate the importance of polymorbidity factor in the development of contrast-induced nephropathy in patients with acute myocardial infarction who underwent computed tomography (CT) coronarography and percutaneous coronary intervention (PCI).Material and Methods. We carried out the retrospective analysis of clinical cases of patients with acute myocardial infarction who underwent CT coronarography and PCI in N. S. Karpovich Emergency Hospital of Krasnoyarsk city in 2015. The sample consisted of 33 patients with a clinical verified diagnosis of contrast-induced nephropathy. We used the “R” and “G*Power” software for the statistical analysis of our data. Nonparametric methods of data analyses, such as analysis of variance of repeated measures and Mann-Whitney U-test were used. We also used the two-factor analysis of variance after logarithmicdata transformation. Data are presented as median and 25% and 75% quartiles.Results. Among 33 sampled patients with diagnosed contrast-induced nephropathy, 15 patients were females and 13 patients were males. The mean age was 70.9 ± 11.5 years. We divided this sample into polymorbidity and non-polymorbidity groups. The mean creatinine level in polymorbidity patients was 127 μmol/L (95; 179). Non-polymorbidity patients had a creatinine level of 130 μmol/L (91; 179). We did not detect any significant impact of polymorbidity factor on the temporal changes in the creatinine level (p > 0.05) in patients with contrast-induced nephropathy. Paired comparison based on both logarithmic transformation data using T-test and non-transformed values using Mann - Whitney U test did not show any significant differences between the creatinine levels in polymorbidity and non-polymorbidity patients. The absence of a strong correlation between creatinine levels and polymorbidity at chosen time intervals in the presence of significantly increasing creatinine values may be explained by the influence of other factors. In our case, we attribute an impact of contrast medium on kidney filtration. Their high variability explains the asymmetric distribution of creatinine values both in the entire sample and in the subgroups. The polymorbidity factor should not require special attention in regard to patients with acute myocardial infarction who need emergency CT coronarography and life-saving PCI.Conclusion. The polymorbidity factor did not significantly affect the development of contrast-induced nephropathy in patients with acute myocardial infarction undergoing CT coronarography and PCI.
Текст научной статьи Фактор полиморбидности в развитии контраст- индуцированной нефропатии у пациентов с острым инфарктом миокарда, перенесших коронароангиографию и чрескожное коронарное вмешательство
–99
Контраст-индуцированная нефропатия (КИН) – острое нарушение функции почек, возникающее в течение 48–72 ч после внутрисосудистого введения рентгеноконтрастного средства (РКС). Развитие КИН характеризуется повышением концентрации сывороточного креатинина > 0,3 мг/дл (или > 26,5 мкмоль/л), или > 1,5 раза по сравнению с исходным уровнем, в течение 48–72 ч внутрисосудистого введения контрастного вещества при отсутствии других причин [1].
Под полиморбидностью следует понимать наличие нескольких синхронно протекающих заболеваний у одного человека в различных стадиях и фазах своего развития. Большинство пациентов с сердечно-сосудистыми заболеваниями (ССЗ) в реальной медицинской практике характеризуются сочетанием двух и более заболеваний и состояний, т. е. сердечно-сосудистой полиморбидно-стью [2, 3].
В связи с широким распространением диагностических и лечебных процедур с использованием рентгеноконтрастных препаратов КИН является актуальной проблемой в клинической практике кардиологов [4].
С целью визуализации коронарных артерий и проведения реваскуляризации миокарда больным ишемической болезнью сердца проводят коронароангиогра-фию (КАГ) и чрескожные коронарные вмешательства (ЧКВ) с использованием рентгеноконтрастных средств. Эти малоинвазивные процедуры требуют использования йодсодержащих РКС, которые не только оказывают прямое токсическое действие на эпителий почечных канальцев, но и вызывают нарушение почечной гемодинамики с медуллярной ишемией [5–7]. В настоящее время превалирует стратегия первичного ЧКВ, если так называемое время «симптом – баллон» не превышает 120 мин [8]. Использование РКС у пациентов с электролитными нарушениями в состоянии шока или застойной сердечной недостаточности допускается только по жизненным показаниям (например, при остром инфаркте миокарда) [9].
Патофизиология КИН до конца не изучена, но в настоящее время большое значение придают нарушению почечной гемодинамики и прямому влиянию РКС на почечные канальцы [10].
Осмотическая нагрузка РКС может плохо переноситься, если почечная функция «скомпрометирована», например у больных с сахарным диабетом или почечной недостаточностью, у которых уже присутствуют гипоксия мозгового слоя и нарушение эндотелийзависимой вазодилатации [5]. Однако введение РКС не всегда провоцирует развитие КИН [11].
У пациентов с острым коронарным синдромом существуют риски торможения фильтрационной функции почек. Среди больных, не получавших РКС, в 23,8% случаев отмечается увеличение содержания креатинина в сыворотке крови. Причем, согласно общепринятым в клинической практике рекомендациям [12, 13], в 6,3% случаев повышение его уровня в течение 3 дней после начала лечения соответствует диагностическим критериям КИН [12].
Среди пациентов с ОИМпST, которым было проведено ЧКВ, статистически значимой разницы в риске госпитальной смертности между группами с нормальной и сниженной функцией почек не получено [14].
Материал и методы
Проведен ретроспективный анализ историй болезни пациентов за 2015 г., проходивших лечение в отделении интенсивной терапии № 3 КГБУЗ «КМКБСМП» им. Н.С. Карповича с острым инфарктом миокарда, на основании чего была сформирована выборка пациентов с клинически верифицированной КИН. Всем пациентам с острым инфарктом миокарда проводили КАГ и ЧКВ с использованием низко- и изоосмолярных РКС. Проводимое исследование было одобрено локальным этическим комитетом Красноярского государственного медицинского университета имени профессора В.Ф. Во-йно-Ясенецкого Министерства здравоохранения Российской Федерации. Основной исследуемой непрерывной переменной представленного исследования выбрали уровень креатинина сыворотки крови, который измеряли после забора крови из поверхностных вен предплечья или посредством центрального венозного доступа в следующие временные интервалы: 1) при поступлении в стационар; 2) через 12 ч после поступления; 3) через 24 ч после поступления; 4) через 48 ч после поступления; 5) через 72 ч после поступления. В представленной выборке выделили группу пациентов с наличием фактора полиморбидности (n = 17). В данную группу вошли пациенты с наличием как минимум двух патогенетически несвязанных заболеваний (таблица).
Статистический анализ полученных данных проводили при помощи комплекса пакетных программ и языка программирования R, а также с использованием программного обеспечения G*Power [15]. Характер распределения измеренных переменных в группах отличался от нормального, на основании чего применяли непараметрические методы исследования: дисперсионный анализ повторных измерений с критерием Фридмана, для пар- ных сравнений независимых переменных применялся U-критерий Манна – Уитни. Корреляционный анализ осуществляли посредством коэффициента корреляции Спирмена. Использовали также параметрический двухфакторный дисперсионный анализ после логарифмического преобразования асимметричных переменных. Полученные значения представлены в виде медианы (Me) и 25- и 75-го квартилей (Q1, Q3). Переменные, которые подчинялись нормальному закону распределения, представлены в виде средней и стандартного отклонения.
Результаты
Из 33 отобранных в выборку человек с диагностированной КИН было 15 женщин и 18 мужчин, средний возраст исследованных пациентов составил 70,9 + 11,5 лет. Представленную выборку разбили на две подкатегории: пациенты с наличием и отсутствием фактора полимор-бидности соответственно. Характер распределения пациентов с наиболее значимыми факторами отражен в таблице (см. табл.).
Таблица. Распределение демографических и клинических факторов у пациентов с острым инфарктом миокарда, осложненным контраст-ин-дуцированной нефропатией
Table. Distribution of demographic and clinical factors in patients with acute myocardial infarction complicated by contrast-induced cardiomyopathy
Показатели уровня креатинина плазмы крови, которая была взята во время поступления пациентов в стационар, в среднем составляли 89,0 (77; 100) мкмоль/л, при этом у пяти пациентов данные показатели превышали нормальные значения: 157–381 мкмоль/л. Уровень креатинина плазмы, измеренный через 12 ч после забора крови, составлял в среднем 124 (102; 152) мкмоль/л, через 24 ч – 133 (91; 169), через 48 ч – 160 (111; 179), через 72 ч – 200 (134; 200) мкмоль/л.
Значения уровня креатинина, как это видно на представленном рисунке 1, имели асимметричный характер распределения, при этом у большинства групп характер асимметрии был положительным. Учитывая наличие относительно выраженного диапазона разброса показателей уровня креатинина, многие значения статистическими методами воспринимались как выбросы, в частности, группа уровня креатинина с забором крови на 72-м ч после поступления у полиморбидных пациентов целиком представлена этими выбросами.
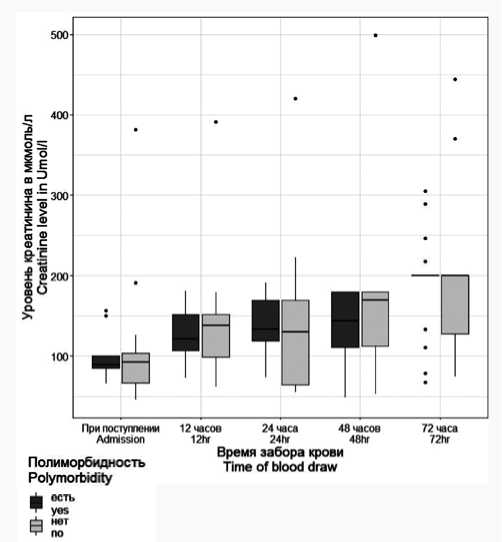
Рис. 1. Распределение показателей креатинина в зависимости от времени забора и наличия полиморбидности
Fig. 1. Distribution of creatinine levels depending on time of blood sampling and the presence of polymorbidity
При помощи критерия Фридмана в формате дисперсионного анализа повторных измерений была оценена значимость временного фактора в отношении показателей уровня креатинина в целом и отдельно в группах с полиморбидными и неполиморбидными пациентами. Во всех трех случаях проведенного дисперсионного анализа повторных измерений отмечена очень высокая значимость временного фактора ( p < 0,0001) в отношении возрастания уровня креатинина у пациентов с КИН. Корреляционный анализ при помощи критерия Спирмена между показателями уровня креатинина на разных временных отрезках показал максимум – среднюю силу
(0,52 при p < 0,05) корреляционной связи, в большинстве сравнений сила связи была низкой (менее 0,29 при p > 0,05).
В среднем уровень креатинина у полиморбидных пациентов имел показатель 127 (95; 179) мкмоль/л, у неполиморбидных - 130 (91; 179) мкмоль/л. Двухфакторный дисперсионный анализ продемонстрировал отсутствие значимого влияния фактора полиморбидности на временные изменения показателей уровня креатинина плазмы крови у пациентов с КИН. Парные сравнения, которые были проведены как с логарифмически преобразованными значениями при помощи Т-теста, так и с непреобразованными значениями при помощи критерия Манна – Уитни, не выявили статистически значимых различий между показателями креатинина у полимор-бидных и неполиморбидных пациентов.
Обсуждение
Асимметричный характер распределения полученных показателей креатинина как в целой выборке, так и в выделенных подгруппах объясняется его высокой вариативностью. В частности, оценка референсных значений креатинина в более объемных выборках также показала достаточно выраженную асимметрию.
Отсутствие выраженных корреляционных связей между значениями креатинина в выбранных временных отрезках при значимо увеличивающихся показателях можно объяснить влиянием другого фактора, в данном случае, воздействием на фильтрационную способность почек рентгеноконтрастного вещества.
В современной научной литературе имеются единичные сообщения о значимости фактора полиморбидно-сти в развитии КИН [16]. Также имеются весьма противоречивые и разрозненные данные о влиянии различных заболеваний на вероятность развития КИН [17].
Настоящее исследование не выявило значимости эффекта фактора полиморбидности на возникновение КИН.
В отношении пациентов с острым инфарктом миокарда, требующих проведения экстренной КАК и ЧКВ по жизненным показаниям, не следует акцентировать внимание на фактор полиморбидности.
Заключение
Таким образом, наше исследование не показало, что наличие полиморбидности является фактором риска в возникновении КИН у пациентов с острым инфарктом миокарда.
Список литературы Фактор полиморбидности в развитии контраст- индуцированной нефропатии у пациентов с острым инфарктом миокарда, перенесших коронароангиографию и чрескожное коронарное вмешательство
- ESUR Guidelines on Contrast Agents. European Society of Urogenital Radiology. URL: http://www.esur.org/fileadmin/content/2019/ESUR_ Guidelines_10.0_Final_Version.pdf/.
- DuGoff E.H., Canudas-Romo V., Buttorff C., Leff B., Anderson G.F. et al. Multiple chronic conditions and life expectancy: a life table analysis. Med. Care. 2014;52(8):688-694. DOI: 10.1097/ MLR. 0000000000000166.
- Оганов Р.Г., Денисов И.Н., Симаненков В.И., Бакулин И.Г., Бакули-на Н.В., Болдуева С.А. и др. Коморбидная патология в клинической практике. Клинические рекомендации. Кардиоваскулярная тера-
- пия и профилактика. 2017;16(6):5-56. DOI: 10.15829/1728-88002017-6-5-56.
- Туренко О.И., Лебедева А.Ю., Гордеев И.Г., Волов Н.А. Проблема контраст-индуцированной нефропатии в кардиологии. Российский кардиологический журнал. 2011;89(3):78-86. DOI: 10.15829/1560-4071-2011-3-78-86.
- Волгина Г.В. Контраст-индуцированная нефропатия: патогенез, факторы риска, стратегия профилактики. Нефрология и диализ. 2006;8(2):176-183.
- Калаева В.В., Каретникова В.Н., Осокина А.В., Груздева О.В., Каш-талап В.В., Евсеева М.В. и др. Факторы риска контраст-инду-
- цированной нефропатии у больных инфарктом миокарда. Клиническая медицина. 2014;9:39-45.
- Tepel M., Aspelin P., Lameire N. Contemporary reviews in cardiovascular medicine contrast-induced nephropathy: A clinical and evidence-based approach. Circulation. 2006;113:1799-1806. DOI: 10.1161/CIRCULATIONAHA.105.595090.
- Немик Д.Б., Матюшин Г.В., Протопопов А.В., Шестерня П.А., Голо-венкин Р.Е., Шульмин А.В. Эффективность ранней догоспитальной тромболитической терапии с последующим чрескожным коронарным вмешательством у пациентов с острым инфарктом миокарда с подъемом сегмента ST (современное состояние проблемы). Сибирское медицинское обозрение. 2015;3:15-24.
- Витько Н.К., Тер-Акопян А.В., Панков А.С., Тагаев Н.Б. Применение рентгеноконтрастных веществ в интервенционной кардиологии и ангиологии: история, осложнения и их профилактика. Russian Electronic Journal of Radiology. 2012;2(1):29-34. URL: www.rejr.ru.
- Доморадская А.И. Контраст-индуцированная нефропатия: факторы риска. Russian Electronic Journal of Radiology. 2011;1(4):27-32. URL: www.rejr.ru.
- Дундуа Д.П., Карташов Д.С., Бабунашвили А.М., Артамонова Ю.В., Кавтеладзе З.А. Неизбежна ли контраст-индуцированная нефропатия в ответ на введение рентгеноконтрастного вещества? Медицинская визуализация. 2010;6:25-31.
- Ватутин Н.Т., Зинкович М.И., Шевелек А.Н. Распространенность нарушения функции почек у пациентов с острым коронарным
- синдромом. Архивъ внутренней медицины. 2015;23(3):30-32. DOI: 10.20514/2226-6704-2015-0-3-30-32.
- Morcos S.K., Thomsen H.S., Webb J.A. Contrast-media-induced nephrotoxicity: a consensus report. Contrast Media Safety Committee, European Society of Urogenital Radiology (ESUR). Eur. Radiol. 1999;9(8):1602—1613. DOI: 10.1007/s003300050894.
- Макарычева О.В., Хмара Т.Н., Назаров А.В., Якушева Н.В., Скрып-ник Д.В., Васильева Е.Ю. и др. Экстренное чрескожное вмешательство и госпитальный прогноз у больных острым инфарктом миокарда с подъемом сегмента ST со сниженной функцией почек. Международный журнал интервенционной кардиоангиологии. 2011;24:84.
- Faul F., Erdfelder E., Buchner A., Lang A. Statistical power analyses using G*Power 3.1: Tests for correlation and regression analyses. Behavior Research Methods. 2009;41(4):1149-1160. DOI: 10.3758/ brm.41.4.1149.
- Вершинина Е.О., Репин А.Н. Контраст-индуцированное острое овреждение почек при плановых эндоваскулярных вмешательствах на коронарных артериях. Клиническая медицина. 2017;95(12):1086-1093. DOI: 10.18821/0023-2149-2017-95-12-1086-1093.
- АрьевА.Л.,ЧесноковА.А.,ДзаховаС.Д.,Овсянникова Н.А.,Арьева Г. Т. Мультиморбидность как один из предикторов риска развития контраст-индуцированной нефропатии в гериатрической практике. Нефрология. 2017;21(1):34-38. DOI: 10.24884/1561-6274-201721-1-34-38.


