Факторы, оказывающие влияние на годовой прогноз при инфаркте миокарда, осложненном левожелудочковой недостаточностью и ассоциированном с хронической ишемией головного мозга
Автор: Лебедева Н.Б., Чеснокова Л.Ю., Тарасов Н.И.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 2 т.35, 2020 года.
Бесплатный доступ
Цель исследования: изучение факторов неблагоприятного годового погноза при инфаркте миокарда (ИМ), осложненном сердечной недостаточностью (СН) с низкой фракцией выброса левого желудочка (ФВ ЛЖ) и ассоциированном с хронической ишемией головного мозга (ХИГМ).Материал и методы. В исследование включены 182 пациента с Q-образующим ИМ, осложненным левожелудочковой недостаточностью на фоне сопутствующей ХИГМ, из них 149 (81,9%) мужчин и 33 (18,1%) женщины. Медиана возраста - 60,4 (53; 69) года. Всем пациентам были проведены эхокардиография, цветное дуплексное сканирование сонных артерий и осмотр ангионевролога. Через год оценивались жесткие конечные точки (КТ).Результаты. В исследуемой группе большинство составили пациенты с ХИГМ II степени. Атеросклеротические бляшки (АСБ) в брахиоцефальных артериях (БЦА) были выявлены у 37,4% пациентов, во всех случаях степень стеноза не превышала 50%. В течение года жесткие КТ развились у 77 (46,1%) пациентов. Многофакторная модель логистической регрессии показала, что наиболее неблагоприятным предиктором смерти в течение первого года в исследуемой группе является ранее перенесенное острое нарушение мозгового кровообращения (ОНМК): ОР = 7,33 (95% ДИ 1,97-27,32), р = 0,003, а наиболее неблагоприятными предикторами риска развития неблагоприятных сердечно-сосудистых событий являются инсульт в анамнезе - ОР = 1,92 (95% ДИ 1,09-3,38), р = 0,025 и наличие каротидной АСБ - ОР = 2,12 (95% ДИ 1,34-3,37), р = 0,001.Выводы. У пациентов с ИМ, осложненным СН и ассоциированным с ХИГМ, наибольшее неблагоприятное влияние на отдаленный прогноз оказывают наличие АСБ в каротидном бассейне и перенесенный ранее инсульт.
Инфаркт миокарда, хроническая ишемия головного мозга, сердечная недостаточность, отдаленный прогноз
Короткий адрес: https://sciup.org/149126170
IDR: 149126170 | УДК: 616.124.2-008.64-06:616.127-005.8-037:616.831-005.4-036.12 | DOI: 10.29001/2073-8552-2020-35-2-106-113
Factors determining an unfavorable one-year prognosis of myocardial infarction complicated by left ventricular failure and associated with chronic cerebral ischemia
Aim. To evaluate factors of unfavorable annual prognosis of myocardial infarction (MI) complicated by heart failure (HF) with reduced ejection fraction (HFrEF) and associated with chronic cerebral ischemia (CCI).Material and Methods. A total of 182 patients with Q wave myocardial infarction complicated by the left ventricular dysfunction concomitant with CCI were included in the study. Of them, 149 (81.9%) patients were men and 33 (18.1%) were women. The mean age was 60.4 (53; 69) years. All patients underwent echocardiography, color duplex scanning of the carotid arteries and examination by an interventional neurologist. Hard endpoints were collected within one year.Results. The majority of the patients included in the study suffered from grade 2 CCI. Atherosclerotic plaques in the brachiocephalic arteries were found in 37.4% of patients; the degree of stenosis did not exceed 50% in all cases. 77 (46.1%) patients achieved hard endpoints within one year. Multivariate logistic regression showed that the most unfavorable predictor of poor 1-year survival was the presence of the positive history of ACVA [RR 7.33 (95% CI 1.97-27.32), p = 0.003], and the most unfavorable predictors of risk of adverse cardiovascular events included prior stroke [RR = 1.92 (95% CI 1.09-3.38), p = 0.025] and carotid atherosclerotic plaques [RR = 2.12 (95% CI 1.34-3.37), p = 0.001].Conclusion. The presence of carotid atherosclerotic plaques and prior stroke affected the long-term prognosis in patients with myocardial infarction complicated by heart failure and chronic cerebral ischemia.
Текст научной статьи Факторы, оказывающие влияние на годовой прогноз при инфаркте миокарда, осложненном левожелудочковой недостаточностью и ассоциированном с хронической ишемией головного мозга
–113
Сердечно-сосдудистые заболевания, обусловленные атеросклерозом, в частности, ишемическая болезнь сердца (ИБС) и мозга продолжают доминировать в структуре смертности как в России, так и в зарубежных странах [1–3]. В настоящее время появляется все больше данных о том, что развитие церебральных сосудистых событий тесно связано с кардиальными факторами, что во многом обусловлено системностью атеросклеротического процесса [4, 5]. Так, при атеросклерозе брахиоцефальных артерий (БЦА) в 33–37% случаев выявляется стенозирующее коронарное поражение, а у большинства больных с цереброваскулярными заболеваниями при обследовании выявляются нарушения перфузии миокарда [6].
Кроме того, по некоторым данным, у половины пациентов с острым коронарным синдромом выявляются ультразвуковые признаки гетерогенности каротидных атеросклеротических бляшек (АСБ), свидетельствующие об их нестабильности [1]. Этот факт подтверждает существование общих патологических механизмов, способствующих возникновению сердечно-сосудистых и церебральных событий.
Европейское общество кардиологов сообщает о том, что инфаркт миокарда (ИМ) по-прежнему занимает первое место среди всех смертельных случаев и сохраняет тенденцию к ежегодному росту [7, 8]. Отдаленный прогноз после перенесенного ИМ определяется многими факторами, и наибольший вклад в снижение выживаемости в данном случае вносит нарушение систолической функции левого желудочка (ЛЖ). Так, пациенты с ИМ и фракцией выброса левого желудочка (ФВ ЛЖ) менее 40% умирают в течение трех лет, а риск внезапной сердечной смерти в пять раз больше, чем в обычной популяции [9– 11]. Существуют данные о том, что у пациентов с ИБС низкая ФВ ЛЖ ассоциируется не только с многососудистым поражением коронарного русла, что ожидаемо, но и со стенозами БЦА [4, 12]. Состояние церебрального кровотока, особенно при наличии каротидных стенозов, во многом определяется состоянием центральной гемодинамики, в которой основную роль играет величина сердечного выброса. С другой стороны, наличие церебральной ишемии и ее усугубление способны дополнительно ухудшать прогноз при ИМ и левожелудочковой недостаточности [13, 14]. Таким образом, хроническая ишемия головного мозга (ХИГМ) может рассматриваться как дополнительный экстракардиальный фактор, способствующий более тяжелому течению острой и хронической ИБС [14, 15].
В связи с этим целью настоящего исследования явилось изучение факторов неблагоприятного годового по-гноза при ИМ, осложненном СН с низкой ФВ ЛЖ и ассоциированном с ХИГМ.
Материал и методы
В исследование были включены 182 пациента с Q-образующим ИМ, осложненным левожелудочковой недостаточностью, госпитализированных в инфарктное отделение Кемеровского кардиологического центра через 7,6 (5,3; 15,2) ч от начала ангинозного приступа, из них 149 (81,9%) мужчин и 33 (18,1%) женщины. Возраст пациентов составил 60,4 (53; 69) года.
Критерии включения: Q-образующий ИМ, ФВ ЛЖ 40% и менее, наличие ХИГМ в анамнезе, Killip II–III. В исследование не включались пациенты с Q-необразующим ИМ, стойкими нарушениями ритма и проводимости, Killip IV, пороками клапанов, тяжелым течением сахарного диабета (СД), а также пациенты, не подписавшие форму информированного согласия.
Исследование проводилось на базе инфарктного отделения в соответствии со стандартами надлежащей клинической практики (Good Clinical Practice) и принципами Хельсинкской декларации Всемирной ассоциации «Этические принципы проведения научных медицинских исследований с участием человека». Протокол исследования и форма информированного согласия были одобрены локальным этическим комитетом.
При поступлении всем пациентам проводили оценку клинико-функционального состояния ЛЖ по данным эхокардиографии (ЭхоКГ) в М-, В- и допплер-режимах на ультразвуковом сканере ACUSON 128 XP/10 (США) по общепринятой методике и селективную коронароангио-графию (КАГ) – на оборудовании фирмы Siemens, ангиографической установкой Angioscop; INNOVA 3100 фирмы GE HealthCare (США).
Анамнестически выявленный диагноз ХИГМ подтверждался при осмотре ангионеврологом, степень тяжести ХИГМ устанавливалась согласно классификации Е.В. Шмидта (1985).
Всем больным на 2-е–3-и сут ИМ проводилось дуплексное сканирование периферических артерий с цветным картированием кровотока и импульсной допплерографией (Sonos-2500, Hewlett Packard).
Через год оценивали следующие жесткие конечные точки (КТ): повторные ИМ, прогрессирующую стенокардию (ПС), потребность в реваскуляризации, острую декомпенсацию хронической сердечной недостаточности (ОДХСН), повторные госпитализации, цереброваскулярные события, сердечно-сосудистую смертность, общую смертность.
Статистическую обработку полученных данных проводили с помощью пакета программ STATISTICA 8.0 for Windows фирмы StartSoft (США) и IBM SRSS STATISTICS 20.0 (США).
Нормальность распределения оценивали по критерию Шапиро – Уилка. Количественные признаки представлены в виде медианы с межквартильным интервалом [ Ме (25; 75)]. Для сравнения двух количественных признаков использовали U-критерий Манна – Уитни, для сравнения частот – критерий Фишера с двусторонней доверительной вероятностью, критерий χ 2 с поправкой Йетса. Выявление независимых предикторов развития неблагоприятных исходов проводили построением однофакторных и многофакторных моделей логистических регрессий. Для оценки каждого фактора в предсказании исследуемого события рассчитывали отношение рисков (ОР) и шансов (ОШ) с 95%-м доверительным интервалом (ДИ). Для многофакторной модели регрессии использовали прямой пошаговый алгоритм (Forward Wald) с расчетом χ 2 и значения площади под ROC-кривой (С-статистика). Статистически значимыми считали различия при р < 0,05.
Результаты
Клинико-анамнестическая характеристика когорты исследования представлена в таблице 1. Подавляющее большинство пациентов составили мужчины с артериальной гипертензией (АГ), ИБС и хронической сердечной недостаточностью (ХСН) в анамнезе. Преобладали пациенты с передним ИМ, многососудистым поражением коронарного русла, с Killip II. Реваскуляризация инфаркт-связанной артерии была выполнена в общей сложности у 81,2% пациентов.
Таблица 1. Клинико-анамнестическая характеристика группы исследования
|
Tablе 1. Clinical and anamnestic characteristics of the study group |
||
|
Наименование показателей Parameters |
n = 182 |
|
|
Возраст, лет, Ме ( Q 25; Q 75) Age, year |
59 (52; 69) |
|
|
Мужчины, n (%) Male, n (%) |
148 (81,3) |
|
|
Артериальная гипертензия, n (%) Essential hypertention, n (%) |
149 (81,9) |
|
|
Инсульт в анамнезе, n (%) Stroke, n (%) |
19 (10,4) |
|
|
Сахарный диабет 2-го типа, n (%) Type 2 diabetes mellitus, n (%) |
45 (24,7) |
|
|
Стенокардия в анамнезе, n (%) Angina pectoris, n (%) |
134 (73,6) |
|
|
Cердечная недостаточность в анамнезе, n (%) Heart failure, n (%) |
152 (83,5) |
|
|
Повторный инфаркт миокард, n (%)а Recurrent myocardial infarction, n (%) |
69 (37,9) |
|
|
Передний инфаркт миокарда, n (%) Anterior myocardial infarction, n (%) |
112 (61,5) |
|
|
Killip II, n (%) |
128 (70,3) |
|
|
Killip III, n (%) |
54 (29,6) |
|
|
Хроническая ишемия головного мозга I ст., n (%) Chronic cerebral ischemic disease I degree, n (%) |
38 (20,8) |
|
|
Хроническая ишемия головного мозга II ст., n (%) Chronic cerebral ischemic disease II degree, n (%) |
122 (67,0) |
|
|
Хроническая ишемия головного мозга III ст., n (%) Chronic cerebral ischemic disease III degree, n (%) |
22 (12,1) |
|
|
Фракция выброса левого желудочка, Ме ( Q 25; Q 75) Left ventricular ejection fraction |
38 (31; 44) |
|
|
Проведена коронарография, n (%) Coronarography, n (%), |
156 (85,7) |
|
|
SYNTAX, Ме ( Q 25; Q 75) |
23 (18; 28,5) |
|
|
Поражение коронарных артерий, n (%) The involvement of coronary arteries, n (%) |
3-сосудистое 3-vessel disease |
69 (37,9) |
|
2-сосудистое 2-vessel disease |
50 (27,4) |
|
|
1-сосудистое 1-vessel disease |
27 (14,8) |
|
|
Проведено чрескожное вмешательство, n (%) Percutaneous coronary intervention, n (%) |
121 (66,4) |
|
|
Проведен тромболизис, n (%) Thrombolysis, n (%) |
27 (14,8) |
|
В исследуемой группе большинство составили пациенты с ХИГМ II степени. У 21 (11,5%) пациента в связи с перенесенным ОНМК была диагностирована ХИГМ III степени тяжести (рис. 1).
Согласно дуплексному сканированию, АСБ в БЦА были выявлены у 37,4% пациентов, во всех случаях степень стеноза не превышала 50%.
На госпитальном этапе из-за рецидива ИМ умерли 5 (2,7%) пaциентов, 10 пациентов в течение года были потеряны для наблюдения. Таким образом, в оценку годового прогноза вошли данные 167 (91,7%) пациентов.
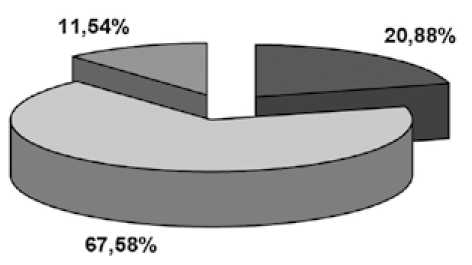
□ ХИГМ I / Chronic cerebral ischemic deasise I □ ХИГМ II / Chronic cerebral ischemic deasise II □ ХИГМ III / Chronic cerebral ischemic deasise III
Рис. 1. Распределение пациентов исследуемой группы по тяжести хронической ишемии головного мозга
Fig. 1. Distribution of patients in the study group according to the severity of chronic cerebral ischemia
Анализ получаемой медикаментозной терапии в исследуемой группе показал достаточно высокую приверженность назначенному лечению. Так, 87% пациентов получали ингибиторы ангиотензинпревращающего фермента (ИАПФ) или сартаны, 96% – бета-блокаторы, 70% – диуретики, 64% – двойную дезагрегантную терапию, 63% – статины.
В течение года жесткие КТ развились у 77 (46,1%) пациентов. Всего была зарегистрирована 141 жесткая КТ, из них 11 смертей, 22 повторных ИМ, 8 ОНМК по ишемическому типу, 30 случаев нестабильной стенокардии, 31 случай ОДХСН. Чрескожное коронарное вмешательство (ЧКВ) со стентированием было проведено 19, коронарное шунтирование – 20 больным.
В результате проведения однофакторного регрессионного анализа выявлены наиболее значимые отдельные факторы риска, ассоциированные с годовой летальностью, которыми явились: ОНМК в анамнезе с высокой степенью вероятности и визуализация каротидной АСБ по данным цветового дуплексного сканирования БЦА ( р = 0,049), таблица 2.
Таблица 2. Однофакторный анализ ассоциации клинико-анамнестических данных с годовой летальностью, n (%)
Tablе 2. Univariable analysis of the associations of clinical and medical history data with annual mortality, n (%)
|
Пaрaметры Indicators |
Живые, n = 168 Alive |
Умершиe, n = 11 Dead |
OШ (95% ДИ) OR (95% CI) |
p |
|
Возрaст > 65 лет Age |
66 (39,3) |
6 (66,7) |
3,09 (0,75– 12,79) |
0,1 |
|
Мужской пoл Male |
136 (81,0) |
9 (1000) |
1,07 (1,02– 1,11) |
0,15 |
|
Курeниe Smoking |
74 (44,3) |
6 (66,7) |
2,51 (1,61– 3,39) |
0,19 |
|
Cахарный диабет Diabetes mellitus |
45 (26,8) |
0 |
0,93 (0,89– 0,98) |
0,072 |
|
Инфаркт миокарда в анамнезe History of myocardial infarction |
60 (35,7) |
5 (55,6) |
2,25 (0,58–8,7) |
0,23 |
|
Инсульт в анамнезe History of stroke |
15 (8,9) |
4 (44,4) |
9,81 (1,98– 33,68) |
0,001 |
Окончание табл. 2
End of table 2
|
Пaрaметры Indicators |
Живые, n = 168 Alive |
Умершиe, n = 11 Dead |
OШ (95% ДИ) OR (95% CI) |
p |
|
Бляшка в каротидной артерии Carotid artery plaque |
62 (36,9) |
6 (66,7) |
3,92 (2,91–16,97) |
0,049 |
|
Killip II |
121 (72,0) |
4 (44,4) |
0,31 (0,08–1,21) |
0,077 |
|
Killip III |
47 (28,0) |
5 (55,6) |
3,22 (0,83–12,5) |
0,077 |
|
ЧКВ инфарктсвязанной артерии Percutaneous coronary intervention |
97 (57,7) |
3 (33,3) |
0,37 (0,09–1,51) |
0,15 |
На следующем этапе в результате построения многофакторной модели логистической регрессии выявлено, что наиболее неблагоприятным предиктором смерти в течение первого года в исследуемой группе явилось ра- нее перенесенное ОНМК: ОР = 7,33 (95% ДИ 1,97–27,32), р = 0,003.
Далее был проведен однофакторный анализ наиболее вероятных предикторов неблагопрятного исхода, связанного с развитем сердечно-сосудистых событий в группах с КТ и без КТ (табл. 3).
Согласно проведенному анализу, факторами, связанными с риском развития сердечно-сосудистых событий в течение года, явились каротидная АСБ и перенесенный ранее инсульт. Проведение ЧКВ инфарктсвязанной артерии ассоциировалось в благоприятным прогнозом.
В результате построения многофакторной модели логистической регрессии выявлено, что наиболее значимыми предикторами риска развития сердечно-сосудистых событий оказались инсульт в анамнезе – ОР = 1,92 (95% ДИ 1,09–3,38), р = 0,025 и наличие каротидной АСБ – ОР = 2,12 (95% ДИ 1,34–3,37), р = 0,001. Выполнение ЧКВ на инфарктсвязанной артерии, напротив, существенно улучшало прогноз: ОР = 0,6 (95% ДИ 0,38–0,95), р = 0,03.
Площадь под ROC-кривой при оценке прогностической мощности многофакторной модели составила 0,612 (95% ДИ 0,523–0,702, р = 0,046), рисунок 2.
Таблица 3. Однофакторный анализ ассоциации клинико-анамнестических данных с риском развития сердечно-сосудистых событий, n (%)
Tablе 3. Univariable analysis of the associations of clinical and anamnestic data with a risk of cardiovascular events, n (%)
|
Пaрaметры Indicators |
Без КТ, n = 100 Without endpoints, n = 100 |
Рaзвитие КТ, n = 77 With endpoints, n = 77 |
OШ (95 % ДИ) OR (95 % CI) |
р |
|
Возрaст > 65 лет Age > 65 years |
35 (35,0) |
37 (48,1) |
1,72 (0,94–3,15) |
0,08 |
|
Мужской пoл Male |
86 (86,0) |
59 976,60 |
0,54 (0,25–1,16) |
0,11 |
|
Курeниe Smoking |
42 (42,0) |
38 (50,0) |
1,38 (0,76–2,52) |
0,29 |
|
Cахарный диабет Diabetes mellitus |
28 (28,0) |
17 (22,1) |
0,73 (0,36–1,46) |
0,37 |
|
Инфаркт миокарда в анамнезe History of myocardial infarction |
35 (35,0) |
30 (39,0) |
1,19 (0,64–2,19) |
0,59 |
|
Инсульт в анамнезe History of sroke |
6 (6,0) |
16 (20,8) |
4,11 (1,52–11,01) |
0,003 |
|
Бляшка в каротидной артерии Carotid artery plaque |
29 (29,0) |
39 (50,6) |
2,51 (1,35–4,68) |
0,003 |
|
Killip II |
76 (76,0) |
49 (63,6) |
0,55 (0,29–1,1) |
0,073 |
|
Killip III |
24 (24,0) |
28 (36,4) |
1,81 (0,94–3,48) |
0,073 |
|
ЧКВ инфарктсвязанной артерии Percutaneous coronary intervention |
63 (63,0) |
37 (48,1) |
0,54 (0,3–0,99) |
0,047 |
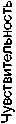

1 – Специфичность
Рис. 2. Прогностическая мощность модели (ROC-кривая) оценки годового прогноза у пациентов с инфарктом миокарда, осложненным левожелудочковой недостаточностью и ассоциированным с хронической ишемией головного мозга
Fig. 2. Predictive power of the model (ROC-curve) of one-year prognosis in patients with myocardial infarction complicated by the left ventricular insufficiency and associated with chronic cerebral ischemia
Обсуждение
Оценка риска развития неблагоприятного прогноза является очень важной для понимания медицинской и социальной значимости заболевания и определения степени агрессивности последующих мероприятий по вторичной профилактике. В настоящее время цереброваскулярные заболевания ввиду общности патогенеза рассматриваются во взаимосвязи с кардиальной патологией в рамках кардионеврологии [15]. Однако данных по изучению факторов, оказывающих влияние на прогноз при развитии ИМ, осложненного сердечной недостаточностью на фоне ХИГМ, в литературе крайне мало.
Систолическая дисфункция ЛЖ, развивающаяся после ИМ, может способствовать усугублению ХИГМ на фоне имеющего атеросклеротического поражения БЦА [12, 15]. Однако, как показывают данные литературы, наличие выраженного брахиоцефального стеноза при этом не является обязательным [16, 17]. По результатам настоящего исследования, ХИГМ у пациентов с ИМ не была связана со стенозирующим каротидным атеросклерозом, а частота визуализации нестенозирующих АСБ оказалась невысокой. Если ранее считалось, что только выраженные стенозы и окклюзии каротидных артерий обладают гемодинамической значимостью, в последние годы доказано, что нет прямой зависимости между степенью их стеноза и клиническими проявлениями ХИГМ [18]. Кроме того, в любом случае, наличие церебрального атеросклероза способно дополнительно ухудшить прогноз у пациентов после перенесенного ИМ [6, 17–19].
Согласно результатам настоящего исследования, годовая летальность в исследуемой группе составила 6,6%, что, вероятно, связано с полнотой реваскуляризации миокарда и наличием оптимальной медикаментозной терапии у большинства пациентов. Проведенный регрессионный анализ показал высокую значимость церебрального атеросклероза, в частности, наличия каротидной АСБ и перенесенного ранее ОНМК для годового прогноза у пациентов с ИМ, развившимся на фоне ХИГМ.
Известно, что развитие острого коронарного синдрома сопровождается изменениями морфологической структуры АСБ и других сосудистых бассейнов. Так, через несколько дней после острого коронарного синдрома в 50% наблюдений отмечались ультразвуковые признаки гетерогенной перестройки АСБ во внутренних сонных артериях, их «активизация» [20]. Этот факт еще раз подтверждает наличие общих патологических механизмов, способствующих возникновению сосудистых катастроф. Как показали результаты, полученные в настоящем исследовании, для когорты пациентов с ХИГМ проявления церебральных сосудистых событий более значимы для отдаленного прогноза, чем низкая ФВ ЛЖ.
Полученные данные согласуются с результатами проспективного исследования CAFES-CAVE, в котором была выявлена значимая связь между увеличением степени брахиоцефальных стенозов и частотой развития кардиальных осложнений, в том числе и у пациентов с ИМ [17]. Так, наличие нестенозирующей каротидной АСБ значимо повышало риск неблагоприятных сердечно-сосудистых событий [21, 22]. Таким образом, ХИГМ может рассматриваться как дополнительный экстракардиальный фактор, способствующий ухудшению прогноза после ИМ с низкой ФВ ЛЖ, в том числе за счет повышенного риска развития ОНМК [23]. В широкомасштабных исследованиях было установлено, что прогрессирующее нарушение систолической функции ЛЖ связано с четырехкратным увеличением риска инсульта [20, 24].
Заключение
У пациентов с ИМ, осложненным СН и ассоциированным с ХИГМ, наибольшее неблагоприятное влияние на отдаленный прогноз оказывают наличие АСБ в каротидном бассейне и перенесенный ранее инсульт. Полученные результаты обусловливают необходимость разработки особых мультидисциплинарных подходов во вторичной профилактике и амбулаторном наблюдении пациентов с низкой ФВ ЛЖ и сопутствующей ХИГМ.
Список литературы Факторы, оказывающие влияние на годовой прогноз при инфаркте миокарда, осложненном левожелудочковой недостаточностью и ассоциированном с хронической ишемией головного мозга
- Бойцов С.А., Шальнова С.А., Деев А.Д. Смертность от сердечно-сосудистых заболеваний в Российской Федерации и возможные механизмы ее изменения. Журнал неврологии и психиатрии им. С.С. Корсакова. 2018;118(8):98-103. DOI: 10.17116/jnevro201811808198.
- Суслина З.А., Варакин Ю.Я. Клиническое руководство по ранней диагностике, лечению и профилактике сосудистых заболеваний головного мозга; 2-е изд. М.: МЕДпресс-Информ; 2017:352.
- Sanchis-Gomar F., Perez-Quilis C., Leischik R., Lucia A. Epidemiology of coronary heart disease and acute coronary syndrome. Ann. Transl. Med. 2016;4(13):256-259. DOI: 10.21037/atm.2016.06.33.
- Kure C.E., Rosenfeldt F.L., Scholey A.B., Pipingas A., Kaye M.D., Bergin P.J. et al. Relationships аmong ^gmt^e function and cerebral blood flow, oxidative stress, and inflammation in older heart failure patients. J. Card. Fail. 2016;22(7):548-559. DOI: 10.1016/j.cardfail.2016.03.006.
- Кашталап В.В., Барбараш О.Л., Коломыцева И.С., Волыкова М.А., Шибанова И.А., Зыков М.В. и др. Прогрессирование мультифокаль-ного атеросклероза после инфаркта миокарда. Кардиология и сердечно-сосудистая хирургия. 2013;6(3):23-28.
- Авилова М.В., Космачева Е.Д. Мультифокальный атеросклероз: проблема сочетанного атеросклеротического поражения коронарного и брахиоцефального бассейнов. Креативная кардиология. 2013; 1:5-13.
- Гарганеева А.А., Округин С.А., Борель К.Н., Кужелева Е.А., Паршин Е.А. Инфаркт миокарда на рубеже двух столетий: демографические и социальные тенденции. Клиническая. медицина. 2016;94(6):463-466. DOI: 10.18821/0023-2149-2016-94-6-463-466.
- McManus D.D., Chinali M., Saczynski J.S., Gore J.M., Yarzebski J., Spencer F.A. et al. 30-year trends in heart failure in patients hospitalized with acute myocardial infarction. Am. J. Cardiol. 2011;107(3):353-359. DOI: 10.1016/j.amjcard.2010.09.026.
- Мареев В.Ю., Фомин И.В., Агеев Ф.Т., Арутюнов Г.П., Баграмбекова Ю.Л., Беленков Ю.Н. и др. Клинические рекомендации. Хроническая сердечная недостаточность. Журнал Сердечная Недостаточность. 2017;18(1):3-40. DOI: 10.18087/rhfj.2017.1.2346.
- Костенко В.А., Ситникова М.Ю., Скородумова Е.А., Федоров А.Н., Скородумова Е.Г. Новая шкала оценки двухлетнего прогноза выживаемости для пациентов, госпитализированных в многопрофильный стационар по поводу острой декомпенсации сердечной недостаточности. Кардиология. 2017;57(6):33-39. DOI: 10.18565/ cardio.2017.6.33-39.
- Brezinov O.P., Klempfner R., Zekry S.B., Sagit B., Goldenberg I., Kuper-stein R. Prognostic value of ejection fraction in patients admitted with acute coronary syndrome: A real world study. Medicine. 2017;96(9):e6226. DOI: 10.1097/MD.0000000000006226.
- Rahmayani F., Paryono I., Setyopranoto I. The role of ejection fraction to clinical outcome of acute ischemic stroke patients J. Neurosci. Rural. Pract. 2018;9(2):197-202. DOI: 10.4103/jnrp.jnrp_490_17.
- Антипенко Е.А., Густов А.В. Хроническая ишемия головного мозга. Современое состояние проблемы. Медицинский совет. 2016;(19): 38-43. DOI: 10.21518/2079-701X-2016-19-38-43.
- Чичкова М.А., Козлова О.С., Аджигитов А.Ю., Чичков А.М. Клинические предикторы развития острого ишемического инсульта у больных с острым инфарктом миокарда. Современные проблемы науки и образования. 2016;5:55-63. URL: http://www.science-education.ru/ru/ article/view?id=25328.
- Фонякин А.В., Машин В.В., Гераскина Л.А., Машин В.Вл. Кардиоген-ная энцефалопатия. Факторы риска и подходы к терапии. Consilium Мedicum. 2012;14(2):5-9.
- Байков В.Ю. Сочетанное атеросклеротическое поражение коронарных и брахиоцефальных артерий - выбор хирургической тактики. Вестник Национального медико-хирургического центра им. Н.И. Пи-рогова. 2013;8(4):108-111.
- Kablak-Ziembicka A., Tracz W., Przewlocki T., Pieniazek P., Sokolow-ski A., Konieczynska M. Association of increased carotid intima-media thickness with the extent of coronary artery disease. Heart. 2004;90(11):1286-1290. DOI: 10.1136/hrt.2003.025080.
- Шмонин А.А., Краснов В.С., Шмонина И.А., Мельникова Е.В. Современная терапия хронического нарушения мозгового кровообращения. Часть 2. Архивъ внутренней медицины. 2014;(4):4-8. DOI: 10.20514/2226-6704-2014-0-4-4-8.
- Чичкова М.А., Козлова О.С., Орлов Ф.В. Особенности сочетания инфаркта миокарда и острого нарушения мозгового кровообращения. Астраханский медицинский журнал. 2016;1:55-63.
- Lam C.S.P., Gamble G.D., Ling L.H., Sim D., Leong K.T.G., Yeo P.S.D.
- et al. Mortality associated with heart failure with preserved vs. reduced ejection fraction in a prospective international multi-ethnic cohort study. Eur. Heart J. 2018;39(20):1770-1780. DOI: 10.1093/eurheartj/ehy005.
- Гарганеева А.А., Кужелева Е.А., Александренко В.А. Популяционное исследование отдаленных исходов острого инфаркта миокарда в Томске. Российский кардиологический журнал. 2017;151(11):27-30. DOI: 10.15829/1560-4071-2017-11-27-30.
- Сумин А.Н., Кухарева И.Н., Трубникова О.А., Коваленко А.В. Стенозы каротидных артерий у больных с ишемическим инсультом: распространенность, выраженность, факторы, ассоциированные с их наличием. Комплексные проблемы сердечно-сосудистых заболеваний. 2013;(3):12-17. DOI: 10.17802/2306-1278-2013-3-12-17.
- Трунова Е.С. Состояние сердца и течение острого периода ишемического инсульта: автореф. дис. ... канд. мед. наук. М.; 2008:28.
- Mathews R., Wang T.Y., Honeycutt E., Henry T.D., Zettler M., Chang M. et al.; TRANSLATE-ACS Study Investigators. Persistence with secondary prevention medications after acute myocardial infarction: Insights from the TRANSLATE-ACS study. Am. Heart J. 2015;170(1):62-69. DOI: 10.1016/j.ahj.2015.03.019.


