Факторы риска и причины развития атипичной несостоятельности эзофагоеюноанастомоза
Автор: Федоров В.Э., Барсуков В.Ю., Поделякин К.А., Масляков В.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Обзоры литературы
Статья в выпуске: 2 т.16, 2021 года.
Бесплатный доступ
Цель. Повышение качества диагностики несостоятельности эзофагоеюноанастомоза после гастрэктомии. Представлено клиническое наблюдение больной раком желудка К., 58 лет. Активная манифестация заболевания началась с профузного желудочного кровотечения, что привело к экстренной операции. Неожиданно в послеоперационном препарате обнаружили анапластический рак желудка. После выписки при контрольной фиброгастроскопии биопсия рубца в желудке повторно верифицировала диагноз. В связи с этим больная уже в плановом порядке вновь поступила на оперативное лечение. Оно состояло в гастрэктомии с еюнопластикой, резекции хвоста поджелудочной железы и лимфодиссекции D2. Результаты. В послеоперационном периоде у пациентки развился поддиафрагмальный абсцесс, его причиной стала несостоятельность пищеводно-тонкокишечного соустья, протекавшая с атипичной клинической картиной. Ключевую роль в развитии несостоятельности сыграла скобка сшивающего аппарата. Заключение. При сочетании множественных факторов риска послеоперационных осложнений после гастрэктомии возможно развитие несостоятельности эзофагоеюноанастомоза с необычной причиной и атипичным течением.
Рак желудка, гастрэктомия, циркулярный сшивающий аппарат, послеоперационные осложнения, несостоятельность анастомоза
Короткий адрес: https://sciup.org/140260102
IDR: 140260102 | DOI: 10.25881/20728255_2021_16_2_146
Risk factors and causes of the development of atypical leakage of the esophagojejunal anastomosis
Purpose. Improving the quality and timeliness of diagnosis of leakage of the esophagojejunal anastomosis after gastrectomy. Methods and materials are presented by the description of a case of examination and treatment of patient K., 58 years old, with a malignant neoplasm of the stomach. The active manifestation of the disease began with profuse gastric bleeding, which led to an emergency operation. Surprisingly, an anaplastic gastric cancer was discovered when examining a postoperative preparation. After discharge with a control fibrogastroscopy performed on an outpatient basis, a biopsy of the scar in the stomach reverified the diagnosis. In this regard, the patient was admitted for surgical treatment in a planned manner. It consisted of gastrectomy with jejunoplasty, pancreatic tail resection and D2 lymphadenectomy. Results. In the postoperative period, the patient developed a subphrenic abscess on the left, the cause of which was the failure of the esophagealsmall intestinal junction, which proceeded with an atypical clinical picture. Risk factors for complications after gastrectomy were identified: a high degree of malignancy of the tumor process, asthenization and anemia after emergency surgery for profuse gastric bleeding. With multiple fibrogastroscopy in this patient, it was found that the key role in the development of leak of esophagojejunostomy was played by the staple bracket used when applying circular esophagojejunostomy. Conclusion. With a combination of multiple risk factors for postoperative complications after gastrectomy, it is possible to develop leakage of esophagojejunal anastomosis with an unusual cause and an atypical course.
Текст научной статьи Факторы риска и причины развития атипичной несостоятельности эзофагоеюноанастомоза
После гастрэктомии встречаются гнойно-воспалительных осложнения с частотой до 86,7% [1–3]. Они представлены абсцессами брюшной полости [4; 5], чаще встречаются после комбинированных хирургических вмешательств [6; 7]. Несостоятельность швов пищеводнокишечного анастомоза является преобладающей причиной летальных исходов после хирургических вмешательств на органах желудочно-кишечного тракта [8; 9]. Её развитию способствует сочетание факторов риска, хотя основное внимание уделяется техническим аспектам [10; 11]. Чаще всего сравнивают механический и ручной способы сшивания пищевода и кишки [12–14]. Натяжение тканей, плохая адаптация сшиваемых поверхностей, прорезывание скобок после извлечения сшивающих аппаратов и другие факторы в таких случаях рассматриваются, как ведущие к осложнениям [14].
Цель исследования : повышение качества диагностики и лечения несостоятельности эзофагоеюноанастомозов после гастрэктомии.
Методы и материалы исследования
Больная К., 58 лет, (история болезни № 16844/620), госпитализирована в хирургическое отделение Дорожной клинической больницы г. Саратова 11.11.2020 г. С марта 2020 г. после еды больная начала ощущать дискомфорт в верхних отделах живота, в июле почувствовала слабость, тошноту, была рвота кофейной гущей. При фиброгастро-скопии (ФГС) выявлена язва желудка до 1,5 см в диаметре. В экстренном порядке пациентке выполнено иссечение субкардиальной язвы желудка. В препарате выявлен анапластический рак, а по линии иссечения язвы обнаружен опухолевый рост.
06.08.2020 при котрольной ФГС были выявлены рубец и инфильтрат, расположенный на малой кривизне желудка в субкардии (Рис. 1). При биопсии диагноз вновь подтвердился.
24.08.2020 г. больная представлена на онкоконсилиум с диагнозом: рак малой кривизны желудка pT4N0M0: реко-

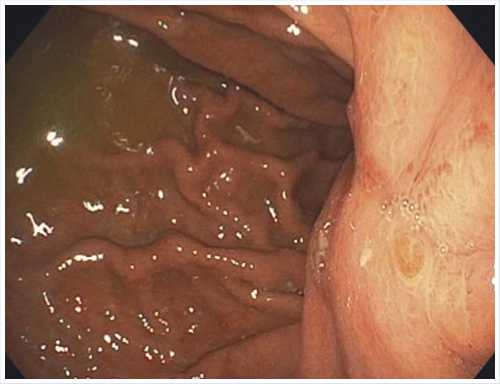
Рис. 1. ФГС больной К., выполненная после экстренной операции: умеренно инфильтрированные ткани вокруг рубца на малой кривизне в субкардии.
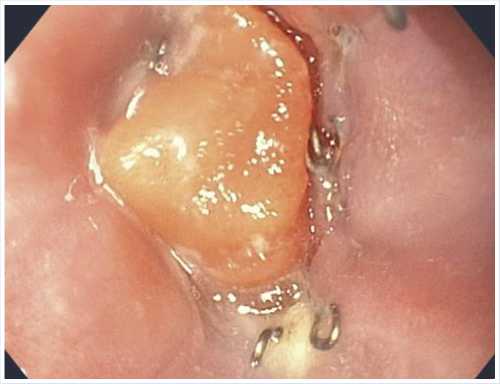
Рис. 2. Контрольная ФГС больной К. 25.11.2020 г.: имеются признаки рубцевания между нижними скобками.
мендована полихимиотерапия, а затем — радикальное хирургическое вмешательство. 12.10.2020 г. курс полихимиотерапии прерван из-за плохого самочувствия. К 13.10.2020 г. состояние больной по ECOG было 0. 11.11.2020 г. при поступлении в хирургическое отделение Дорожной клинической больницы пульс — 75 ударов в мин., ритмичный, АД — 130 и 80 мм рт. ст, частота дыхательных движений (ЧДД) — 16 в мин. Живот был незначительно болезненный в эпигастрии.
16.11.2020 г. больной произведена гастрэктомия с еюнопластикой и резекцией хвоста поджелудочной железы, лимфодиссекция D2. Во время операции эофагоеюноанастомоз наложен «конец в бок» циркулярным сшивающим аппаратом диаметром 21 мм. Еюнопластика выполнена по Hunt-Rodino в виде J-po-uch [16–18]. При интраоперационной цитологии получено подозрение на рак желудка.
На 2-е сутки послеоперационного периода у больной был подъем температуры до 37,8 °С, а затем состояние стало удовлетворительным. На 7 сутки больная выпила 100 мл раствора метиленового синего — из дренажа в левом подреберье краситель не выделялся. На 8 сутки проведена рентгеноскопия желудка — затеков не выявлено. 25.11.2020 г. при ФГС признаков несостоятельности эзофагое-юноанастомоза не выявлено (Рис. 2).
30.11.2020 г. больная выписана на амбулаторное лечение. Через 2 суток у больной повысилась температура до 39 °С, появился озноб. 03.12.2020 паци- ентка вновь госпитализирована в тот же хирургический стационар (история болезни № 17941/662). Ее состояние было тяжелым за счет гипертермии до 39 °C, озноба, интоксикационного синдрома, гипотонии. Острых болей в животе не отмечала. Пульс — 95 ударов в мин., ритмичный, АД — 115 и 68 мм рт. ст. ЧДД — 16 в мин. Живот при пальпации был безболезненный. В общем анализе крови 03.12.2020 г. лейкоцитоз — 14,8·109/л.
Диагноз дифференцировался между флебитом селезеночной вены и несостоятельностью эзофагоеюноанасто-моза с развитием поддиафрагмального абсцесса.
Больная выпила 100 мл раствора метиленового синего — из дренажа в левом подреберье краситель не выделялся.
03.12.2020 при рентгенографии обнаружено высокое стояние левого купола диафрагмы до уровня IV ребра, уплотнение ткани базальных сегментов. Данная картина могла быть обусловлена гиповентиляцией базальных сегментов от сдавления органами брюшной полости. При рентгеноскопии выпитый контраст не выходил за контуры желудка.
03.12.2020 г. на УЗИ селезенка не увеличена, однородная. Селезеночная вена не расширена. По краю селезенки имеется гипоэхогенная зона до 9 мм. В плевральном синусе выпот до 2 см.
Учитывая гипертермию, данные обзорной рентгенографии грудной и брюшной полости, УЗИ, лейкоцитоз, принято решение о вскрытии поддиафрагмального абсцесса в левом подребе- рье. 04.12.2020 г. операция произведена: выделилось 70 мл гнойного отделяемого из полости 9x4x4 см.
09.12.2020 г. больной еще раз произведено рентгенологическое исследование: контраст сразу поступает в петли тонкой кишки, затеков не выявлено.
При ФГС на 24 сутки после гастрэктомии (Рис. 3) установлено, что эзофа-гоэнтероанастомоз диаметром 2,0 см, вместо ранее имеющейся скобки обнаружена лигатура.
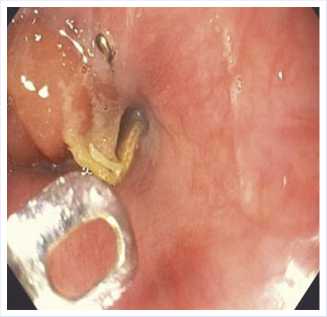
Рис. 3. Контрольная ФГС 10.12.2020 г.: лигатурный абсцесс с фиксированным узлом.
У больной сохранялась гипертермия, поэтому 18.12.2020 выполнена ФГС (Рис. 4).
20.01.2021 г. произведена ререлапаротомия: пищеводно-еюнальный анастомоз находится в спайках и инфильтрированных тканях, визуально перфорации не обнаружено.

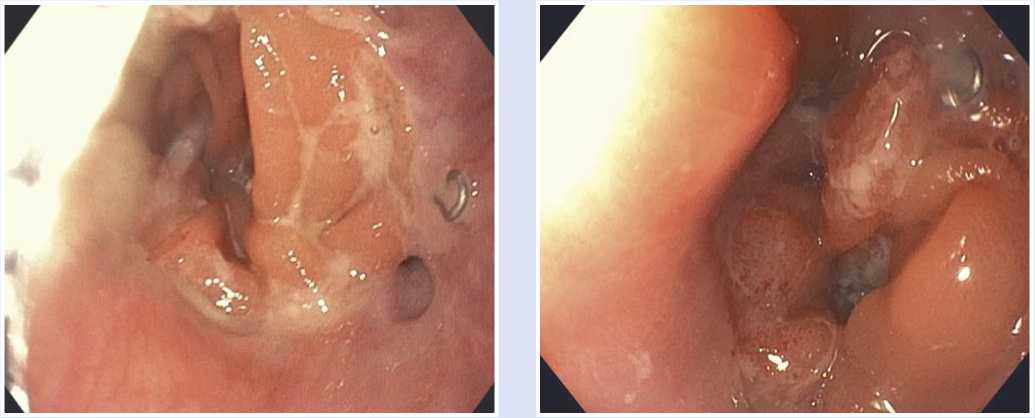
Рис. 4. ФГС больной К. (32-е сутки после гастрэктомии): на месте имевшейся скобки обнаружено перфорация.
Рис 5. ФГС больной К. перед выпиской из стационара (45-е сутки после гастрэктомии): перфоративное отверстие отсутствует.
Результаты
После третьей операции состояние больной стало улучшаться. Температура нормализовалась. При контрольной ФГС 06.01.2021 г. несостоятельности анастомоза не обнаружено (Рис. 5). 11.01.2021 г. больная выписана на амбулаторное лечение.
Обсуждение
В.С. Волков (2010) писал «о значительном изменении структуры послеоперационных осложнений после стандартных и расширенно-комбинированных гастрэктомий с лимфодис-секцией в объеме D2 за счет уменьшения, прежде всего, частоты несостоятельности пищеводно-кишечных анастомозов и увеличения количества гнойно-септических осложнений, превышающих 30%» [19]. В нашем случае она не сразу подтвердилась, а сначала проявился только лигатурный абсцесс пищеводно-кишечного соустья, а затем — поддиафрагмальный гнойник слева. Атипизму клиники способствовала сумма факторов риска. Первым из них стал анапластический рак с прорастанием в жировую клетчатку, что соответствует 3-ей степени злокачественности опухоли и критерию T4 по классификации TNM (8 издание, 2017 г.) [20]. Вторым — нерадикальное экстренное оперативное вмешательство, выполненное на фоне геморрагического шока. Третьим — стала химиотерапия. Четвертый — это объем повторной онкологической операции, выполненной через короткое время после экстренной.
Первый этап несостоятельности, скрытый, длился 16 суток и состоял в инфицировании скобки. Второй — начинался с перфорации пищеводнокишечного соустья и длился 19 суток. Третий — это реабилитация после операций.
Выводы:
-
1. После гастрэктомии при сочетании факторов риска послеоперационных осложнений возможно развитие атипичной несостоятельности эзо-фагоеюноанастомоза, когда скобка сшивающего аппарата стала проводником инфекции.
-
2. Следующим этапом ее развития стало образование подпеченочного абсцесса, а затем, после миграции скобки, возникновение перфорации анастомоза.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
— 2018. — Т. 10. — №1. — С. 4-7. [Ladur AI, Zaika AN, Barguti A, et al. Causes of failure of anastomosis sutures after gastrectomy. Novo-obrazovanie. 2018; 10(1): 4-7. (In Russ).] doi: 10.26435/neoplasm.
v10i1.234.
Список литературы Факторы риска и причины развития атипичной несостоятельности эзофагоеюноанастомоза
- Kotan C, Kisli E, Sonmez R, et al. Noncurative total gastrectomy and oesophagogastrectomy in the treatment of advanced gastric carcinoma in a country with high incidence. Acta Chir Belg. 2005; 105(5): 519-522. doi: 10.1080/ 00015458.2005.11679772.
- Mulholland MW, Doherty GM. Complications in Surgery. Lippincott Williams Wilkins. Philadelphia; Baltimore; N.Y.; L., 200: 396-473.
- Yang YS, Chen LQ, Yan XX, et al. Preservation versus non-preservation of the duodenal passage following total gastrectomy: a systematic review. J. Gastrointest Surg. 2013; 17(5): 877-886.
- Волков В.Е., Волков С.В., Игонин Ю.А. и др. Диагностика и лечение гнойно-септических осложнений у больных, перенесших гастрэк-томию // Вестник Чувашского университета. — 2014. — №2. — С. 199-205 [Volkov VE, Volkov SV, Igonin JuA, et al. Diagnosis and treatment of purulent-septic complications in patients undergoing gastrectomy. Vestnik Chuvashskogo universiteta. 2014; 2: 199-205 (In Russ).]
- Andreollo NA, Lopes LR, Coelho Neto S Postoperative complications after total gastrectomy in the gastric cancer. Analis of 300 patients. ABCD Arq Brus. Chir. Dig. 2011; 24(2): 126-130.
- Давыдов М.И., Тер-Аванесов М.Д. Современная стратегия хирургического лечения рака желудка // Современная онкология. — 2000. — Т. 2. — №1. — С. 4-10. [Davydov MI, Ter-Avanesov MD Modern strategy for surgical treatment of stomach cancer. Sovrem-ennaja onkologija. 2000; 2(1): 4-10. (In Russ).]
- Давыдов М.И., Туркин И.Н., Полоцкий Б.Е. Современная хирургия рака желудка: от D2 к D3 // IX Российский онкологический конгресс: материалы конгресса. — 2005. — С. 41-43 [Davydov MI, Turkin IN, Polockij BE Modern gastric cancer surgery: from D2 to D3. IX Rossijskij onkologicheskij kongress: materi-aly kongressa. 2005: 41-43 (In Russ).]
- Ручкин Д.В., Ян Ц. Еюногастропластика как альтернативный способ реконструкции пищеварительного тракта после гастрэктомии // Хирургия. Журнал им. Н.И. Пирогова. — 2015. — №9. — С. 57-62 [Ruchkin DV, Jan C Eunogastroplasty as an alternative way to reconstruct the digestive tract after gastrectomy. Hirurgija. Zhurnal im. N.I. Pirogova. 2015; 9: 57-62 (In Russ).]
- Oka S, Sakuramoto S, Chuman M, et al. Successful treatment of refractory complete separation of an esophagojejunal anastomosis after laparoscopic total gastrectomy: a case report. BMC Res. Notes. 2017; 10(1): 267. doi: 10.1186/s13104-017-2589-6.


