Факторы риска неудач и эмбрионических потерь при экстракорпоральном оплодотворении
Автор: Рудакова Е.Б., Лобода О.А., Полторака Е.В., Бурова О.М., Пилипенко М.А.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Оригинальные статьи
Статья в выпуске: 4-1 т.23, 2008 года.
Бесплатный доступ
На основании проведенных исследований выяв- лены факторы риска неудач ЭКО, установлена роль хронического эндометрита в генезе неудач ЭКО и значение патологии системы гемостаза для развития эмбрионических потерь.
Экстракорпоральное оплодотворение, хронический эндометрит, патология гемостаза
Короткий адрес: https://sciup.org/14918918
IDR: 14918918 | УДК: 618.177-089.888-06-053.13
Risk factors of failures and embryonic losses under in vitro fertilization
The results of the investigation performed revealed risk factors of failed in vitro fertilization; the role of chronic endometritis in the genesis of unsuccessful attempts of the in vitro fertilization and the importance of hemostasis system pathology for embryonic losses development were established.
Текст научной статьи Факторы риска неудач и эмбрионических потерь при экстракорпоральном оплодотворении
Проблема лечения бесплодия в настоящее время приобретает не только медико-социальное, но и экономическое значение. На сегодняшний день широкое распространение получил метод лечения бесплодия путем экстракорпорального оплодотворения прео-вуляторных ооцитов (ЭКО) и переноса дробящихся эмбрионов в полость матки (ПЭ). Несмотря на постоянное совершенствование данного метода, его эффективность, по данным многоцентровых исследований, сравнительно низкая (20-35%). Согласно данным отчета Всемирного конгресса (WCFS 1995), бла14
гоприятный исход беременности после ЭКО и ПЭ имеет место в 73,1% случаев, у 21% женщин беременность прерывается в период до 18-20 недель [1]. В этом аспекте представляет интерес изучение факторов риска неудач ЭКО и причин эмбрионических потерь.
МАТЕРИАЛ И МЕТОДЫ
Первым этапом исследования был ретроспективный анализ 40 амбулаторных карт пациенток, которые проходили лечение сочетанных форм бесплодия с использованием метода ЭКО. Для изучения структуры причин неудач ЭКО у пациенток учитывались данные клинического, лабораторного, инструментального методов обследования. На втором этапе исследования, с целью оценки роли хронического эндометрита (ХЭ) в генезе неудач ЭКО, было обследовано 34 пациентки, которые готовились к проведению ЭКО после предшествующей неудачной попытки, с помощью клинического, ультразвукового, микробиологического и морфологического [2] методов. ИГХ-исследование биоптатов эндометрия с ХЭ проводилось с использованием моноклональных антител («Novoсastra», UK) к эстрогеновым (ЭР) и прогестероновым (ПР) рецепторам. Интенсивность реакции на ЭР и ПР в ядрах клеток эпителия желез и стромальных клеток оценивалась по методу гистологического счета «quickscore» (Detre S. и соавт., 1995).
Для выявления места в структуре причин эмбриони-ческих потерь нарушений в системе гемостаза (СГ) была проанализирована 21 амбулаторная карта пациенток, имевших прервавшуюся беременность после ЭКО в первом триместре, оценивалось наличие волчаночного антикоагулянта (ВА), состояние сосудисто-тромбоцитарного (спонтанная агрегация и с использованием индукторов) и коагуляционного звеньев гемостаза (АЧТВ, ПТИ, фибриноген, РФМК, XII А-зависимый фибринолиз).
Статистические методы. Количественные данные представлены как среднее ± стандартное отклонение (M±σ). Анализ данных проводился с использованием метода кривых регрессий нелинейного типа; для оценки статистической значимости различий между сравниваемыми группами применялся ранговый непараметрический критерий Манна-Уитни (U тест); для выявления силы корреляционной связи использовались непараметрические коэффициенты корреляции: ранговый Спирмена (rs) и парный Тау Кэндалла (rk). Критический уровень значимости при проверке статистических гипотез в данном ис- следовании принимался равным 0,05. Обработка данных проводилась программой «Statistica 7».
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
По данным уровня ХГ, на 14-й день после ПЭ у 18 пациенток (45%) наступила имплантация, у 22 пациенток (55%) беременность отсутствовала. При анализе причин неудач ЭКО выявлены следующие факторы, которые статистически значимо увеличивают риск несостоявшейся имплантации: возраст женщин старше 35 лет (rk=0,03, р=0,005), сниженный фолликулярный резерв (rk=0,25, р=0,01), полип эндометрия (rk=0,23, р=0,02) и хронический эндометрит (rk=0,24, р=0,02) в анамнезе, доза рФСГ более 250 ед. (rk=0,56, р=0,00), выполнение пункции на 16-17-й день цикла (rk=0,32, р=0,00), перенос эмбриона на 1-2-е сутки после пункции (rk=0,28, р=0,01), число про-пунктированных фолликулов до 5 (rk=0,24, р=0,03), толщина М-эхо эндометрия меньше 8 мм (rk=0,34, р=0,00), отсутствие синдрома гиперстимуляции яичников (rk=0,40, р=0,00). Значимой корреляционной связи между другими факторами и вероятностью
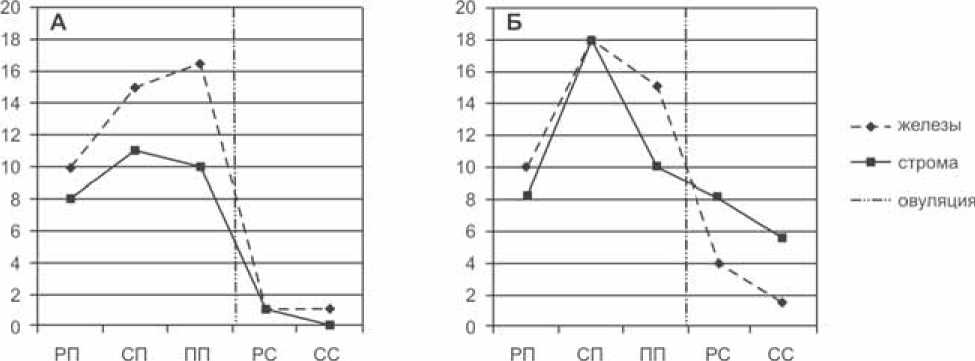
Рис. 1. Показатели экспрессии рецепторов к эстрогену (А) и прогестерону (Б) при ХЭ
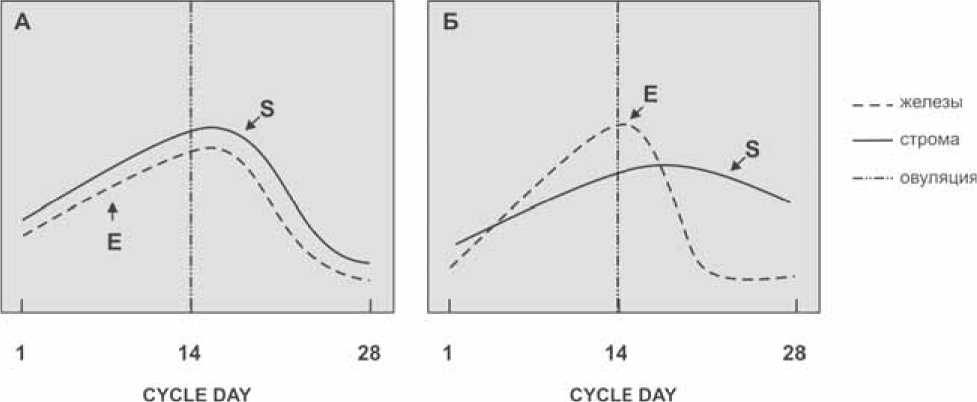
Рис. 2. Динамика экспрессии ER (А) и PR (Б) в нормальном эндометрии (по Moutsasou P., Sekeris C. E. [3])
наступления беременности после ЭКО не выявлено (р>0,05). Из 18 женщин с установленным фактом имплантации по данным ХГ, на УЗИ беременность на 28-й день после ПЭ была подтверждена у 11 женщин (61%), у 7 (39%) отмечались преэмбрионичес-кие потери. При статистическом анализе факторов риска преэмбрионических потерь значимых показателей не выявлено (р>0,05), что свидетельствует о необходимости дальнейшего детального изучения.
Из 34 пациенток, готовящихся к проведению ЭКО после предшествующей неудачной попытки, у 19 (56%) на основании клинико-аппаратного обследования был заподозрен хронический эндометрит. Морфологически ХЭ был выявлен у 25 женщин (74%): у 19 с клиникой ХЭ и у 6 без подозрения на данную патологию. По данным ИГХ-исследования выявлено, что экспрессия ЭР и ПР при ХЭ отличается от таковой в норме (при сравнении с литературными данными [3, 4]) (рис 1, 2). Отмечается смещение пика уровня экспрессии ЭР и ПР в сторону средней и поздней стадий фазы пролиферации (подтверждается при построении диаграмм рассеяния с расчетом кривых регрессий нелинейного типа), в то время как в нормальном эндометрии пик приходится на овуляцию. Было выявлено статистически значимо более раннее истощение рецепторного аппарата: резкое снижение экспрессии рецепторов с началом фазы секреции (при попарном сравнении уровня экспрессии рецепторов в среднюю и позднюю стадии фазы пролиферации с ранней стадией фазы секреции с помощью критерия Манна-Уитни, p<0,05). Наличием данных изменений рецепторного аппарата можно объяснить неспособность половых гормонов обеспечить полноценное циклическое преобразование эндометрия и тем самым подготовить его к приему бластоцисты.
Была оценена эффективность проведения патогенетической терапии в комплексном лечении пациенток с ХЭ путем применения в первой группе (n=5) только этиотропной терапии ХЭ, во второй – этиотропной и патогенетической терапии (n=6). В первой группе эффективность циклов ЭКО составила 20%, во второй – 67%. При сравнительной оценке толщины М-эхо в цикле ЭКО перед переносом эмбриона в первой группе женщин данный показатель составлял 7±1,22 мм, во второй – 10±1,79 мм. Толщина М-ЭХО эндометрия во второй группе женщин была статистически значимо выше, чем в первой (U=0,00, n=11, р<0,05). Выявлена значительная корреляционная связь между толщиной эндометрия и наступлением беременности (rs=0,866; n=11, р<0,001).
При анализе СГ пациенток, имеющих ранние эм-брионические потери, выявлено, что у 6 пациенток (28,5%) наблюдалась гиперагрегация тромбоцитов с гиперкоагуляцией, у 8 (38%) гиперагрегация тромбоцитов сопровождалась отсутствием изменений в коагулограмме, у 6 пациенток (28,5%) гипоагрегация тромбоцитов сочеталась с гиперкоагуляцией, у 1 па-16
циентки (4,8%) была выявлена гипоагрегация при нормальной коагуляции, то есть в данной группе у всех женщин отмечалась патология СГ с преобладанием активации сосудисто-тромбоцитарного и внутрисосудистого звеньев. В исследуемой группе ВА был выявлен у 5 женщин (23,8%), исходя из чего можно предположить, что у остальных женщин патология СГ вызвана другими причинами, в том числе наследственными тромбофилиями (что необходимо подтвердить в последующих исследованиях).
ВЫВОДЫ
Одной из основных причин несостоявшейся имплантации в программе ЭКО является ХЭ. В связи с недостаточной эффективностью клинико-аппаратных методов диагностики ХЭ (чувствительность 76%, специфичность 100%), морфологическое исследование биоптатов эндометрия с применением ИГХ является необходимым звеном в обследовании женщин перед ЭКО после первой неудачной попытки. Патогенетическая терапия является обязательным элементом в комплексном лечении ХЭ, так как при её проведении увеличивается вероятность имплантации за счет устранения морфофункциональных нарушений эндометрия, о чем косвенно свидетельствует его лучший ответ на гормональную стимуляцию в цикле ЭКО.
Ведущей причиной ранних эмбрионических потерь является патология СГ, которая обусловливает неполноценность имплантации и нарушение плацентации [5]. Данный факт свидетельствует о необходимости комплексного исследования СГ у всех женщин, вступающих в программу ЭКО, т.к. своевременная коррекция данной патологии позволит повысить частоту успешных исходов беременности после ЭКО.
Список литературы Факторы риска неудач и эмбрионических потерь при экстракорпоральном оплодотворении
- Экстракорпоральное оплодотворение и его новые направления в лечении женского и мужского бесплодия: Руководство для врачей//под ред. В.И. Кулакова, Б.В. Леонова. -М.: Медицинское информационное агенство, 2000. -782 с.
- Mazur M. Diagnosis of endometrial biopsies and curettings: a practical approach//M. Mazur, R. J. Kurman. -NY.: Springer, 2005. -394 p.
- Moutsasou P., Sekeris C. E. Estrogen and Progesterone Receptors in the Endometrium//Annals of the New York Academy of Science. -1995. -Vol. 816. -P. 99-115.
- Henry N. Jabbour, Rodney W. Kelly, Hamish M. Fraser, Hilary O. D. Critchley Endocrine Regulation of Menstruation//Endocrine Reviews. -2004. -Vol. 27, № 1. -P. 17-46.
- Сидельникова В. М. Привычная потеря беременности: руководство для врачей//М.: ТриадаХ, 2005. -304 с.


