Факторы влияния на выживаемость пациентов с хронической болезнью почек на гемодиализе
Автор: Мелентьева Анастасия Александровна, Барышева Ольга Юрьевна, Тихова Галина Петровна
Журнал: Ученые записки Петрозаводского государственного университета @uchzap-petrsu
Рубрика: Медицинские науки
Статья в выпуске: 6 (151), 2015 года.
Бесплатный доступ
Выявление предикторов летального исхода имеет большое значение для прогноза исхода лечения гемодиализом (ГД) и выбора оптимальной тактики коррекции этих нарушений у больных на ГД, а также профилактики их развития до начала заместительной почечной терапии. Цель настоящей работы - выяснение влияния на выживаемость больных минерально-костных нарушений, оцененных у пациентов, получающих ГД. В ретроспективный анализ были включены 508 больных, в качестве заместительной почечной терапии получавших лечение ГД. Из этой группы была выделена группа пациентов с летальным исходом (162 человека). Длительность лечения ГД составила от 3 месяцев до 21 года (в среднем 4,5 ± 0,4 года). Установлено, что ежегодное количество пациентов, имеющих минерально-костные нарушения на фоне хронической болезни почек (ХБП) и получающих лечение ГД, составляет от 74,4 до 85,6 %. При этом средний уровень фосфора в исследуемой популяции находился в диапазоне от 2,16 до 2,95 ммоль/л, общий кальций от 2,22 до 2,34 ммоль/л. Показано, что высокий риск летального исхода среди обследованных пациентов наблюдался при уровне фосфора 3,0 ммоль/л (р = 0,09), ПТГ 2,5 ммоль/л. Предложена формула для прогностического расчета риска летального исхода в зависимости от стажа ГД для конкретного больного, соответствующего параметрам исследованной популяции.
Хроническая болезнь почек, минерально-костные нарушения, кальций, фосфор, паратиреиодный гормон, выживаемость, смертность
Короткий адрес: https://sciup.org/14750954
IDR: 14750954 | УДК: 616.61-008.64
Survival rate impact factors in patients treated by hemodialysis for chronic kidney disease
Identification of lethal outcome predictors is of great importance for the forecast of possible treatment outcome in case of hemodialysis and a choice of optimum correction tactics in patients treated by dialysis. It is also essential in prophylaxis and control of disorders prior to the replacement kidney therapy. The purpose of the study was to clarify their influence on the survival rate of the invalid mineral and bone violations revealed in the patients treated by hemodialysis. The retrospective analysis included 508 patients treated by hemodialysis as a replacement kidney therapy. A group of patients with lethal outcome (162 persons) was allocated from the control group of patients. The duration of hemodialysis treatment ranged from 3 months to 21 year (on average 4,5 ± 0,4 years). It was established that the annual number of patients with mineral and bone disorders in chronic kidney disease and receiving treatment by hemodialysis raged from 74,4 to 85,6 %. Thus, the average level of phosphorus in the studied population ranged from 2,16 to 2,95 mmol/l, the general calcium - from 2,22 to 2,34 mmol/l. It is shown that the high risk of lethal outcome in the group of examined patients was observed at phosphorus level 3,0 mmol/l (r = 0,09), PTG 2,5 mmol/l. The formula of prognostic lethal outcome calculation, incorporating duration of treatment by hemodialysis for any specific patient, is offered.
Текст научной статьи Факторы влияния на выживаемость пациентов с хронической болезнью почек на гемодиализе
В настоящее время ХБП представляет собой «немую эпидемию» и является существенной проблемой здравоохранения как в России, так и во всем мире, что связано со значительным ростом числа пациентов с ХБП. По данным литературы, признаки ХБП имеет как минимум каждый десятый житель Земли, таким образом, в нашей стране не менее 14 млн человек страдают от патологии почек. Ежегодно увеличивается количество затрат на проведение заместительной почечной терапии (ЗПТ), а также лечение осложнений терминальной стадии хронической почечной недостаточности (тХПН). В рамках системы здравоохранения Medicare США на лечение гемодиализом одного пациента с тХПН в среднем расходуется около 87 945 долл. США, а в России затраты в
течение года на одного пациента составляют не менее 1–1,5 млн руб. [9]. Увеличение продолжительности жизни пациентов с тХПН, получающих ЗПТ, является одним из величайших достижений современной медицины. Однако, несмотря на улучшение технологии проведения диализа, инновации в структуре диализирующих растворов и мембран, разработку новых препаратов для лечения анемии и минерально-костных нарушений (МКН), уровень смертности остается достаточно высоким и составляет более 20 % в год [10].
В течение последних лет с целью идентификации факторов риска неблагоприятного исхода среди данной популяции пациентов были проведены многочисленные исследования.
Лидирующей причиной смерти пациентов с тХБП является сердечно-сосудистая патология [2], [10], [16], [18], на долю которой, по мнению различных авторов, приходится от 40 до 60 %, из которых 20 % составляет внезапная сердечная смерть (ВСС), причем последняя наблюдается в 100 раз чаще у пациентов с ХПН по сравнению с общей популяцией. Риск развития летального исхода при наличии патологии сердечно-сосудистой системы (ССС) у пациентов с ХБП в 10–30 раз выше по сравнению с общей популяцией [2], [7], [10], [16], [19]. При этом ежегодная смертность пациентов на диализе от кардиоваскулярных причин в возрасте 30 лет сопоставима со смертью пациентов в возрастной группе 75–80 лет [2], что позволило отнести пациентов с ХБП к группе высокого сердечно-сосудистого риска. По данным многочисленных исследований, признаки ремоделирования сердца и сосудов отмечаются более чем у половины больных с умеренным снижением функции почек, задолго до необходимости проведения ЗПТ [9].
Преобладание в структуре смертности кардиоваскулярных осложнений связано с наличием у пациентов с тХПН не только традиционных «фремингемских» факторов риска сердечно-сосудистых осложнений (ССО) (возраст, курение, стресс, мужской пол, наличие сахарного диабета, ожирения, артериальной гипертензии, дислипидемии, гиподинамии), но и присутствием нетрадиционных факторов риска, связанных с уремией (продолжительность диализа, анемия, состояние питания, гипергомоцистеинемия, гипоальбумине-мия, нарушения минерально-костного гомеостаза (уровни в сыворотке крови кальция и фосфора, паратиреоидного гормона (ПТГ), нарушение метаболизма витамина D, повышение уровня FGF-23 и экспрессии остеогенных факторов) и кислотнощелочного равновесия, хроническое воспаление, снижение экспрессии фетуина-А). Кроме того, возрастание ССО ассоциировано с отсутствием однозначной доказательной базы в отношении назначения гиполипидемической терапии пациентам с ХБП [2], [3], [18]. Данные факторы достоверно связаны с риском развития и прогрессирования атеросклероза, дестабилизацией атеросклеротической бляшки, развитием миокардиального фиброза и поражения клапанного аппарата сердца [16]. Развитие ИБС, в том числе ОКС, сердечной недостаточности, гипертрофии левого желудочка (ГЛЖ), нарушений миокардиальной структуры и функции – главная причина смерти среди данной популяции пациентов [16]. Кроме того, высокая частота встречаемости ИБС среди пациентов с тХБП обусловлена не только атеросклеротическим поражением сосудов, но и развитием кальциноза медии на фоне дисбаланса между промоутерами и ингибиторами кальцификации, что является одним из проявлений минерально-костных нарушений при ХБП [14]. С развитием острого инфаркта миокарда (ОИМ) у пациентов на ГД связано около 20 % летальных исходов [2].
К факторам риска ССО у пациентов, получающих ЗПТ методом ГД, относятся: артериальная гипертензия (АГ), гипертрофия левого желудочка (ГЛЖ), наличие хронической сердечной недостаточности (ХСН), нарушений ритма, электролитного дисбаланса (калий, магний, кальций) и объемов циркулирующей жидкости [2]. В последнее время большое внимание при оценке сердечно-сосудистого риска у пациентов с ХБП уделяется оценке пульсового давления – как независимому, достоверно влияющему на выживаемость пациентов фактору. В исследовании CREED study было продемонстрировано, что значение пульсового давления ≥ 70 мм рт. ст. было ассоциировано с двукратным возрастанием риска неблагоприятного исхода от ССО по сравнению со значением пульсового давления в пределах 50 мм рт. ст. [8].
Кроме того, в ходе исследований было установлено, что у пациентов, получающих лечение ГД, риск смерти возрастает при наличии повышения уровня С-реактивного белка (СРБ) [1], [18]. Qureshi и соавт. (см. [1]) в своих исследованиях продемонстрировали, что при лечении ГД повышение уровня СРБ наблюдалось значительно чаще у пациентов с диагностированной ИБС, что соответствует современным представлениям о воспалительном генезе развития и прогрессирования атеросклероза.
На долю инфекционных осложнений, связанных с бактериемией и сепсисом, приходится до 20 %, это второе место среди причин смертности пациентов с тХБП [9], [14]. При этом причины смерти, ассоциированные с проведением ЗПТ, включают наличие (в качестве сосудистого доступа) центрального венозного катетера [14], [17], [18] и кальцифицирующей уремической артери-олопатии, развивающейся на фоне нарушений минерально-костного метаболизма. Последняя является редко встречающимся осложнением у пациентов с тХПН (2–5 %) и характеризуется развитием тяжелых некротических поражений кожи и подкожной клетчатки в результате кальцификации медии артерий и артериол, а также высокой летальностью до 80 % вследствие септических осложнений [4], [15].
По данным литературы, наиболее часто выявляемой культурой микроорганизмов в крови пациентов с тХБП является в 28–65 % грамполо-жительная флора (S. aureus) и около 45 % – грам-отрицательная флора. При этом обнаружение грамположительных микроорганизмов, в частности золотистого стафилоккока, связано с более высокими показателями смертности, в первую очередь за счет обнаружения метициллин-резис-тентных штаммов (MRSA) [13], [14].
Влияние демографических показателей – пола и возраста – в развитии неблагоприятных исходов у пациентов с ХБП обсуждается. В последнее время возраст рассматривается как фактор риска неблагоприятного клинического исхода в сочетании с коморбидным фоном (особенно при наличии сахарного диабета) у пациентов с тХПН, получающих лечение ГД, и перестает играть самостоятельную роль [1], [17]. По данным литературы, имеются сообщения о преобладании риска смертельного исхода среди лиц мужского пола по сравнению с женщинами и среди лиц белой расы по сравнению с афроамериканцами [11], [17].
С целью исследования структуры смертности и факторов, влияющих на неблагоприятный прогноз у пациентов с ХБП 5-й стадии, получающих ЗПТ методом ГД, было проведено ретроспективное исследование на базе отделения гемодиализа ГБУЗ «Республиканская больница имени В. А. Баранова».
МАТЕРИАЛЫ И МЕТОДЫ
Ретроспективное исследование включало анализ 508 историй болезни пациентов, получающих лечение хроническим гемодиализом на базе ГБУЗ «Республиканская больница имени В. А. Баранова» за период с 2009 по 2013 год.
На основании анализа данных для оценки структуры смертности и построения кривой дожития в зависимости от стажа ГД была набрана когорта пациентов, состоящая из 162 человек с ХБП 5-й (Д) стадии. Средний возраст больных составил 48,5 ± 1,0 года (min = 19, max = 74 года): из них 83 пациента мужского пола (средний возраст 46,6 ± 1,5 года) и 79 пациентов женского пола (средний возраст 50,4 ± 1,5 года). Средний стаж лечения ГД составил 4,5 ± 0,4 года (min = 3 месяца, max = 21 год). Лечение проводилось на аппаратах фирмы «Fresenius 4008» c использованием капиллярных диализаторов площадью 1,3–2,1 м2 и уровнем кальция диализирующего раствора 1,5 ммоль/л.
Лидирующей причиной развития тХПН, требующей проведения ЗПТ, являлся хронический гломерулонефрит 46,9 % (n = 76), на втором месте – нефропатия неустановленного генеза 11,7 % (n = 19) и диабетическая нефропатия 11,7 % (n = 19), в меньшем процентном соотношении – поликистоз почек 10,5 % (n = 17) и хронический пиелонефрит 6,8 % (n = 11). Хроническая болезнь почек 5-й (Д) стадии в исходе других нозологических причин (гипертонический нефросклероз, вторичный амилоидоз почек, аномалия развития мочевыводящих путей, ишемическая болезнь почек) зарегистрирована у 12,4 % пациентов (n = 20).
Всем пациентам с помощью стандартных методик квалифицированными специалистами лаборатории ГБУЗ «Республиканская больница имени В. А. Баранова» проводилось определение в образцах сыворотки крови концентраций фосфора, общего кальция и паратиреоидного гормона (ПТГ).
Статистическая обработка данных, полученных в результате исследования, включала описа- тельную статистику, для исследования кривых дожития применялась модель пропорциональных рисков Кокса (регрессия Кокса). Результаты описательной статистики представлены в виде среднего значения и ошибки среднего (M ± m) для тех показателей, выборочное распределение которых не имело статистически достоверного различия с нормальным законом распределения (критерий Колмогорова – Смирнова и критерий Шапиро – Уилкса). Статистическая достоверность межгруппового различия частот проверялась по критерию хи-квадрат на уровень значимости 0,05. Для бинарных переменных были рассчитаны абсолютные (N) и относительные (%) частоты. Все расчеты и процедуры статистического анализа данных проводились с помощью программы Statistica версии 10.0, а также пакета программ для статистического анализа StatTools версии 1.0 производства компании «ИнтелТек Лаб».
РЕЗУЛЬТАТЫ
Количество летальных исходов за весь период наблюдения с 2009 по 2013 год (n = 162) составило 24,7 %. Структура смертности пациентов с ХБП 5-й (Д) стадии, получающих лечение ГД на базе ГБУЗ «Республиканская больница имени В. А. Баранова», представлена на рис. 1.
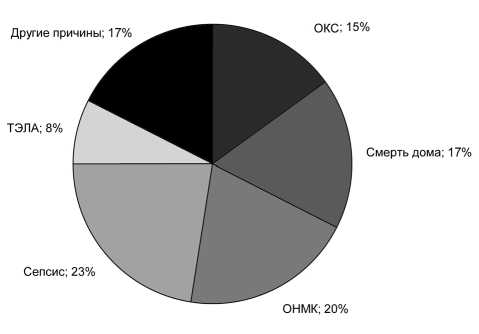
Рис. 1. Структура смертности пациентов с ХБП 5-й (Д) стадии по данным отделения гемодиализа ГБУЗ «Республиканская больница имени В. А. Баранова» за период наблюдения с 2009 по 2013 год
Исходный стаж ГД в исследуемой когорте пациентов составлял от 3 месяцев до 21 года, что позволило применить модель пропорциональных рисков Кокса для построения кривых дожития во всей исследуемой группе пациентов. Результаты представлены на рис. 2.
На линейном участке кривой дожития (интервал стажа ГД от 0 до 18 лет) коэффициент корреляции между стажем ГД и долей выживших пациентов составил 0,98, что позволило применить линейную регрессионную модель для описания зависимости динамики риска летального исхода (%) от стажа ГД (количество лет).
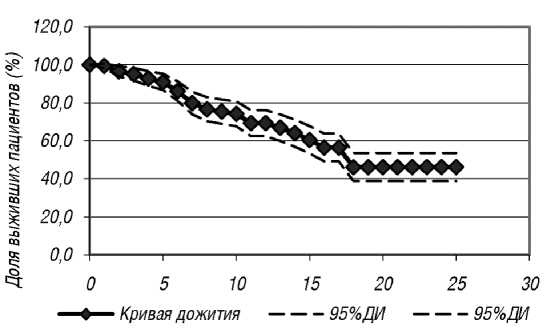
Стаж ГД (лет)
Рис. 2. График кривой дожития пациентов с ХБП 5-й (Д) стадии (n = 162) в зависимости от стажа лечения гемодиализом. Кривая дожития обозначена сплошной линией, пунктирными линиями – верхний и нижний пределы 95 % ДИ
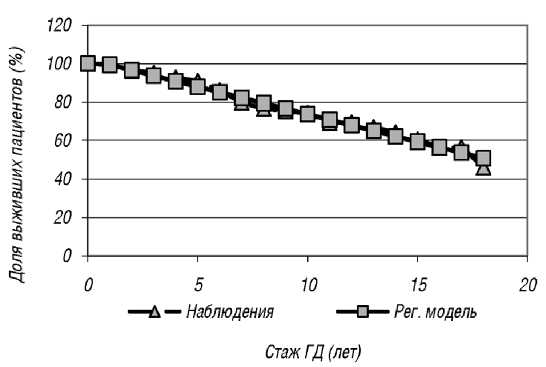
Рис. 3. Сопоставление графика кривой дожития для общей группы исследуемых пациентов (n = 162) в зависимости от стажа лечения ГД с отрезком регрессионной прямой, рассчитанной по линейной регрессионной модели
Регрессионная формула:
Sur = -0,029 х Y + 1,023, где Sur – доля выживших пациентов, Y – стаж ГД в годах.
Оба коэффициента полученной формулы статистически достоверны на уровне значимости 0,0001 по Стьюденту.
Исходя из предложенной модели, можно утверждать, что в данной популяции больных с ХБП каждый год стажа лечения ГД увеличивает риск летального исхода на 2,9 %.
При сопоставлении линейного участка кривой дожития, полученного в результате исследования, и отрезка регрессионной прямой, рассчитанного по линейной регрессионной модели на рис. 3, видно, что эти параметры практически совпадают. Это позволяет предложить полученную формулу в качестве прогностического расчета риска летального исхода в зависимости от стажа ГД для любого конкретного больного, соответствующего параметрам исследованной популяции. Исходя из литературных данных о наличии взаимосвязи между минерально-костными нарушениями и риском неблагоприятного исхода среди пациентов с ХБП 5-й (Д) стадии, с целью изучения влияния фосфора, кальция и ПТГ сыворотки на смертность последние (n = 508) были разбиты на группы в зависимости от лабораторных показателей исследуемых величин. Интервал значений ПТГ у пациентов на гемодиализе выбран в диапазоне от 2 до 9 верхних границ нормального диапазона, что соответствует 130–600 пг/мл или 14,4–66 пмоль/л (согласно нормальным диапазонам концентраций, изложенным в национальных рекомендациях по минеральным и костным нарушениям при ХБП [17]), для общего кальция от ≤ 2,15 до > 2,5 ммоль/л и для фосфора от ≤ 0,81 до > 3,0 ммоль/л. Результаты представлены на рис. 4–6.
Средние концентрации исследуемых величин, влияющих на смертность пациентов с ХБП 5-й
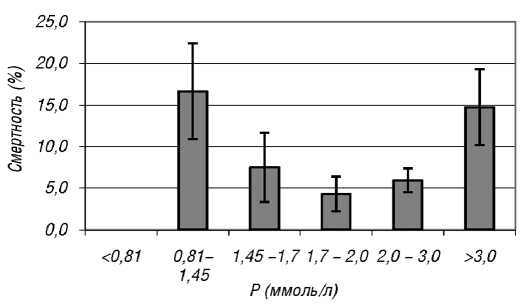
Рис. 4. Влияние различных уровней фосфора сыворотки (ммоль/л) на смертность пациентов с ХБП 5-й стадии, получающих лечение ГД (M ± m)
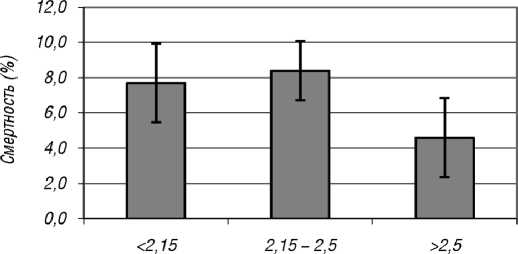
Са (ммоль/л)
Рис. 5. Влияние различных уровней кальция сыворотки (ммоль/л) на смертность пациентов с ХБП 5-й стадии, получающих лечение ГД (M ± m)
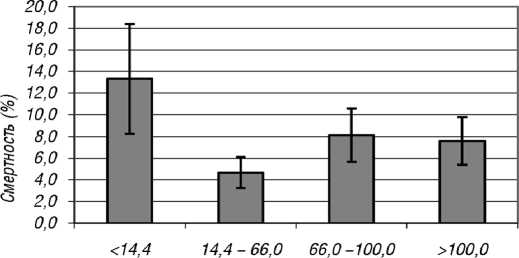
ПТГ (пмоль/л)
Рис. 6. Влияние различных уровней ПТГ сыворотки (пмоль/л) на смертность пациентов с ХБП 5-й стадии, получающих лечение ГД (M ± m)
Средние концентрации (M ± m) уровней фосфора, кальция, ПТГ и доля больных, имеющих минерально-костные нарушения, за период наблюдения с 2009 по 2013 год среди пациентов с ХБП 5-й стадии, получающих лечение ГД
По результатам исследования было установлено, что ежегодное количество пациентов, имеющих минерально-костные нарушения на фоне ХБП и получающих лечение ГД, составляет от 74,4 до 85,6 %. При этом средний уровень фосфора в исследуемой популяции находился в диапазоне от 2,16 до 2,95 ммоль/л, общий кальций от 2,22 до 2,34 ммоль/л, концентрация ПТГ в пределах от 79,03 до 103,17 пмоль/л, что позволяет отнести большинство пациентов с ХБП,
получающих лечение гемодиализом на базе ГБУЗ «Республиканская больница имени В. А. Баранова», к группе высокого риска неблагоприятного исхода. В то же время в ходе исследования было установлено, что не только осложнения тХПН, но и длительность ЗПТ влияют на выживаемость пациентов с тХПН. Предложена формула для прогностического расчета риска летального исхода в зависимости от стажа ГД для конкретного больного, соответствующего параметрам исследованной популяции.
В настоящее время нарушения минеральнокостного обмена и влияние дисбаланса кальция, фосфатов и ПТГ на смертность пациентов с тХПН широко обсуждаются в литературе. Проведенные эпидемиологические исследования демонстрируют прямую зависимость между смертностью пациентов с ХБП и концентрациями кальция, фосфора и ПТГ сыворотки [12]. Своевременная коррекция этих факторов на пред-диализном этапе позволит улучшить прогноз больных с ХБП, получающих заместительную почечную терапию.
* Работа выполнена в рамках Программы стратегического развития ПетрГУ на 2012–2016 гг.
SURVIVAL RATE IMPACT FACTORS IN PATIENTS TREATED BY HEMODIALYSIS FOR CHRONIC KIDNEY DISEASE
Список литературы Факторы влияния на выживаемость пациентов с хронической болезнью почек на гемодиализе
- Бикбов Б. Т., Кирхман В. В., Ушакова А. И. Предикторы летального исхода у больных на гемодиализе//Нефрология и диализ. 2004. № 2. С. 154-163.
- Бокерия Л. А., Ярустовский М. Б., Бокерия О. Л., Биниашвили М. Б. Внезапная сердечная смерть при заболевании почек//Анналы аритмологии. 2009. № 2. С. 39-45.
- Волгина Г., Селезнев Д., Балкарова О. Внекостная кальцификация у пациентов с хронической болезнью почек//Врач. 2012. № 7. С. 2-8.
- Земченков А. Ю., Герасимчук Р. П. Активаторы рецепторов витамина D и сосудистая кальцификация (обзор литературы)//Нефрология и диализ. 2009. № 4. С. 276-289.
- Земченков А. Ю., Герасимчук Р. П. Рекомендации по МКН-ХБП: преемственность, современное состояние и перспективы//Нефрология и диализ. 2011. № 1. С. 20-30.
- Милованова Л. Ю., Милованов Ю. С. Нарушения фосфорно-кальциевого обмена при хронической болезни почек III-V стадий//Клиническая нефрология. 2011. № 1. C. 58-68.
- Смирнов А. В., Добронравов В. А., Каюков И. Г. Кардио-ренальный континуум: патогенетические основы превентивной нефрологии//Нефрология. 2005. № 3. С. 7-15.
- Суворов А. В., Зубеева Г. Н., Обухова С. В. Влияние значений артериального давления на прогноз и выживаемость диализных пациентов//Современные технологии в медицине. 2012. № 2. С. 135-137.
- Швецов М. Ю. Хроническая болезнь почек как общемедицинская проблема: современные принципы нефропрофи-лактики и нефропротективной терапии//Consilium Medicum. 2014. № 7. С. 3-14.
- Block G. A., Klassen P. S., Lazarus J. M. Mineral metabolism, mortality,and morbidity in maintenance hemodialysis//J. Am. Soc. Nephrol. 2004. № 15. P. 2208-2218.
- Bloembergen W. E., Port F. K., Mauger E. A. Causes of death in dialysis patients: racial and gender differences//J. Am. Soc. Nephrol. 1994. Vol. 5. № 5. P. 1231-1242.
- Chertow G. M., Burke S. K., Raggi P. Sevelamer attenuates the progression of coronary and aortic calcification in hemodialysis patients//Kidney International. 2002. Vol. 62. P. 245-252.
- Fram D., Taminato M., Ponzio V. Risk factors for morbidity and mortality of bloodstream infection in patients undergoing hemodialysis: a nested case-control study. Available at: http://www.biomedcentral.com/1756-0500/7/882
- Fusaraki M., Samonis G., Valachis A. Incidence, clinical, microbiological features and outcome of bloodstream infections in patients undergoing hemodialysis//Int. J. Med. Sci. 2013. Vol. 10. № 12. P. 1632-1638.
- National Kidney Foundation. K/DOQI Clinical Practice Guidelines for Bone Metabolism and Disease in Chronic Kidney Disease//Am. J. Kidney Dis. 2003 (suppl. 3). № 42. Р 1-202.
- Petrovic D., Obrenovic R., Trbojevic-Stancovic J. Cardiovascular mortality in hemodialysis patients: clinical and epidemiological analysis//J. Med. Biochem. 2011. Vol. 30. № 4. Р. 302-308.
- Rayner H. C., Pisoni R. L., Bommer J. Mortality and hospitalization in hemodialysis patients in five European countries: results from the Dialysis Outcomes and Practice Patterns Study (DOPPS)//Nephrol. Dial. Transplant. 2004. № 19. P. 108-120.
- Sameiro-Faria M., Ribeiro S., Costa E. Risk factors for mortality in hemodialysis patients: two-year follow-up study//Disease Markers. 2013. Vol. 35. № 6. P. 791-798.
- Stenvinkel P. Chronic kidney disease: a public health priority and harbinger of premature cardiovascular disease//Journal of Internal Medicine. 2010. Vol. 268. P. 456-467.
- Stojceva-Taneva О., Selim Gj., Tozija L. Early mortality rate in end-stage renal disease patients initiating hemodialysis//Contributions, Sec. Biol. Med. Sci. MASA. 2006. Vol. XXVII. № 2. P. 29-35.


