Фенацилтиоцианат: кристаллическая структура, конформационные особенности и антидотная активность продукта конденсации с изатином
Автор: Вячеслав Константинович Киндоп, Александр Валерьевич Беспалов, Виктор Викторович Доценко, Алена Константиновна Смирнова, Владислава Владимировна Шраменко, Владимир Викторович Шарутин
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 4 т.17, 2025 года.
Бесплатный доступ
Фенацилбромид взаимодействует с тиоцианатом калия в ацетоне с образованием фенацилтиоцианата (1), строение которого детально изучено методом рентгеноструктурного анализа (РСА). РСА проводили на дифрактометре D8 Quest фирмы Bruker (MoKα-излучение, λ = 0,71073 Å, графитовый монохроматор) при 293,15 К. Данные РСА: [(1) C9H7NOS, M = 177,22; моноклинная сингония, пр. гр. Р21/c; размер кристалла 0,59 × 0,29 × 0,18 мм; параметры ячейки: a = 10,922(19) Å, b = 5,600(8) Å, c = 15,18(2) Å; β = 105,62(5), V = 894(2) Å3, Z = 4; выч = 1,316 г/см3; = 0,310 мм–1; F(000) = 368,0; обл. сбора по 2q: 7,6–41,2; –10 ≤ h ≤ 10, –5 ≤ k ≤ 5, –14 ≤ l ≤ 15; всего отражений 5869; независимых отражений 909 (Rint = 0,0593); GOOF = 1,047; R-фактор 0,0657]. Квантово-химические расчеты молекулярной геометрии и колебательного спектра фенацилтиоцианата (1) осуществляли в программном пакете ORCA 6.0.1 с использованием гибридного DFT функционала B3LYP с дисперсионной поправкой D4 в валентно-расщепленном базисном наборе def2-TZVP. Выявлены наиболее устойчивые конформеры фенацилтиоцианата (1), проведен сравнительный анализ экспериментальных и расчетных ИК-спектров. Полученный реакцией фенацилтиоцианата 1 с изатином в присутствии триэтиламина 2-оксо-1-(2-оксоиндолин-3-илиден)-2-фенилэтан-1-тиолат триэтиламмония (2) показал умеренно выраженный антидотный эффект в отношении гербицида 2,4-Д в условиях лабораторного эксперимента на проростках подсолнечника сорта Мастер.
Тиоцианатокетоны, тиоцианатоацетофенон, изатин, квантово-химические расчеты, антидотная активность, молекулярная структура, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147252521
IDR: 147252521 | УДК: 547.572.1+546.267.5 | DOI: 10.14529/chem250409
Phenacyl thiocyanate: crystal structure, conformational features and herbicide safening effects of the condensation product with isatin
Phenacyl bromide interacted with potassium thiocyanate in acetone to form phenacyl thiocyanate (1), the structure of which was studied in detail by X-ray diffraction analysis. X-ray analysis was performed on a Bruker D8 Quest diffractometer (MoKα radiation, λ = 0.71073 Å, graphite monochromator) at 293.15 K. The X-ray diffraction data: [(1) C9H7NOS, M = 177.22; monoclinic system, space group Р21/c; crystal size 0.59 × 0.29 × 0.18 mm; cell parameters: a = 10.922(19) Å, b = 5.600(8) Å, c = 15.18(2) Å; β = 105.62(5), V = 894(2) Å3, Z = 4; calc = 1.316 g/cm3; = 0.310 mm–1; F(000) = 368.0; collection area for 2 : 7.6–41.2; –10 ≤ h ≤ 10, –5 ≤ k ≤ 5, –14 ≤ l ≤ 15; total reflections 5869; independent reflections 909 (Rint = 0.0593); GOOF = 1.047; R-factor = 0.0657]. Quantum-chemical studies of the molecular geometry and vibrational spectrum of phenacyl thiocyanate (1) were performed with ORCA 6.0.1 software package using the hybrid DFT functional B3LYP with dispersion correction D4 with split valence basis set def2- TZVP. The most stable conformers of phenacyl thiocyanate (1) have been found, and the experimental and calculated IR spectra have been compared. Triethylammonium 2-oxo-1-(2-oxoindolin-3-ylidene)-2- phenylethane-1-thiolate (2), prepared by the reaction of phenacyl thiocyanate 1 with isatin in the presence of triethylaminem has shown a moderate herbicide safening effect against 2,4-D herbicide in the laboratory experiment on cv. Master sunflower seedlings.
Текст научной статьи Фенацилтиоцианат: кристаллическая структура, конформационные особенности и антидотная активность продукта конденсации с изатином
α-Роданокетоны (α-тиоцианатокетоны) обладают несколькими активными реакционными центрами, что делает эти соединения привлекательными агентами для тонкого органического синтеза [1,2]. Чаще всего роданокарбонильные соединения используются как электрофильные субстраты, которые под действием малононитрила, аминов, гидразинов, восстановителей и проч. превращаются в производные тиазола или 1,3-оксатиолана (например, [3–6]). Намного менее изучено применение α-тиоцианатокетонов в качестве метиленактивных соединений. При этом продукты взаимодействия зачастую подвергаются дальнейшей гетероциклизации с образованием продуктов, который трудно получить иным путем. Так, описано [7–9] азосочетание с роданоке-тонами 1 , приводящее к производным 5-ацил-1,3,4-тиадиазола (схема 1). Реакция 1 с 3-арил-2-цианотиоакриламидами или с ароматическими альдегидами и цианотиоацетамидом [10,11] приводит к функциональным дигидротиофенам 2 . Донорно-акцептоные циклопропаны 3 могут быть получены трехкомпонентной реакцией тиоцианатокетонов с альдегидами и метиленактивными соединениями – например, кислотой Мельдрума [12]. Реакцией фенацилтиоцианатов с 3-формилхромонами недавно были получены 2,4-ди(ароил)тиофены 4 [13], а в реакции с изатином получены 1-(2-оксоиндолин-3-илиден)-2-ароилэтантиолаты 5 [14] либо родственные им сульфиды 6 [15].
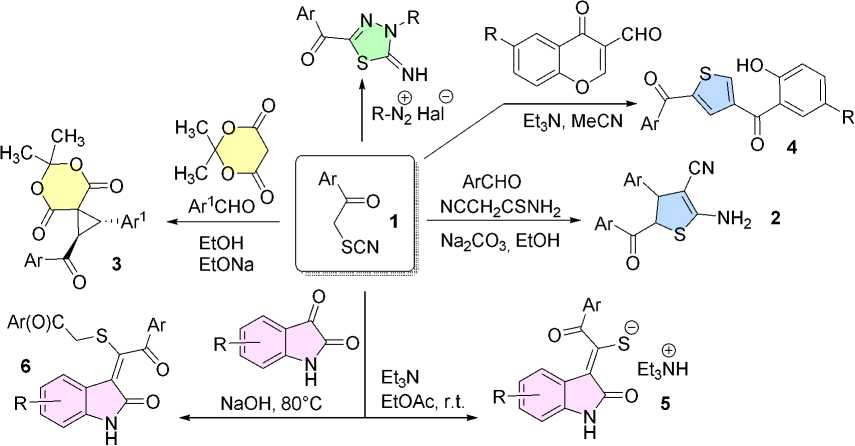
В настоящей работе детально изучено строение родоначального соединения 1 – фенацилтиоцианата. Особенности строения установлены методом РСА и с помощью квантовохимических расчетов. Также показано, что продукт реакции фенацилтиоцианата с изатином обнаруживает антидотное действие в отношении гербицида 2,4-Д в лабораторном эксперименте на проростках подсолнечника.
Экспериментальная частьСинтез фенацилтиоцианата (1).
Растворяли 60,26 г (0,30 моль) α-бромацетофенона в 120 мл ацетона при легком нагревании. В полученный раствор медленно и при перемешивании добавили 30,0 г (0,40 моль) роданида аммония. Смесь перемешивали 5 ч, при этом наблюдалось образование осадка бромида аммония. Далее реакционную массу выливали в пятикратный объем холодной воды, выпавший светложелтый кристаллический осадок отфильтровывали, получали неочищенный фенацилтиоцианат массой 47,01 г (90 %). Для очистки продукт перекристаллизовывали из метанола, либо растворяли в ацетоне, кипятили с активированным углем, отфильтровывали от угля и выливали в трехкратный объем воды. Получали продукт в виде светло-желтых или бесцветных игл, т. пл. 78–80 °С. Спектр ЯМР 1Н (400 МГц, ДМСО- d 6 , δ, м.д., J /Гц): 5,12 с (2Н, СН 2 ); 7,55–7,58 м (2Н, Н Ph); 7,69– 7,73 м (1Н, H Ph); 8,01 д.д (2Н, 3 J = 8,3 Гц, 4 J = 1,2 Гц, H Ph). Спектр ЯМР 13С DEPTQ (101 МГц, DMSO- d 6 , δ, м. д.): 41,8 (CH 2 ), 112,9 (SC≡N), 128,6* (C3H C5H Ph), 129,0* (C2H C6H Ph), 134,28 (C1 Ph), 134,31* (C4H Ph), 192,3 (C=O). *Сигналы в противофазе. ИК спектр, ν, см–1: 2156 (S-C≡N); 1672 (C=O); 1575 (Ar). C 9 H 7 NOS. Вычислено, %: C 61,00, H 3,98, N 7,90. Найдено, %: C 60,82; H 4,01; N 7,77.
Синтез 2-оксо-1-(2-оксоиндолин-3-илиден)-2-фенилэтан-1-тиолата триэтиламмония (2) . К суспензии 1,77 (10 ммоль) α-тиоцианатоацетофенона 1 и 1,47 г (10 ммоль) изатина в 15 мл EtOAc добавляли 1,2 г (12 ммоль) триэтиламина. Смесь интенсивно перемешивали до полного растворения и полной конверсии исходных реагентов (мониторинг методом ТСХ, 12 ч). При этом образовывался оранжевый осадок продукта реакции. Осадок отфильтровывали, промывали EtOAc, диэтиловым эфиром, петролейным эфиром и высушивали при 60 °С. Продукт представляет собой оранжевый порошок, умеренно растворимый в горячем этаноле и горячей воде, хорошо растворимый в ДМСО, ДМФА, плохо растворимый в этилацетате, ацетоне и диэтиловом эфире, петролейном эфире. Спектр ЯМР 1Н (ДМСО- d 6 , δ, м.д., J /Гц): 1,13 (т, 9 Н, 3 NСН 2 С Н 3 ,
-
3 J = 7,1); 3.03 (кв, 6 Н, 3 NС Н 2 СН 3 , 3 J = 7,1); 6,68 (д, 1 Н, H Ar, 3 J = 7,1); 6,80–6,84 (м, 1 Н, H-Ar); 6,91–6,94 (м, 1 Н, H-Ar); 7,34–7,44 (м, 3 Н, 3 H-Ar); 7,78 (д, 2 Н, H2 H6 Ph, 3 J = 7,2); 8,74 (д, 1 Н, H Ar, 3 J = 7,1); 9,56 (уш.с, 1 Н, NH). Спектр ЯМР 13С DEPTQ (ДМСО- d 6 , δ, м.д., J /Гц): 8,8* (3 NCH 2 C H 3 ); 45,7 (3 N C H 2 CH 3 ); 107,4* (C7H индол); 116,8 (=С–S); 119,4* (C5H индол); 120,4* (C6H индол); 123,2* (C4H индол); 127,1 (С3а индол); 127,7* (С3Н С5Н Ph); 129,1* (С2Н С6Н Ph); 131,2* (С4Н Ph); 136,8 (C7a индол); 139,0 (C1 Ph); 166,5 (C=O индол); 184,0 (C3 индол); 192,8 (C=O). *Сигнал в противофазе.
ИК-спектры соединений записывали на ИК-спектрометре Bruker Vertex 70 в режиме НПВО в области 4000–400 см–1.
Спектры ЯМР 1Н и 13С регистрировали на приборе Bruker Avance III HD 400MHz (400,17 и 100,63 МГц соответственно) в растворе ДМСО-d 6 . В качестве стандарта использовали остаточные сигналы растворителя.
Контроль за ходом реакций, определение индивидуальности и идентификации полученных соединений осуществлялись методами ТСХ. Тонкослойную хроматографию проводили в системе: ацетон/петролейный эфир – 3/1 на пластинах Sorbfil-А (ООО «Имид», Краснодар), детектирование – пары йода, УФ-излучение (λ макс = 254 нм).
Температуры плавления определялись в приборе ПТП для определения температуры плавления с открытым капилляром.
РСА кристаллов фенацилтиоцианата 1 проведен на дифрактометре D8 Quest фирмы Bruker (Mo K α-излучение, λ = 0,71073 Å, графитовый монохроматор) при 293,15 К. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT- Plus [16]. Все расчеты по определению и уточнению структуры выполнены по программам SHELXL/PC [17] и OLEX2 [18]. Структуры определены прямым ме-
. Основные кристаллографические данные и результаты уточнения структур приведены в табл. 1, длины связей и валентные углы – в табл. 2.
Длины связей и валентные углы в молекуле фенацилтиоцианата 1
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структуры тиоцианата 1
|
Параметр |
1 |
|
Стехиометрическая формула |
C 9 H 7 NOS |
|
М |
177,22 |
|
Сингония |
Моноклинная |
|
Пространственная группа |
Р 2 1 / с |
|
a , Å |
10,922(19) |
|
b , Å |
5,600(8) |
|
c, Å |
15,18(2) |
|
α , град. |
90,00 |
|
β, град. |
105,62(5) |
|
γ , град. |
90,00 |
|
V , Å3 |
894(2) |
|
Z |
4 |
|
ρ выч, г/см |
1,316 |
|
µ , мм–1 |
0,310 |
|
F (000) |
368,0 |
|
Размер кристалла, мм |
0,59 × 0,29 × 0,18 |
|
Диапазон сбора данных по 2 θ , град. |
7,6–41,2 |
|
Диапазон индексов |
–10 ≤ h ≤ 10, –5 ≤ k ≤ 5, –14 ≤ l ≤ 15 |
|
Число измеренных рефлексов |
5869 |
|
Чисто независимых рефлексов |
909 |
|
R int |
0,0593 |
|
GOOF |
1,047 |
|
Число параметров |
109 |
|
R -факторы по I > 2 σ ( I ) |
R 1 = 0,0391, wR 2 = 0,0737 |
|
R -факторы по всем рефлексам |
R 1 = 0,0657, wR 2 = 0,0833 |
|
Остаточная электронная плотность (max/min), e/A3 |
0,19/–0,15 |
Таблица 2
|
Связь |
d , Å |
Угол |
ω, град. |
|
S1–C9 |
1,691(5) |
C9-S1-C8 |
98,34(18) |
|
S1–C8 |
1,811(4) |
N1-C9-S1 |
176,9(4) |
|
O1–C7 |
1,225(4) |
C7-C8-S1 |
106,8(2) |
|
N1–C9 |
1,144(4) |
O1-C7-C8 |
118,4(3) |
|
C8–C7 |
1,513(5) |
O1-C7-C1 |
122,0(3) |
|
C7–C1 |
1,481(5) |
C1-C7-C8 |
119,6(3) |
|
C1–C2 |
1,388(4) |
C2-C1-C7 |
122,8(3) |
|
C1–C6 |
1,386(5) |
C6-C1-C7 |
118,5(3) |
|
C2–C3 |
1,378(5) |
C6-C1-C2 |
118,7(3) |
|
C3–C4 |
1,375(5) |
C3-C2-C1 |
119,9(3) |
|
C4–C5 |
1,382(5) |
C4-C3-C2 |
121,0(3) |
|
C6–C5 |
1,377(5) |
C3-C4-C5 |
119,6(4) |
|
– |
– |
C5-C6-C1 |
121,2(3) |
|
– |
– |
C6-C5-C4 |
119,6(4) |
Квантово-химические расчеты
Квантово-химические расчеты молекулярной геометрии и колебательного спектра фенацил тиоцианата 1 осуществляли в программном пакете ORCA 6.0.1 [19, 20], с использованием гибридного DFT функционала B3LYP [21, 22] с дисперсионной поправкой D4 [23, 24] в валентно-расщепленном базисном наборе def2-TZVP. Сравнение рассчитанных колебательных частот с экспериментальными осуществляли с учетом поправочного коэффициента 0,9673 [25]. Для расчета энергии различных конформеров в среде ацетона использовали модель проводящего континуума (CPCM) [26]. Для генерации Input-файлов применяли программу Gabedit 2.5 [27]. Для визуализации молекулярной геометрии и колебательных частот использовали программу ChemCraft 1.8.
Методика оценки 2-оксо-1-(2-оксоиндолин-3-илиден)-2-фенилэтан-1-тиолата триэтиламмония 2 на антидотную активность
Проросшие семена подсолнечника сорта Мастер с длиной зародышевого корешка 2–4 мм помещают на 1 ч в раствор 2,4-дихлорфеноксиуксусной кислоты (2,4-Д) в концентрации 10–3 % в расчёте получения 40–60 % ингибирования роста гипокотиле. После гербицидного воздействия проростки промывают водой и помещали в раствор испытываемого на тиолата 2 в концентрациях 10–2, 10–3, 10–4, 10–5 % (вариант гербицид+антидот).
Спустя 1 ч семена промывают водой и раскладывают на полосы фильтровальной бумаги (размер 10×75 см) по 20 штук, которые сворачивают в рулоны и помещают в стаканы с 50 мл воды. Дальнейшее проращивание семян проводят в термостате в течение 3 суток при температуре 28 °С. Температура растворов и промывной воды 28 °С. Семена варианта «гербицид» (эталон сравнения) выдерживают 1 ч в растворе 2,4-Д в концентрации 10–3 % и 1 ч в воде. Семена контрольного варианта 2 часа выдерживают в воде. Повторность опыта трехкратная. В каждой повторности используют по 20 штук семян. Защитный (антидотный) эффект определяют по увеличению длины гипокотиле и корня в варианте гербицид+антидот относительно названных величин в варианте «гербицид» (эталон) в процентах. Статистическая обработка экспериментальных данных проведена с использованием t -критерия Стъюдента при Р = 0,95. Результаты исследований приведены в табл. 3.
Таблица 3
Антидотная активность 2-оксо-1-(2-оксоиндолин-3-илиден)-2-фенилэтан-1-тиолата триэтиламмония (2) к гербициду 2,4-Д на проростках подсолнечника сорта Мастер
|
Препарат |
Концентрация, % |
Длина гипокотиле |
Длина корня |
||
|
мм |
К 2,4-Д, % |
мм |
К 2,4-Д, % |
||
|
Контроль |
0 |
56 |
– |
88 |
– |
|
2,4-Д |
10–3 |
39 |
– |
35 |
– |
|
2,4-Д+ |
10 –2 |
45 |
115* |
47 |
134* |
|
соединение 2 |
10 –3 |
45 |
115* |
49 |
140* |
|
10–4 |
43 |
110* |
54 |
154* |
|
|
10 –5 |
49 |
126* |
45 |
129* |
|
* Различия между вариантами достоверны при Р = 0,95.
Обсуждение результатов
Известно несколько методов синтеза фенацилтиоцианата 1 [1]. Препаративно наиболее удобным представляется подход, основанный на нуклеофильном замещении атома галогена на тиоцианатную группу в реакции α-галогенкетонов с роданидами щелочных металлов или аммония. Несмотря на то, что тиоцианат 1 известен еще с XIX века [28], детали строения и синтетический потенциал в качестве метиленактивного соединения оставались практически не изучены. Фенацилтиоцианат 1 был синтезирован реакцией фенацилбромида с тиоцианатом аммония в кипящем ацетоне. Реакцией изатина с тиоцианатом 1 в этилацетате в присутствии три-этиламина [14, 29] был получен 2-оксо-1-(2-оксоиндолин-3-илиден)-2-фенилэтан-1-тиолат три-этиламмония 2 :
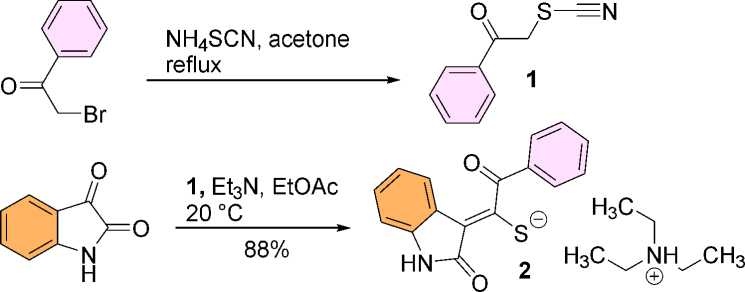
Образцы монокристаллов для проведения РСА могут быть получены перекристаллизацией неочищенного продукта 1 из водного ацетона либо из метанола, при этом соединение 1 выделяется в виде длинных светло-желтых игл, растворимых в ацетоне, хлористом метилене, горячих спиртах, ДМСО, ДМФА, этилацетате, нерастворимых в воде и петролейном эфире. Общий вид молекулы 1 (данные РСА) представлен на рис. 1.
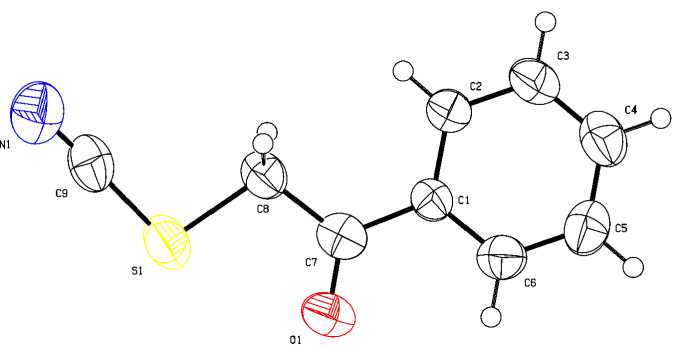
Рис. 1. Общий вид молекулы 1
Предварительный квантово-химический конформационный анализ показал, что молекула фенацилтиоцианата ( 1 ) может существовать в виде четырех различных конформеров, структура которых представлена на рис. 2.
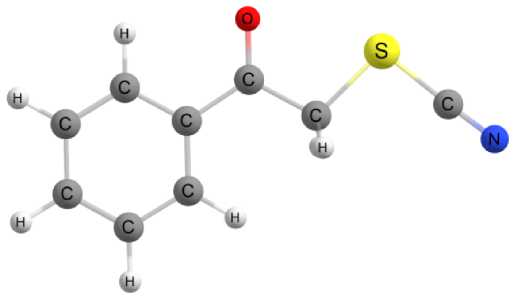
К1 (ΔG = 0 кДж/моль)
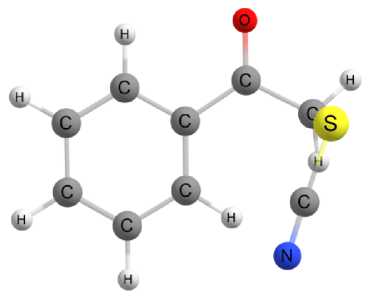
К2 (ΔG = 7,3 кДж/моль)
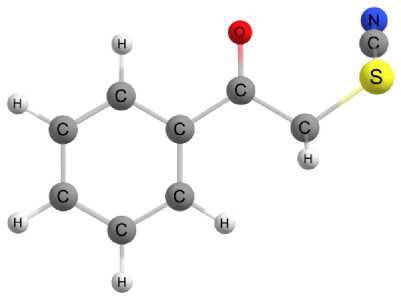
К3 (ΔG = 3,2 кДж/моль)
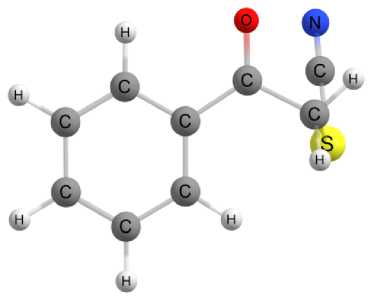
К4 (ΔG = 4,0 кДж/моль)
Рис. 2. Оптимизированные молекулярные структуры наиболее устойчивых конформеров фенацилтиоцианата (1). Расчет на уровне B3LYP-D4/def2-TZVP с использованием модели CPCM для учета влияния растворителя (ацетон)
По данным расчетов, наиболее устойчивым в среде ацетона является конформер К1 , что согласуется с результатами рентгеноструктурного анализа, согласно которым фенацилтиоцианат в кристаллическом состоянии также находится в данной конформации. Следует отметить, что разница в энергии между конформерами К1 , К3 и К4 сравнительно невелика, что указывает на возможность их совместного существования в растворе.
Отнесение полос поглощения в ИК-спектре фенацилтиоцианата ( 1 ) производили на основании результатов квантово-химического расчёта, результаты которого приведены в табл. 4. Как можно заметить, расчётный спектр достаточно хорошо коррелирует с экспериментальным при использовании стандартного поправочного коэффициента, а средняя абсолютная процентная ошибка (MAPE) в определении колебательных частот составляет 1,28 %. Экспериментальный и расчетный ИК-спектры фенацилтиоцианата ( 1 ) представлены на рис. 3 и 4.
Таблица 4
Сравнение экспериментальных колебательных частот в ИК-спектре фенацилтиоцианата (1) с данными квантово-химического расчета
|
Эксперимент, см–1 |
Расчетные полосы поглощения, см–1 |
Отнесение |
|
|
без коэффициента |
с коэффициентом* |
||
|
3057 |
3207 |
3102 |
ν С-H Ar |
|
3038 |
3191 |
3087 |
|
|
2985 |
3112 |
3010 |
ν as СH 2 |
|
2939 |
3063 |
2963 |
ν s СH 2 |
|
2156 |
2260 |
2186 |
ν C≡N |
|
1672 |
1740 |
1683 |
ν C=O |
|
1593 |
1643 |
1589 |
ν C=C Ar |
|
1578 |
1623 |
1570 |
|
|
1448 |
1487 |
1438 |
|
|
1379 |
1446 |
1399 |
δ s СH 2 |
|
1325 |
1345 |
1301 |
скелетные |
|
1296 |
1314 |
1271 |
ω СH 2 |
|
1200 |
1218 |
1178 |
δ пл. С-H Ar |
|
1136 |
1149 |
1111 |
τ СH 2 |
|
997 |
1012 |
979 |
скелетные |
|
885 |
909 |
879 |
ρ СH 2 |
|
756 |
770 |
745 |
δ внепл. С-H Ar |
|
687 |
702 |
679 |
νС-S |
|
629 |
645 |
624 |
скелетные |
|
557 |
576 |
557 |
δCO |
|
415 |
444 |
429 |
δSCN |
|
МАPЕ, % |
3,22 |
1,28 |
– |
– Поправочный коэффициент 0,9673 [25].
Продукт реакции фенацилтиоцианата 1 с изатином, 2-оксо-1-(2-оксоиндолин-3-илиден)-2-фенилэтан-1-тиолат триэтиламмония 2 , был испытан на антидотную активность в отношении гербицида 2,4-Д. Известно, что гербицид 2,4-Д (2,4-дихлорфеноксиуксусная кислота) обладает заметной токсичностью для подсолнечника: доза 15–18 г/га по действующему веществу приводит к 40–60%-ному снижению урожая [30]. Для устранения негативного действия пестицидов на культурные растения используют так называемые антидоты гербицидов (herbicide safeners). После обнаружения Отто Хоффманом в начале 1960-х антидотного эффекта некоторых соединений в отношении гербицида барбан [31] и по текущий момент (обзорные работы см. [32–34]) антидоты гербицидов широко используются в агрохимической практике.
Нами была изучена антидотная активность соединения 2 по отношению к 2,4-Д на проростках подсолнечника в условиях лабораторного эксперимента по известной методике [30]. Установлено, что 2-оксо-1-(2-оксоиндолин-3-илиден)-2-фенилэтан-1-тиолат триэтиламмония 2 обнаруживает умеренно выраженный антидотный эффект и снижает отрицательное действие 2,4-Д на гипокотили проростков подсолнечника на 10–26 %, а на корни проростков – на 29–54 % при использовании в трех и более концентрациях. Результаты антидотной активности 2-оксо-1-(2-оксоиндолин-3-илиден)-2-фенилэтан-1-тиолата триэтиламмония 2 суммированы в табл. 3.
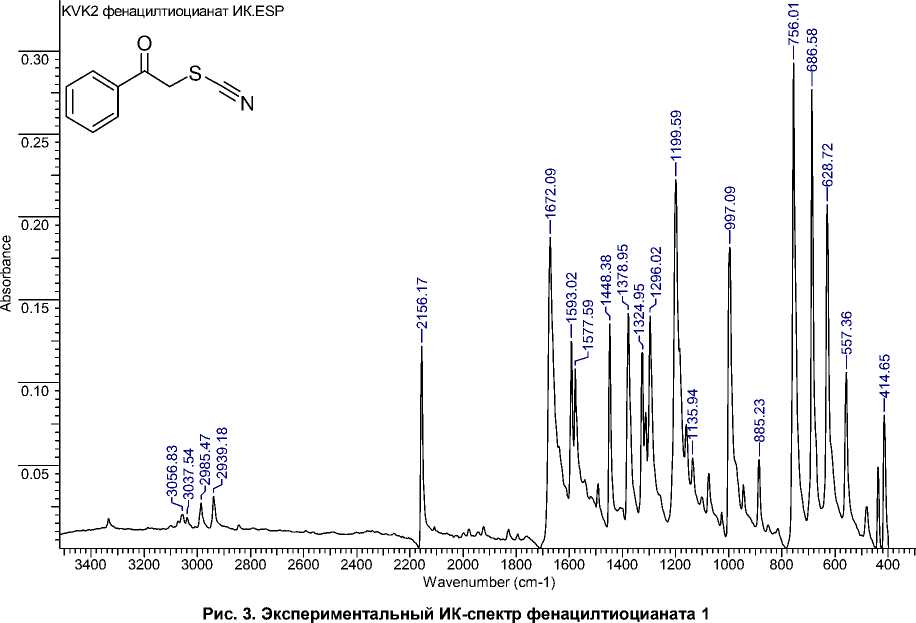
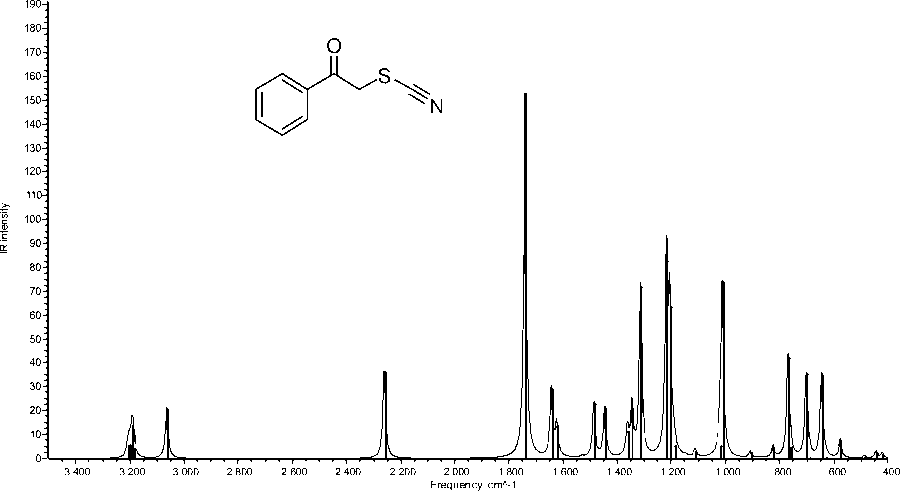
Рис. 4. Рассчитанный на уровне B3LYP-D4/def2-TZVP ИК-спектр фенацилтиоцианата 1
Выводы
Квантово-химическими методами и РСА детально исследовано строение фенацилтиоцианата (1), полученного реакцией фенацилбромида с тиоцианатом калия в ацетоне. Данные квантовохимического расчета оптимальной конформации фенацилтиоцианата коррелируют с данными РСА, расчетный (на уровне B3LYP-D4/def2-TZVP) ИК-спектр хорошо соответствует экспери- ментальному. Продукт реакции фенацилтиоцианата 1 с изатином, 2-оксо-1-(2-оксоиндолин-3-илиден)-2-фенилэтан-1-тиолат триэтиламмония (2), показал умеренный антидотный эффект в отношении гербицида 2,4-Д в условиях лабораторного эксперимента на проростках подсолнечника сорта Мастер.


