Фенольные соединения листьев Tanacetum balsamita L
Автор: Кроль Т.А., Осипов В.И., Балеев Д.Н.
Журнал: Овощи России @vegetables
Рубрика: Садоводство, овощеводство, виноградарство и лекарственные культуры
Статья в выпуске: 6 (74), 2023 года.
Бесплатный доступ
Резюме: Tanacetum balsamita L., многолетнее корневищное растение семейства Asteraceae, относится к пищевым, лекарственным и пряно-ароматическим растениям. Экстракты T. balsamita обладают гепатопротекторным, антисептическим и антигельминтным действием. Надземные части T. balsamita содержат эфирное масло и фенольные соединения. Изучаемый вид входит в состав «Биоколлекции видов лекарственных и ароматических растений открытого и защищенного грунта» Ботанического сада лекарственных растений ФГБНУ ВИЛАР. Цель исследования -изучение качественного состава листьев T. balsamita методом ультра-эффективной жидкостной хроматографии с диодно-матричным детектированием в сочетании с масс-спектрометрией. Объектом исследования были листья T. balsamita, собранные в период цветения. Проводили трехкратную экстракцию 80% ацетоном. Для проведения качественного анализа фенольных соединений использовали ультра-эффективную жидкостную хроматографическую систему, включающую фотодиодный детектор и тройной квадрупольный масс-спектрометр. Идентификация соединений была основана на интерпретации спектральных данных УФи МС-спектров, поиске в доступных базах масс-спектрометрических данных химических соединений и сравнении с литературными данными.
Лекарственные растения, tanacetum balsamita l, ультра-эффективная жидкостная хроматография, фенольные соединения, кофеоилхинные кислоты, флавоноиды
Короткий адрес: https://sciup.org/140303355
IDR: 140303355 | УДК: 633.811:581.543 | DOI: 10.18619/2072-9146-2023-6-66-70
Phenolic compounds in leaves of Tanacetum balsamita L
Tanacetum balsamita L. is a perennial rhizomatous plant of the Asteraceae family. T. balsamita is cultivated as medicinal, aromatic plants and food plant. Extract of costmary exhibits hepato-protective, antiseptic and anthelmintic properties. The herb of T. balsamita contains essential oils and phenolic compounds. This species included in the "Biocollection of medicinal and aromatic plants of open and protected ground", Botanical garden of the VILAR. The main aim was to study the composition of phenolic compounds in the leaves of T. balsamita with application of ultra-performance liquid chromatography coupled with diode array detection and mass spectrometry. The object of the study was the leaves of T. balsamita. Samples were extracted with 1 ml of 80% aqueous acetone. An ultra-performance liquid chromatographic system with a photodiode detector and a triple quadrupole mass spectrometer was used for analysis of phenolic compounds. The UV and MS data of phenolic compounds were used for their identification or tentative characterization with application of mass spectrometry databases and data published in the literature.
Текст научной статьи Фенольные соединения листьев Tanacetum balsamita L
Оригинальная статья / Original article
Forcitation: Krol T.A., Ossipov V.I., Baleev D.N. Phenolic compounds in leaves of Tanacetum bal-samita L. Vegetable crops of Russia. 2023;(6):66-70. (In Russ.)
Р од Tanacetum (Asteraceae), включающий порядка 160 видов, широко распространён в странах с умеренным климатом северного полушария [1, 2]. Многие виды данного рода содержат биологически активные вещества, обладающие антикоагулянтной, противомик-робной и цитотоксической активностью [3, 4, 5]. Некоторые виды обладают антигельминтным, гепатопро-текторным, спазмолитическим и вяжущим действием [6, 7]. Один из представителей данного рода, пижма обыкновенная (Tanаcetum vulgare L.), включен в государственную фармакопею РФ (ФС.2.5.0031.15) [8]. На основе экстракта ее цветков разработан и выпускается препарат Танацехол [9]. Другой вид, пижма бальзамическая (Tanacetum balsamita L.), используется с древних времен в народной медицине многих стран [2, 10]. Ее культиви- руют в качестве пищевого, лекарственного и пряно-ароматического растения [11]. Свежие и сушеные листья используются при приготовлении салатов и в качестве приправы благодаря лимонно-мятному аромату и сладковато-вяжущему вкусу [10].
Tanacetum balsamita L. (syn. Chrysanthemum balsamita (L.) Baill, Balsamita major (L.) Desf) - многолетнее корневищное растение высотой 30-120 см [12, 13]. Листья серовато-зелёного цвета, цельные, овальные или эллиптические, по краю зубчатые. Молодые листья покрыты серебристыми волосками. Нижние листья черешковые, верхние – сидячие. Полушаровидные мелкие корзинки собраны в рыхлое щитковидное соцветие. Плод – семянка [12, 13]. Родина этого растения – Малая Азия. В природе произрастает в Западном и Южном Закавказье, в Армении, на севере Ирана [10].
Надземные части T. balsamita содержат до 1,2% эфирного масла [14]. Эфирное масло включает α-туйон, β -туйон, камфору, транс-хризантенилацетат, 1,8-цинеол и карвон [2, 15]. В настоящее время у T. balsamita выделяют четыре хемотипа: карвоновый, камфорный, камфорно-туйоновый и карвон– α -туйоновый [13]. В листьях присутствуют полифенольные соединения, содержание которых составляет порядка 64,50 мг/100 г [16]. В T. balsamita идентифицировано более 100 вторичных метаболитов [10]. Фенольные соединения представлены гидроксико-ричными кислотами (производные кофеоилхинной кислоты) и флавоноидами (гликозиды апигенина, лютеоли-на, диосметина, акацетина и кверцетина) [2, 16].
На базе Всероссийского научно-исследовательского института лекарственных и ароматических растений имеются коллекции лекарственных и эфирномасличных растений, обладающие уникальным генетический потенциалом, на основе которых создаются новые адаптированные сорта с высоким содержанием биологически активных соединений [17]. Семейство Asteraceae широко представлено в «Биоколлекции видов лекарственных и ароматических растений открытого и защищенного грунта». Изучение химического состава растений, представленных в биоколлекции, является важной и актуальной задачей. Целью нашего исследования было изучение качественного состава листьев T. balsamita , произрастающей в Ботаническом саду лекарственных растений ФГБНУ ВИЛАР, методом ультра-эффективной жидкостной хроматографии с диодно-матричным детектированием в сочетании с масс-спектрометрией (УЭЖХ-ДД-МС).
Материалы и методы
Объект исследований. Объектом исследования были листья T. balsamita , собранные в период цветения в 2019 году. Растения произрастали на территории Ботанического сада лекарственных растений ФГБНУ ВИЛАР. Исследования проводились с использованием биообъектов Уникальной научной установки «Биоколлекции ФГБНУ ВИЛАР».
Подготовка образцов. Охлажденные листья замораживали, лиофильно высушивали (Labconco FreeZone 2.5 L, США) и измельчали (MM 400, Retsch, Германия). Образец сухих листьев массой 15 мг (CPA 225D, Sartorius, Германия) экстрагировали 1 мл 80% ацетона (для хроматографии, Компонент-Реактив, Россия) в течение 60 минут при комнатной температуре и постоянном перемешивании (VORTEX Genie 2, Scientific Industries, США). Экстракт центрифугировали в течение 20 минут при 14000 об/мин (Eppendorf 5430R, Германия) и упаривали досуха при 45°С (концентратор CentriVap, Labconco, США). Экстракция образца трехкратная. Полученный сухой экстракт растворяли в 1 мл деионизованной воды в течение 60 минут, центрифугировали в течение 20 минут при 14000 об/мин, разбавляли в 5 раз деионизованной водой (Direct-Q3, Merck, Германия) и фильтровали (PTFE filter Clean 2, 0,45 µм, Thermo Fisher Scientific, США).
УЭЖХ анализ. Для УЭЖХ-ДД-МС анализа использовали ультра-эффективную жидкостную хроматографическую систему (УЭЖХ, Acquity UPLC® 2.9.0, Waters Corporation, Милфорд, США), которая включала фотодиодный детектор (190-500 нм) и тройной квадрупольный масс-спектрометр Xevo TQ (Waters Corporation, Милфорд, США). В градиентной программе использовали 0,1% муравьиную кислоту (А) и ацетонитрил (Б): 0-0,5 мин, 0,1% Б в А; 0,5-5,0 мин, 0,1-30,0% Б в А (линейный градиент); 5,0-6,0 мин, 30-35% Б в А (линейный градиент). Скорость потока элюента составляла 0,5 мл/мин, объем введённого образца – 5 мкл [18]. Использовали регистрацию отрицательных ионов. Масс-спектрометрические данные анализировали с использованием программы DataAnalysis 4.0.
Идентификация фенольных соединений. Идентификация соединений была основана на интерпретации спектральных данных УФ- и МС-спектров, поиске в доступных базах масс-спектрометрических данных химических соединений (HMDB) [19] и сравнении с литературными данными [10].
Результаты и их обсуждение
В результате проведенного анализа фенольный профиль экстракта из листьев T. balsamita (рис. 1) был представлен 17 соединениями (фенольные кислоты и флавоноиды). Четыре соединения не были идентифицированы (табл.).
Соединения 1, 3, 8, 9 и 11 имели УФ-спектр, характерный для кофейной кислоты с максимумами поглощения в области 244, 297 пл, 325 нм (рис. 2). В масс-спектре соединения 1 присутствовали депротонированный ион [М-Н]- m/z 353 и его димер m/z 707 [2М-Н]-, а также характерный фрагмент с m/z 191, соответствующий иону [Хинная кислота-H]-. Это позволило идентифицировать данное соединение как кофеоилхинную кислоту. Соединение 3 имело ион [M-H]- с m/z 367 и [2M-H]- с m/z 734, что соответствует ферулоилхинной кислоте.
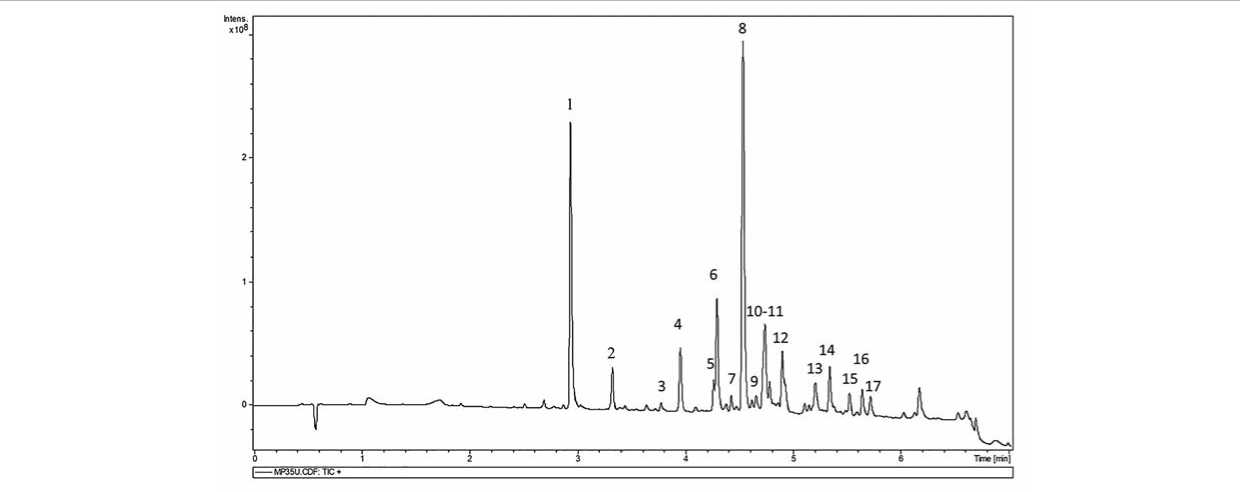
Рис. 1. УЭЖХ-УФ (280 нм) профиль фенольных соединений листьев T.balsamita. Обозначения: 1 – кофеоилхинная кислота; 2 – гексозид феруловой кислоты,изомер 1; 3 – ферулоилхинная кислота; 4 – гексозид феруловой кислоты,изо-мер 2;5 – лютеолин-7-глюкозид;6 – лютеолин-гексуронид;7 – лютеолин-O-гексозид-O-ацетилгексозид;8 – дикофе-оилхинная кислота,изомер 1; 9 – дикофеоилхинная кислота,изомер 2; 10 – лютеолин-7-O-(6 ″ -ацетилглюкозид); 11 – дикофеоилхинная кислота,изомер 3;12 – хризоэриол-гексуронид; 13 – неизвестное соединение; 14 – производное хризоэриола; 15 – неизвестное соединение; 16 – производное лютеолина,17 – спинацетин/аксилларин
Fig. 1. UPLC-UV (280 nm) profile of phenolic compounds ofleaves T.balsamita. Number compounds from Table 1: 1 – caf-feoylquinic acid;2 – ferulic acid hexoside,isomer 1; 3 - feruloylquinic acid; 4 – ferulic acid hexoside,isomer 2;5 - luteolin-7-gluco-side;6 - luteolin-hexuronide;7 – luteolin-O-hexoside-O-acetylhexoside;8 – dicaffeoylquinic acid,isomer 1;9 – dicaffeoylquinic acid, isomer 2; 10 – luteolin-7-O-(6 ″ -acetylglucoside); 11 – dicaffeoylquinic acid,isomer 3; 12 - chrysoeriol-hexuronide; 13 -unknown compound; 14 - chrysoeriol derivative; 15 - unknown compound; 16 - luteolin derivative,17 - spinacetin/axillarin
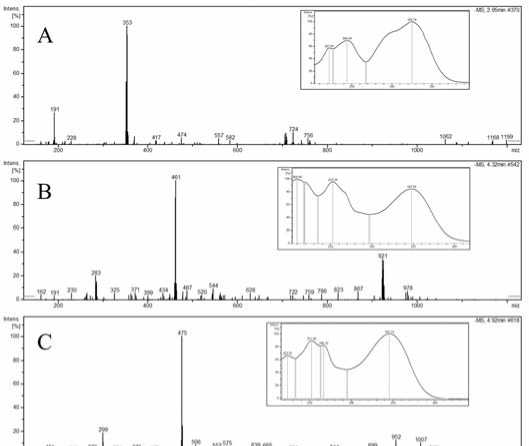
Рис. 2. Примеры МС- и УФ-спектров соединений листьев T. balsamita:
А – кофеоилхинная кислота;В – лютеолин-гексуронид; С – хризоэриол-гексуронид
Fig.2. Examples of MS spectra and UV spectra compounds ofleaves T.balsamita:
A – caffeoylquinic acid; B - luteolin-hexuronide; C - chrysoeriol-hexuronide
Идентификация подтверждается наличием m/z фрагментов 191 и 193, соответствующих хинной и феруловой кислотам.
Анализ масс-спектров соединений 8, 9 и 11 показал наличие основного депротонированного иона [M-H]-сm/z 515, иона [2М-Н]-с m/z 1031 и фрагментов исходного иона с m/z 353 и 191, соответствующих кофеоилхинной и хинной кислотам. Данные соединения были идентифицированы как изомеры дикофеоилхинной кислоты. Для установления их точной структуры необходимы дополнительные исследования. Кофеоилхинные и дикофеоилхинные кислоты обладают широким спектром фармакологиче- ских свойств. Они проявляют противовоспалительную, противоопухолевую, гепатопротекторную, антимикробную и антиоксидантную активность, оказывают нейро-протекторное действие [20].
УФ-спектр соединений 2 и 4 имел максимумы поглощения при 243, 301 и 325 нм. Основными ионами в масс-спектре этих соединений были ионы с m/z 355 и 711, соответствующие [M-H]- и [2M-H]-. Соединения 2 и 4 были идентифицированы как изомеры гексозида феруловой кислоты, что подтверждается присутствием в масс-спектрах m/z фрагмента 193, который соответствует иону [Феруловая кислота-H]-.
Таблица. Результаты УЭЖХ-УФ-МС идентификации фенольных соединений листьев T. balsamita Table. Results of UPLC-UV-MS identification of phenolic compounds in leaves of T. balsamita
|
№ |
Соединение (молекулярная формула) |
Rt, мин. |
УФ макс., нм |
Значение m/z аддукта или фрагмента |
||
|
[M-H]- |
[2M-H]- |
фрагменты |
||||
|
1 |
Кофеоилхинная кислота (С 16 Н 18 О 9 ) |
2.93 |
244; 297пл; 325 |
353 |
707 |
191 |
|
2 |
Гексозид феруловой кислоты (изомер 1) (C 16 H 20 O 9 ) |
3.32 |
229; 302 |
355 |
711 |
193 |
|
3 |
Ферулоилхинная кислота (С 17 Н 20 О 9 ) |
3.77 |
243; 301; 325 |
367 |
734 |
173; 191; 193; 297 |
|
4 |
Гексозид феруловой кислоты (изомер 2) (C 16 H 20 O 9 ) |
3.95 |
237; 294; 319 |
355 |
711 |
193 |
|
5 |
Лютеолин-7-глюкозид (C 21 H 20 O 11 ) |
4.25 |
253; 348 |
447 |
895 |
283; 285 |
|
6 |
Лютеолин-гексуронид (C 21 H 18 O 12 ) |
4.28 |
253; 348 |
461 |
923 |
283; 285 |
|
7 |
Лютеолин-O-гексозид-O-ацетилгексозид (C 29 H 32 O 17 ) |
4.41 |
254; 264; 348 |
651 |
- |
173; 191; 263; 285 |
|
8 |
Дикофеоилхинная кислота (изомер 1) (С 25 Н 24 О 12 ) |
4.52 |
244; 304; 325 |
515 |
1031 |
177; 191; 353 |
|
9 |
Дикофеоилхинная кислота (изомер 2) (С 25 Н 24 О 12 ) |
4,65 |
243; 324 |
515 |
1032 |
191; 353 |
|
10 |
Лютеолин-7-O-(6″-ацетилглюкозид) (C 23 H 22 O 12 ) |
4.71 |
254; 344 |
489 |
- |
175; 246; 283; 285; 325 |
|
11 |
Дикофеоилхинная кислота (изомер 3) (С 25 Н 24 О 12 ) |
4.75 |
251; 329 |
515 |
1031 |
191; 353 |
|
12 |
Хризоэриол-гексуронид (C 22 H 20 O 12 ) |
4.89 |
252; 266; 345 |
475 |
951 |
161; 299 |
|
13 |
Неизвестное соединение |
5.19 |
266; 336 |
487 |
975 |
269; 283; 299; |
|
14 |
Производное хризоэриола |
5.33 |
252; 266; 345 |
517 |
- |
161; 199; 299 |
|
15 |
Неизвестное соединение |
5.51 |
229; 283; 326 |
519 |
- |
301 |
|
16 |
Производное лютеолина |
5.63 |
253; 348 |
531 |
- |
193; 283 |
|
17 |
Спинацетин/аксилларин (C 17 H 14 O 8 ) |
5.70 |
257; 293; 351 |
345 |
- |
300; 315; 330 |
Соединения 5, 6, 7 и 10 имели характерный для лютео-лина УФ-спектр с максимумами поглощения в области 253-254 и 344-348 нм (рис. 2). При изучении масс-спектров данных соединений было установлено присутствие одинакового m/z фрагмента 285, который соответствует m/z агликона лютеолина. В масс-спектре соединения 5 обнаружен ион [M-H]- с m/z значением 447 и его димер с m/z значением 895 [2M-H]-. Данный флавоноид идентифицирован как лютеолин-7-глюкозид, что подтверждается также анализом литературных данных [10]. Соединение 6 идентифицировано как лютеолин-гексуро-нид по наличию в масс-спектре ионов 461 [M-H]- и 923 [2M-H]-. Соединения 7 и 10 идентифицированы как лютео-лин-O-гексозид-O-ацетилгексозид ( m/z 651) и лютеолин-7-O-(6″-ацетилглюкозид) ( m/z 489) соответственно. Соединение 16 дало основной ион с m/z 531. УФ-спектр данного соединения соответствует лютеолину. Точно идентифицировать данное соединение не удалось, возможно это может быть лютеолин-7-[6-O-(2-метилбути-рил)-глюкозид]. Однако для более точной идентификации необходимо проведение дальнейших исследований.
Лютеолин является природным флавоном растений, который чаще всего присутствует в гликозилированной форме. Он обладает антиоксидантными, противоопухолевыми, противовоспалительными, противомикробны-ми, кардиопротекторными, антидиабетическими, нейро-протекторными и противоаллергическими свойствами [21; 22]. Лютеолин-7-О-глюкозид проявляет противовоспалительную активность и противоопухолевую активность (в отношении клеточной линии MCF-7). Он может служить для разработки препаратов при лечении воспалительных заболеваний кожи, а также сердечно-сосудистых заболеваний [22].
УФ-спектр соединений 12 и 14 имел максимумы поглощений в области 252, 266 и 345 нм, что характерно для хризоэриола (рис. 2). Анализ масс-спектра показал присутствие одинакового фрагмента с m/z 299, что соответствует хризоэриолу. Соединение 12 идентифицировано как хризоэриол-гексуронид (m/z 475). Соединение 14 (m/z 517) не удалось идентифицировать, однако, на основании полученных данных, можно предположить, что это производное хризоэриола. Хризоэриол представляет собой флавон, являющийся 3'-метоксипроизводным лютеолина. Обладает широким спектром фармакологической активности: противоопухолевой, противовоспалительной, антибактериальной, противогрибковой и анти-остеопорозной [23].
Соединение 17 имело характерный для флавоноидов УФ-спектр с максимумами поглощения в области 257, 293 и 351 нм. Анализ масс-спектра соединения 17 показал наличие основного депротонированного иона с m/z 345. Данное соединение можно идентифицировать как спинацетин или аксилларин, которые ранее были обнаружены в T. balsamita [10]. Спинацетин представляет собой O-метилированный флавонол.
Заключение
В результате проведенного УЭЖХ-ДД-МС анализа в листьях T. balsamita было обнаружено 17 фенольных соединений, 13 из которых были идентифицированы. Флавоноиды были представлены пятью производными лютеолина, двумя производными хризоэриола и спина-цетином/аксилларином. Фенольные кислоты – кофеоил-хинной, ферулоилхинной и тремя изомерами дикофео-лилхинной кислоты. Были идентифицированы два изомера гексозида феруловой кислоты. В листьях T. balsamita основными соединениями были кофеоилхинная и дико-феоилхинная кислоты. Исходя из полученных результатов в дальнейших исследованиях можно продолжить изучение противовоспалительной активности.
Aboutthe Authors:
Tatiana A.Krol – Cand. Sci. (Agriculture),
, Correspondence Author,
Vladimir I.Ossipov – Dr. Sc. (Biology),
,
Dmitriy N.Baleev – Cand. Sci. (Agriculture),
,
Список литературы Фенольные соединения листьев Tanacetum balsamita L
- Khatib S., Sobeh M., Faraloni C., Bouissane L. Tanacetum species: Bridging empirical knowledge, phytochemistry, nutritional value, health benefits and clinical evidence. Frontiers in Pharmacology. 2023;(14):1169629. DOI: 10.3389/fphar.2023.1169629.
- Bączek K.B., Kosakowska O., Przybył J.L., Pióro-Jabrucka E., Costa R., Mondello L., Gniewosz M., Synowiec A., Węglarz Z. Antibacterial and antioxidant activity of essential oils and extracts from costmary (Tanacetum balsamita L.) and tansy (Tanacetum vulgare L.). Industrial Crops and Products. 2017;(102):154-163. DOI: 10.1016/j.indcrop.2017.03.009.
- Ivănescu B., Tuchiluș C., Corciovă A., Lungu C., Mihai C. T., Gheldiu A. M., Vlase L. Antioxidant, antimicrobial and cytotoxic activity of Tanacetum vulgare, Tanacetum corymbosum and Tanacetum macrophyllum extracts. Farmacia. 2018;66(2):282-288.
- Yapıcı İ., Altay A., Öztürk Sarıkaya B., Korkmaz M., Atila A., Gülçin İ., Köksal E. In vitro Antioxidant and Cytotoxic Activities of Extracts of Endemic Tanacetum erzincanense Together with Phenolic Content by LC ESI QTOF MS. Chemistry & Biodiversity. 2021;18(3):e2000812. DOI: 10.1002/cbdv.202000812.
- Vukic M.D., Vukovic N.L., Obradovic A.D., Galovičová L., Čmiková N., Kačániová M., Matic M. M. Chemical Composition and Biological Activity of Tanacetum balsamita Essential Oils Obtained from Different Plant Organs. Plants. 2022;11(24):3474. DOI: 10.3390/plants11243474.
- Babich O., Larina V., Krol O., Ulrikh E., Sukhikh S., Gureev M. A., Prosekov A., Ivanova S. In Vitro Study of Biological Activity of Tanacetum vulgare Extracts. Pharmaceutics. 2023;15(2):616. DOI: 10.3390/pharmaceutics15020616.
- Ak G., Gevrenova R., Sinan K.I., Zengin G., Zheleva D., Mahomoodally M.F., Senkardes I., Brunetti L., Leone S., Di Simone S.C., Recinella L., Chiavaroli A., Menghini L., Orlando G., Ferrante C. Tanacetum vulgare L. (Tansy) as an effective bioresource with promising pharmacological effects from natural arsenal. Food and Chemical Toxicology. 2021;153:112268. DOI: 10.1016/j.fct.2021.112268.
- Государственная Фармакопея Российской Федерации XIV изд. - М., 2018 [Электронный ресурс]. URL: https://pharmacopoeia.ru/gosudarstvennaya-farmakopeya-14-izdaniya (дата обращения: 15.05.2023).
- Карабаева В.В., Вичканова С.А., Сидельникова Г.Ф., Джумаян А.Р., Терентьева Т.Л. Новый взгляд на результаты применения танацехола в условиях поликлиники. Вопросы биологической, медицинской и фармацевтической химии. 2015;(7):26-29. EDN WAIPYP.
- Gevrenova R., Zengin G., Sinan K.I. Zheleva-Dimitrova D., Balabanova V., Kolmayer M., Voynikov Y., Joubert O. An In-Depth Study of Metabolite Profile and Biological Potential of Tanacetum balsamita L. (Costmary). Plants. 2023;12(1):22. DOI: 10.3390/plants12010022.
- Sharif M., Najafizadeh P., Asgarpanah J., Mousavi Z. In vivo analgesic and anti-inflammatory effects of the essential oil from Tanacetum balsamita L. Brazilian Journal of Pharmaceutical Sciences. 2020; 56. DOI: 10.1590/s2175-97902019000418357.
- Грязнов М.Ю., Тоцкая С.А. Биологические особенности Tanacetum balsamita L. в Нечерноземной зоне России. «Биологические особенности лекарственных и ароматических растений и их роль в медицине». Сборник трудов конференции. М: Щербинская типография; 2016. С. 206-207. EDN WEGURP.
- Hassanpouraghdam M.B., Tabatabaie S.J., Nazemiyeh H., Vojodi L., Aazami M.A., Shoja A.M. Chrysanthemum balsamita (L.) Baill.: a forgotten medicinal plant. Facta Universitatis. Series: Medicine and Biology. 2008; 15(3):119-24.
- Venskutonis P.R. Costmary (Chrysanthemum balsamita) Oils. Essential Oils in Food Preservation, Flavor and Safety. Academic Press. 2016. Р. 365-375. DOI:10.1016/b978-0-12-416641-7.00041-9
- Jaimand K. Rezaee M.B. Chemical constituents of essential oils from Tanacetum balsamita L. ssp. balsamitoides (Schultz-Bip.) Grierson. from Iran. Journal of Essential Oil Research. 2005;17(5):565-566. DOI: 10.1080/10412905.2005.9698996.
- Varga E. , Domokos E., Orbán K., Kursinszki L., Imre B., Tóth G. Antioxidant activity and phenolic composition of costmary (Chrysanthemum balsamita L.) flower. Planta Medica. 2019;(18):P-129. DOI: 10.1055/s-0039-3399854.
- Коротких И.Н., Балеев Д.Н., Морозов А.И., Мизина П.Г., Сидельников Н.И. Селекция лекарственных и ароматических растений в ВИЛАР: достижения и перспективы. Вавиловский журнал генетики и селекции. 2021;25(4):433-441. DOI: 10.18699/VJ21.048. EDN IPVCMM.
- Engstrom M.T., Palijarvi M., Salminen J.P. Rapid fingerprint analysis of plant extracts for ellagitannins, gallic acid, and quinic acid derivatives and quercetin-, kaempferol-and myricetin-based flavonol glycosides by UPLC-QqQ-MS/MS. Journal of agricultural and food chemistry. 2015;63(16):4068-4079. DOI: 10.1021/acs.jafc.5b00595.
- Wishart D.S., Feunang Y.D., Marcu A., Guo A. C., Liang K., Vázquez-Fresno R., Scalbert A. HMDB 4.0: the human metabolome database for 2018. Nucleic acids research. 2018;46(D1):D608-D617. DOI: 10.1093/nar/gkx1089.
- Alcázar Magaña A., Kamimura N., Soumyanath A., Stevens J.F., Maier C.S. Caffeoylquinic acids: Chemistry, biosynthesis, occurrence, analytical challenges, and bioactivity. The plant journal. 2021;107(5):1299-1319. DOI: 10.1111/tpj.15390.
- Aziz N., Kim M. Y., Cho J. Y. Anti-inflammatory effects of luteolin: A review of in vitro, in vivo, and in silico studies. Journal of ethnopharmacology. 2018;225:342-358. DOI: 10.1016/j.jep.2018.05.019.
- De Stefano A., Caporali S., Di Daniele N., Rovella V., Cardillo C., Schinzari F., Minieri M., Pieri M., Candi E., Bernardini S., Tesauro M., Terrinoni A. Anti-inflammatory and proliferative properties of luteolin-7-O-glucoside. International journal of molecular sciences. 2021;22(3):1321. DOI: 10.3390/ijms22031321.
- Aboulaghras S., Sahib N., Bakrim S., Benali T., Charfi S., Guaouguaou F., El Omari E. N., Gallo M., Montesano D., Zengin G., Taghzouti K., Bouyahya A. Health benefits and pharmacological aspects of chrysoeriol. Pharmaceuticals. 2022;15(8):973. DOI: 10.3390/ph15080973.


