Феномен «метаболически здорового ожирения» как состояние латентного риска здоровью
Автор: С.И. Ксенева, О.Ю. Трифонова, Е.А. Пыхтунова, А.А. Золотарев, В.В. Удут
Журнал: Анализ риска здоровью @journal-fcrisk
Рубрика: Медико-биологические аспекты оценки воздействия факторов риска
Статья в выпуске: 1 (52), 2026 года.
Бесплатный доступ
Пристальное внимание клиницистов к феномену «метаболически здорового ожирения» определяется двумя взаимодополняющими позициями: 1) изучаемый фенотип ожирения в условиях действия дополнительных факторов риска может явиться промежуточным звеном перехода к «метаболическому нездоровью»; и если это так, то 2) подобный фенотип представляет собой объект поиска триггеров превенции развития заболевания. Группы анализируемых донозологических состояний были в силу отсутствия биохимически оправданных изменений разделены по индексу массы тела – интегральному признаку состоятельности метаболизма. Это сделано с учетом аксиоматичности многоуровневой организации метаболических процессов, где физиологический оптимум поддерживается таргетно на клеточном уровне, а компенсация нарастающих девиаций требует «подключения» управляющей системы – нейрогуморальной, включая контур вегетативной регуляции, что находит отражение в изменении структур обеспе-чения метаболического гомеостаза. Осуществлена оценка резерва и устойчивости регуляторных метаболических систем в анализе потенциального кардиометаболического риска у лиц с фенотипом «метаболически здорового ожирения». Проведено одномоментное поперечное обследование сплошной выборки здоровых добровольцев в возрасте от 18 до 43 лет с индексом массы тела от 18,5 до 30,0 кг/м2 и верифицированным диагнозом «здоров». Общепринятыми лабораторными методами исследования проводился биохимический анализ крови через час после стандартизованного приема пищи, дополнительно в плазме крови определяли содержание инсулина и кортизола. При оценке реакции метаболического статуса состояния уровня здоровья в качестве универсального раздражителя использована стандартизированная пищевая нагрузка, позволившая выявить максимумы задействованности регуляторов мета-болизма или «напряженность» системы. Проведенный анализ характеристики силы статистической связи между анализируемыми величинами наглядно продемонстрировал, что у здоровых добровольцев с увеличением массы тела и присоединением гиперинсулинемии происходит поступательное вовлечение более «высокого» уровня регуляции обменных процессов: от первого уровня, клеточного, запускающего строго обозначенную конкретную реакцию для достижения определенного физиологического эффекта и определяющего точечный контроль, через органный, характеризующий нарастающее напряжение локальных взаимодействий, к организменному – с формированием физиологических реакций, ориентированных на долговременные эффекты. Нейрогормональное переподчинение регуляции метаболизма при гиперинсулинемии знаменует собой функциональный рубеж в эволюции «метаболически здорового ожирения». Этот процесс является центральным звеном в индивидуальной траектории риска, маркируя переход от состояния компенсированного псевдоздоровья к фазе активного формирования донозологических нарушений. Его выявление и оценка должны составлять основу персонализированной стратификации риска и своевременного профилактического вмешательства.
Метаболически нейтральное ожирение, регуляция обмена веществ, метаболический синдром, сахарный диабет, метаболический фенотип, гормоны, инсулин, кортизол
Короткий адрес: https://sciup.org/142247489
IDR: 142247489 | УДК: 616-092.12 | DOI: 10.21668/health.risk/2026.1.12
Metabolically healthy obesity as a latent health risk
The phenomenon of ‘metabolically healthy obesity’ is of great interest to researchers around the world. This is determined by two complementary standpoints: 1) the investigated obesity phenotype, under exposure to additional risk factors, may represent an intermediate state leading to ‘metabolic unhealthiness’; and 2) if this is true, this phenotype is a research object for searching triggers of diseases prevention. Due to absence of biochemically substantiated changes, groups of analyzed pre-nosologic states were divided per body mass index as an integral sign of metabolism effectiveness. This was made allowing for the obviously multi-level structure of metabolic processes where the physiological optimum as the main target is maintained at the cellular level and compensation for growing deviations requires involvement of the managing nuerohumoral system, vegetative regulation included. This is manifested through changes in structures that support metabolic homeostasis. The aim of this study was to estimate the reserve and stability of regulatory metabolic systems within analyzing potential cardiometabolic risks for people with ‘metabolically healthy obesity’. A single-time cross-sectional study was conducted on a continuous sample of 34 healthy volunteers aged 18 to 43 years with body mass index of 18.5 to 30.0 kg/m2 and a verified diagnosis of ‘healthy’. Using standard laboratory methods, biochemical blood tests were performed one hour after a standardized meal, and insulin and cortisol levels were additionally determined in blood plasma. Standardized food load was used as a universal irritant in estimating changes in the metabolic status as a health measure. This allowed us to reveal the maximum involvement of metabolic regulators or the system ‘tension’. We analyzed strength of statistical relationships between analyzed indicators. The analysis clearly showed that ‘higher’ levels of metabolic regulations steadily became more and more involved in healthy volunteers as their body weight grew and hyperinsulinemia occurred. This involvement grew from the first cellular level that induced a strictly identified specific response aimed at achieving a justified physiological effect and determined point control through the organ level where local interactions became more tensed to the body level where physiological responses occurred with their orientation at long-term effects. When control over metabolism regulation goes to the nuerohumoral system in hyperinsulinemia presence, this means a certain functional mark in evolution of ‘metabolically healthy obesity’. This process is the key link in an individual risk trajectory since it marks the transition from compensated pseudo-health to a phase when prenosologic disorders are formed quite actively. Personalized risk stratification and timely preventive interventions should rely on revealing and estimating this process.
Текст научной статьи Феномен «метаболически здорового ожирения» как состояние латентного риска здоровью
Ксенева Светлана Игоревна – доктор медицинских наук, главный врач клиники (e-mail: ; тел.: 8 (382) 241-88-93; ORCID: .
Трифонова Ольга Юрьевна – доктор медицинских наук, кардиолог клиники (e-mail: ; тел. 8 (382) 241-88-82; ORCID: .
Золотарев Алексей Александрович – аспирант лаборатории физиологии, молекулярной и клинической фармакологии (e-mail: ; тел.: 8 (382) 241-88-82; ORCID: .
Пыхтунова Екатерина Александровна – клинический фармаколог клиники (e-mail: ; тел.: 8 (382) 241-88-82; ORCID: .
Удут Владимир Васильевич – член-корреспондент РАН, доктор медицинских наук, профессор, заместитель директора по научной и лечебной работе (e-mail: ; тел.: 8 (382) 241-83-74; ORCID: .
В научной литературе всё большее распространение получает концепция «метаболически здорового ожирения». Этот термин описывает состояние, при котором у человека имеется избыточная масса тела, но отсутствуют клинически значимые метаболические нарушения (дислипидемия, нарушенная резистентность к инсулину и др.) [1–3]. Согласно данным проспективных исследований, в течение шестилетнего периода от 30 до 40 % лиц с метаболически здоровым фенотипом ожирения трансформируются в категорию с метаболически нездоровым статусом [4]. Полученные результаты свидетельствуют, что феномен «метаболически здорового ожирения» представляет собой, по-види-мому, транзиторное состояние. Под воздействием дополнительных факторов риска оно способно эволюционировать в метаболически нездоровую форму [5, 6]. Механизмы метаболической регуляции у людей с «метаболически нейтральным» ожирением представляют особый научный интерес. В здоровом организме обмен веществ – это саморегулирующаяся система с четкой иерархией. Ключевыми являются три уровня контроля: клеточный – осуществляется через секрецию биологически активных веществ, которые взаимодействуют с рецепторами собственной или соседних клеток; системный – обеспечивает поддержание постоянства внутренней среды органов; организменный – поддерживает гомеостаз за счет интеграции нервной и гуморальной регуляции [7]. Каждый вышестоящий уровень регуляции координирует деятельность нижележащих, активируясь в ответ на изменения внешней среды. Простейшим примером изменения внешней среды может служить стандартный прием пищи, покрывающий базовые потребности человека, при этом механизм метаболической регуляции поддерживает гомеостаз, балансируя три ключевых процесса: приток веществ и энергии в клетку, их депонирование и элиминацию конечных продуктов обмена. Меняется ли иерархия регуляции обмена веществ у лиц с «метаболически нейтральным» ожирением – вопрос, который может лежать в основе этого феномена и, соответственно, методах превенции перехода его в метаболически неблагоприятный статус.
Цель исследования – оценка изменения структур регуляции метаболических процессов у здоровых добровольцев, различающихся массой тела и гормональным статусом, в условиях стандартизированной пищевой нагрузки.
Материалы и методы. Обследование было организовано на клинической базе НИИФиРМ им. Е.Д. Гольдберга ТНИМЦ и представляло собой одномоментное поперечное исследование сплошной выборки. В него были включены 34 условно здоровых добровольца в возрасте 18–43 лет (19 мужчин и 15 женщин). Перед началом работы каждый участник подписал информированное добровольное согласие, одобренное локальным этическим комитетом (протокол № 12 от 28.12.2022), что соответствует принципам Хельсинкской декларации Всемирной медицинской ассоциации.
Отбор участников проводился по следующим критериям: европеоидная раса, отказ от курения за 6 месяцев до исследования, подтвержденное отсутствие соматической патологии по данным комплексного обследования и индекс массы тела в интервале 18,5–30,0 кг/м². Выполнялся стандартный диагностический комплекс: анализ жалоб, сбор анамнеза и физикальный осмотр. В ходе осмотра проводили антропометрию с измерением роста и массы тела для вычисления ИМТ по классической формуле.
Биохимический анализ плазмы крови выполнялся через 60 мин после нагрузки пищей калорийностью 500 ккал. Содержание инсулина и кортизола определялось с помощью коммерческих ИФА-на-боров на ридере Stat Fax 2100 (AWARENESS TECHOLOGY Inc., USA) по протоколам производителей. В частности, уровень инсулина измеряли с использованием тест-системы DRG International, Inc. (Германия). Измерения представлены в мкЕД/мл для инсулина и мкг/дл для кортизола.
Полученные результаты были подвергнуты вариационно-статистическому анализу. Количественные показатели выражены в виде M ± m (среднее арифметическое ± стандартная ошибка среднего). Для определения тесноты связи между параметрами в зависимости от характера их распределения рассчитывали коэффициент корреляции Пирсона ( R ) с соответствующими поправками или коэффициент Спирмена (ρ). Анализу подлежали исключительно сильные корреляции ( R > 0,6), отражающие жесткую линейную зависимость между анализируемыми переменными.
Результаты и их обсуждение. В данную статью включены результаты одномоментного поперечного исследования, в рамках которого обследована сплошная выборка здоровых добровольцев, не имеющих ожирения. Исследование биохимических и гормональных показателей проводилось через час после стандартизованного приема пищи в 500 ккал. Считается, что с 10–15-й мин после прие- ма пищи у здоровых лиц наблюдается выраженное повышение инсулина, что способствует компенсации возникшей гипергликемии, но через 60 мин уже должны регистрироваться нормальные значения глюкозы и инсулина [5]. В проведенном нами исследовании мы получили результат, отличный от ожидаемого, – у 10 добровольцев отмечался повышенный уровень глюкозы, максимально до 8,3 ммоль/л, а у 14 человек уровень инсулина составил от 25 до 85,5 мкЕД/мл. Не представлялось возможности использовать полученные данные для диагностики инсулинорезистентности, так как ее оценка производится по расчетным индексам, основанным на отношениях тощаковых (базальных) значений иммунореактивного инсулина и глюкозы плазмы натощак. Для понимания полученных результатов для анализа данных добровольцы были разделены по индексу массы тела (ИМТ) на две группы: с нормальной массой тела (ИМТ от 18,50 до 24,99 кг/м2) – 13 человек, и с повышенной массой тела (ИМТ выше 25–29,99 кг/м2) – 21 доброволец. По результатам данных гормонального обследования из группы добровольцев с повышенной массой тела была дополнительно выделена еще одна группа – имеющие отклонения в уровне инсулина от референсных значений (табл. 1).
В каждой из трех подгрупп здоровых добровольцев был проведен анализ данных для оценки показателей, характеризующих силу статистической связи между двумя любыми величинами (рис. 1).
У здоровых добровольцев с ИМТ от 18,50 до 24,99 кг/м2 было выявлено восемь положительных корреляционных связей ( R > 0,6, рис. 1), при этом все показанные взаимосвязи объяснимы с точки зрения нормальной физиологии. Понятна взаимосвязь уровня триглицеридов со скрининговыми маркерами функционирования печени: повышение уровня триглицеридов закономерно отражается на показателях работы печени, реализующей энергетическую и пластическую функцию липидов в организме. Повышение уровня глюкозы в крови после приема пищи является физиологическим стимулом для секреции инсулина β-клетками поджелудочной железы, в норме эти два показателя находятся в неразрывной связи [9, 10]. Наблюдаемые корреляции свидетельствуют о механизме точечного контроля: изменения параметров внутренней среды избирательно активируют физиологические процессы, направленные на удовлетворение конкретной потребности и достижение заданного эффекта. Механизм такого контроля является основой метаболической гибкости. В оценке индивидуальных рисков наличие такого паттерна реакций следует интерпретировать как признак адекватного адаптационного ответа и важный позитивный компонент в общей картине функционального состояния организма, снижающий уязвимость к сбоям.
У добровольцев с ИМТ 25,0–29,9 кг/м2 выявлено 17 корреляционных связей ( R > 0,6), три из них – отрицательные (рис. 2).
Таблица 1
Результаты обследования добровольцев в зависимости от индекса массы тела и уровня инсулина
|
Показатель |
Все добровольцы, принявшие участие в исследовании, n = 34 ( M ± m ) |
Добровольцы с ИМТ от 18,50 до 24,99 кг/м2, n = 13 ( M ± m ) |
Добровольцы с ИМТ от 24,99 до 29,99 кг/м2, n = 21 ( M ± m ) |
Добровольцы с ИМТ от 24,99 до 29,99 кг/м2 и уровнем инсулина плазмы более 25 мкЕД/мл, n = 10 ( M ± m ) |
|
Возраст, лет |
30,76 ± 6,5 |
29,24 ± 6,6 |
33,42 ± 5,62 |
34,17 ± 3,87 |
|
Рост, см |
172,61 ± 8,37 |
170,86 ± 7,02 |
175,67 ± 9,92 |
178 ± 10,33 |
|
Вес, кг |
72,64 ± 14,19 |
65 ± 7,87 |
86,0 ± 12,92 |
86,83 ± 14,37 |
|
ИМТ, кг/м2 |
24,21 ± 3,2 |
22,21 ± 1,73 |
27,72 ± 1,78 |
27,2 ± 1,7 |
|
Инсулин, мкЕД/мл |
27,48 ± 19,51 |
24,66 ± 17,16 |
32,4 ± 23,02 |
50,62 ± 18,74 |
|
Кортизол, мкг/дл |
6,44 ± 2,71 |
6,46 ± 3,08 |
6,42 ± 2,04 |
6,4 ± 2,91 |
|
Глюкоза, ммоль/л |
5,72 ± 1,02 |
5,63 ± 0,89 |
5,86 ± 1,26 |
6,53 ± 1,53 |
|
Общий холестерин, ммоль/л |
4,13 ± 0,89 |
3,95 ± 0,69 |
4,45 ± 1,12 |
4,02 ± 0,99 |
|
Триглицериды, ммоль/л |
1,43 ± 0,86 |
1,11 ± 0,58 |
1,99 ± 1,0 |
1,93 ± 0,99 |
|
Аспартатаминотрансфераза, Ед/л |
17,18 ± 7,36 |
15,92 ± 3,91 |
19,38 ± 11,03 |
15,88 ± 1,86 |
|
Аланинаминотрансфераза, Ед/л |
15,84 ± 9,2 |
14,11 ± 7,76 |
18,86 ± 11,01 |
15,87 ± 6,46 |
|
Общий белок, г/л |
65,12 ± 3,04 |
65,54 ± 3,19 |
64,38 ± 2,73 |
63,33 ± 2,28 |
|
Общий билирубин, мкмоль/л |
9,56 ± 6,22 |
10,6 ± 6,97 |
7,74 ± 4,31 |
8,65 ± 5,82 |
|
Мочевина, ммоль/л |
3,55 ± 0,69 |
3,43 ± 0,73 |
3,75 ± 0,61 |
3,63 ± 0,76 |
|
Мочевая кислота, мкмоль/л |
268,48 ± 58,85 |
252,67 ± 49,18 |
296,17 ± 66,07 |
280,67 ± 43,01 |
|
Креатинин, мкмоль/л |
67,55 ± 11,11 |
65,29 ± 10,67 |
71,5 ± 11,2 |
75,33 ± 8,59 |
|
Щелочная фосфатаза, Ед/л |
55,21 ± 20,4 |
53,66 ± 23,79 |
57,93 ± 12,98 |
60,52 ± 13,4 |
|
ГГТП, Ед/л |
18,13 ± 10,65 |
15,97 ± 9,18 |
21,92 ± 12,33 |
22,37 ± 15,75 |
|
Калий, ммоль/л |
4,39 ± 0,31 |
4,43 ± 0,34 |
4,33 ± 0,25 |
4,27 ± 0,19 |
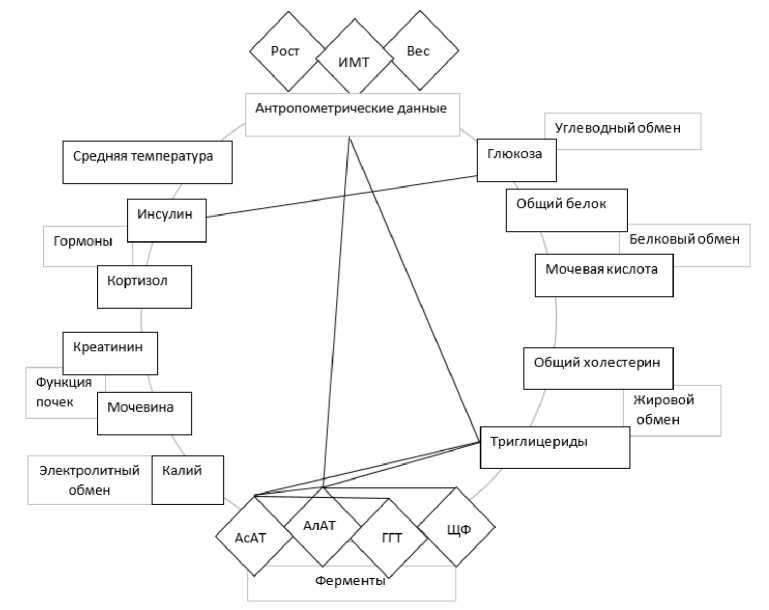
Рис. 1. Корреляционные связи ( R > 0,6) между показателями у здоровых добровольцев с ИМТ 18,5–24,9 кг/м2 (яркими линиями обозначены положительные связи, бледными – отрицательные)
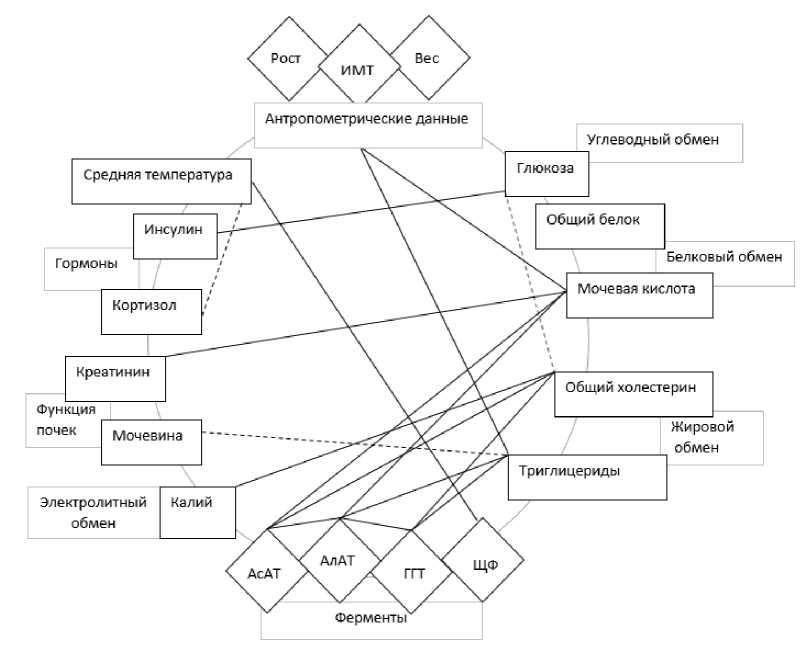
Рис. 2. Корреляционные связи ( R > 0,6) между показателями у здоровых добровольцев с ИМТ 24,9–29,9 (сплошными линиями обозначены положительные связи, пунктирными – отрицательные)
Выявленные корреляции подтверждают глубокую взаимосвязь углеводного, белкового и липидного обменов. Эта интеграция основана на метаболических отношениях, в рамках которых нутриенты служат друг для друга субстратами и продуктами превращений, что обеспечивается единым энергообменом и совпадающими конечными продуктами катаболизма [7]. Процессы биосинтеза белков, липидов и полисахаридов конкурируют за источники энергии. Кроме того, пути их метаболизма тесно переплетены, поскольку используют общие предшественники и промежуточные продукты [11]. Появляются также объяснимые нормальной физиологией взаимосвязи. Концентрация мочевой кислоты, представляющей собой основной метаболит пуринового обмена, обнаруживает корреляцию с антропометрическими данными. Увеличение ИМТ приводит к интенсификации липогенеза, который усиливает функционирование пентозофосфатного пути. Следствием данной активации является накопление ри-бозо-5-фосфата – важнейшего промежуточного соединения для последующего образования пуриновых оснований [12]. Выявленная отрицательная направленность корреляционной связи между уровнем мочевины в плазме крови и триглицеридами в группе здоровых добровольцев с ИМТ 24,9–29,9 кг/м2 можно объяснить доминированием метаболической активности гепатоцитов в отношении липидного обмена над их пластической функцией: синтезом мочевины, являющейся конечным продуктом катаболизма белков. На этом уровне наглядно продемонстрирована центральная роль печени в координации обменных процессов и поддержании гомеостаза [13]. Печень интегрирует метаболические сигналы из системного кровотока и выступает главным регулятором гомеостаза глюкозы и аминокислот. Важнейшим аспектом ее работы является адаптация обмена веществ к характеру питания, которая достигается, в частности, путем направления потоков питательных веществ, в том числе посредством перераспределения потоков питательных веществ между разными органами и тканями [14]. Напряженность тканевых механизмов, направленных на удовлетворение энергетических потребностей организма, проявляется в выявленных взаимосвязях между маркерами катаболизма и показателями основных видов обмена. Так, катаболизм жиров включает в себя липолиз до глицерина и жирных кислот для дальнейшего ресинтеза триглицеридов или включение продукта его окисления в гликолиз или в глюконеогенез [15], поэтому неожиданным оказалось выявление отрицательной корреляционной взаимосвязи между уровнем глюкозы крови и концентрацией общего холестерина. Вероятно, у здоровых добровольцев отмечается более длительное, чем в группе добровольцев с нормальным ИМТ, но все же физиологическое повышение уровня глюкозы после приема пищи, однако механизм потребления ее избытка инсулинзависимыми тканями не нарушен. Полученные данные свиде- тельствуют, что у лиц с избыточной массой тела сохранена физиологическая способность к утилизации глюкозы, однако регуляция этого процесса требует большего функционального напряжения метаболических и управляющих систем. Наблюдаемые корреляции отражают компенсаторную мобилизацию резервов для поддержания гомеостаза. Подобное состояние повышенного функционального напряжения можно рассматривать как маркер снижения адаптационного резерва и, вследствие этого, фактор потенциального риска срыва компенсации при дополнительной нагрузке.
В группе добровольцев с ИМТ 25,0–29,9 кг/м2 и уровнем инсулина более 25 мкЕД/мл выявлено 46 корреляционных связей ( R > 0,6), при этом 18 – отрицательных (рис. 3).
Обнаружены множественная взаимосвязь уровня мочевины с обменными процессами, отражающая общий конечный путь диссимиляции для углеводного, липидного и белкового обменов. Метаболический путь окисления ацетил-КоА в цикле трикарбоновых кислот выполняет две фундаментальные функции. В ходе этого цикла генерируются восстановительные эквиваленты (НАД∙Н и НАДФ∙Н), которые направляются в дыхательную цепь для производства АТФ, при этом конечным продуктом окисления является CO 2 . Углекислый газ является важным строительным блоком для последующих реакций анаболизма, включая образование малонил-КоА для синтеза жирных кислот, а также биосинтез мочевины, пуринов и пиримидинов. Таким образом, мочевина является тем метаболитом, который непосредственно связывает конечные продукты обмена основных нутриентов – углекислый газ и аммиак.
В дополнение к выявленным ранее появляются дополнительные множественные связи между показателями обменов веществ и биохимических печеночных тестов. Принимая во внимание, что у данных добровольцев отмечается повышенный уровень инсулина, что отличает их от добровольцев первых двух групп, стоит акцентировать внимание на анаболическом эффекте инсулина, способствующего синтезу и накоплению гликогена и жира в тканях. Регуляторная функция инсулина проявляется в стимуляции потребления и окисления глюкозы, а также в усилении синтеза гликогена, одновременно с чем он угнетает гликогенолиз и глюконеогенез. Наряду с влиянием на углеводный обмен, инсулин активизирует липогенез из метаболитов углеводов и подавляет процесс липолиза, тем самым регулируя и жировой обмен [16]. Способствуя утилизации глюкозы, инсулин также создает субстратную базу для про-теиногенеза, ускоряя синтез белков из производных углеводного обмена. Совместное действие этих механизмов реализует гипогликемический эффект инсулина – снижение содержания глюкозы в крови. Действие инсулина в печени переключает метаболизм с катаболизма на анаболизм: подавление
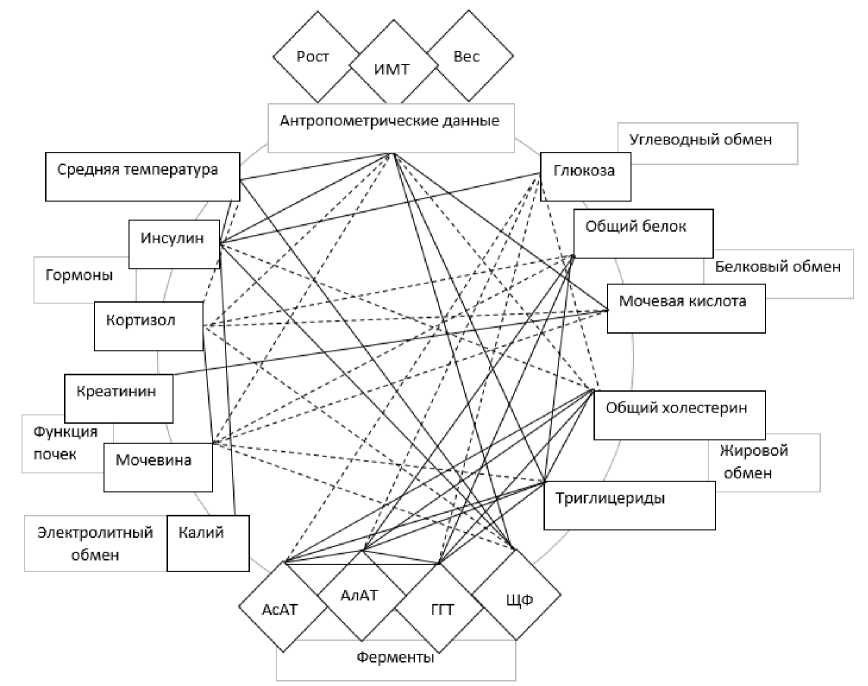
Рис. 3. Корреляционные связи (R > 0,6) между показателями у здоровых добровольцев с ИМТ 24,9-29,9 кг/м2и уровнем инсулина более 25 мкЕД/м (сплошными линиями обозначены положительные связи, пунктирными – отрицательные)
гликогенфосфорилазы способствует накоплению гликогена, а активация гликолиза обеспечивает образование ацетил-КоА для последующего синтеза липидов [17]. Инсулин блокирует синтез глюкозы, инактивируя ферменты глюконеогенеза. Одновременно он усиливает липогенез за счет активации ацетил-КоА-карбоксилазы, что приводит к накоплению малонил-КоА – ключевого промежуточного продукта в образовании жирных кислот, и одновременно ингибирует липопротеинлипазу, ответственную за гидролиз триглицеридов [18]. Возможное объяснение появившимся отрицательным связям в этой группе добровольцев между уровнем глюкозы, общим холестерином и показателями ферментативной активности печени может быть в формировании инсулинорезистентности при избыточной массе тела, когда в жировой ткани развивается резистентность к антилиполитическому действию инсулина. Высвобождение свободных жирных кислот в воротную вену является результатом усиленного липолиза в висцеральных жировых клетках. В печени эти кислоты не только стимулируют продукцию атерогенных липопротеинов, но и вызывают инсулинорезистентность, блокируя связывание инсулина. Как следствие, синтез гликогена подавляется, тогда как его распад и глюконеогенез, напротив, активизируются.
Особый интерес представляет появившаяся интеграция кортизола в регуляцию обменных процессов. Безусловно, поддержание гемостаза требует сложного взаимодействия ряда органов и систем организма, включая нейроэндокринную [19]. Данное проявление нейрогормональной регуляции подчеркивает ее системный характер – способность координировать работу разнообразных клеток. Это отражает уровень напряжения регуляторных механизмов, необходимый для поддержания гомеостаза, и определяет функциональное состояние организма через формирование физиологических реакций долговременного действия. Данный сдвиг регуляторного паттерна можно рассматривать как процесс метаболического перепрограммирования, направленный на поддержание равновесия, но одновременно повышающий уязвимость организма к дисфункции при хроническом перенапряжении. Таким образом, активность этого нейроэндокринного контура регуляции становится значимым прогностическим фактором, определяющим индивидуальную траекторию здоровья или риска в долгосрочной перспективе.
Выводы. Приведенные данные по структурам регуляции метаболических процессов у здоровых добровольцев в зависимости от ИМТ и гормонального статуса позволили выявить принципиально различающиеся механизмы поддержания оптимума мета- болических процессов. Показано, что при ИМТ от 18,50 до 24,9 кг/м2 реакция на стандартизированную пищевую нагрузку обеспечивается локально под контролем прямых действий продуктов метаболизма. При ИМТ от 25,0 до 29,9 кг/м2 и нормальном гормональном статусе к утилизации метаболических субстратов углеводного ряда имеет место подключение вспомогательных метаболических путей жирового и белкового обменов при сохраняющейся локальной ауторегуляции. При присоединении нарушений гормонального статуса у здоровых добровольцев с ИМТ от 25,0 до 29,9 кг/м2 в ответ на стандартизированную пищевую нагрузку к метаболической регуляции in situ имеет место подключение нейрогуморального контура организма. Предельная сложность с сохранением физиологичности регуляции метаболических процессов в этой группе здоровых добровольцев чревата высоким риском возникновения нарушений и развитием патологических процессов. Таким образом, феномен «метаболически здорового ожирения» следует квалифицировать как состояние латентного риска, требующее динамического надзора и углубленной персонализированной оценки резервов адаптации. Поиск предикторов исчерпания компенсаторных возможностей, а не единого триггера, является приоритетной задачей для своевременного управления кардиометаболическим риском в этой популяции.
Финансирование . Источник финансирования исследования не предусмотрен.


