Фермент-индуцирующее действие оригинального антиконвульсанта галодиф - модулирующий временной фактор, перспективы клинического применения при терапии пароксизмальных расстройств
Автор: Шушпанова Т.В., Новожеева Т.П., Васильева О.А., Удут В.В.
Журнал: Сибирский вестник психиатрии и наркологии @svpin
Рубрика: Психофармакотерапия
Статья в выпуске: 4 (121), 2023 года.
Бесплатный доступ
Введение. Совершенствование фармакотерапии возможно путём создания новых лекарственных средств и оптимизации терапевтического мониторинга. Данный подход может быть реализован при условии изучения особенностей биотрансформации препарата ферментами монооксигеназной системы печени (МОС), его фармакокинетики и фармакодинамики в организме.
Антиконвульсант, галодиф, пароксизм, печень, цитохром р450, микросомальная система окисления, фармакокинетика
Короткий адрес: https://sciup.org/142239824
IDR: 142239824 | УДК: 615.241:612.354.2:616.853 | DOI: 10.26617/1810-3111-2023-4(121)-61-69
The enzyme-inducing effect of the original anticonvulsant galodif is a modulating time factor, prospects for clinical use in the treatment of paroxysmal disorders
Introduction. Improving pharmacotherapy is possible through the creation of new drugs and optimization of therapeutic monitoring. This approach can be implemented provided that the characteristics of the biotransformation of the drug by enzymes of the liver monooxygenase system (MOS), its pharmacokinetics and pharmacodynamics in the body are studied.
Текст научной статьи Фермент-индуцирующее действие оригинального антиконвульсанта галодиф - модулирующий временной фактор, перспективы клинического применения при терапии пароксизмальных расстройств
В настоящее время существует острая необходимость в разработке эффективных и безопасных методов лечения социально значимых заболеваний и создании новых фармакотерапевтических средств. Несмотря на значительные успехи, достигнутые в эпилептологии, у значительной части (более 30%) пациентов не удается добиться полного контроля над приступами, в связи с чем остается актуальным создание новых антиэпилептических препаратов (АЭП), рациональных комбинаций существующих АЭП с учетом их механизмов действия [1, 2, 3]. Повышенный интерес представляют препараты с отличным от других АЭП механизмом действия [3, 4, 5, 6].
Разработка оригинальных инновационных соединений, обладающих модуляторным действием на нейрональные рецепторы, в частности рецепторы γ -аминомаслянной кислоты (ГАМК), способствует созданию новых лекарственных препаратов и является значимой стратегией в лечении пароксизмальных расстройств, эпилепсии, болезней зависимости с выраженным компульсивным влечением к ПАВ [7, 8, 9]. Совершенствование фармакотерапии возможно путём создания новых лекарственных средств. Оптимизация фармакотерапии практически осуществима путём использования разных форм и различных путей введения лекарственных средств, за счет включения оптимальных дозовых режимов, обеспечивающих максимальный терапевтический эффект при отсутствии (или минимальной выраженности) нежелательных реакций, разработки способов прогнозирования эффективности лечения и устранения возможных осложнений, на основе подбора рациональных комбинаций препаратов и предупреждения их нежелательного фармакокинетического взаимодействия, а также с помощью терапевтического мониторинга [9, 10]. Большинство этих подходов может быть реализовано лишь при условии изучения особенностей биотрансформации препарата ферментами монооксигеназной системы печени, фармакокинетики и фармакодинамики препарата в организме.
Применяемые в терапии пароксизмальных состояний антиконвульсанты, оказывающие противосудорожное, антипароксизмальное действие, снижающие компульсивное влечение к приему ПАВ, также могут обладать выраженным фермент-индуцирующим действием в отношении цитохром Р450-зависимой монооксигеназной системы (МОС) печени, стимулируя детоксикационную функцию печени. ГАМК-стимулирующее действие антиконвульсанта галодиф с противосудорожной активностью, усиливающее процессы торможения в головном мозге, эффективно для купирования пароксизмальных расстройств, эпилепсии, тревожно-депрессивной симптоматики, раздражительности и агрессивности в структуре алкогольного абстинентного синдрома (отмены алкоголя), снижения компульсивного влечения к алкоголю. Ранее нами были изучены фермент-индуцирующие свойства цитохром Р-450 зависимой МОС печени и фармакокинетических параметров оригинального отечественного антиконвульсанта галодиф в зависимости от различных сроков длительности действия препарата [9].
В отечественной и зарубежной литературе представлены данные, которые свидетельствуют о том, что не обнаружено клинически значимых фармакокинетических взаимодействий между АЭС и лекарственными средствами, метаболизированными CYP3A4, CYP2C19, CYP1A2 или CYP2C9. При этом сопутствующее использование психотропных препаратов, метаболизируемых CYP2D6, может потребовать корректировки дозы [4, 10, 11]. Представлено, что антиконвульсант галодиф обладает выраженным противосудорожным действием, снижающим алкогольную мотивацию [8, 12], и выраженным фермент-индуцирующим действием в отношении цитохром Р450-зависимой МОС печени [9]. Длительное его применение может сопровождаться как изменением фармакокинетики самого галодифа, так и назначаемых совместно с ним лекарственных средств. Это побудило нас исследовать фармакокинетику галодифа в важном органе-мишени – печени – с учетом различной длительности введения его в организм.
ЦЕЛЬ ИССЛЕДОВАНИЯ
Изучить параметры фармакокинетики галодифа, оценить фермент-индуцирующее действие на микросомальную цитохром Р450-зависимую систему окисления печени экспериментальных белых крыс в зависимости от длительности введения.
МАТЕРИАЛЫ И МЕТОДЫ
Экспериментальное исследование выполнено на 50 белых беспородных крысах-самцах массой 200-220 граммов, полученных из питомника НИИ фармакологии и регенеративной медицины им. Е.Д. Гольдберга Томского НИМЦ РАН (г. Томск). Животных содержали в условиях лабораторного вивария, на стандартной диете, при нормальном световом режиме. Содержание экспериментальных животных соответствовало правилам, принятым Европейской конвенцией по защите животных, используемым при выполнении экспериментальных и иных научных целей (Страсбург, 1986), и правилам лабораторной практики (приказ № 267 от 19.06.2003 Минздрава РФ).
Галодиф является оригинальным противосудорожным препаратом, разработанным для лечения и профилактики эпилепсии и алкогольной зависимости. Галодиф представляет собой нециклическое производное мочевины (1-[(3-хлорфенил)(фенил)метил]мочевина). В отличие от своих предшественников, является действующим веществом, не требующим трансформации в печени, что значительно снижает его токсичность и уменьшает побочные эффекты
Галодиф вводили в форме суспензии на 1% крахмальной слизи внутрижелудочно в эффективной дозе 100 мг/кг. Продолжительность введения составила 1, 5 и 15 дней, что обусловлено фазными изменениями активности монооксигеназной системы печени при назначении галодифа: активация после 3-4 введений, ослабление индуктивного ответа к концу 1 месяца [13]. Животных из экспериментальных групп декапитировали, перфузировали печень ледяным 1,15% раствором хлорида калия. Микросомальную фракцию из гомогената печени крыс получали по методу, предложенному И.И. Карузиной, А.И. Арчаковым [14], с использованием высокоскоростного центрифугирования 50000 g при температуре 2-4°С, в течение 2- часов. Полученные осадки ресуспендировали в фосфатном буфере рН 7,4, концентрация белка в препаратах микросом составляла 20-30 мг/мл. Анализ микросом проводили в течение первых 6 часов после выделения. Содержание белка в микросомальной фракции оценивали по микрометоду Лоури. Содержание цитохромов семейства CYР450 в микросомальной фракции оценивали по методу Omura, Sato [15], принцип которого основан на сравнении дифференциальных спектров окисленного и восстановленного CYР450. Спектры снимали на дифференциальном спектрофотометре Хитачи-557 (сканирующий двухлучевой режим).
Определение галодифа в микросомальной фракции печени крыс проводили методом экстракции галодифа из гомогената печени крыс хлороформом при нейтральном рН при центрифугировании со скоростью 3000 об/мин в течение 5 минут для полного разделения фаз. Хлороформный слой отбирали, измерение проводили на спектрофотометре при длине волны 433 нм. Концентрацию галодифа рассчитывали в соответствии с калибровочным графиком, построенным по растворам субстанции галодифа в возрастающей концентрации в изопропаноле (0,5-200 мкг/мл). Калибровочный график сохранял линейность в пределах 0,5-100 мкг/мл. Перед расчётом по графику из величины оптической плотности опытной пробы вычитали величину оптической плотности нулевой пробы для компенсации вклада в оптическую плотность эндогенных веществ. Количественный анализ галодифа осуществляли с учетом взаимодействия первичной алифатической аминогруппы молекулы галодифа с n-диметиламинобензальдегидом. Параметры фармакокинетики рассчитывали модельнонезависимым методом статистических моментов. Статистическую значимость различий оценивали по λ-критерию Колмогорова-Смирнова.
Данные представлены в виде М±SD. Различия считали статистически значимыми при p <0,05. Все расчёты осуществляли с помощью пакета программ STATISTICA для Windows v. 12.0.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В ходе выполнения исследовании оценивали фармакокинетику галодифа в органе-мишени печени при длительном режиме его введения, проводили сопоставление параметров фармакокинетики с индуцирующим действием препарата в отношении микросомальной системы окисления печени, оценивали роль индуцирующих свойств в реализации противосудорожных свойств галодифа. Проведено сопоставление параметров фармакокинетики с показателями ферментиндуцирующего действия препарата при его введении в зависимости от различных сроков введения препарата: 1, 5 и 15 дней.
Оценивали биохимические показатели состояния монооксигеназ печени и параметры фармакокинетики галодифа в зависимости от различной длительности его введения экспериментальным животных. Показано, что 1-кратное введение галодифа в дозе 100 мг/кг через 24 часа после введения препарата статистически значимо не изменяет уровень цитохрома Р450 в микросомальной фракции печени крыс (табл. 1).
Т а б л и ц а 1. Значения параметров фармакокинетики галодифа в ткани печени в зависимости от различной длительности введения препарата
|
Параметр |
1-кратное введение |
5-кратное введение |
15-кратное введение |
|
Т 1/2 , ч |
18,82 ± 6,25 |
2,22 ± 0,52** |
10,79 ± 2,90** |
|
MRT, ч |
22,41 ± 7,07 |
2,95 ± 0,73* |
3,97 ± 1,03* |
|
MDT, ч |
11,77 ± 3,97 |
9,10 ± 2,42* |
0,97 ± 0,080* |
|
MET, ч |
10,64 ± 2,84 |
3,00 ± 0,65** |
12,05 ± 4,10** |
|
АUС, мкг ⋅ ч/мл |
15,01 ± 4,86 |
3,68 ± 0,79* |
19,28 ± 7,13* |
Статистическая значимость различий по λ -критерию Колмогорова-Смирнова в ‒ р<0,01, ** ‒ р<0,05.
П р и м е ч а н и е.
сравнении с 1-кратным введением:
Фармакокинетика галодифа при 1-кратном введении характеризуется высокой величиной периода полувыведения (Т1/2) и низким значением общего клиренса. Высокие показатели среднего времени удерживания (MRT) и среднего времени элиминации (MET) свидетельствуют о задержке препарата в организме. Значительная величина площади под кривой «концентрация-время» указывает на большой объем содержания галодифа в организме (табл. 1, рис. 1, 2, 3 и 4).
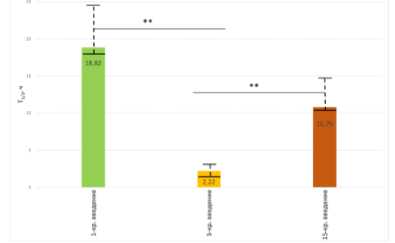
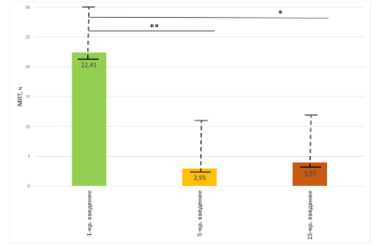
Р и с у н о к 1. Фармакокинетический параметр Т½ ‒ Р и с у н о к 2. Фармакокинетический параметр MRT ‒ время полувыведения галодифа в ткани печени крыс среднее время удерживания галодифа в ткани печени в зависимости от продолжительности введения: крыс в зависимости от продолжительности введения: 11-кратное, 5-кратное, 15-кратное кратное, 5-кратное, 15-кратно
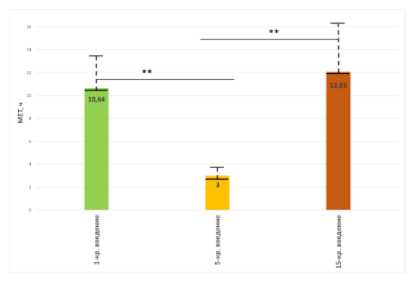
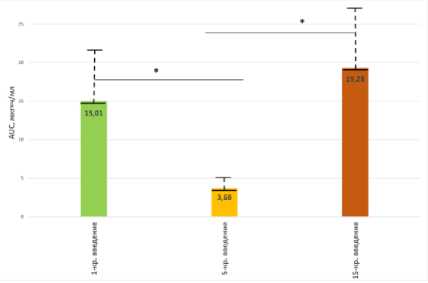
Р и с у н о к 3. Фармакокинетический параметр MET Р и с у н о к 4. Фармакокинетический параметр AUC ‒ ‒ среднее время элиминации галодифа в ткани площадь под фармакокинетической кривой галодифа печени крыс в зависимости от продолжительности в ткани печени крыс в зависимости от введения: 1-кратное, 5-кратное, 15-кратное продолжительности введения: 1-кратное, 5-кратное, 15- кратное
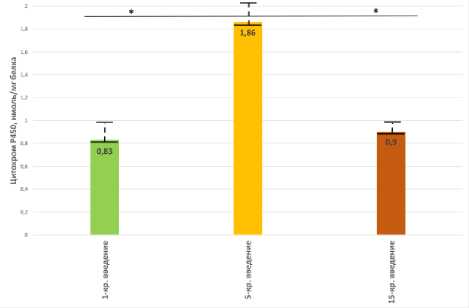
Рисунок 5. Уровень цитохрома Р450 в зависимости от продолжительности введения: 1-кратное, 5-кратное, 15-кратное
Выявленные большой период полувыведения препарата (Т^), относительно высокие величины MRT и МЕТ свидетельствуют о существенной задержке галодифа в ткани печени при 1-кратном введении. Значительная величина площади под кинетической кривой ( AUC ) также указывает на длительную циркуляцию препарата в организме крыс после 1-кратного введения. При этом тканевая доступность галодифа для печени не высока, поэтому значительное количество препарата, задерживаемое в ткани, по-видимому, обусловлено замедленной его элиминацией.
Наши данные совпадают с аналогичными публикациями о том, что в молекулярном механизме действия индукторов фазе индукции предшествует фаза ингибирования (торможения) образования/распада фермент-субстратных комплексов [11]. Установлено, что 1-кратное введение галодифа в дозе 100 мг/кг через 24 часа не изменяло статистически значимо уровень цитохрома Р450 в микросомальной фракции печени крыс (рис. 5). Этот эффект обусловлен как липофильными свойствами галодифа, так и способностью связываться с гемсодержащими ферментами, в том числе с цитохромами семейства CYP Р450 микросомальной МОС печени [13].
В результате 5-кратного введения галодифа наблюдаются существенные изменения параметров фармакокинетики: уменьшается период его полувыведения, возрастает общий клиренс, снижаются значения среднего времени удерживания, элиминации и распределения, что подтверждает ускорение выведения галодифа из организма. Вследствие уменьшения биологической доступности галодифа резко снижается величина AUC, по-видимому, за счет его ускоренной элиминации. По результатам 5-кратного введения галодифа в дозе 100 мг/кг в микросомальной фракции печени крыс значительно возрастает уровень цитохрома Р450, что характеризует стимуляцию функциональной активности монооксигеназ [11, 13]. В случае 5-кратного введения в дозе 100 мг/кг галодиф проявляет выраженные свойства индуктора монооксигеназ и, следовательно, может ускорять биотрансформацию и элиминацию экзогенных и эндогенных субстратов, в том числе и собственный метаболизм. Очевидно, что этот эффект обусловлен индуцирующими свойствами галодифа в отношении микросомальной системы окисления печени. Полученные данные по фармакокинетике свидетельствуют об ускорении собственной биотрансформации галодифа, описанной в отношении многих антиконвульсантов-индукторов МОС -фенобарбитала, карбамазепина, гексамидина [10, 13, 16]. Вероятность ускорения собственного метаболизма следует учитывать в клинической практике при назначении галодифа. Таким образом, несмотря на процессы индукции МОС гепатоцитов и возможные процессы аутоиндукции и ускорения элиминации, печень остается важной биомишенью для фармакологического воздействия молекул галодифа и через 5 суток его ежедневного введения в дозе 100 мг/кг.
После курсового 15-кратного введения галодифа в дозе 100 мг/кг возросший при кратковременном введении уровень цитохрома Р450 снижается, а сам препарат проявляет умеренные свойства индуктора монооксигеназ печени и, возможно, модифицирует элиминацию из организма экзогенных и эндогенных субстратов, в том числе и собственную биотрансформацию и элиминацию. Этот факт подтверждают полученные данные по фармакокинетике 15-дневного введения галодифа.
Представленные структурированные фармакокинетические параметры галодифа (табл. 1, рис. 1-4) свидетельствуют об ускоренной элиминации по сравнению с 1-кратным назначением. Общий клиренс снижен в сравнении с 5-дневным введением, однако увеличен по сравнению с 1-кратным введением препарата. Площадь под фармакокинетической кривой значительно возрастает по сравнению с величиной AUC после 5-дневного введения, но существенно ниже таковой при 1-кратном введении. При курсовом 15-кратном введении галодифа крысам его выведение из организма замедляется. Содержание цитохрома Р-450 в ткани печени повышено по сравнению с 1-кратным введением галодифа, однако отличается от соответствующих показателей активности МОС после 5-кратного введения [8, 11]. Полученные результаты согласуются с имеющимися данными о стимулирующем максимальном ответе МОС в период от 3 до 8 дней. Этот факт подтверждает фармакокинетический профиль галодифа в ткани печени при 15-кратном введении.
Исходя из величин параметров фармакокинетики галодифа в ткани печени при 5дневном введении можно заключить, что по-прежнему имеет место ускоренная элиминация препарата. Однако величина Т% заметно возрастает по сравнению с таковой в условиях 5-кратного введения галодифа. В то время как MRT существенно не изменяется, увеличивается МЕТ, достигая уровня среднего времени элиминации при 1-кратном назначении препарата. АUС также резко возрастает до величины площади под фармакокинетической кривой, наблюдавшейся при 1-кратном введении, что может свидетельствовать о повышении тканевой доступности препарата. Таким образом, судя по расчетным параметрам фармакокинетики, можно сделать вывод о повышении тканевой доступность галодифа в ткани печени животных в условиях его длительного введения.
ЗАКЛЮЧЕНИЕ
Полученные результаты коррелируют с показателями функционального состояния МОС печени ‒ наблюдается выраженная индукция цитохрома Р450. Параметры элиминации препарата из печени также свидетельствуют о выраженной тканевой доступности молекул галодифа. При 15-кратном введении галодифа элиминация препарата из организма замедляется по сравнению с 5-кратным введением, оставаясь ускоренной относительно 1-кратного назначения.
Фармакокинетические параметры элиминации препарата из печени одновременно с этим свидетельствуют о выраженном ускорении прохождения молекул галодифа через гепатобилиарный тракт.
Наиболее клинически важные взаимодействия используемых в клинической практике антиконвульсантов возникают в результате индукции или ингибирования метаболизма назначаемых лекарств [16]. В отличие от индукции ферментов цитохрома Р450 микросомальной оксидазной системы печени, ингибирование ферментов приводит к снижению метаболического клиренса лекарственного препарата, концентрация которого в сыворотке может увеличиваться, что приводит к дополнительным токсическим эффектам [8, 11]. При алкогольной зависимости это является наиболее важным в связи с постоянным токсическим воздействием на организм человека [17].
Для того чтобы избежать нежелательных взаимодействий, необходимо знать, как лекарственное средство влияет на цитохром Р450-зависимый окислительный метаболизм ксенобиотиков целевого контингента больных (например, при длительном назначении препарата больным эпилепсией, пациентам с пароксизмальными расстройствами, включая больных с зависимостью от ПАВ, для предотвращения развития рецидива и алкогольного делирия).
Список литературы Фермент-индуцирующее действие оригинального антиконвульсанта галодиф - модулирующий временной фактор, перспективы клинического применения при терапии пароксизмальных расстройств
- Akiyama T, Otsubo H. Antiepileptic drugs in North America. Brain Nerve. 2010 May;62(5):519-26. Japanese. PMID: 20450099.
- Мухин К.Ю., Пылаева О.А. Эффективность и переносимость леветирацетама (препарат Кеппра®) в лечении эпилепсии: обзор литературы Русский журнал детской неврологии. 2015. Т. 10, № 2. С. 38-53. https://doi.org/10.17650/2073-8803-2015-10-2-38-53
- Nevitt SJ, Sudell M, Cividini S, Marson AG, Tudur Smith C. Antiepileptic drug monotherapy for epilepsy: a network meta-analysis of individual participant data. Cochrane Database Syst Rev. 2022 Apr 1;4(4):CD011412. doi: 10.1002/14651858. CD011412.pub4. PMID: 35363878; PMCID: PMC8974892.
- Johannessen Landmark C, Patsalos PN. Drug interactions involving the new second- and third-generation antiepileptic drugs. Expert Rev Neurother. 2010 Jan;10(1):119-40. doi: 10.1586/ern.09.136. PMID: 20021326.
- Patsalos PN, Spencer EP, Berry DJ. Therapeutic Drug Monitoring of Antiepileptic Drugs in Epilepsy: A 2018 Update. Ther Drug Monit. 2018 Oct;40(5):526-548. doi: 10.1097/FTD. 0000000000000546. PMID: 29957667.
- Киссин М.Я., Бондаренко И.И. Опыт применения лакосамида в комплексной терапии пациентов с фармакорезистентной парциальной эпилепсией. Журнал неврологии и психиатрии им. С.С. Корсакова. 2013. Т. 113, № 9. C. 23-28.
- Шушпанова Т.В., Семке В.Я., Бохан Н.А., Новожеева Т.П., Бадыргы И.О., Дорошенко А.С., Худолей В.Н. Эффективность оригинального антиконвульсанта галодифа у больных с компульсивным влечением к алкоголю, ассоциированным с изменением уровней стероидных гормонов. Сибирский вестник психиатрии и наркологии. 2012. № 3 (72). С. 65-71.
- ShushpanovaTV, BokhanNA, LebedevaEV, MandelAI, NovozheevaTP, SolonskyAV, SchastnyiED, SemkeAV, KazennykhTV, UdutVV, ArbitGA, FilimonovVD. Treatment of alcoholic patients using anticonvulsant urea derivative influences the metabolism of neuro-active steroid hormones – the system of stress markers. Journal Addiction Research & Therapy. 2016;7(2):271. doi:10.4172/2155-6105.1000271
- ШушпановаТ.В., БоханН.А., СтанкевичК.С., НовожееваТ.П., МандельА.И., СчастныйЕ.Д., КисельН.И., ШушпановаО.В., УдутВ.В., СафроновС.М., БоевР.С., КнязеваЕ.М. ИнновационныймодуляторГАМКрецепторов‒ активатормикросомальнойцитохром-Р450 оксидазнойсистемыпечениубольныхалкоголизмом. Химико-фармацевтический журнал. 2020. Т. 54, № 11. С. 9-16. https://doi.org/10.30906/0023-1134-2020-54-11-9-16(in Russian).
- Rodrigues C, Chiron C, Rey E, Dulac O, Comets E, Pons G, Jullien V. Population pharmacokinetics of oxcarbazepine and its monohydroxy derivative in epileptic children. Br J Clin Pharmacol. 2017 Dec;83(12):2695-2708. doi: 10.1111/bcp.13392. Epub 2017 Sep 20. PMID: 28771787; PMCID: PMC5698580.
- Новожеева Т.П., Смагина М.И., Черевко Н.А., Фатеева С.Н. Бензобарбитал и фторбензобарбитал – индукторы фенобарбиталового типа монооксигеназной системы печени. Бюллетень сибирской медицины. 2011. Т. 10, № 5. С. 78-81.
- Шушпанова Т.В., Семке В.Я., Новожеева Т.П., Бохан Н.А. Терапия оригинальным антиконвульсантом галодиф влияет на свойства бензодиазепиновых рецепторов тромбоцитов и уровни нейроактивных стероидных гормонов у больных алкоголизмом. Сибирский вестник психиатрии и наркологии. 2013. № 2 (77). С. 73-78.
- Ляхович В.В., Цырлов И.Б. Индукция ферментов метаболизма ксенобиотиков. Новосибирск: Изд-во Наука, 1981. 240 с.
- Карузина И.И., Арчаков А.И. Выделение микросомальной фракции печени и характеристика ее окислительных систем. В книге: Современные методы в биохимии / под ред. В.Н. Ореховича. М.: Изд-воМедицина, 1977. С. 49-62.
- Omura T, Sato R. The carbon monoxide-binding pigment of liver microsomes. I. Evidence for its hemoprotein nature. J Biol Chem. 1964 Jul; 239:2370-8. PMID: 14209971.
- Zaccara G, Perucca E. Interactions between antiepileptic drugs, and between antiepileptic drugs and other drugs. Epileptic Disord. 2014 Dec;16(4):409-31. doi: 10.1684/epd.2014.0714. PMID: 25515681.
- Кисель Н.И., Бедарев Р.И., Мандель А.И., Шушпанова Т.В., Мазурова Л.В., Новожеева Т.П., Солонский А.В., Гарганеева Н.П., Бурдовицина Т.Г., Гончикова И.А., Попова Т.А. Алгоритм персонализированной терапии больных алкоголизмом с коморбидными нарушениями детоксицирующей функции печени и когнитивными расстройствами. Сибирский вестник психиатрии и наркологии. 2022. № 4 (117). С. 33-43. https://doi.org/10.26617/1810-3111-2022-4(117)-33-43


