Физиологические эффекты Грелина
Автор: Логинова Ольга Александровна, Орлова Екатерина Григорьевна, Ширшев Сергей Викторович
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Иммунология
Статья в выпуске: 4, 2018 года.
Бесплатный доступ
Грелин - пептидный гормон, обладающий широким спектром эффектов в организме человека. Он принимает участие в регуляции энергетического и жирового обмена, ростовых процессов, полового созревания, половых циклов, беременности, в контроле поведенческих реакций, а также обладает выраженными иммуномодулирующими и противовоспалительными свойствами. В обзоре представлены данные о структуре грелина и его рецепторов, уровне гормона при физиологических и патологических состояниях, а также его основные биологические эффекты.
Грелин, рецептор грелина, грелин-о-ацилтрансфераза (гоат), эффекты грелина
Короткий адрес: https://sciup.org/147227053
IDR: 147227053 | УДК: 612.018.2: | DOI: 10.17072/1994-9952-2018-4-443-453
Physiological effects of Ghrelin
Ghrelin is a peptide hormone with a wide range of effects in the human body. Ghrelin participates in the regulation of energy and fat metabolism, growth processes, puberty, sexual cycles, pregnancy, control of behavioral reactions, and also has pronounced immunomodulatory and anti-inflammatory properties. The review presents data on the structure of ghrelin and its receptors, the level of the hormone under physiological and pathological conditions, as well as the main biological effects of the hormone.
Текст научной статьи Физиологические эффекты Грелина
Дальнейшие исследования показали, что гре-лин вырабатывается у многих классов животных (млекопитающих, птиц, рыб) в различных органах и тканях, а его биологическая активность оказалась более разнообразна, чем предполагали изначально, и включает широкий спектр эндокринных и неэндокринных эффектов [Dixit, Taub, 2005; Delporte, 2013].
Синтез грелина
ми, почками, щитовидной железой, лимфоидными органами и клетками иммунной системы [Mori et al., 2000; Gualillo et al., 2001; Korbonits et al., 2001; Tena-Sempre, 2008]. Кроме этого, в аркуатных ядрах гипоталамуса, которые являются важнейшей структурой в реализации эффектов грелина, также обнаруживается небольшое число грелин-продуцирующих нейронов [Cabral et al., 2017].
У всех позвоночных грелин закодирован в ghrl гене. У человека ген ghrl находится на правом плече третьей хромосомы в регионе 3p26-p25. ghrl имеет длину 511 пар оснований и содержит 5 экзонов (зрелая молекула грелина кодируется экзонами 1 и 2) и 4 интрона. ghrl несет 2 транскрипционных старт-сайта, что приводит к экспрессии двух различных транскриптов – грелина и обестатина [Smith et al., 1997]. Образование грелина происходит в несколько этапов: на первом транслируется последовательность для препрогрелина, содержащего 117 аминокислот (ак), из которых 23 ак составляют сигнальный пептид и 94 ак – прогрелин; на втором этапе прогрелин претерпевает ряд последовательных стадий, в ходе которых происходит его модификация. Сначала в энтероэндокринных клетках происходит процесс ограниченного протеолиза (протеазой PC 1/3 в позиции Arg28/Ala29) с образованием N-концевой молекулы грелина. Затем, при участии фермента грелин-О-ацилтрансферазы (англ. Ghrelin O-acyltransferase, GOAT), катализируется связь одного n-октаноил радикала, что приводит к образованию ацилированного пептида, состоящего из 28 ак (с Arg на С-конце) с молекулярной массой 3,314 кДа и содержащего n-октановый сложный эфир на 3-сериновом остатке (Ser3). По всей видимости, биологические свойства грелина определяются его уникальной посттрансляционной модификацией, благодаря которой становится возможным его взаимодействие со своим основным рецептором – GHS-R1a [Van der Lely et al . , 2004].
Помимо грелина, в результате альтернативного сплайсинга, из препрогрелина может образовываться деацилгрелин, состоящий из 27 ак (с Pro на С-конце) и обестатин, содержащий 23 ак [Kanamoto et al., 2004; Zhang et al., 2005; Hosoda et al., 2003].
Деацилгрелин (англ. Desacylghrelin, DAG) – неацилированная изоформа гормона, был обнаружен спустя несколько лет после открытия грелина [Hosoda et al., 2000]. Эффекты деацилгрелина активно исследуются. Уже установлено, что деацил-грелин вовлечен в регуляцию энергетического гомеостаза и, как и ацилированная изоформа грели-на, способен пересекать гематоэнцефалический барьер (ГЭБ) и индуцировать активность нейронов в аркуатных ядрах гипоталамуса, активируя, как предполагается, собственные специфические ми- шени. Показано, что деацилгрелин обладает некоторой кардиопротективной и антипролифератив-ной активностью, предположительно, за счет связывания с особыми подтипами рецептора, которые на данный момент еще не обнаружены [Fernandez et al., 2016]. С другой стороны, отмечается, что деацилгрелин может иметь противоположные ацилированному грелину эффекты, в частности, оказывает анорексигенный эффект.
Таким образом, обе существующие изоформы гормона имеют широкий спектр эффектов и играют фундаментальную роль при различных физиологических процессах в организме млекопитающих, хотя в некоторых случаях могут перекрывать или оказывать противоположные друг другу эффекты [Stark et al., 2016].
Динамика уровня грелина в крови
У здоровых худощавых людей концентрация грелина пульсирующая, с циркадными (суточными) и ультрадианными (от 0.5 до 20 ч.) ритмами, с подъемом уровня ночью [Yildiz et al . , 2004; Liu et al . , 2008] (рисунок). Уровень циркулирующего в крови грелина модулируется количеством потребляемой энергии – повышается в состоянии голода и снижается через 60-120 мин. после приема пищи [Tschöp et al., 2001].
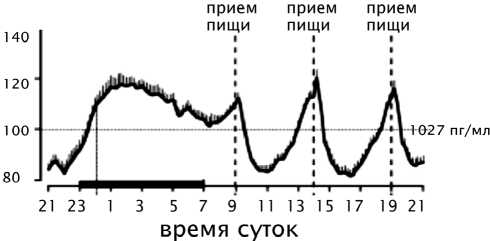
Суточные изменения общего уровня грелина (ацилгрелин+деацилгрелин) в плазме крови, % от суточного показателя [Spiegel et al . , 2011]
Кроме этого, уровень грелина в сыворотке крови находится под влиянием коротких и долгосрочных изменений в энергетическом гомеостазе, роста и полового созревания [Muccioli et al., 2011]. Исследователи отмечают увеличение уровня грелина в сыворотке крови в течение первых двух лет после рождения, с последующим понижением до завершения полового созревания и еще более заметным снижением у людей старше 70 лет. Гендерные различия по уровню циркулирующего грелина до сих пор являются спорными [De Souza et al., 2004].
Структура рецептора грелина
Как уже упоминалось ранее, первый сиротский (орфанный) рецептор для GHSs в гипофизе и гипоталамусе был открыт в 1996 г. и получил название – GHS-R [Howard et al., 1996]. На сегодняшний день известны две изоформы рецептора для ацилированного грелина – GHS-R типа 1a (GHS-R1a) и GHS-R типа 1b (GHS-R1b) [Yuan et al., 2014]. Рецепторы для деацилированной формы грелина до сих пор не идентифицированы.
Рецепторы грелина относятся к суперсемейству рецепторов, сопряженных с G-белком (англ. G-protein coupled receptors, GPCRs). GPCRs принимают участие в распознавании ароматических веществ, остатков аминокислот, нуклеотидов, пептидов, белков, а также ионов Ca2+ и света. Существует несколько механизмов, которые позволяют различным лигандам, взаимодействующим с GPCRs, активировать ядро домена, индуцируя изменение его конформации [Howard et al., 1996]. Рецепторы семейства GPCRs контролируют активность ферментов, ионных каналов и транспортных везикул посредством катализа гуанозиндифосфата (ГДФ) до гуанозинтрифосфата (ГТФ) на гетеродимерных G α-βγ -белках [Watts, Neve, 2005].
Выделяют 5 семейств GPCRs, часть из которых содержит по несколько подтипов, но все они имеют общий план строения их центральной части – трансмембранных спиралей [Bockaert, Pin, 1999]. Все рецепторы данного типа начинаются с внеклеточного N-концевого домена и заканчиваются внутриклеточным С-концевым доменом [Baldwin, 1993].
GHS-R1a состоит из 366 ак и имеет молекулярную массу 41 кДа. GHS-R1a содержит 7 трансмембранных α-спиральных гидрофобных домена, соединенных тремя внутриклеточными и тремя вне- клеточными петлями [Baldwin, 1993]. GHS-R1a связывает лиганд в полости, формируемой III-VI трансмембранными доменами [Bockaert, Pin, 1999], имеет конститутивную активность, и большинство изученных эффектов грелина осуществляется при взаимодействии именно с этим рецептором [Howard et al., 1996].
Другой рецептор грелина – GHS-R1b состоит из 289 ак. Преимущественно GHS-R1b активируется короткими пептидами, которые взаимодействуют с внеклеточными петлями и N-концевым доменом [Trumpp-Kallmeyer et al., 1995]. В состав GHS-R1b входит 5 трансмембранных доменов, его мРНК имеет широкое представление в различных тканях, но его физиологическая роль в организме изучена недостаточно [Van der Lely et al . , 2004].
GHS-R1a и GHS-R1b экспрессируются в виде сплайс-вариантов [Howard et al., 1996] и могут образовывать гетеродимеры, что предположительно позволяет им действовать как доминантнонегативный мутаген полнометражного рецептора грелина [Leung et al., 2007]. Помимо этого, GHS-R1a может образовывать гетеродимеры с рецепторами дофамина, меланокортина, серотонина, модифицируя их сигнальные пути, что приводит к развитию неклассических эффектов [Wellman, Abizaid, 2015].
Физиологические эффекты грелина
Грелин проявляет неэндокринный эффект, модулируя нейрогенез и синаптическую пластичность. Присутствие грелина может изменять морфологию нейронов и связанных с ними функций, улучшая таким образом концентрацию, процесс обучения и память. Помимо этого, установлена взаимосвязь концентрации гормона и циклами сон-бодрствование. [Pinto et al . , 2004; Dhillo et al . , 2007].
Роль грелина в регуляции энергетического гомеостаза . Основной эффект грелина реализуется через гипоталамические структуры. Грелин усиливает синтез AgRP (англ. Agouti-related protein, AgRP) и NPY (англ. Neuropeptide Y, NPY) в соответствующих орексигенных нейронах, подавляя активность анорексигенных POMC/CART (англ. Proopiomelanocortin и Сocaine amphetamine-related transcript)-нейронов [Dixit, Taub, 2005]. NPY играет первостепенную роль в реализации кратковременных эффектов грелина. Активация NPY происходит при связывании с GHS-R1a, тогда как AgRP обеспечивает реализацию как краткосрочных, так и долгосрочных эффектов гормона. AgRP усиливает аппетит при взаимодействии с рецепторами ме-ланокортина, локализованных непосредственно в головном мозге, и, таким образом, ингибирует анорексигенные влияния а-меланоцитостиму-лирующего гормона. Важно отметить – грелин может воздействовать на ЦНС различными путями: с током крови пересекать ГЭБ или передавать сигнал в ядра гипоталамуса благодаря наличию рецепторов к грелину на разветвлениях блуждающего нерва, густо опутывающих брюшную полость [Сowley et al . , 2003; Dixit, Taub, 2005].
Чистый орексигенный эффект грелина, возбуждающий аппетит, является функционально противоположным другому метаболическому гормону – лептину. Лептин подавляет активность AgRP и NPY, но стимулирует POMC/CART-нейроны, подавляя аппетит, т.е. обладает анорексигенным эффектом [Dixit, Taub, 2005; Wynne et al . , 2005]. Помимо лептина, гормон обестатин наделен функционально противоположными грелину эффектами – его воздействие необходимо для уменьшения потребления пищи, повышения массы тела и поддержания функций ЖКТ. В целом, метаболические гормоны грелин, лептин, обестатин, гастрин и др. регулируют энергетический и жировой обмен, дополняя друг друга в предоставлении информации
ЦНС о состоянии систем энергетического баланса [De Smet et al., 2007].
Роль грелина в регуляции репродуктивной системы . Грелин выступает в качестве нейроэндокринного модулятора, вовлеченного в контроль широкого спектра биологических функций, в том числе и репродуктивной [Repasi et al . , 2011]. Гре-лин принимает участие в регуляции полового созревания, половых циклов и беременности. Об этом свидетельствует экспрессия самого гормона и его рецепторов, а также наличие выраженных эффектов в репродуктивных органах и тканях [Muc-cioli et al . , 2011]. Возможность регуляции грели-ном репродуктивной физиологии крайне разнообразна и осуществляется несколькими путями: через собственные рецепторы грелин влияет на секрецию гонадотропинов – лютеинизирующего (ЛГ) и фолликулостимулирующего гормонов (ФСГ), оказывая непосредственное влияние на половые циклы и сроки полового созревания; и опосредованно – угнетая синтез гипоталамического гонадотропин-рилизинг гормона (ГнРГ) в гипофизе, что влечет за собой понижение выработки ЛГ и ФСГ клетками-гонадотрофами гипофиза [Fernández-Fernández et al . , 2004]. Еще один вариант опосредованной супрессии грелином пульсирующей секреции ЛГ происходит вследствие индуцированного грелином снижения экспрессии мРНК кисспептина, который является одним из важнейших нейроэндокринных регуляторов в системе управления репродуктивной осью и полового созревания [Muccioli et al . , 2011]. Наличие рецепторов грелина в фолликулах, желтом теле и миометрии предполагает потенциальную роль грелина в непосредственном управлении овариальной функцией. Показано, что в культуре человеческих гранулезных лютеиновых клеток грелин оказывает тормозящее влияние на стерои-догены (прогестерон и эстрадиол), причем независимо от присутствия хорионического гонадотропина человека, действуя через свои функциональные рецепторы [Viani et al . , 2008].
Беременность сопровождается значительным изменением уровня грелина, поскольку гормон синтезируется и плацентой. Это обусловлено усилением потребности матери и плода в питательных веществах и энергии. Максимальный уровень гре-лина отмечается в середине II триместра, затем его уровень начинает плавно снижаться, и вскоре после родов достигает своих обычных значений [Fuglsang et al., 2005]. При этом известно, что нарушения жирового обмена приводят к прерыванию беременности [Tena-Sempre, 2008]. Снижение относительного уровня грелина на 30–40% при беременности может сопровождается угрозой невынашивания и спонтанными абортами иммунного генеза [Шестопалов и др, 2011]. С другой стороны, и относительное повышение уровня грелина в I триместре беременности, например, при голодании, может приводить к нарушению имплантации и ограничению инвазии трофобласта. Во II триместре грелин стимулирует пролиферацию клеток плаценты [Nakahara et al., 2006], а физиологическое снижение его уровня в III триместре связывают с подготовкой организма к родам [Muccioli et al., 2011]. Кроме того, грелин – небольшая молекула, способная преодолевать маточно-плацентарный барьер. При этом ткани плода также секретируют гре-лин, обеспечивая развитие тканей и органов [Cha-noine, Wong, 2004].
Роль грелина в регуляции клеток иммунной системы . Как известно, клетки иммунной системы очень чувствительны к изменениям эндокринного фона и обмена веществ. Гормоны и питательные вещества могут влиять на иммунный ответ и экспрессию цитокинов, и наоборот, провоспа-лительные цитокины и различные факторы роста, вырабатываемые во время воспаления или в ответ на повреждение, распространяясь по всему телу, оказывают влияние на секрецию гормонов, нейроэндокринные функции и метаболизм [Gregori, 2011].
В некоторых случаях, изменения уровня грели-на сопровождаются глубокими нарушениями иммунитета, что предполагает значимую роль гормона в их патогенезе. Известно, что уровень грелина и количество GHS-R регулируются в состояниях острого и хронического воспаления, а также при аутоиммунных процессах [Hattori, 2001; Nagaya et al., 2001; Muccioli et al . , 2002; Baatar et al . , 2011; Colldén et al . , 2017]. В связи с этим, повышение уровня грелина в плазме или сыворотке крови рассматривается некоторыми исследователями как признак, связанный с тяжестью заболевания и/или наличием осложнений [Dixit et al . , 2004].
Рецепторы грелина экспрессированы на Т-лимфоцитах (в том числе на регуляторных Т-клетках, Treg), В-лимфоцитах, NK-клетках (англ. Natural killer, NK), нейтрофилах, макрофагах, моноцитах и дендритных клетках [Gnanapavan et al., 2002; Hattori, 2009]. При активации клеток отмечается увеличение количества рецепторов грелина, что подтверждает предположение о возможности регуляции грелином иммунного ответа, клеточного развития и дифференцировки [Dixit et al., 2004]. Кроме того, грелин ингибирует экспрессию рецепторов к лептину на Т-клетках человека, что может вызывать дозозависимое подавление индуцированной лептином продукции цитокинов. Это свидетельствует о существовании реципрокной системы регуляции, в которой лептин и грелин активируют клетки иммунной системы и регулируют вос- паление [Романцова, Волкова, 2005; Шестопалов и др., 2011].
Грелин может регулировать развитие иммунных реакций за счет подавления выработки активированными Т-клетками провоспалительных цитокинов, таких, как интерлейкин (англ. Interleukin, IL) -1 β , фактор некроза опухоли- α , IL-6, IL-17, IL-12, гранулоцитарно-макрофагальный колониестимулирующий фактор; за счет угнетения транскрипционного фактора NF- κ B (англ. Nnuclear factor κB), ответственного за их синтез [Dixit et al., 2004; Романцова, Волкова, 2005; Dixit, Taub, 2005]. В том числе, противовоспалительные эффекты грелина связывают с подавлением продукции IL-8 и активных форм кислорода, а также с ограничением миграции нейтрофилов, макрофагов и моноцитов в очаг воспаления, что в совокупности с усилением продукции IL-10 и трансформирующего фактора роста опухоли- β 1 дендритными клетками, способствуют формированию и поддержанию пула Treg [Романцова, Волкова, 2005; Gon-zalez-Rey et al . , 2006; El-Eter et al . , 2007; Орлова, Ширшев, 2010]. Показано, что грелин, в концентрации отражающей его уровень при беременности, может усиливать формирование регуляторных NK-клеток и их миграцию в плаценту, а также усиливать экспрессию рецептора к IL-7 (CD127) и продукцию IL-4 CD4+-клетками, за счет чего будет способствовать формированию Т-хелперов (Th) 2 типа [Орлова, 2011; Орлова, Ширшев, 2012; Шир-шев и др, 2012, 2014]. Кроме этого, показано, что грелин играет важную роль при дифференцировке тимоцитов за счет стимуляции продукции IL-4 и апоптоза CD4+ и CD8+ клеток и контролирует формирование Treg [Орлова, Ширшев, 2013].
Экспериментальные исследования энцефаломиелита и рассеянного склероза у мышей показали, что введение гормона уменьшает выраженность воспалительного процесса в ЦНС и периферической крови, где отмечается уменьшение численности аутореактивных Th1-клеток и IL-17-продуцирующих Т-хелперов [Souza-Moreira et al . , 2013].
Исследования нескольких групп показали, что грелин играет важную роль в регуляции структуры и функций тимуса. Это связано с тем, что рецепторы к грелину экспрессируются как на монопози-тивных CD4+- и CD8+ - клетках, так и на дубльпо-зитивных, которые несут двойной набор GHS-R. При этом количество GHS-R на тимоцитах уменьшается с возрастом и соответствует темпам возрастной инволюции тимуса, а введение гормона стареющим мышам способствует изменению структурно-функциональных показателей тимуса – уменьшению процента жировой ткани с восстановлением нормально функционирующих зон, усилением дифференцировки тимоцитов и мигра- ции общих лимфоидных предшественников из костного мозга [Dixit et al., 2004, 2007].
Таким образом, на уровне иммунной системы грелин оказывает выраженный противовоспалительный эффект за счет регуляции процессов дифференцировки, пролиферации, апоптоза и продукции цитокинов [Van der Lely et al . , 2004; Орлова, Ширшев, 2010, 2013; Baatar et al . , 2011].
Перспективы использования грелина в медицинской практике . Изменения уровня грелина, наблюдаемые при некоторых патологических состояниях, открывают перспективы использования эндогенного гормона для их коррекции. Особый интерес представляет возможность лечения грели-ном нейродегенеративных расстройств, таких, как рассеянный склероз, болезнь Альцгеймера и болезнь Паркинсона, а также замедления старения в целом.
В сосудистой ткани, где широко распространены рецепторы грелина, гормон оказывает прямое воздействие. Внутривенное введение грелина здоровым людям вызывает расширение кровеносных сосудов и увеличивает сердечный выброс, а у больных с хронической сердечной недостаточностью улучшает работу сердца и снижает среднее артериальное давление, не влияя на частоту сердечных сокращений и не вызывая побочных эффектов в почках [Colldén et al . , 2017].
Еще одно важное свойство грелина заключается в подавлении инсулинрезистентности кардиомиоцитов (индуцированной глюко- и липотоксич-ностью), что свидетельствует о возможной эффективности грелина для лечения болезней миокарда при сахарном диабете [Iglesias et al . , 2004].
Работа выполнена в рамках государственного задания; номер госрегистрации темы: 01201353248.
Список литературы Физиологические эффекты Грелина
- рлова Е.Г. Регуляция лептином и грелином индукции Т-регуляторных лимфоцитов // Вестник Уральской медицинской академической науки. 2011. Т. 35, № 2/1. С. 55-56.
- Орлова Е.Г., Ширшев С.В. Регуляция грелином функциональной активности моноцитов человека в модели in vitro // Доклады Академии наук. 2010. Т. 434(6). С. 821-824.
- Орлова Е.Г., Ширшев С.В. Регуляция лептином и грелином продукции интерферона-гамма и интерлейкина-4 в системе in vitro // Вестник Пермского университета. 2012. Вып. 3. С. 81-83.
- Орлова Е.Г., Ширшев С.В. Роль лептина и грелина в индукции дифференцировки ИЛ17-продуцирующих и Т-регуляторных лимфоцитов // Бюллетень экспериментальной биологии и медицины 2013. Т. 156, № 12. С. 786-791.
- Романцова Т.И., Волкова Г.Е. Лептин и грелин: антагонизм и взаимодействие в регуляции энергетического обмена // Ожирение и метаболизм. 2005. № 2. С. 2-9.
- Шестопалов А.В. и др. Грелин и соматотропный гормон при физиологически протекающей беременности // Журнал акушерства и женских болезней. 2011. № 2. С. 68-72.
- Ширшев С.В. и др. Гормональная регуляция продукции IFN-g и IL-4 тимоцитами // Вестник Уральской медицинской академической науки. 2012. № 4(41). С. 76-77.
- Ширшев С.В. и др. Роль гормонов, ассоциированных с гестацией, в регуляции экспрессии молекул, отвечающих за функциональную активность NK-клеток // Доклады Академии наук. 2014. Т. 457, № 5. C. 618-621.
- Baatar D. et al. The effects of ghrelin on inflammation and the immune system // Molecular and Cellular Endocrinology. 2011. Vol. 340. P. 44-58.
- Baldwin J.M. The probable arrangement of the helices in G protein-coupled receptors // The EMBO Journal. 1993 Vol. 12. P. 1693-1703.
- Bockaert J., Pin J.P. Molecular tinkering of G protein-coupled receptors: An evolutionary success // The EMBO Journal. 1999. Vol. 18. P. 1723-1729.
- Bowers C.Y. On a peptidomimetic growth hormonereleasing peptide // The Journal of Clinical Endocrinology & Metabolism 1994. Vol. 79. P. 940-942.
- Cabral A. et al. Is ghrelin synthesized in the central nervous system? // International Journal of Molecular Sciences. 2017. Vol. 15, № 18 (3). ppi. E638.
- Cekic C. et al. Evaluation of the relationship between serum ghrelin, Creactive protein and interleukin-6 levels, and disease activity in inflammatory bowel diseases // Hepatogastroenterology. 2008. Vol. 61, № 133. P. 1196-1200.
- Chanoine J.P., Wong A.C. Ghrelin gene expression is markedly higher in fetal pancreas compared with fetal stomach: effect of maternal fasting // Endocrinology. 2004. Vol. 145. P. 3813-3820.
- Collden G. et al. Therapeutic Potential of Targeting the Ghrelin Pathway // International Journal of Molecular Sciences. 2017. Vol. 18(4). pii: E798.
- Cowley M.A. et al. The distribution and mechanism of action of ghrelin in the CNS demonstrates a novel hypothalamic circuit regulating energy homeostasis // Neuron. 2003. Vol. 37. P. 649-661.
- De Smet B. et al. Effect of peripheral obestatin on gastric emptying and intestinal contractility in rodents // Neurogastroenterology &Motility. 2007. Vol. 19. P. 211-217.
- De Souza M.J. et al. Fasting ghrelin levels in physically active women: relationship with menstrual disturbances and metabolic hormones // The Journal of Clinical Endocrinology & Metabolism. 2004. Vol. 89. P. 3536-3542.
- Delporte C. Structure and Physiological Actions of Ghrelin // Scientifica. 2013. 25 p.
- Dhillo W.S. et al. The neuroendocrine physiology of kisspeptin in the human // Reviews in Endocrine and Metabolic Disorders. 2007. Vol. 8. P. 41-46.
- Dixit V.D. et al. Ghrelin inhibits leptin- and activation-induced proinflammatory cytokine expression by human monocytes and T cells // The Journal of Clinical Investigation. 2004. Vol. 1. P. 57-66.
- Dixit V.D. et al. Ghrelin promotes thymopoiesis during aging // The Journal of Clinical Investigation. 2007. Vol. 117, № 10. P. 2778-2790.
- Dixit V.D., Taub D.D. Ghrelin and immunity: a young player in an old field // Experimental gerontology. 2005. Vol. 40. P. 900-910.
- Diz Chaves Y. et al. GH responses to GHRH and GHRP-6 in Streptozotocin (STZ)-diabetic rats // Life Science. 2003. Vol. 14, № 73(26). P. 3375- 3385.
- El-Eter E. et al. In vivo and in vitro antioxidant activity of ghrelin: Attenuation of gastric ischemic injury in the rat // Journal of Gastroenterology and Hepatology. 2007. Vol. 22, № 11. P. 1791-1799.
- Fernandez G. et al. Des-acyl ghrelin directly targets the arcuate nucleus in a ghrelin-receptor independent manner and impairs the orexigenic effect of ghrelin // Neuroendocrinolology. 2016. Vol. 28, № 2. P. 205-219.
- Fernández-Fernández R. et al. Novel signals for the integration of energy balance and reproduction // Molecular and Cellular Endocrinology. 2006. Vol. 25, № 254-255. P. 127-132.
- Fernández-Fernández R. et al. Ghrelin effects on gonadotropin secretion in male and female // Neuroscience Letters. 2004. Vol. 362, № 2. P.103-107.
- Fuglsang J. et al. Ghrelin and its relationship to growth hormones during normal pregnancy // Clinical Endocrinology. 2005. Vol. 62. P. 554-559.
- Gnanapavan S. et al. The tissue distribution of the mRNA of ghrelin and subtypes of its receptor, GHS-R, in humans // The Journal of Clinical Endocrinology & Metabolism. 2002. Vol. 87. P. 2988.
- Gonzalez-Rey E. et al. Therapeutic action of ghrelin in a mouse model of colitis // Gastroenterology. 2006. Vol. 30. P. 1707-1720.
- Granado M. et al. Anti-inflammatory effect of the ghrelin agonist growth hormone-releasing peptide-2 (GHRP-2) in arthritic rats // American Journal of Physiology-Endocrinology and Metabolism. 2005. Vol. 288. P. 486-492.
- Gray P.C. et al. Regulation of ion channels by cAMPdependent protein kinase and A-kinase anchoring proteins // Current Opinion in Neurobiology. 1998. Vol. 8, № 4. P. 330-334.
- Gregori S. Dendritic cells in networks of immunological tolerance // Tissue Antigens. 2011. Vol. 77. P. 89-99.
- Gualillo O. et al. Ghrelin, a novel placental-derived hormone // Endocrinology. 2001. Vol. 142. P. 788-794.
- Hattori N. Expression, regulation and biological actions of growth hormone (GH) and ghrelin in the immune system // Growth Hormone & IGF Research. 2009. Vol. 19. P. 187-197.
- Hattori N. et al. GH, GH Receptor, GH Secretagogue Receptor, and Ghrelin Expression in Human T Cells, B Cells, and Neutrophils // The journal of Clinical Endocrinology & Metabolism. 2001. Vol. 86. P. 4284-4291.
- Hosoda H. et al. Ghrelin and des-acyl ghrelin: two major forms of rat ghrelin peptide in gastrointestinal tissue // Biochemical and Biophysical Research Communications. 2000. Vol. 279, Iss. 3. P. 909-913.
- Hosoda H. et al. Structural divergence of human ghrelin. Identification of multiple ghrelin-derived molecules produced by post-translational processing // The Journal of Biological Chemistry. 2003. Vol. 278. P. 64-70.
- Howard A.D. et al. A receptor in pituitary and hypothalamus that functions in growth hormone release // Science. 1996. Vol. 16, I.8. P. 974-977.
- Kanamoto N. et al. Genomic structure and characterization of the 5'-flanking region of the human ghrelin gene // Endocrinology. 2004. Vol. 145, № 9. P. 4144-4453.
- Koch A. et al. Regulation and prognostic relevance of serum ghrelin concentrations in critical illness and sepsis // Critical Care. 2010. Vol. 14. P. 94- 98.
- Kojima M. et al. Ghrelin is a growth-hormonereleasing acylated peptide from stomach // Nature. 1999. Vol. 402. P. 656-660.
- Kojima M., Kangawa K. Ghrelin: structure and function // Physiology Review. 2005. Vol. 85, № 2. P. 495-522.
- Korbonits M. et al. Presence of ghrelin in normal and adenomatous human pituitary // Endocrine. 2001. Vol. 14. P. 101-104.
- Korbonits M. et al. Ghrelin - a hormone with multiple functions // Frontiers in Neuroendocrinology. 2004. Vol. 25. P. 27-68.
- Leung P.K. et al. The truncated ghrelin receptor polypeptide (GHS-R1b) acts as a dominant-negative mutant of the ghrelin receptor // Cellular Signaling. 2007. Vol. 19. P. 1011-1022.
- Liu J. et al. Novel ghrelin assays provide evidence for independent regulation of ghrelin acylation and secretion in healthy young men // The Journal of Clinical Endocrinology & Metabolism. 2008. Vol. 93. P. 1980-1987.
- Mori K. et al. Kidney produces a novel acylated peptide, ghrelin // FEBS Letter. 2000. Vol. 486. P. 213-216.
- Muccioli G. et al. Beyond the metabolic role of ghrelin: a new player in the regulation of reproductive function // Peptides. 2011. Vol. 32. P. 2514-2521.
- Muccioli G. et al. Neuroendocrine and peripheral activities of ghrelin: implications in metabolism and obesity // European Journal of Pharmacology. 2002. Vol. 440. P. 235-254.
- Nagaya N. et al. Hemodynamic and hormonal effects of human ghrelin in healthy volunteers // American journal of physiology. Regulatory, integrative and comparative physiology. 2001. Vol. 280. P. 1483-1487.
- Nakahara K. et al. Maternal ghrelin plays an important role in rat fetal development during pregnancy // Endocrinology. 2006. Vol. 147. P. 1333- 1342.
- Petersenn S. Structure and regulation of the growth hormone secretagogue receptor // Minerva Endocrinologica. 2002. Vol. 27. P. 243-256.
- Pinto S. et al. Rapid rewiring of arcuate nucleus feeding circuits by leptin // Science. 2004. Vol. 304. P. 110-115.
- Repasi A. et al. Ghrelin and reproductive disorders // Molecular and Cellular Endocrinology. 2011. Vol. 340. P. 70-79.
- Smith R.G. et al. Peptidomimetic regulation of growth hormone secretion // Endocrine Reviews. 1997. Vol. 5. P. 621-645.
- Soriano-Guillén L. et al. Ghrelin levels in obesity and anorexia nervosa: effect of weight reduction or recuperation // The Journal of Pediatrics. 2004. Vol. 144, № 1. P. 36-42.
- Souza-Moreira L. et al. Therapeutic effect of ghrelin in experimental autoimmune encephalomyelitis by inhibiting antigen-specific Th1/Th17 responses and inducing regulatory T cells Brain // Behavior and Immunity. 2013. № 30. P. 54-60.
- Spiegel K. et al. Twenty-four-hour profiles of acylated and total ghrelin: relationship with glucose levels and impact of time of day and sleep // The journal of Clinical Endocrinology & Metabolism. 2011. Vol. 96, № 2. P. 486-493.
- Stark R. et al. Des-acyl ghrelin and ghrelin Oacyltransferase regulate hypothalamic-pituitaryadrenal axis activation and anxiety in response to acute stress // Endocrinology. 2016. Vol. 157, № 10. P. 3946-3957.
- Stasi C., Milani S. Functions of ghrelin in brain, gut and liver // CNS Neurological. Disorders - Drugs and Targets. 2016. Vol. 15, № 8. Р. 956-963.
- Tena-Sempere M. Ghrelin as a pleotrophic modulator of gonadal function and reproduction // Nature clinical practice. Endocrinology & metabolism. 2008. Vol. 4, № 12. P. 666-674.
- Tena-Sempere M. Ghrelin: novel regulator of gonadal function // Journal of. Endocrinology Investigation. 2005. Vol. 28, Suppl. 5. P. 26-29.
- Trumpp-Kallmeyer S. et al. Towards understanding the role of the first extracellular loop for the binding of peptide hormones to G-protein coupled receptors // Pharmaceutica Acta Helvetiae. 1995. Vol. 70, № 3. P. 255-262.
- Tschöp M. et al. Post-prandial decrease of circulating human ghrelin levels // Journal of Endocrinology Investigation. 2001. Vol. 24. P. 19-21.
- Van der Lely A.J. et al. Biological, physiological, pathophysiological, and pharmacological aspects of ghrelin // Endocrine Reviews. 2004. Vol. 25. P. 426-457.
- Viani I. et al. Ghrelin inhibits steroid biosynthesis by cultured granulosa-lutein cells // Journal of Clinical Endocrinology and Metabolism. 2008. Vol. 93. P. 1476-1481.
- Watts V.J., Neve KA. Sensitization of adenylate cyclase by G-alpha i/o-coupled receptors // Pharmacology & Therapeutics. 2005. Vol. 106, № 3. P. 405-421.
- Wellman M., Abizaid A. Growth Hormone Secretagogue Receptor Dimers: A New Pharmacological Target // eNeuro. 2015. Vol. 2 (2). P. e005314.2015 1-16.
- Wynne K. et al. Appetite control // Endocrinology. 2005. Vol. 184, № 2. P. 291-318.
- Yildiz B.O. et al. Alterations in the dynamics of circulating ghrelin, adiponectin, and leptin in human obesity // Proceedings of the National Academy of Sciences USA. 2004. Vol. 101, № 28. P. 10434- 10439.
- Yuan M.J. et al. Potential new role of the GHSR-1amediated signaling pathway in cardiac remodeling after myocardial infarction (Review) // Oncology Letters. 2014. Vol. 8, № 3. P. 969-971.
- Zhang J.V.O. et al. Obestatin, a peptide encoded by the ghrelin gene, opposes ghrelin's effects on food intake // Science. 2005. Vol. 310. P. 996-999.


