Физиологические механизмы регуляции альфа-1-адренорецепторов артерий к норэпинефрину при симпатолизисе на фоне 5-дневной холодовой адаптации
Автор: Ананьев В.Н., Ананьев Г.В., Ананьева О.В.
Журнал: Человек. Спорт. Медицина @hsm-susu
Рубрика: Физиология
Статья в выпуске: 2 т.25, 2025 года.
Бесплатный доступ
Цель: исследовать механизмы реактивности а1-адренорецепторов артериальных сосудов на норэпинефрин при функциональном симпатолизисе после 5-дневной холодовой адаптации.
Кролики, 5-дневная холодовая адаптация, симпатолизис, электростимуляция мышц, норэпинефрин, а1-адренорецепторы артерий
Короткий адрес: https://sciup.org/147251206
IDR: 147251206 | УДК: 612.815:574.24 | DOI: 10.14529/hsm250201
Physiological mechanisms of arterial alpha-1-adrenoceptor regulation by norepinephrine during sympatholysis following 5-day cold adaptation
Aim. This study investigated the regulatory mechanisms of arterial α1-adrenoceptor reactivity to norepinephrine (NE) during functional sympatholysis following 5-day cold adaptation.
Текст научной статьи Физиологические механизмы регуляции альфа-1-адренорецепторов артерий к норэпинефрину при симпатолизисе на фоне 5-дневной холодовой адаптации
В.Н. Ананьев1, , Г.В. Ананьев2, , О.В. Ананьева3, , 1 Институт медико-биологических проблем РАН, Москва, Россия
V.N. Ananev1, , G.V. Ananev2, , O.V. Ananeva3, ,
Введение. Адаптация к холоду организма исследуется длительное время. По данным разных авторов показано [8, 17], что при адаптации к холоду имеют значение температура, длительность адаптации, вид животных, возраст и национальность людей и другие факторы. Наступление адаптации к холоду оценивается разными авторами по-своему, одной точки зрения нет, поэтому трудно сравнивать разные исследования между собой.
Значительный научный интерес вызывают механизмы краткосрочной холодовой адаптации [7, 10], так как в настоящее время ши- роко распространены краткосрочные поездки из теплого климата в холодный на 3–10 дней. Это могут быть спортивные поездки на лыжные базы, соревнования, походы, вахтовая работа на Севере и т. д. Адаптация к холоду, по данным многочисленных публикаций, происходит при перераспределении кровотока за счет увеличения тонуса альфа-адренорецепторов [15] и уменьшения кровотока в артериях кожно-мышечной области при уменьшении теплоотдачи. Выработка тепла происходит за счет мышечной дрожи и несократительного термогенеза. Большое значение в выработке тепла играет бурая жировая ткань, которая активируется при холоде [12–14].
Важную роль в регуляции сердечнососудистой системы играет механизм функционального симпатолизиса, когда при работе мышц кровоток в них увеличивается в десятки раз, а кровоток в мышцах без их сокращения уменьшается [3, 4]. Механизмы симпатолизиса еще не полностью изучены, и есть различные точки зрения на этот механизм. Изучение действия холода учеными в Арктике [10] после погружений мужчин в воду (3,3 °C) два раза в день приводило к значительному повышению в крови эпинефрина и норэпинефрина как во время погружений, так и в течение дня. Даже однократное охлаждение в течение 10 мин при 14 °C в воде у людей приводит к повышению концентрации гормонов стресса кортизола, эпинефрина и норэпинефрина, что было опубликовано в работе группы авторов [5].
Gordon K. и др. при изучении адаптации к холоду 7 мужчин, которые ежедневно погружались в холодную воду на 1 час (14 °C) в течение семи дней подряд, наблюдали, что термогенез стал больше, а дрожь снизилась на 36 % [7]. Доказана роль норэпинефрина [13] в термогенезе через β 3 -AR в адипоцитах, что при холоде активирует термогенез.
Различные параметры наступления холода могут вызвать инфаркт миокарда, что показано при исследовании в Швеции [11] у 120380 пациентов, перенёсших инфаркт миокарда. Это подтверждает публикация авторов [16] о том, что длительное пребывание человека на Крайнем Севере может привести к возникновению сердечно-сосудистых заболеваний. В то же время в работе [9] доказана эффективность восстановления в спорте при погружении в холодную воду. Авторы в работах [6, 14] сообщают, что умеренная холодовая акклиматизация снижает последствия различных патологических состояний, в том числе инфаркта миокарда. Исследования учёных [15] выяснили, что симпатическая система через α 1 -адренергические рецепторы при симпато-лизисе направляет кровоток в работающую мышцу.
Анализ литературных источников показал, что механизмы усиления кровотока в работающих мышцах в виде симпатолизиса изучены еще не полностью, особенно на фоне 5 дней холодовой адаптации. Встречаются работы, описывающие симпатолизис у человека и животных при комфортных температу- рах внешней среды и на фоне 30 дней адаптации к холоду [1, 2], но нет ни одной публикации о механизмах симпатолизиса после 5 дней холодовой адаптации, чему и посвящено наше исследование.
Методы и организация исследования. В рамках исследования были проведены опыты на кроликах-самцах весом от 2,5 до 3,5 кг. В качестве анестезии использовался гексенал, вводимый внутривенно в дозе 30 мг/кг. Также применялся гепарин в дозе 1000 единиц на килограмм массы тела. Опыты проведены в четырех сериях: две серии без воздействия холода и две серии после пяти дней адаптации к холоду. В опытах без холода вошла контрольная группа из 20 кроликов (№ 1) и группа на фоне симпатолизиса – из 15 кроликов (№ 2). На фоне адаптации к холоду, которая проводилась в течение пяти дней с ежедневным охлаждением по шесть часов при температуре – 10 °C, были проведены две серии опытов. Одна серия (№ 3) включала 15 животных после периода 5 дней адаптации к холоду (5-ДХА). Вторая серия (№ 4) проводилась на фоне 5 дней холодовой адаптации при симпатолизисе (СЛ). У всех кроликов вместо сердца мышцы задней конечности перфузировали собственной кровью через бедренную артерию насосом постоянного расхода. У всех кроликов после введения 8 возрастающих доз норэпинефрина от 0,5 до 30 мкг/кг по изменению перфузионного давления (ПД) датчиком давления фирмы «Моторола» MPX5100DP в бедренной артерии определяли активность а1-адренорецепто-ров артерий. Данные давления через аналогоцифровой преобразователь (на базе ADS1286) вводились и записывались в компьютер. Сим-патолизис (СЛ) как уменьшение тонуса бедренной артерии при сокращении мышц моделировали электростимуляцией мышц задней конечности (10 В, 5 Гц, L = 5 мс). Полученные данные «доза – эффект» анализировались в двойных обратных координатах Lineweaver– Burk графическим и математическим методом, что позволило определить чувствительность (1/К) а1-адренорецепторов к норэпинефрину (NE) и количество активных а1-адренорецеп-торов (Pm) в бассейне бедренной артерии.
Статистическую обработку полученных данных производили с помощью программы SPSS Statistics 25.0. Для проверки нормальности распределения данных использовались критерии Шапиро – Уилка и Колмогорова – Смирнова. Для проверки значимости различий
Активность а1-адренорецепторов (М ± m, мм рт. ст.) артерий конечности кролика на 8 доз норэпинефрина в четырех сериях опытов
Dose-dependent response of arterial α1-adrenoceptors (M ± m, mmHg) to norepinephrine in four series of experiments
|
Серия Experimental series |
Доза, мкг/кг (Y) Dose, mcg/kg (Y) |
0,5 (Y) |
1,0 (Y) |
2,0 (Y) |
5,0 (Y) |
10 (Y) |
15 (Y) |
20 (Y) |
30 (Y) |
|
№ 1 |
Контроль (№ 1) Control (№ 1) (М1± m1) |
65 ±2,1 |
94 ±1,7 |
122 ±3,5 |
148 ±4,2 |
159 ±4,6 |
163 ±5,1 |
165 ±4,2 |
167 ±4,5 |
|
№ 2 |
Симпатолиз Sympatholysis (М2 ± m2) |
3 ±0,12 * |
6 ±0,14 * |
11 ±0,3 * |
26 ±0,8 * |
45 ±1,2 * |
60 ±1,8 * |
71 ±1,1 * |
88 ±1,7 * |
|
№ 3 |
Холод 5 дней Cold adaptation (М3 ± m3) |
49 ±0,75 * ■ |
77 ±1,5 * ■ |
106 ±1,3 * ■ |
138 ±1,1 * ■ |
153 ±2,2 ■ |
159 ±1,8 ■ |
162 ±1,3 ■ |
165 ±2,0 ■ |
|
№ 4 |
Холод 5 дней при симпатолизе Cold adaptation + sympatholysis (Sym) (М4 ± m4) |
6 ±0,14 *▲ ■ |
11 ±0,24 *▲ ■ |
22 ±0,51 *▲ ■ |
50 ±1,7 *▲ ■ |
83 ±1,8 *▲ ■ |
107 ±1,9 *▲ ■ |
125 ±1,7* ▲ ■ |
150 ±2,1 *▲ ■ |
Примечание: * – p ≤ 0,01 изменения достоверны к контролю (№ 1); ▲ – p ≤ 0,01 изменения достоверны к Холоду 5 дней (№ 3); ■ - p < 0,05 изменения достоверны к Симпатолизису (№ 2).
Note: * – p ≤ 0.01 compared to control group (№ 1); ▲ – p ≤ 0.01 compared to cold adaptation group (№ 3); ■ - p < 0.05 compared to sympatholysis group (№ 2).
между двумя группами использовался t-тест Стьюдента для независимых выборок.
Результаты. Во всех группах кроликов (№ 1–4) на все 8 доз введения в бедренную артерию NE происходило дозозависимое увеличение перфузионного давления (см. таблицу, рис. 1). При симпатолизисе в результате электростимуляции мышц (№ 2) на все дозы NE от 0,5 до 30 мкг/кг ПД повышалось намного меньше, чем в контроле (№ 1). Такой механизм позволяет увеличивать кровоток в работающей мышце, чем интенсивней работает мышца, тем больше в ней кровоток. Норэпинефрин сокращает артерии, поэтому важно знать механизм, как в работающей мышце происходит значительное снижение прессорного действия NE на артерии мышцы. Анализ реактивности (см. таблицу, рис. 1) артерий к NE контрольной группы (№ 1) и кроликов при сокращении мышц при симпатолизисе (№ 2) показал, что симпатолизис снижает прессорную реактивность а1-AR артерий, а значит, увеличивает кровоток при низких дозах (0,5 мкг/кг) – в 21,6 раза, при средних (5 мкг/кг) – в 5,3 раза, при высоких дозах (30 мкг/кг) – только в 1,9 раза.
Пятидневная холодовая адаптация (№ 3) без симпатолизиса привела к изменению функ- циональных свойств а1-AR артерий (см. таблицу, рис. 2), где прессорное действие NE достоверно (p < 0,05) было меньше контроля (№ 1) при дозах NE от 0,5 до 5 мкг/кг, а при увеличении дозы NE от 10 до 30 мкг/кг различия были не достоверны (p > 0,05).
Анализ результатов различий реактивности артерий между сериями (№ 1) и (№ 3) по Лайниуверу – Берку показал, что это обусловлено большей чувствительностью (1/К) а1-AR в контроле, где 1/К = 1,2. После холода (№ 3) чувствительность а1-AR артерий уменьшилась на 33,3 % и составила 1/К = 0,8 (рис. 2, 3). Количество активных (Pm) а1-AR артерий в контроле (№ 1) и на фоне 5 дней холода (№ 3) не изменилось и было одинаково Pm = = 172 мм рт. ст. (p < 0,05).
После 5-ДХА физиологический механизм увеличения кровотока в работающих мышцах (симпатолизис) сохранился, но был гораздо меньше, чем у кроликов без холода (см. таблицу), особенно на высокие дозы NE. Отсюда можно заключить, что кратковременная 5-ДХА снижает кровоток в работающих мышцах, поэтому в этот период адаптации проблематично получить хорошие спортивные результаты, значит, нужна более длительная холодовая адаптация в течение 30 дней, что было пока- зано в нашей работе [2], где кровоток после 30 дней холодовой адаптации при симпатоли-зисе достоверно увеличился.
Анализ реактивности артерий к NE при 5-ДХА кроликов при симпатолизисе (№ 4) показал, что СЛ снижает прессорную реактивность а1-AR артерий к NE, а значит, увеличивает кровоток: при низких дозах (0,5 мкг/кг) – в 8,16 раза, при средних (5 мкг/кг) – в 2,76 раза, при высоких дозах (30 мкг/кг) – только в 1,1 раза (№ 4), что было гораздо меньше, чем при СЛ без холода (№ 2). Эти данные позволяют сделать заключение, что эффективность сим-патолизиса (увеличение кровотока при сокращении мышц) на фоне 5-ДХА значительно уменьшается с увеличением дозы норэпинефрина (№ 4) и достоверно меньше СЛ без холода (№ 2). На фоне 5-ДХА при симпатолизи- се (№ 4) (см. таблицу, рис. 1) на все дозы NE ПД повышалось намного меньше, чем в серии опытов без симпатолизиса (№ 3).
Для примера, введение (см. таблицу, рис. 1) дозы NE 0,5 мкг/кг посл е 5-ДХА в бедренную артерию (№ 3) ПД у в еличилось на 49 ± ± 0, 7 5 мм рт. ст., а при с и мпатолизисе (№ 4) только на 6 ± 0,14 мм рт. ст., значит, прессорное действие NE на а1-AR артерий при 5-ДХА и СЛ уменьшилось в 8,16 раза (p < 0,05). При 5-ДХА ввод дозы NE 30 мкг/кг (с м . рис. 1) в бедренную артерию (№ 3) увеличилось ПД на 165 ± 2 мм рт. ст., а при СЛ (№ 4) – на 150 ± ± 2,1 мм рт. ст., действие NE при СЛ н а а1-AR при 5-ДХА уменьшилось в 1,1 раза (p < 0,05).
После 5-ДХА при симпатолизисе (№ 4) происходило значительное уменьшение прессорного действия всех доз NE на артерии
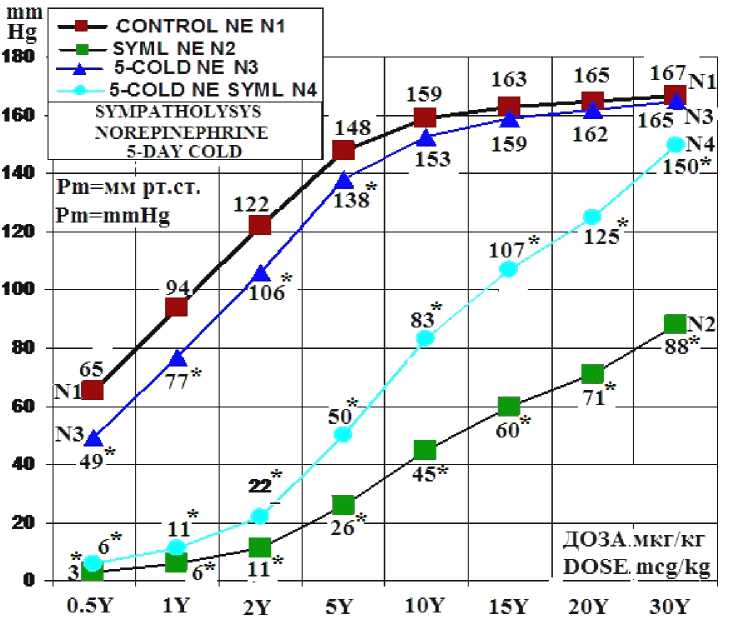
Рис. 1. Увеличение перфузионного давления в бедренной артерии в 4 группах кроликов на 8 доз норэпинефрина (NE): в контрольной группе (CONTROL) животных (№ 1), кроликов при симпатолизисе (SIMPL) (№ 2), животных после 5 дней (5-COLD) холодовой адаптации (№ 3), животных после 5 дней холодовой адаптации (COLD NE SIMPL) при симпатолизисе (№ 4). Ось абсцисс: доза норэпинефрина в мкг/кг (Y). Ось ординат: увеличение перфузионного давления (мм р т. ст.). Примечание. * – p ≤ 0,05 изменения достоверны к контролю (№ 1), другие дост о верности между данными опытов – в таблице
Fig. 1. Dose-response relationship of norepinephrine-induced perfusion pressure changes across experimental groups: control group (№ 1), sympatholysis (№ 2), cold adaptation (№ 3), cold adaptation + sympatholysis (№ 4). X-axis: norepinephrine dose, mcg/kg (Y). Y-axis: perfusion pressure increase (mmHg). Note. * – p ≤ 0.05 compared to control group (№ 1), complete intergroup comparisons presented in Table
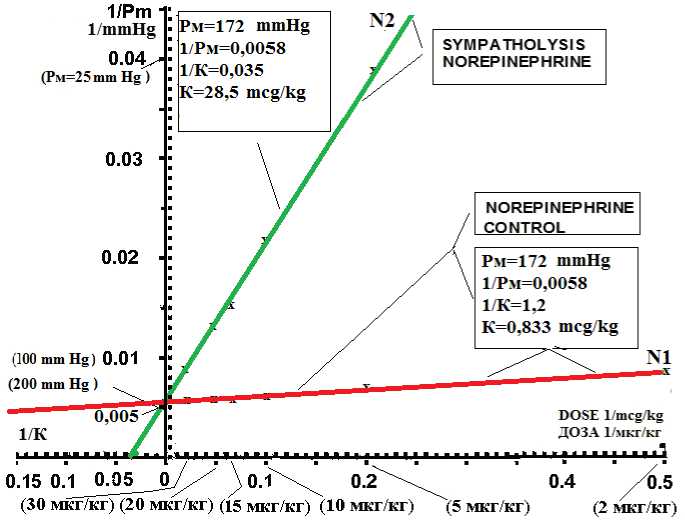
Рис. 2. Увеличение перфузионного давления в бедренной артерии в 2 группах кроликов на 8 доз норэпинефрина в контрольной группе животных ( № 1) и кроликов при симпатолизисе ( № 2) в двойных обратных координатах Лайниувера – Берка. Ось абсцисс: доза норэпинефрина в обратной величине 1/(мкг/кг). Ось ординат: перфузионное давление в обратной величине 1/(мм рт ст.)
Fig. 2. Lineweaver – Burk transformation of norepinephrine dose-response curves across experimental groups: control group ( № 1) and sympatholysis ( № 2). X-Axis: inverse norepinephrine dose 1/(mcg/kg). Y-Axis: inverse perfusion pressure change 1/(mmHg)
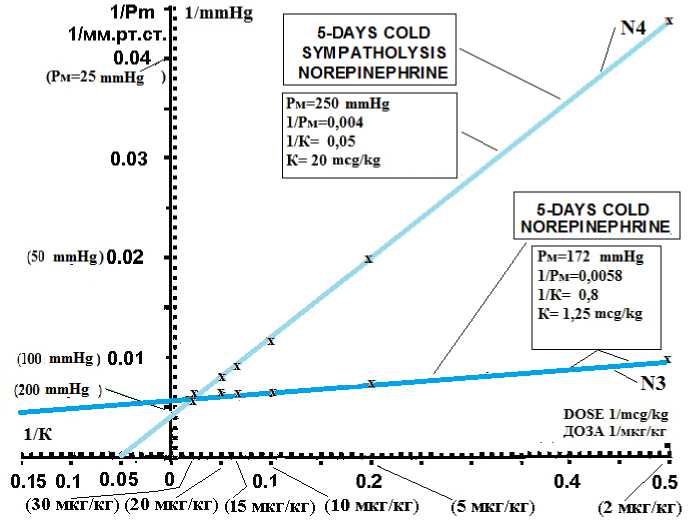
Рис. 3. Увеличение перфузионного давления в бедренной артерии в 2 группах кроликов на 8 доз норэпинефрина у животных после 5 дней ( № 3) холодовой адаптации и у животных после 5 дней ( № 4) холодовой адаптации при симпатолизисе при анализе в двойных обратных координатах Лайниувера – Берка. Ось абсцисс: доза норэпинефрина в обратной величине 1/(мкг/кг). Ось ординат: перфузионное давление в обратной величине 1/(мм рт. ст.) Fig. 3. Lineweaver – Burk transformation of norepinephrine dose-response curves across experimental groups: cold adaptation ( № 3) and cold adaptation + sympatholysis ( № 4). X-Axis: inverse norepinephrine dose 1/(mcg/kg). Y-Axis: inverse perfusion pressure change 1/(mmHg)
по сравнению с реакциями артерий только при 5-ДХА (№ 3). Наши опыты показали, что после 5-ДХА при мышечном сокращении кровоток увеличивался, как и у животных без холода, но в гораздо меньшей степени.
Анализ реактивности а1-AR артерий к NE после 5-ДХА (№ 3) с опытами с симпатолизи-сом (№ 4) по методу Lineweaver – Burk показал, что после 5 дней холода при симпатоли-зисе количество активных (Pm) а1-адрено-рецепторов артерий значительно возросло – в 1,45 раза (на 45,3 %) до Pm = 250 мм рт. ст. по сравнению с опытами (№ 3) без СЛ, где Pm = 172 мм рт. ст. (см. рис. 1, 2). Значительное (см. рис. 2, 3) повышение количества а1-AR и их чувствительности (с 1/К = 0,035 в № 2) а1-AR при СЛ на фоне 5-ДХА (до 1/К = 0,05 в № 4) было механизмом уменьшения кровотока при сокращении мышц на фоне 5-ДХА, что уменьшило прогрев поверхности тела и способствовало сохранению тепла.
Заключение. Наше исследование доказало, что изменения функциональной активно- сти а1-AR артерий после 5 дней холодовой адаптации показывают физиологические механизмы регуляции кровотока в работающих мышцах, когда при значительном холоде секреция норэпинефрина возрастает. В результате эффект симпатолизиса уменьшается (уменьшается кровоток), уменьшается прогрев «оболочки тела» и, соответственно, отдача тепла в окружающую среду, что предотвращает гибель организма от холода. Таким образом, после 5 дней холодовой адаптации симпато-лизис (увеличение кровотока в работающих мышцах) значительно уменьшается по сравнению с опытами без симпатолизиса. Это происходит за счет увеличения (Pm) количества активных а1-AR к NE и большей их чувствительности (1/К) (см. рис. 1–3). Результаты опытов 5-дневной холодовой адаптации показывают, что физические нагрузки на этом фоне не будут эффективными, так как кровоток будет гораздо меньше в работающих мышцах по сравнению с симпатолизисом в мышцах без 5-дневной холодовой адаптации.


