Физиологические особенности гемоцитов Therea olegrandjeani
Автор: Гребцова Е.А., Присный А.А.
Статья в выпуске: 1 т.257, 2024 года.
Бесплатный доступ
Цель исследования заключалась в составлении гемоцитарной формулы имаго Therea olegrandjeani, изучении устойчивости каждого гемоцитарного типа к осмотической нагрузке и общей жизнеспособности клеток. Фагоциты проявляют стойкость к изменению осмолярности среды благодаря резерву плазмалеммы и мембранным органеллам. Прогемоциты ввиду отсутствия складчатости мембраны способны противостоять лишь кратковременному воздействию гипотонических условий, активируя чувствительные к объему пути переноса ионов. Гранулоциты и сферулоциты обладают механизмами регуляторного уменьшения объема, что позволяет возвращать размеры к исходному состоянию. Жизнеспособность клеток стремительно снижается после 10 минут пребывания в условиях, отличных от физиологически нормальных.
Гемолимфа, гемоциты, мембранный резерв клеток, осмотическая нагрузка
Короткий адрес: https://sciup.org/142240443
IDR: 142240443 | УДК: 591.111.1: | DOI: 10.31588/2413_4201_1883_1_257_55
Physiological features of hemocytes of Therea olegrandjeani
The aim of the study was to compile the hemocytic formula of imago Therea olegrandjeani, to study the resistance of each hemocytic type to osmotic load and the overall viability of cells. Phagocytes are resistant to changes in the environment osmolarity due to the reserve of the plasmalemma and membrane organelles. Due to the lack of membrane folding, progemocytes are able to withstand only short-term effects of hypotonic conditions, activating volume-sensitive ion transport pathways. Granulocytes and spherulocytes have mechanisms of regulatory volume reduction, which makes it possible to return the size to its normal state. Cell viability decreases rapidly after 10 minutes of being in conditions other than physiologically normal.
Текст научной статьи Физиологические особенности гемоцитов Therea olegrandjeani
Способность к саморегуляции объема является важным условием для поддержания функциональной активности гемоцитов. Мембранный резерв представляет собой один из важнейших параметров клеток. Способность противостоять осмотической нагрузке может достигаться различными механизмами в зависимости от рассматриваемого гемоцитарного типа. Преобладание микровозвышений на поверхности плазмалеммы, обилие везикул и лизосом в цитоплазме позволяют фагоцитам демонстрировать устойчивость к осмотическому стрессу и выполнять свою прямую функцию – захват инородных объектов [1, 2].
Использование современных подходов в изучении физиологии клетки позволяет выявить ряд закономерностей, которые могут характеризовать сравнительные аспекты реализации функций клеток лимфоидного ряда в филогенезе. Одним из актуальных направлений исследований является изучение гемоцитарных реакций беспозвоночных животных в условиях экспериментального осмотического стресса.
Цель данного исследования – составить гемоцитарную формулу имаго Therea olegrandjeani, изучить устойчивость каждого гемоцитарного типа к осмотической нагрузке и определить общую жизнеспособность клеток гемолимфы.
Материал и методы исследований. Гемолимфу получали нелетальным способом из кончика усика, делили на 3 равных объема (20 мкл) и помещали в разные условия: изотоническую (0,97 % NaCl), гипертоническую (1,50 % NaCl) и сильно гипотоническую (0,25 % NaCl) среды. Определяли жизнеспособность с помощью автоматического счетчика клеток в каждой группе, спустя 3, 10 и 30 минут инкубации посредством окрашивания трипановым синим. Для регистрации морфологических изменений в эти же временные точки проводили наблюдения с помощью световой микроскопии (Nikon Eclipse Ti-E) с добавлением нейтрального красного красителя в режиме реального времени. Фиксировали исчезновение гемоцитарных типов, нарушение целостности мембран, размеры клеток, характер распределения гранул в клетке. Эксперимент проводили в трех повторностях.
Рассчитаны показатели абсолютного и относительного мембранного резерва. При вычислении площади круглых клеток использовали формулу площади круга, в случае клеток с неправильной формой, принимали их форму за эллипс и использовали формулу площади эллипса.
Рассчитывали абсолютную величину мембранного резерва (∆S) как разность между площадью клетки в сильно гипотоническом растворе и площадью клетки в изотонической среде [3].
AS = S(Cr) - S(И) , (1)
где AS - резерв плазмалеммы (gm2); S(Cr) - площадь клетки, после инкубации в сильно гипотонической среде (gm2); S(H) – площадь клетки, после инкубации в изотонической среде (µm2).
С целью сравнения использования мембранного резерва в сильно гипотоническом растворе гемоцитами насекомых определяли относительный мембранный резерв (MR) с использованием формулы [3]:
MR = (AS/Б(СГ))-100 % , (2)
где MR – доля используемого мембранного резерва (%); AS - резерв плазматической мембраны (gm2); S(Cr) -площадь клетки, после инкубации в сильно гипотонической среде (µm2).
Результат исследований.
Гемоцитарная формула имаго T. olegrandjeani представлена прогемоцитами (11 %), плазмоцитами (23 %), гранулоцитами (44 %), сферулоцитами (16 %), коагулоцитами (6 %).
Линейные параметры прогемоцитов и их ядер после трех минут пребывания в растворе с пониженной осмолярностью сохранились прежними. Спустя 10 минут наблюдения гемоциты погибали из-за разрыва плазмалеммы без предварительного увеличения объема. Ввиду изначально сглаженного микрорельефа прогемоцитов [1], они способны противостоять гипоосомотическому стрессу лишь короткое время.
Отсутствие значимого увеличения размеров прогемоцитов в условиях пониженного осмотического давления, указывает на то, что клетки способны компенсировать отклонение от оптимального физиологического состояния. В этот период активируются механизмы транспорта ионов, реагирующие на малейшее изменение объема клеток, и обеспечивают уменьшение прогемоцитов до прежних размеров [4].
Размеры и морфология плазмоцитов не изменились по истечении трех минут инкубации в условиях пониженной осмолярности. Спустя 10 минут зафиксировано отсутствие псевдоподий и утрата подвижности. При дальнейшем наблюдении в режиме live зафиксировано повреждение лизосомальных мембран – в присутствии нейтрального красного цвет переходил от красного к бурому. Впоследствии происходили видимые разрывы плазмалеммы.
К 10 минуте гранулоциты значительно увеличились в размерах (Рисунок 1), однако ризоподии на поверхности все еще присутсвовали. Окрашенные нейтральным красным красителем клетки сохраняли красный оттенок. К 15-20 минуте площадь 83 % гранулоцитов достигла максимальных значений, у большинства гранулоцитов наблюдали частичное разрушение гранул и отсутствие псевдоподий. Однако в популяции этих гемоцитов оставались клетки меньшего размера без признаков нарушения внутриклеточных мембран. Это свидетельствует о том, что гранулоцитам в отличие от прогемоцитов требуется некоторое время для активации механизмов, позволяющих удалить избыток воды.
По истечении 10 минут диаметр сферулоцитов увеличился всего на 7-10 %. К концу экспериментального периода зафиксировано увеличение линейных параметров клеток на 23 %. Способность компонентов внутриклеточных мембран встраиваться в плазмалемму обеспечивает целостность сферулоцитов.
При попадании в гипотонический раствор коагулоциты немедленно набухали, наблюдались множественные повреждения мембраны и выход содержимого цитоплазмы во внешнюю среду.
Прижизненное окрашивание клеток трипановым синим позволило проанализировать жизнеспособность клеток в условиях осмотического стресса. Контрольный образец гемолимфы инкубировали в изотоническом растворе. Процент живых клеток составил 92,0 %.
Доля неповрежденных гемоцитов после трехминутной инкубации в сильно гипотонической среде составила 75,7 %. Отмеченная неустойчивость прогемоцитов и коагулоцитов позволяет предположить, что именно они оказались в числе погибших клеток. Спустя 10 минут инкубации количество живых клеток не превышало 71 %. К 30 минуте инкубации процент мертвых гемоцитов достиг 73 % (Рисунок 2).
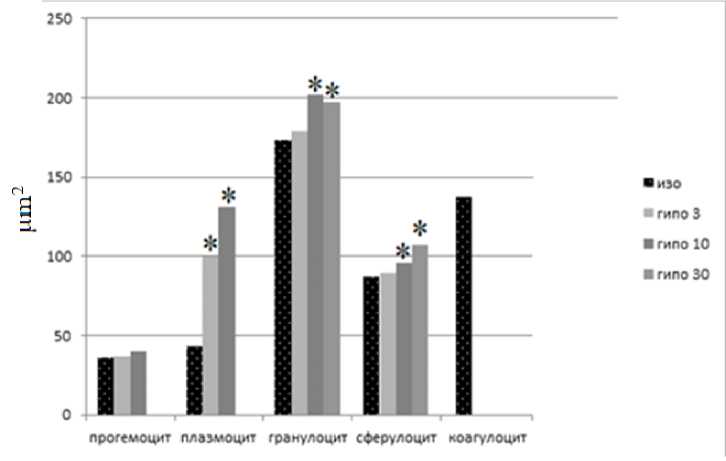
Рисунок 1 – Динамика изменения площади гемоцитов в условиях пониженного осмотического давления. Примечание: * – статистически достоверные различия между значениями параметров гемоцитов в условиях изотонии и при осмотической нагрузке по критерию Стьюдента при P<0,05
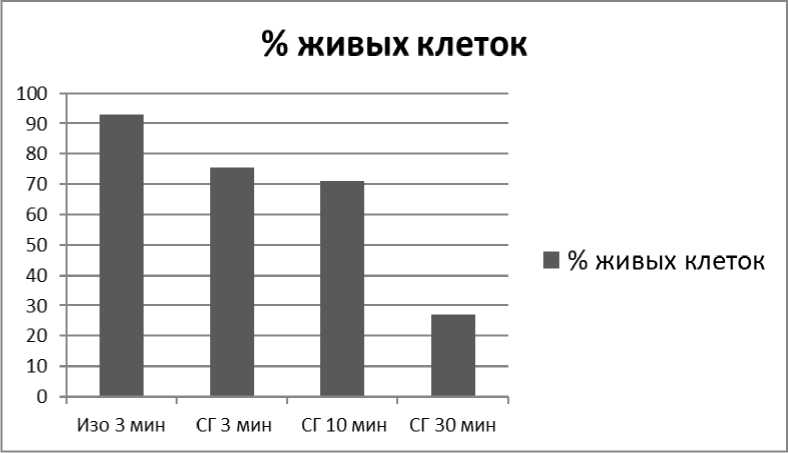
Рисунок 2 – Динамика жизнеспособности клеток при длительной гипоосмотической
нагрузке. «Изо» – изотонический раствор, «Сг» – сильно гипотонический раствор
При определении мембранного резерва учитывали максимальную площадь, зафиксированную для каждого гемоцитарного типа. Мгновенное разрушение коагулоцитов свидетельствует об отсутствии складчатости мембран (Таблица 1).
Таблица 1 – Показатели абсолютного ∆S и относительного мембранного резерва MR гемоцитов
|
Тип клеток |
∆S (µm2) |
MR (%) |
|
прогемоциты |
3,68 |
9,2 |
|
плазмоциты |
87,48 |
66,77 |
|
гранулоциты |
61,87 |
26,27 |
|
сферулоциты |
29,39 |
25,24 |
|
коагулоциты |
0 |
0 |
Значительное уменьшение линейных параметров прогемоцитов было хорошо заметно уже в первые минуты пребывания в условиях повышенной осмолярности. К 10 минуте клетки теряли округлые очертания, приобретали неправильную угловатую форму.
После трехминутной инкубации в гипертонической среде диаметр ядер плазмоцитов уменьшился на 8-13 %, лобоподии клеток сменились игольчатыми выростами. По истечении 10 минут происходило дальнейшее уменьшение гемоцитов, их контуры становились нечеткими, ядро не идентифицировалось.
Постепенное уменьшение площади гранулоцитов не привело к снижению жизнеспособности спустя 10 минут пребывания в гипертонической среде. Однако уже к 30 минуте только 32 % гранулоцитов не имели серьезных повреждений и увеличили свои линейные параметры до состояния 93 % от первоначальных размеров (Рисунок 3). Это свидетельствует о запуске процесса регуляторного восстановления объема. Оставшиеся клетки окрашивались трипановым синим.
К 30 минуте пребывания в среде с повышенной осмолярностью отмечено уменьшение размеров сферулоцитов, что привело к более плотному расположению гранул,
Коагулоциты к 10-ой минуте инкубации в гипертонической среде погибали.
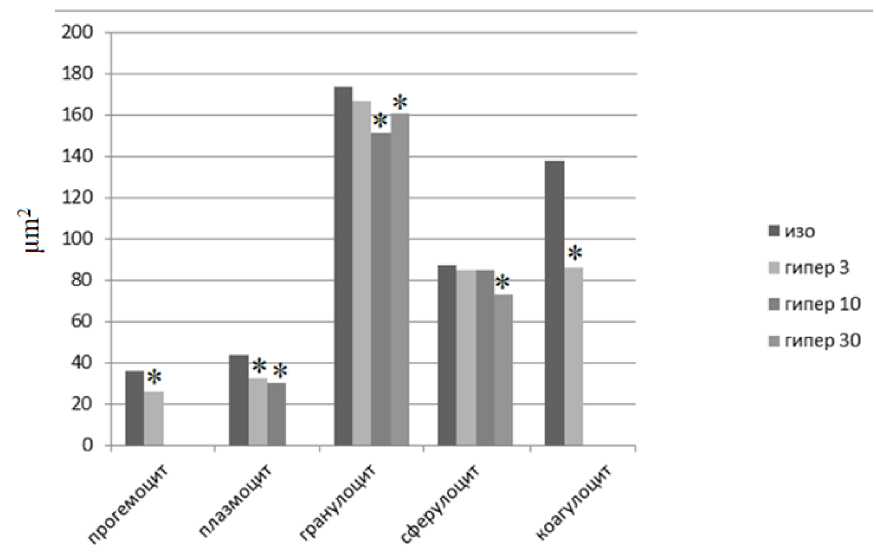
Рисунок 3 – Динамика изменения площади гемоцитов в условиях повышенного осмотического давления. Примечание: * – статистически достоверные различия параметров гемоцитов в условиях изотонии и при осмотическом стрессе по критерию Стьюдента при P<0,05
Сферулоциты и некоторые клетки из популяции гранулоцитов T. olegrandjeani проявляют устойчивость в условиях осмотической нагрузки благодаря запуску механизмов регуляторного восстановления объема. При набухании в гипотонической среде клетки могут задействовать элементы микрорельефа поверхности и сеть внутриклеточных мембран для предотвращения повреждений плазмалеммы. Возвращение размеров клеток к физиологической норме обеспечивается активацией путей переноса ионов [2, 4].
В условиях гипертонической нагрузки регуляторное увеличение объема происходит в ответ на малейшее отклонение размеров клеток от физиологической нормы. При оценке общей жизнеспособности в условиях гипертонической нагрузки к третьей минуте инкубации количество живых клеток составило – 91,3 %, к 10 минуте – 57,6 %, к 30 минуте – 32,3 %.
Заключение. В гемолимфе имаго T. olegrandjeani представлено пять гемоцитарных типов. Плазмоциты и гранулоциты играют главную роль в осуществлении защитных реакций. Высокие показатели мембранного резерва связаны с повышенной складчатостью плазмалеммы, что позволяет не только обеспечивать реакции фагоцитоза, но и противостоять пониженному осмотическому давлению. Кроме того, гранулоциты обладают механизмами регуляторного уменьшения объема. Максимальную устойчивость к осмотической нагрузке продемонстрировали сферулоциты. Клетки проявили наибольшую жизнеспособность при десятиминутном воздействии гипотонической среды, нежели гипертонической. Однако спустя 30 минут и в тех, и в других условиях значения выровнялись, и число живых клеток в обоих случаях не превышало 33 %.
Список литературы Физиологические особенности гемоцитов Therea olegrandjeani
- Гребцова Е. А. Морфофункциональная характеристика и осморегуляторные реакции гемоцитов представителей отряда Dictyoptera: диссертация.. кандидата биологических наук: 03.03.01 / Гребцова Елена Александровна; [Место защиты: Белгород. гос. аграр. ун-т им. В.Я. Горина]. - Белгород, 2017. - 184 с. EDN: OWUEPF
- Зацепина Г. Н. Изменение адаптационной способности и кинетики адаптации Т-лимфоцитов к гипотонии в патологических состояниях организма млекопитающих / Г. Н. Зацепина, С. В. Егудина, О. В. Тарнопольская // Биофизика. - 1992. - Т. 37. - Вып. 1. - С. 142-148.
- Орлов, С. Н. Регуляция объема клеток: механизмы, сопряженные клеточные реакции и патофизиологическое значение / С. Н. Орлов, К. Н. Новиков, // Физиологический журнал им. И М. Сеченова. - 1996. - Т. 82. - № 8-9. - С. 1-15.
- Орлов, С. Н. Механизмы активации ионного транспорта при изменении объема клеток / С. Н. Орлов, Т. Г. Гурло // Цитология. -1991. - Т. 33. -№ 11. - С. 101-110.
- Mc Manus, M. L. Regulation of Cell Volume in Health and Disease / M. L. Mc Manus, K. B. Churchwell [et. al.] // The New England Journal of Medicine. -1995 - № 19. - P. 123-134.
- Sardini, A. Cell Volume Horneostasis: The Role of Volurne-Sensitive Chloride Channels, Editor(s): E. Edward Bittar, Michael Pusch / A. Sardini // Advances in Molecular and Cell Biology, Elsevier -2006 - V. 38 - P. 199-214.


