Формы периодической кататонии при расстройствах шизофренического спектра: различия в уровнях активности тромбоцитарных ферментов
Автор: Бокша Ирина Сергеевна, Савушкина Ольга Константиновна, Прохорова Татьяна Андреевна, Терешкина Елена Борисовна, Воробьева Елена Анатольевна, Пискарв Михаил Валерьевич, Бурбаева Гульнур Шингожиевна
Журнал: Сибирский вестник психиатрии и наркологии @svpin
Рубрика: Биологические исследования
Статья в выпуске: 2 (123), 2024 года.
Бесплатный доступ
Актуальность. Приступы периодической кататонии при шизофрении и других расстройствах шизофренического спектра представляют проблему для разработки дифференцированных индивидуальных терапевтических подходов. Цель исследования: сравнительный анализ уровней активности тромбоцитарных ферментов глутаматного, энергетического и глутатионового метаболизма у пациентов с различными клиническими формами приступов (гипо-, пара- и мультикинетической) периодической кататонии, формирующимися при шизофрении и расстройствах шизофренического спектра. Материал и методы. Исследование выполнено сотрудниками отдела по изучению пограничной психической патологии и психосоматических расстройств и лаборатории нейрохимии ФГБНУ НЦПЗ. В исследование включены пациенты (n=39) основной группы, из них 16 мужчин и 23 женщины, с гипокинетической, паракинетической и мультикинетической формами приступов периодической кататонии при шизофрении и расстройствах шизофренического спектра (шизоаффективном или шизотипическом) и добровольцы без диагностированных психических расстройств (n=22, 9 мужчин и 13 женщин) контрольной группы. Уровни активности ферментов (цитохром с-оксидазы, глутаматдегидрогеназы, активируемой фосфатом глутаминазы, глутатионредуктазы, глутатион-S-трансферазы) в экстрактах тромбоцитов пациентов основной группы и добровольцев контрольной группы определяли спектрофотометрическими кинетическими методами.
Расстройства шизофренического спектра, шизофрения, периодическая кататония, цитохром с-оксидаза, глутаматдегидрогеназа, активируемая фосфатом глутаминаза, глутатионредуктаза, глутатион-s-трансфераза, тромбоциты
Короткий адрес: https://sciup.org/142241566
IDR: 142241566 | УДК: 616.895.84-055.1-055.2,465?16/?57,:616-008.831 | DOI: 10.26617/1810-3111-2024-2(123)-13-23
Forms of periodic catatonia in schizophrenia spectrum disorders: differences in the levels of platelet enzyme activity
Background. Attacks of periodic catatonia in schizophrenia and other schizophrenia spectrum disorders pose a challenge for the development of differentiated individual therapeutic approaches. Objective of the study: comparative analysis of the levels of activity of platelet enzymes of glutamate, energy and glutathione metabolism in patients with various clinical forms of attacks (hypo-, para- and multikinetic) of periodic catatonia, developing in schizophrenia and schizophrenia spectrum disorders. Material and Methods. The study was carried out by employees of the Department for the Study of Borderline Mental Pathology and Psychosomatic Disorders and the Laboratory of Neurochemistry of the Federal State Budgetary Scientific Institution “Mental Health Research Center”. The study included patients (n=39) of the main group, including 16 men and 23 women, with hypokinetic, parakinetic and multikinetic forms of attacks of periodic catatonia in schizophrenia and schizophrenia spectrum disorders (schizoaffective or schizotypal) and volunteers without diagnosed mental disorders (n=22, 9 men and 13 women) in the control group. The activity levels of enzymes (cytochrome c oxidase, glutamate dehydrogenase, phosphate-activated glutaminase, glutathione reductase, glutathione-S-transferase) in platelet extracts of patients in the main group and volunteers in the control group were determined by spectrophotometric kinetic methods.
Текст научной статьи Формы периодической кататонии при расстройствах шизофренического спектра: различия в уровнях активности тромбоцитарных ферментов
Анализ зарубежных и отечественных результатов нейрохимических исследований, в том числе проведенных в ФГБНУ НЦПЗ, показывает, что нарушение метаболизма нейромедиаторов, включая глутамат, вносит ключевой вклад в патогенез шизофрении и расстройств шизофренического спектра (РШС) [1, 2, 3, 4]. Кроме того, в качестве существенной составляющей патогенеза шизофрении рассматриваются митохондриальные аномалии (в аспектах нарушений энергетической и антиоксидантной систем) [5].
Однако прямые исследования патофизиологических механизмов в мозге при психических заболеваниях затруднены, поэтому в качестве биохимической модели рассматриваются тромбоциты периферической крови. Действительно, в тромбоцитах содержатся элементы глутаматной метаболической системы [6, 7], представленные её центральными ферментами глутаматдегидрогеназой и активируемой фосфатом глутаминазой, а также присутствуют ферменты митохондриальной дыхательной цепи, в том числе цитохром с- оксидаза. В работах сотрудников ФГБНУ НЦПЗ продемонстрирована информативность определения уровней активности тромбоцитарных ферментов - глутаматдегидрогеназы и цитохром с- оксидазы при расстройствах шизофренического спектра для индивидуальной предикции эффективности антипсихотической терапии больных эндогенными психозами [1, 8]. Помимо того, в тромбоцитах присутствуют ферменты - компоненты антиоксидантной глутатион-зависимой системы - глутатионредуктаза и глутатион-S-трансфраза. Глутатионредуктаза играет важную роль в поддержании пула восстановленного глутатиона, служащего субстратом глутатион-S-трансферазы. Глутатион-S-трансфераза представлена семейством ферментов, обезвреживающих ксенобиотики, а также эндогенные метаболиты, в том числе продукты перекисного окисления, конъюгируя их с восстановленным глутатионом. Устойчивость и чувствительность организма к любому воздействию, в частности к фармакотерапии, зависит от активности глутатион-S-трансферазы в совокупности с другими ферментами глутатионового обмена, включая глутати-онредуктазу. Отечественными [9] и зарубежными исследователями [10] обнаружена связь полиморфизма Р1-варианта гена, кодирующего глута-тион-S-трансферазу, с развитием тардивной дискинезии у больных шизофренией. Уровень глута-тион-S-трансферазы в спинномозговой жидкости снижен у больных шизофренией [11], таким образом, её активность может играть определенную роль в патогенезе, клинической картине РШЗ и в чувствительности к антипсихотической фармакотерапии. Ранее в исследовании, выполненном на базе лаборатории нейрохимии НЦПЗ, обнаружено снижение активности тромбоцитарных глутатионредуктазы и глутатион-S-трансферазы у больных с ультравысоким риском развития психоза (первые юношеские депрессии с аттенуированными симптомами шизофрении) [12], у пациентов с первым психотическим приступом [13], хронически текущей шизофренией и расстройствами шизофренического спектра [14] по сравнению с соответствующими контрольными группами.
Определение связей между уровнями активности цитохром с-оксидазы, глутаматдегидрогеназы, глутатион-S-трансферазы, глутатионредукта-зы в клетках крови и резистентностью / чувствительностью к антипсихотической терапии проводятся в ФГБНУ НЦПЗ при обследовании пациентов с РШС различных половозрастных групп, однако ранее внимание не было сосредоточено на синдроме кататонии, присутствующем у большинства пациентов с шизофренией и РШС. В ФГБНУ НЦПЗ проведены клинические исследования и разработана клиническая систематика форм приступов периодической кататонии (ФППК) при шизофрении и РШС [15, 16]. Так, двигательные расстройства при гипокинетической форме приступов периодической кататонии манифестируют в структуре затяжных депрессий с преобладанием тревожных и обсессивнокомпульсивных дименсий, реализующихся в клиническом континууме шизотипического расстройства. При паракинетической ФППК моторные феномены манифестируют в клинической картине психогенно спровоцированных затяжных истероаффективных психозов, дебютирующих в рамках шизоаффективного расстройства или приступообразной шизофрении. При мультикине-тической ФППК развитие выраженных клинических проявлений моторных расстройств наблюдается в структуре кататоно-параноидных и катато-но-онейроидных приступов в процессе течения параноидной шизофрении.
В свете новой предложенной клинической систематики ФППК представляет интерес поиск связи уровней активности ферментов крови (глутаматдегидрогеназа, глутатионредуктаза, глута-тион-S-трансфераза, активируемая фосфатом глутаминаза, цитохром с-оксидаза) с клиническими особенностями ФППК у больных шизофренией и РШС. В настоящей работе измерялись уровни активности ферментов глутаматного метаболизма - глутаматдегидрогеназы и активируемой фосфатом глутаминазы, энергетического метаболизма -цитохром с-оксидазы, глутатионовой антиоксидантной системы - глутатионредуктазы и глута-тион-S-трансферазы в тромбоцитах крови пациентов с шизофренией и РШС с тремя различными ФППК. Оценка активности этих ферментов в тромбоцитах крови больных, страдающих приступами периодической кататонии, проводилась впервые.
ЦЕЛЬ ИССЛЕДОВАНИЯ
Сравнительный анализ уровней активности тромбоцитарных ферментов глутаматного, энергетического и глутатионового метаболизма у пациентов с различными ФППК (гипокинетической, паракинетической и мультикинетической), формирующимися при шизофрении и РШС.
МАТЕРИАЛЫ И МЕТОДЫ
Сравнительное клинико-биологическое обследование проведено совместно сотрудниками отдела по изучению пограничной психической патологии и психосоматических расстройств и лаборатории нейрохимии ФГБНУ НЦПЗ.
В основную группу исследования включены пациенты (n=39), из них 16 мужчин и 23 женщины, в возрасте 16-57 лет, медиана возраста 21 год [19; 27], с разными ФППК: гипокинетической, паракинетической и мультикинетической [16]. В основу классификации положена психопатологическая структура кататонических расстройств, коррелирующая со степенью тяжести двигательных симптомокомплексов.
Критерии включения: соответствие диагнозов рубрикам МКБ-10 шизофрения, шизоаффективное расстройство или шизотипическое расстройство (F20, F25, F21), приступообразное течение эндогенного заболевания, наличие в структуре текущего эпизода симптомов кататонии, которые определяли при помощи шкалы Буша-Френсиса для оценки тяжести моторных расстройств (BFCRS).
Критерии исключения: проявления тяжелого органического поражения ЦНС, психические нарушения вследствие употребления алкоголя или других психоактивных веществ, наличие тяжелой соматической патологии в стадии декомпенсации, наличие выраженных экстрапирамидных нарушений на момент поступления в стационар на фоне приема антипсихотических препаратов.
Практически у половины больных (n=19, 49%) из 39 было диагностировано шизотипическое расстройство, более чем у трети (n=14, 36%) - шизофрения, у 6 (15%) - шизоаффективное расстройство. Оценка выраженности кататонических расстройств и тяжести состояния проводилась перед началом курса фармакотерапии. Для количественной балльной оценки тяжести психического состояния и эффективности терапии были использованы шкалы PANSS и BFCRS.
В контрольную группу, соответствующую основной группе пациентов по возрастно-половому составу, вошло 22 добровольца без диагностированных психических расстройств (9 мужчин и 13 женщин) от 19 до 53 лет (медиана 25 лет).
Кровь на биохимические анализы отбирали до начала курса фармакотерапии больных. Выделение тромбоцитов из образцов венозной крови, взятой в вакутейнеры с цитратом натрия, и приготовление экстрактов из них проводили методами, описанными ранее [12].
Активность всех перечисленных ферментов определяли спектрофотометрическими кинетическими методами с использованием планшетного спектрофотометра xMark (Bio-Rad, США).
Активности глутаматдегидрогеназы (суммарная активность изоформ ГДГ I+II) и цитохром с-оксидазы определяли собственными оригинальными методами, описанными нами ранее [1].
Активность активируемой фосфатом глутаминазы в тромбоцитах определяли с использованием реакции гидролиза глутамина до глутамата, концентрацию которого измеряли в сопряженной реакции глутаматдегидрогеназы с восстановлением НАД+ по возрастанию оптической плотности при 340 нм [17].
Активности глутатионредуктазы и глутатион-S-трансферазы определяли описанными ранее методами: глутатионредуктазы - по окислению НАДФН в реакции восстановления окисленного глутатиона [13], глутатион-S-трансферазы - по скорости ферментативного образования конъюгатов глутатиона с 1-хлор-2,4-динитробензолом [12]. После определения концентрации белка по методу Лоури (с набором реактивов Bio-Rad, США) для всех ферментов рассчитывали удельную активность.
Первичные результаты наблюдения клиникопсихопатологической динамики у пациентов с шизофренией и РШС и биохимических исследований вносили в базу данных. Для статистической обработки данных использовали программное обеспечение Statistica 10.0 (Statsoft), непараметрический модуль (U-критерий Манна-Уитни), многомерный разведочный анализ (кластерный анализ методом каппа-средних). Различия и корреляции считали статистически значимыми при p<0,05.
РЕЗУЛЬТАТЫ
На первом этапе по клиническим признакам РШС (шизофрения, шизоаффективное и шизотипическое расстройства) сформированы группы пациентов, в которых проведено сравнение выявленных уровней активности ферментов. В соответствии с клиническими проявлениями симптомов кататонии выделены группы больных с тремя ФППК - гипокинетической (n=13), паракинетиче-ской (n=11) и мультикинетической (n=15).
В таблице 1 приведены медианы и квартили удельной активности ферментов (выраженные в ед/мг белка) в основной группе пациентов с тремя разными формами приступов периодической кататонии и в контрольной группе.
При парном сравнении с использованием U-критерия Манна-Уитни уровней активности ферментов у пациентов основной группы с каждой из ФППК и у добровольцев контрольной группы обнаружено, что активность цитохром с-оксидазы статистически значимо не различалась. Активность глутаматдегидрогеназы статистически значимо (p<0,05) снижена при всех трех ФППК, активность активируемой фосфатом глутаминазы снижена только при паракинетической форме.
Активности глутатионредуктазы и глутатион-S-трансферазы были статистически значимо (p<0,05) снижены только при гипокинетической форме, а активность глутатион-S-трансферазы статистически значимо (p<0,005) снижена также и при мультикинетической ФППК.
Таблица 1. Сравнительное распределение уровней активности тромбоцитарных ферментов в основной группе пациентов с разными формами приступов кататонии и в контрольной группе
|
Тро мбоцитарный ферме нт. сд/м г |
Форма приступов кататонии |
Контрольная группа(п=22) |
||
|
Гипокинетическая (п=!3) |
Паракинетическая (п=11) |
Мультикинетическая (п=15) |
||
|
Цитохром с-оксидаза |
4,7 [4,1; 5,61 |
4,4|4,3;5,2| |
4,8|3,7;6,4] |
5,2 (4,9; 6,3] |
|
Активируемая ^юсфатом глутаминаза |
24,9 |22,1; 38,7] |
21.9* [18.8: 29,3[ |
23,1 114,3;33,8| |
30.8 123.3; 44.11 |
|
Глута матде гидрогеназа |
5.0* [2,9; 6,2] |
5.5* [4,5; 6,1] |
5.8* [4,6; 6,4| |
6.4 [5,5; 7,4] |
|
Глутатионредуктаза |
7,6* [5,8; 8,0] |
9.4 |7,5; 11.8| |
8,2 (6.7; 10,0] |
9.1 [7.9; 11.11 |
|
Глу тат ио и S -тра нс (]) сраза |
12,3* [8,9; 15,8] |
12,9 |10.5: 17,0| |
12.2** [11.2; 13,9| |
16,6 113,4; 17,31 |
При м с ч а н и е. Статистически значимые различия: * - р<0,05, ** - р<0,01 (U-критерий Манна-Уитни).
На втором этапе исследования за основу были взяты показатели биохимического исследования. С применением кластерного анализа выделены кластеры пациентов.
Уровни удельной активности ферментов у пациентов основной группы продемонстрировали значительную вариабельность, значения находились в существенно различающихся диапазонах, поэтому перед проведением кластерного анализа полученные данные нормировали по максимуму активности каждого фермента в выборке [18]. Кластерный анализ основной группы пациентов включал кластеризацию случаев, осуществляемую по 5 признакам - нормированным уровням активности ферментов, таких как глутаматдегидрогеназа, глутатионредуктаза, глутатион-S-трансфераза, активируемая фосфатом глутаминаза, цитохром с -оксидаза).
По итогам кластеризации с предустановленным числом кластеров, равным 2, получены два кластера К1 (n=18) и К2 (n=21), сравнимые между собой по численности пациентов.
На рисунке 1 приведены средние нормированные значения активности каждого фермента для К1 и К2.
На рисунке 2 представлены диаграммы с ненормированными уровнями активности (выраженными в ед/мг) каждого из пяти ферментов в кластерах К1 и К2 у пациентов основной группы и добровольцев контрольной группы.
В выделенных кластерах К1 и К2 у пациентов основной группы по сравнению с контрольной группой обнаружено статистически значимое снижение уровней активности ферментов: в К1 -цитохром с -оксидазы и активируемой фосфатом глутаминазы (p<0,05), в К2 - глутаматдегидрогеназы, глутатионредуктазы и глутатион-S-трансферазы (p<0,001).
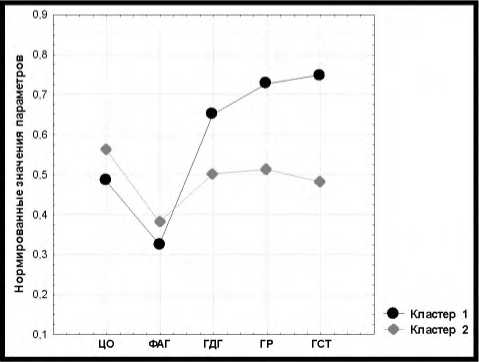
Рисунок 1. Средние значения нормированных биохимических параметров в кластерах
Оценено распределение пациентов с тремя различными ФППК по кластерам К1 и К2 (табл. 2).
Критерий х2 показал высокий уровень статистической значимости неравномерного распределения только для пациентов с гипокинетической и паракинетической ФППК (х2=12,3, р<0,004 с поправкой Йетса). То есть пациенты с гипокинетической ФППК статистически значимо чаще попадали в К2 (с активностями глутаматдегидрогеназы, глутатионредуктазы и глутатион-S-трансферазы, значимо сниженными относительно добровольцев контрольной группы). Пациенты с паракинетической ФППК значимо чаще попадали в К1 со сниженными активностями цитохром с-оксидазы и активируемой фосфатом глутаминазы по сравнению с добровольцами контрольной группы. В то время как пациенты с мультикине-тической ФППК равномерно распределились между кластерами К1 и К2.
Активность цитохром с-оксидазы, Ед/мг
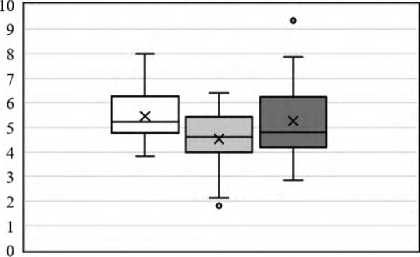
□ Контроль □ Кластер 1 ■ Кластер 2
.Активность глутаминазы.
активируемой фосфатом, Ед/мг
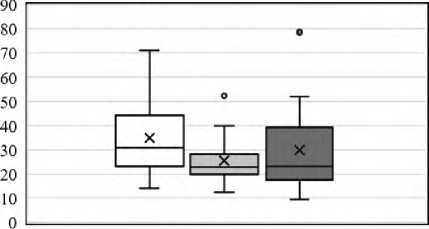
□ Контроль □ Кластер 1 ■ Кластер 2
Активность глутаматдегидрогеназы, Ед/мг
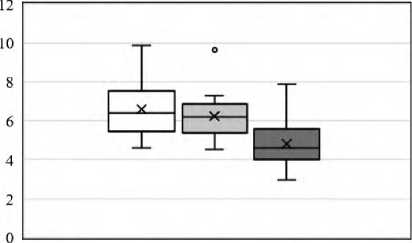
□ Контроль □ Кластер 1 ■ Кластер 2
Активность глутатионредуктазы, Ед/мг
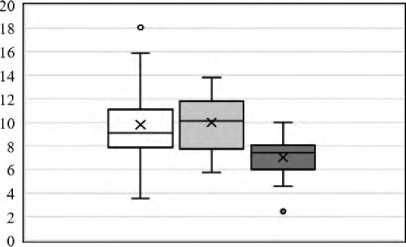
□ Контроль □ Кластер 1 □ Кластер 2
Активность глутатион S-трансферазы, Ед/мг
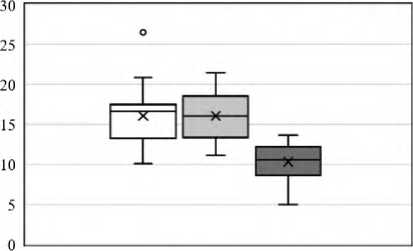
□ Контроль □ Кластер I ■ Кластер 2
Рисунок 2. Активность тромбоцитарных ферментов у больных основной группы с разными формами кататонических приступов и у добровольцев контрольной группы
Таблица 2. Сравнительное распределение пациентов основной группы с разными формами приступов кататонии по кластерам К1 и К2
|
Кластер |
Форма приступов кататонии (число пациентов и % от их числа в кластере) |
||
|
Г и по кинетическая (п=13) |
Пара кинетическая (п=! 1) |
Мульти кинетическая (11=15) |
|
|
К1 (11=18) |
п=4 (22%) |
11=7 (39%) |
11=7 (39%) |
|
К2 (п=21) |
п=9 (43%) |
п=4 (19%) |
п=8 (38%) |
ОБСУЖДЕНИЕ
По материалам собственного исследования впервые удалось обнаружить вариативную картину биохимических изменений (относительно контрольной группы) в тромбоцитах при разных ФППК. Это удалось сделать с использованием двух подходов: 1) выделение трех групп пациентов с учетом клинико-психопатологической симптоматики РШС, оцениваемой в динамике, и обнаружение биохимических отклонений в группах пациентов с разными ФППК от значений в контрольной группе; 2) выделение двух групп пациентов по биохимическим признакам и обнаружение асимметричного неравномерного распределения пациентов в зависимости от ФППК.
Кроме того, в настоящем исследовании при сравнении группы больных с РШС в целом и контрольной группы добровольцев было обнаружено статистически значимое снижение уровней активности глутаматдегидрогеназы в тромбоцитах крови, что согласуется с полученными ранее данными при обследовании больных шизофренией без фокуса на кататонию. Действительно, нарушения функционирования глутаматергической системы занимают важнейшее место в патогенезе шизофрении [4], а глутаматдегидрогеназа является ключевым ферментом метаболизма глутамата, причем уровень активности тромбоцитарной глутаматдегидрогеназы может служить биомаркером, не только связанным с клинико-психопатологической симптоматикой, но и её изменением под действием фармакотерапии [1]. Так, ранее нами установлено снижение активности глутаматдегидрогеназы в тромбоцитах больных шизофренией с хроническим течением заболевания в период обострения психотической симптоматики [1]. Обнаружено снижение уровней активности глутаматдегидрогеназы и у больных с юношескими депрессиями с аттенуированными симптомами шизофрении [12] по сравнению с соответствующими контрольными группами.
Исследования по изучению активности активируемой фосфатом глутаминазы в тромбоцитах у пациентов с РШС и периодической кататонией ранее не проводились. В соответствии с полученными данными можно констатировать статистически значимое снижение активности активируемой фосфатом глутаминазы как в общей группе больных, так и в группе пациентов с паракинети-ческой кататонией. С другой стороны, при распределении больных на кластеры по биохимическим признакам в кластер К1, характеризующийся сниженной активностью активируемой фосфатом глутаминазы, выявлена статистически значимо более высокая частота пациентов с паракине-тической формой кататонии.
В ряде исследований зарегистрированы изменения активности различных компонентов дыхательной цепи митохондрий в тромбоцитах у пациентов с шизофренией. Так, в ранее опубликованных работах в тромбоцитах пациентов с шизофренией было обнаружено повышение активности митохондриального комплекса I, но не цитохром с-оксидазы (комплекса IV) [19]. Другие исследователи выявили разнонаправленное изменение активности комплекса I в тромбоцитах пациентов, а именно статистически значимое повышение в остром состоянии и снижение его активности у пациентов с резидуальными симптомами [20]. Ранее мы обнаружили снижение активности цитохром с-оксидазы тромбоцитов в острой психотической фазе заболевания у пациентов с хроническим течением шизофрении в сравнении с контрольной группой [21], в то же время в недифференцированной группе больных с юношескими депрессиями с аттенуированными симптомами шизофрении активность цитохром с -оксидазы значимо не отличалась от контрольной группы [12].
Хотя в настоящем исследовании в недифференцированной группе пациентов в целом мы не обнаружили значимых изменений в активности цитохром с -оксидазы по сравнению с контрольной группой, однако при выделении кластера К1 активность цитохром с -оксидазы в нем оказалась статистически значимо пониженной. Это может быть связано с тем, что в этот кластер статистически значимо чаще попадали пациенты с пара-кинетической ФППК. Фактически при выделении по клиническому признаку группы пациентов с паракинетической ФППК медиана активности цитохром с -оксидазы в данной группе (4,4 ед/мг) оказалась ниже, чем в контрольной (5,2 ед/мг), но различие не достигло статистической значимости. Мы считаем настоящее исследование пилотным ввиду малочисленности группы с паракинетиче-ской ФППК (11 пациентов), что представляет ограничение исследования. Окончательный вывод о снижении активности цитохром с -оксидазы при паракинетической ФППК можно будет сделать при условии увеличения группы.
Еще одним фактором развития многих психических заболеваний, в том числе и шизофрении, признан окислительный стресс. В настоящем исследовании в недифференцированной группе больных РШС с периодической кататонией оказались статистически значимо сниженными уровни активности глутатион-зависимых ферментов глутатионредуктазы и глутатион-S-трансферазы по сравнению с контрольной группой, что указывает на участие окислительного стресса в развитии патологического процесса. Ранее мы уже наблюдали снижение активности глутатион-зависимых ферментов в тромбоцитах у больных с РШС [13] и параноидной шизофренией с хроническим течением заболевания [22], а в настоящем исследовании обнаружены особенности изменений активности глутатионредуктазы и глутатион-8-трансферазы в зависимости от ФППК. Так, у больных с гипокинетической кататонией снижена активность глутатионредуктазы и глу-татион-S-трансферазы, с мультикинетической формой - только активность глутатион-8-трансферазы, в то же время у пациентов с пара-кинетической ФППК уровни активности обоих ферментов не отличаются от уровня контрольной группы. С другой стороны, в кластер К2 со сниженными активностями обоих ферментов вошло значимо больше пациентов с гипокинетической ФППК.
Неоднородность периодической кататонии представляет проблему как для терапии, так и для прогноза состояния пациентов, что весьма важно, учитывая возможную резистентность пациентов. Представляется актуальным выделение более гомогенных групп (классификации внутри выборки в целом) больных на основе биохимических параметров крови (активности ферментов тромбоцитов) с целью разработки индивидуальных подходов к терапии больных с РШС, страдающих приступами периодической кататонии.
ЗАКЛЮЧЕНИЕ
При разных ФППКнаблюдается гетерогенная степень отклонения активности тромбоцитарных ферментов от контрольных диапазонов. Параки-нетическая и гипокинетическая ФППК, по-видимому, ассоциированы с разными картинами изменений активности изученных ферментов глутаматного, энергетического и глутатионового метаболизма. Дальнейшее исследование активности ферментов крови у пациентов с кататоническими расстройствами является перспективным для выявления специфических биомаркеров различных ФППК.
В статье приведено сокращенное обозначение терминов: РШС - расстройства шизофренического спектра, ФППК - формы приступов периодической кататонии.
Список литературы Формы периодической кататонии при расстройствах шизофренического спектра: различия в уровнях активности тромбоцитарных ферментов
- Savushkina OK, Tereshkina EB, Prokhorova TA, Boksha IS, Burminskii DS, Vorobyeva EA, Morozova MA, Burbaeva GS. Platelet glutamate dehydrogenase activity and efficacy of antipsychotic therapy in patients with schizophrenia. J Med Biochem. 2020 Jan 10;39(1):54-59. doi: 10.2478/jomb-2019-0018. PMID: 32549778; PMCID: PMC7282235.
- Egerton A, Grace AA, Stone J, Bossong MG, Sand M, McGuire P. Glutamate in schizophrenia: Neurodevelopmental perspectives and drug development. Schizophr Res. 2020 Sep;223:59-70. doi: 10.1016/j.schres.2020.09.013. Epub 2020 Oct 16. PMID: 33071070.
- Dogra S, Conn PJ. Metabotropic Glutamate Receptors As emerging targets for the treatment of schizophrenia. Mol Pharmacol. 2022 May;101(5):275-285. doi: 10.1124/molpharm.121.000460. Epub 2022 Mar 3. PMID: 35246479; PMCID: PMC9092465.
- Uno Y, Coyle JT. Glutamate hypothesis in schizophrenia. Psychiatry Clin Neurosci. 2019 May;73(5):204-215. doi: 10.1111/pcn.12823. Epub 2019 Mar 6. PMID: 30666759.
- Rajasekaran A, Venkatasubramanian G, Berk M, Debnath M. Mitochondrial dysfunction in schizophrenia: pathways, mechanisms and implications. Neurosci Biobehav Rev. 2015 Jan;48:10-21. doi: 10.1016/j.neubiorev.2014.11.005. Epub 2014 Nov 15. PMID: 25446950.
- Asor E, Ben-Shachar D. Platelets: A possible glance into brain biological processes in schizophrenia. World J Psychiatry. 2012 Dec 22;2(6):124-33. doi: 10.5498/wjp.v2.i6.124. PMID: 24175178; PMCID: PMC3782191.
- Baier PC, Koch JM, Seeck-Hirschner M, Ohlmeyer K, Wilms S, Aldenhoff JB, Hinze-Selch D. A flow-cytometric method to investigate glutamate-receptor-sensitivity in whole blood platelets ‒ results from healthy controls and patients with schizophrenia. J Psychiatr Res. 2009 Mar;43(6):585-91. doi: 10.1016/j.jpsychires.2008.07.005. Epub 2008 Aug 20. PMID: 18718602.
- Прохорова Т.А., Бокша И.С., Савушкина О.К., Терешкина Е.Б., Воробьева Е.А., Помыткин А.Н., Каледа В.Г., Бурбаева Г.Ш. Активность тромбоцитарной глутаматдегидрогеназы у больных с эндогенными психозами. Журнал неврологии и психиатрии им. С.С. Корсакова. 2016. Т. 116, № 3. С. 44-48. doi: 10.17116/jnevro20161163144-48.
- Иванова С.А., Бойко А.С., Федоренко О.Ю., Щигорева Ю.Г., Рудиков Е.В., Бородюк Ю.Н., Семке А.В., Бохан Н.А. Полиморфизм гена фермента глутатион-S-трансферазы двигательные нарушения у больных шизофренией. Фундаментальные исследования. 2013. № 9 (часть 4). С. 650-654.
- Kang SG, Lee HJ, Choi JE, An H, Rhee M, Kim L. Association study between glutathione S-transferase GST-M1, GST-T1, and GST-P1 polymorphisms and tardive dyskinesia. Hum Psychopharmacol. 2009 Jan;24(1):55-60. doi: 10.1002/hup.988. PMID: 19051221.
- Do KQ, Trabesinger AH, Kirsten-Krüger M, Lauer CJ, Dydak U, Hell D, Holsboer F, Boesiger P, Cuénod M. Schizophrenia: glutathione deficit in cerebrospinal fluid and prefrontal cortex in vivo. Eur J Neurosci. 2000 Oct;12(10):3721-8. doi: 10.1046/j.1460-9568.2000.00229.x. PMID: 11029642.
- Савушкина О.К., Бокша И.С., Омельченко М.А., Терешкина Е.Б., Прохорова Т.А., Воробьева Е.А., Бурбаева Г.Ш. Активность ферментов глутаматного, энергетического и глутатионового обмена при первых юношеских депрессиях с аттенуированными симптомами шизофрении. Журнал неврологии и психиатрии им. С.С. Корсакова. 2022. Т. 122, № 8. С. 136-144. doi: 10.17116/jnevro2022122081136.
- Прохорова Т.А., Терешкина Е.Б., Савушкина О.К., Бокша И.С., Воробьева Е.А., Омельченко М.А., Помыткин А.Н., Каледа В.Г., Бурбаева Г.Ш. Активность ферментов глутатионового обмена в форменных элементах крови у пациентов с высоким риском манифестации эндогенных психозов и больных с первым психотическим приступом. Журнал неврологии и психиатрии им. С.С. Корсакова. 2019. Т. 119, № 4. С. 47-54. doi:10.17116/jnevro201911904147.
- Терешкина Е.Б., Савушкина О.К., Бокша И.С., Прохорова Т.А., Воробьева Е.А., Омельченко М.А., Помыткин А.Н., Каледа В.Г., Бурбаева Г.Ш. Глутатионредуктаза и глутатион-S-трансфераза в форменных элементах крови при шизофрении и расстройствах шизофренического спектра. Журнал неврологии и психиатрии им. С.С. Корсакова. 2019. Т. 119, № 2. С. 61-65. doi:10.17116/jnevro201911902161.
- Пискарёв М.В., Лобанова В.М., Румянцева Е.Б. Кататония в структуре аффективных и шизоаффективных расстройств послеродового периода. Психиатрия. 2023. Т. 21, № 3. С. 54-63. doi:10.30629/2618-6667-2023-21-3-54-63.
- Пискарев М.В., Лобанова В.М., Ильина Н.А. Периодическая кататония при расстройствах шизофренического спектра. Журнал неврологии и психиатрии им. С.С. Корсакова 2023. Т. 123, № 8. С. 98-106. doi.org/10.17116/jnevro202312308198.
- Curthoys NP, Weiss RF. Regulation of renal ammoniagenesis. Subcellular localization of rat kidney glutaminase isoenzymes. J Biol Chem. 1974 May 25;249(10):3261-6. PMID: 4364420.
- Смородинский С.С., Батин Н.В. Методы анализа и принятия решений в слабоструктурированных задачах: учебное пособие по курсу «Методы и системы принятия решений» для студентов специальности «Автоматизированные системы обработки информации». Минск: Изд-во «Белорусский государственный университет информатики и радиоэлектроники», 2002. 116 с.
- Ben-Shachar D, Zuk R, Gazawi H, Reshef A, Sheinkman A, Klein E. Increased mitochondrial complex I activity in platelets of schizophrenic patients. Int J Neuropsychopharmacol. 1999 Dec;2(4):245-253. doi: 10.1017/S1461145799001649. PMID: 11285140.
- Dror N, Klein E, Karry R, Sheinkman A, Kirsh Z, Mazor M, Tzukerman M, Ben-Shachar D. State-dependent alterations in mitochondrial complex I activity in platelets: a potential peripheral marker for schizophrenia. Mol Psychiatry. 2002;7(9):995-1001. doi: 10.1038/sj.mp.4001116. PMID: 12399953.
- Burbaeva G Sh, Boksha I S, Turishcheva M S, Savushkina O K, Beniashvili A G, Rupchev GE, Morozova MA. Platelet cytochrome c-oxidase activity in patients with acute schizophrenia in the course of their treatment with risperidone. Health. 2011Jan; 3(1):13-19. doi: 10.4236/health.2011.31003
- Савушкина О.К., Бокша И.С., Прохорова Т.А., Терешкина Е.Б., Бурминский Д.С., Морозова М.А., Воробьева Е.А., Бурбаева Г.Ш. Активность эритроцитарных и тромбоцитарных глутатионредуктазы и глутатион-S-трансферазы при параноидной шизофрении. Журнал неврологии и психиатрии им. С.С. Корсакова. 2018. Т. 129, № 11. С. 48-52. doi:10.17116/jnevro201811811148.


