Генерализованное лимфогенное метастазирование с поражением паренхиматозных органов при раке желудка (случай из практики)
Автор: Завьялова М.В., Завьялов А.В., Пудова Е.С., Куценко И.Г., Егунова М.А., Кляус К.А., Орл Д.А., Вторушин С.В., Перельмутер В.М.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Случай из клинической практики
Статья в выпуске: 1 т.24, 2025 года.
Бесплатный доступ
Генерализованное метастатическое поражение паренхиматозных органов при раке желудка чаще всего объясняют гематогенным распространением опухолевых клеток. Обширное лимфогенное метастазирование поражает отдаленные регионы лимфоузлов и серозные оболочки. Практически отсутствуют сведения о массивном метастатическом поражении паренхиматозных органов в результате опухолевой эмболии их лимфатических сосудов. Данный случай демонстрирует именно такое распространение опухолевого процесса. Цель исследования - демонстрация случая летального исхода при раке желудка с генерализованным лимфогенным метастатическим поражением паренхиматозных органов. Описание случая летального исхода. Представлен случай летального исхода с обширным лимфогенным метастазированием рака желудка с поражением паренхиматозных органов. Пациентка, 56 лет, получала симптоматическое лечение в течение 11 койко-дней в стационаре общехирургического профиля с Диагнозом: Рак желудка, IV стадия. Состоявшееся желудочное кровотечение . Во время патологоанатомического исследования обнаружена обширная лимфоваскулярная инвазия с массивной эмболией лимфатических сосудов брюшины, плевры, перикарда, забрюшинной клетчатки и практически всех органов за исключением головного мозга. Опухолевые эмболы в лимфатических сосудах интенсивно экспрессировали субъединицы интегринов a6 и b4, а также субъединицу ламинина γ 2.
Генерализованное лимфогенное метастазирование, рак желудка, опухолевая мболия лимфатических сосудов, субъединицы интегринов α6 и β4, субъединица ламинина γ2
Короткий адрес: https://sciup.org/140309641
IDR: 140309641 | УДК: 616.33-006.6-033.2:611-018.98 | DOI: 10.21294/1814-4861-2025-24-1-189-198
Generalized Lymphogenous Metastasis Involving Parenchymal Organs in Gastric Cancer (Case Report)
Generalized metastases to parenchymatous organs in gastric cancer are usually associated with hematogenous spread of cancer cells. Generalized lymphogenous metastasis involves the spread of cancer cells to distant lymph nodes and serous membranes. There is very little information on generalized metastases to parenchymatous organs due to tumor embolism of their lymphatic vessels.
Текст научной статьи Генерализованное лимфогенное метастазирование с поражением паренхиматозных органов при раке желудка (случай из практики)
Оба яичника увеличены, замещены плотной светло-серой тканью (рис. 1В). В параметрии и в серозной оболочке маточных труб и матки – множественные нечетко отграниченные узлы светло серого цвета, плотной консистенции. Один из узлов (диаметром 5 см) врастал в стенку матки более чем на 2/3 толщины миометрия (рис. 1 Г).
Многочисленные диффузно расположенные плотные светло-серые узелки, диаметром от 2 до 10 мм, определялись в париетальной и висцеральной плевре (рис. 2 В, Г), легких, перикарде (рис. 2 Д, Е), миокарде, капсуле и поверхности печени, парарек-тальной клетчатке и серозной оболочке прямой кишки. Восьмой сегмент левого легкого и надпочечники диффузно уплотнены, замещены светло-серой
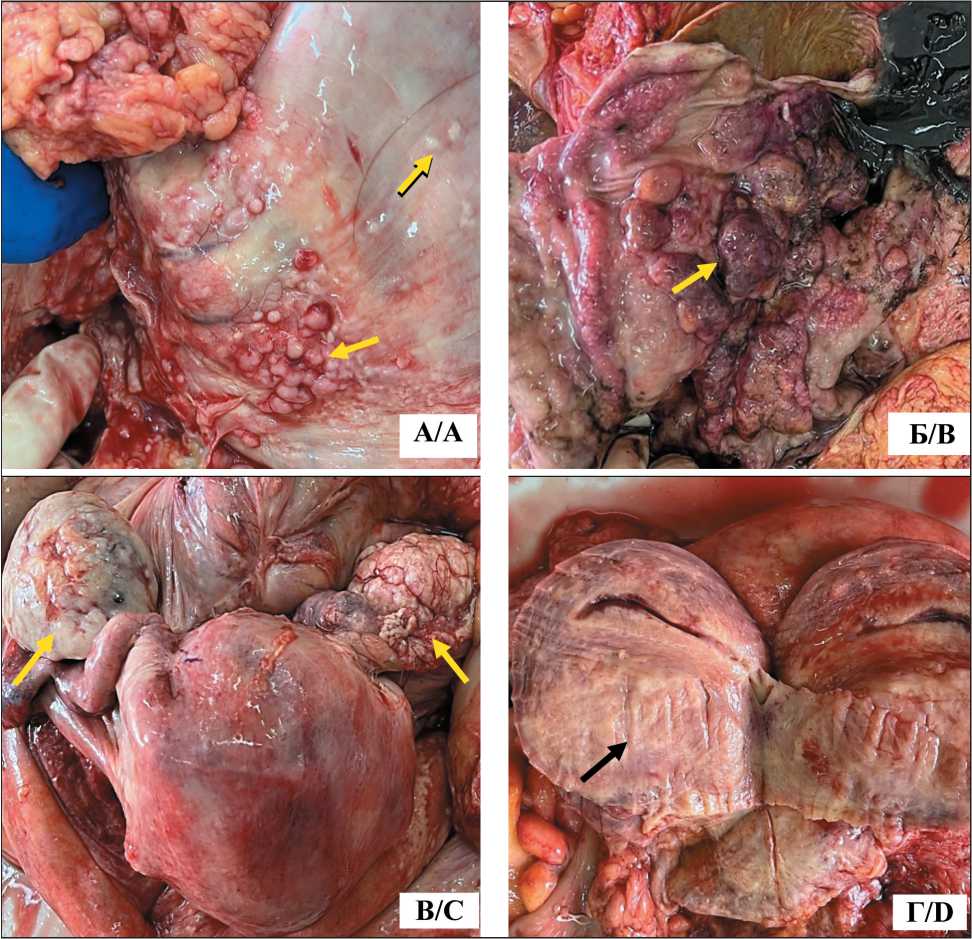
В – яичники значительно увеличены, замещены плотной светло-серой тканью (желтые стрелки); Г – со стороны серозной оболочки в стенку матки врастает нечетко отграниченный плотный светло-серый узел (черная стрелка).
Примечание: рисунок выполнен авторами
Fig. 1. Macroscopic image: A – serous membrane of the stomach with numerous light gray dense foci (yellow arrows); B – in the stomach there is a proliferation of tuberous tissue with areas of decay imbibed with blood (yellow arrow); C – ovaries are significantly enlarged, replaced by dense light gray tissue (yellow arrows); D – from the side of the serous membrane, a vaguely demarcated dense light gray node grows into the wall of the uterus (black arrow). Note: created by the authors
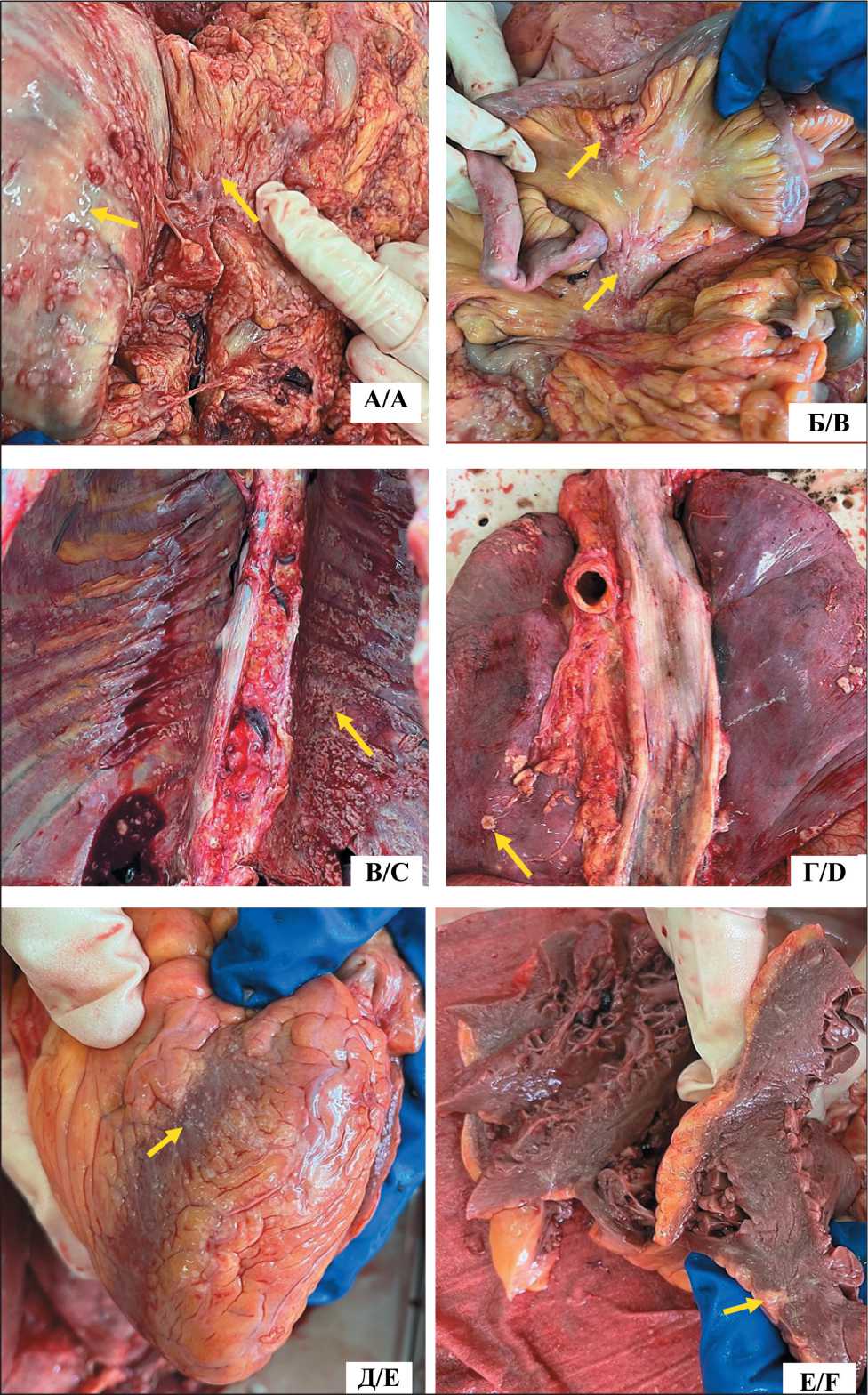
Рис. 2. Макроскопическая картина: А – висцеральная брюшина с многочисленными светло-серыми плотными узлами (желтая стрелка); Б – висцеральная брюшина с многочисленными светло-серыми плотными узлами (желтая стрелка); В – париетальная плевра с многочисленными светло-серыми плотными узлами (желтая стрелка); Г – висцеральная плевра с многочисленными светло-серыми плотными узлами (желтая стрелка); Д – висцеральный перикард с многочисленными светло-серыми плотными узлами (желтая стрелка); Е – со стороны висцерального перикарда в миокард врастает плотная светло-серая ткань (желтая стрелка). Примечание: рисунок выполнен авторами
Fig. 2. Macroscopic image: A – visceral peritoneum with numerous light gray dense nodes (yellow arrow); B – visceral peritoneum with numerous light gray dense nodes (yellow arrow); C – parietal pleura with numerous light gray dense nodes (yellow arrow); D – visceral pleura with numerous light gray dense nodes (yellow arrow); E – visceral pericardium with numerous light gray dense nodes (yellow arrow); F – from the side of the visceral pericardium, dense light gray tissue grows into the myocardium (yellow arrow).
Note: created by the authors тканью. Перибронхиальные, бифуркационные, пара-трахеальные, левый надключичный, правые и левые аксиллярные лимфоузлы, пупочное кольцо были увеличенными, плотными, замещенными светло-серой тканью. В области ворот печени, гепатодуоденаль-ной связки – конгломерат увеличенных лимфоузлов, замещенных плотной светло-серой тканью.
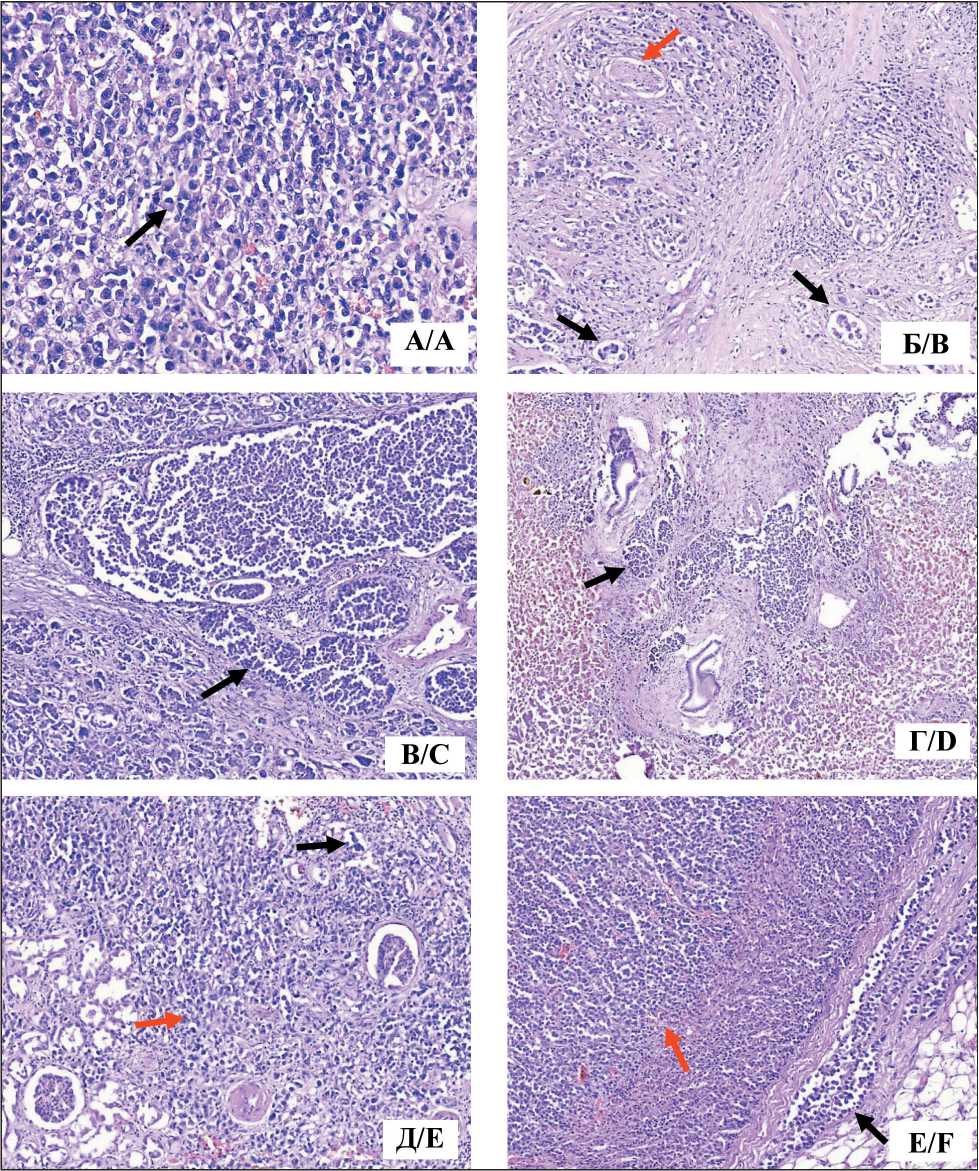
сосудах и многочисленные очаги разрастания опухолевой ткани, замещающие паренхиму перечисленных органов. Опухолевые эмболы обнаруживались и в лимфатических сосудах трабекул селезенки (рис. 3 Б–Е).
В легких определялось разрастание опухоле-вой ткани в плевре, опухолевые эмболы в лимфатических сосудах плевры, а также опухолевые эмболы в лимфатических сосудах по ходу ветвей легочной артерии, легочных вен с формированием «муфтообразных опухолевых инфильтратов», в стенках бронхов, в межальвеолярных перегородках, а также многочисленные поля разрастания опухолевой ткани с десмопластической реакцией стромы. Перибронхиальные, бифуркационные и паратрахеальные лимфоузлы были тотально замещены опухолевой тканью. Опухолевые эмболы обнаруживались в афферентных и эфферентных лимфатических сосудах.
В перикарде выявлены многочисленные опухолевые эмболы в лимфатических сосудах и очаги разрастания опухолевой ткани. Опухолевая ткань врастала со стороны эпикарда в миокард, в котором также обнаруживались многочисленные опухолевые эмболы в лимфатических сосудах.
В лимфатических сосудах широкой связки матки, серозной оболочки маточной трубы, сероз-ной оболочки матки выявлялись многочисленные опухолевые эмболы (рис. 4 А). Опухолевая ткань со стороны серозной оболочки врастала в ткань стенки матки, инвазируя более 2/3 толщины миометрия. В лимфатических сосудах брюшины, покрывающей яичники, а также в ткани яичников обнаруживались многочисленные опухолевые эмболы и обширные поля разрастания опухолевой ткани, замещающие ткань яичников за исключением структуры белых тел (рис. 4 Б–Г).
Разрастание опухолевой ткани с замещением паренхимы органов и многочисленные опухолевые эмболы определялись во всех макроскопически измененных органах, лимфатических узлах, в афферентных и эфферентных лимфатических сосудах, что является уникальной чертой описанного клинического случая. Кроме того, обнаруживалось тотальное метастатическое поражение левого надключичного лимфоузла, правых и левых аксиллярных лимфоузлов, пупочного кольца, пара-ректальной клетчатки.
При уточнении типа сосудов, содержащих опухолевые эмболы, методом иммуногистохими-
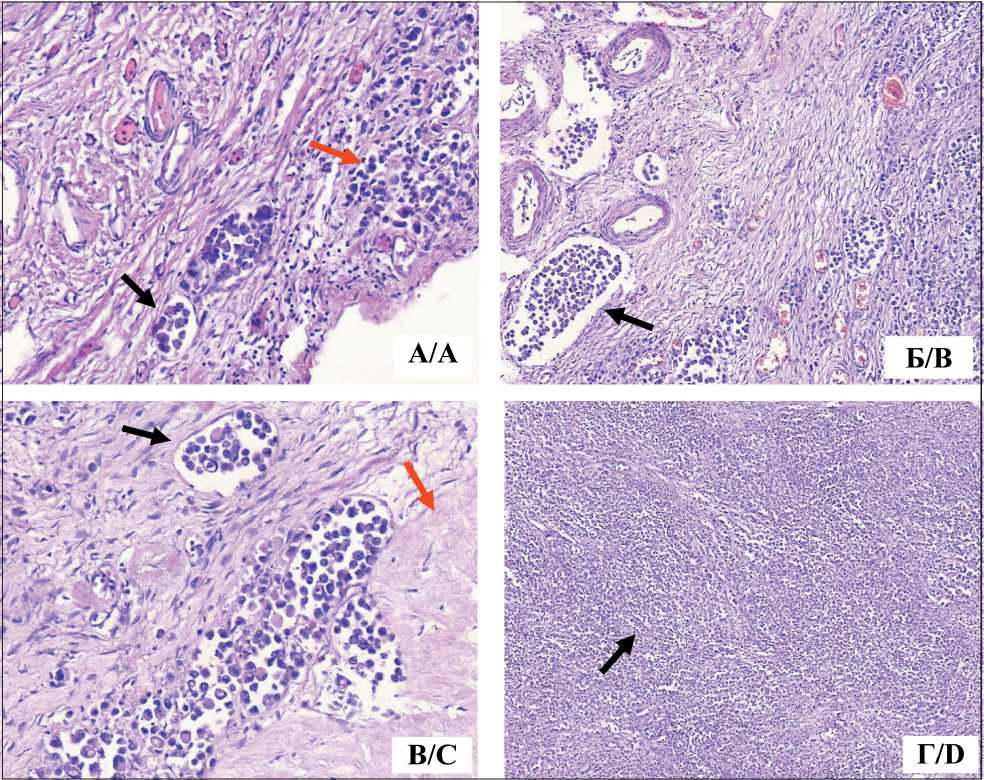
Рис. 4. Микрофото. Окраска гематоксилином и эозином: А – опухолевые эмболы в лимфатических сосудах серозной оболочки матки (черная стрелка), разрастание опухолевой ткани (красная стрелка), ×400; Б – опухолевые эмболы в лимфатических сосудах брюшины, покрывающей яичник (черная стрелка), ×200; В – опухолевые эмболы в лимфатических сосудах яичника (черная стрелка), белое тело (красная стрелка), ×400; Г – разрастание опухолевой ткани в яичнике (черная стрелка), ×100.
Примечание: рисунок выполнен авторами
Fig. 4. Microphoto. Hematoxylin and eosin staining: A – tumor emboli in the lymphatic vessels of the serous membrane of the uterus (black arrow), proliferation of tumor tissue (red arrow), ×400; B – tumor emboli in the lymphatic vessels of the peritoneum covering the ovary (black arrow), ×200; C – tumor emboli in the lymphatic vessels of the ovary (black arrow), white body (red arrow), ×400; D – proliferation of tumor tissue in the ovary (black arrow), ×100. Note: created by the authors
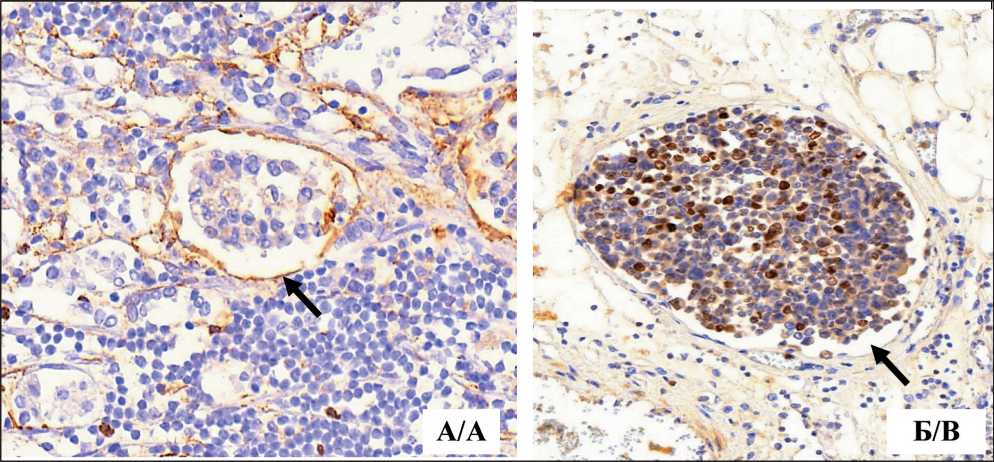
Рис. 5. Микрофото. Иммуногистохимическое исследование: А – позитивная экспрессия Podoplanin (Clone D2-40) в эндотелии лимфатических сосудов, содержащих опухолевые эмболы (черная стрелка), ×400; Б – позитивная экспрессия Ki67 в клетках опухолевого эмбола (черная стрелка), ×200. Примечание: рисунок выполнен авторами
Fig. 5. Microphoto. Immunohistochemical study: A – positive expression of Podoplanin (Clone D2-40) in the endothelium of lymphatic vessels containing tumor emboli (black arrow), ×200; B – positive expression of Ki67 in tumor embolus cells (black arrow), ×200.
Note: created by the authors
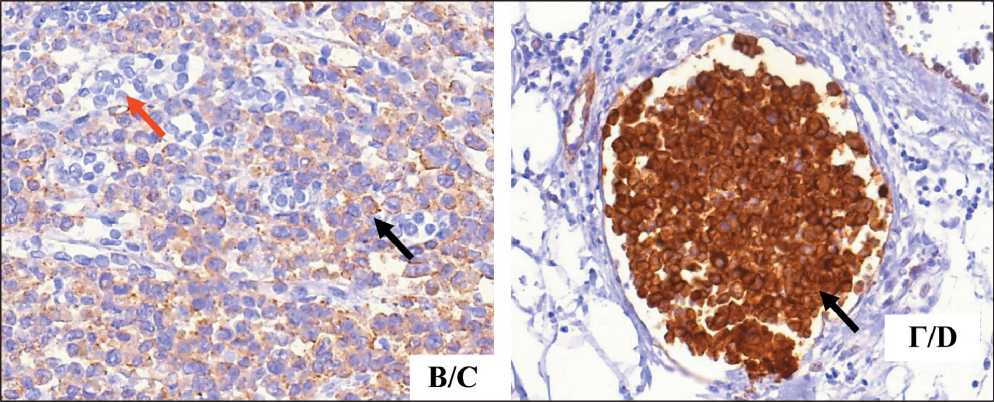
Рис. 6. Микрофото. Иммуногистохимическое исследование: А – гетерогенная экспрессия интегрина α6 в клетках первичной опухоли: позитивная (черная стрелка) и негативная (красная стрелка), ×600; Б – гомогенная позитивная экспрессия интегрина α6 в клетках опухолевого эмбола (черная стрелка), ×400; В – гетерогенная экспрессия интегрина β4 в клетках первичной опухоли: позитивная (черная стрелка) и негативная (красная стрелка), ×600; Г – гомогенная позитивная экспрессия интегрина β4 в клетках опухолевого эмбола (черная стрелка), ×400. Примечание: рисунок выполнен авторами
Fig. 6. Microphoto. Immunohistochemical study: A – heterogeneous expression of α6 integrin in primary tumor cells: positive (black arrow) and negative (red arrow), ×600; B – homogeneous positive expression of α6 integrin in tumor embolus cells (black arrow), ×400; C – heterogeneous expression of β4 integrin in primary tumor cells: positive (black arrow) and negative (red arrow), ×600n; D – homogeneous positive expression of β4 integrin in tumor embolus cells (black arrow), ×400. Note: created by the authors
ческого исследования с применением Anti-Human Podoplanin (Clone D2-40) оказалось, что эмболизи-рованы были лимфатические сосуды. В опухолевых эмболах определялась высокая пролиферативная активность (рис. 5).
Было выполнено исследование экспрессии субъединиц интегринов α6 и β4 в случаях генерализованного канцероматозного лимфангита с массивным метастатическим поражением лимфоузлов разных регионов. Оказалось, что в первичной опухоли действительно наблюдалась гетерогенная экспрессия субъединиц α6 и β4, в то время как в опухолевых эмболах в лимфатических сосудах присутствовала гомогенная позитивная экспрессия – все опухолевые клетки экспрессирова- ли этот маркер (рис. 6). Кроме того, как в клетках первичной опухоли, так и в клетках опухолевых эмболов определялась позитивная гетерогенная экспрессия ламинина ɣ2 (рис. 7).
Заключение
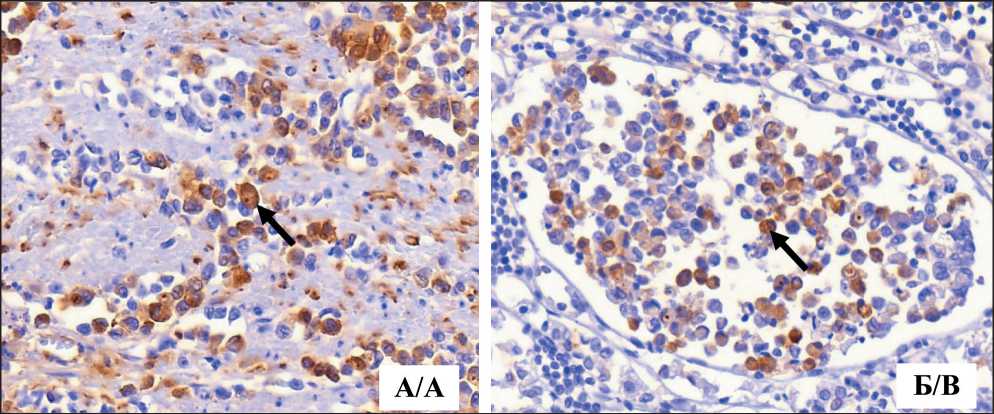
Рис. 7. Микрофото. Иммуногистохимическое исследование: А – позитивная гетерогенная экспрессия ламинина ɣ2 в клетках первичной опухоли (черная стрелка), ×600; Б – позитивная гетерогенная экспрессия ламинина ɣ2 в клетках опухолевого эмбола (черная стрелка), ×400. Примечание: рисунок выполнен авторами
Fig. 7. Microphoto. Immunohistochemical study: A – positive heterogeneous expression of laminin ɣ2 in the cells of the primary tumor (black arrow), ×600; B – positive heterogeneous expression of laminin ɣ2 in tumor embolus cells (black arrow), ×400.
Note: created by the authors
к возникновению желудочного кровотечения. Выраженный периневральный рост обусловливал развитие нарастающего болевого синдрома.
В нашем исследовании дискогезивные клетки опухолевых эмболов в лимфатических сосудах ин- тенсивно экспрессировали субъединицы интегринов a6 и b4, а также ламинин – лиганд гетеродимера α6β4. Эти факты позволяют нам предположить, что существенным звеном развития канцероматозного лимфангита может быть приобретение опухолевыми клетками способности к «якорь-независимому» существованию и сниженной способности клеток опухоли к адгезии, которые обусловлены экспрессией интегрина α6β4. Способность интегрина α6β4 предотвращать развитие апоптоза (аноикиса) опухолевых клеток, открепившихся от базальной мембраны, описана в литературе [12]. С фундаментальной точки зрения этот случай открывает перспективы для изучения механизма, запускающего каскад процессов, реализующихся генерализованным лимфогенным метастазированием. Знание этого механизма поможет контролировать течение опухолевого процесса, оптимизировать терапевтические стратегии у данной категории онкологических больных.


