Генотипирование линий подсолнечника с различной устойчивостью к ложной мучнистой росе с помощью STS-маркеров
Автор: Маркин Н.В., Тихобаева В.Е., Усатенко Т.В., Горбаченко О.Ф., Усатов А.В.
Рубрика: Селекция и семеноводство
Статья в выпуске: 2 (151-152), 2012 года.
Бесплатный доступ
Проведена оценка устойчивости 16 Rf-линий подсолнечника селекции Донской опытной станции масличных культур им. Л.А. Жданова ВНИИМК к наиболее распространенным в Ростовской области расам ложной мучнистой росы - 330 и 710. В лабораторных условиях методом искусственного заражения определены линии, контрастно различающиеся по устойчивости к этим расам ЛМР и с помощью 9 STS-маркеров трех Pl-локусов - Pl 5, Pl 6 и Pl 8, ассоциированных с устойчивостью подсолнечника к ЛМР, линии были генотипированы. Два маркера локуса Pl 6 - НаР2 и НаР3 позволяют идентифицировать устойчивые к ЛМР линии.
Ложная мучнистая роса (лмр), sts-маркеры, маркер-вспомогательная селекция, подсолнечник
Короткий адрес: https://sciup.org/142151097
IDR: 142151097 | УДК: 575.12:633.854.78
Genotyping of sunflower lines with various resistance to downy mildew by means of STS markers
There was conducted the evaluation of resistance of 16 Rf-lines of sunflower (obtained in breeding programs of the Don experimental station of VNIIMK) to the 330 and 710 races of downy mildew that are the most widespread in the Rostov region. Under laboratory conditions the method of artificial infection defined the lines that are differing contrastively in their resistance to these races of downy mildew. These lines were genotyped by means of STS markers of three Pl loci (Pl 5, Pl 6 and Pl 8) connected with sunflower resistance to downy mildew. Two markers HaP2 and HaP3 of the Pl 6 locus allow us to identify lines resistant to downy mildew.
Текст научной статьи Генотипирование линий подсолнечника с различной устойчивостью к ложной мучнистой росе с помощью STS-маркеров
Введение. Ложная мучнистая роса (ЛМР) подсолнечника, вызываемая грибом Plasmopara halstedii (Farl.) Berl. & de Toni – одно из наиболее вредоносных заболеваний культивируемого подсолнечника. Поражение посевов этим грибом может составлять до 70 % [1]. Поэтому селекция подсолнечника на устойчивость к ЛМР является одной из приоритетных задач.
Селекция сельскохозяйственных культур на устойчивость к болезням и вредителям трудоемка и связана с созданием инфекционных фонов, проведением вегетационных исследований в лабораторных и полевых условиях. Перспективным является использование специфичных молекулярных маркеров для оценки селекционного материала на ранних этапах развития растений, что может существенно сократить объем работ в полевых условиях.
Устойчивость к широкому кругу патогенов, включающему вирусы, бактерии, грибы, насекомые и нематоды обусловливают гены устойчивости – R-гены. Они содержат консервативные последовательности, которые определяют различные функции. Выделяют не менее пяти классов R-генов: внутриклеточные протеин-киназы; рецептор-подобные протеинки-назы, содержащие богатые лейцином повторы (LRR); внутриклеточные LLR белки, содержащие сайт связывания с нуклеотидами (NBS), и мотив «лейциновая молния» (LZ); внутриклеточные NBS-LRR белки, несущие домен гомологичный Toll, и interleukin-1 рецепторам (TIR); LLR белки, обеспечивающие связывание с мембраной внеклеточных белков [2].
Исследования генетических основ резистентности растений подсолнечника к паразиту Plasmopara halstedii позволили определить специфические доминантные гены – Pl-гены, обусловливающие устойчивость к различным расам P. halstedii. По данным литературы, в мировой популяции P. halstedii насчитывают около 37 рас, из которых можно выделить порядка шести-семи рас доминирующих в мире [3]. Гены Pl1 и Pl2 были идентифицированы в 70-е годы прошлого века и связаны с устойчивостью к 100 и 300 расам ЛМР [4]. После успешного внедрения этих генов в инбредные линии в течение последующих двух десятилетий появились новые расы этого патогена, преодолевающие обнаруженные ранее гены устойчивости. Позднее был обнаружен ген Pl6, у дикого вида H. annuus, который отвечает за устойчивость к 11 расам ЛМР. В настоящее время показано, что локус Pl6 содержит, по меньшей мере, 11 тесно сцепленных генов, каждый из которых дает устойчивость к одной из рас ЛМР [2]. Ген Pl8 является аналогом гена Pl6, но идентифицирован не у H. annuus, а у H. argophyllus, а Pl7 – у H. praecox. Дальнейший анализ показал, что гены Pl1/Pl2/Pl6 комплекса относятся к 1-ой группе сцепления и причислены к TIR-NBS-LRR группе устойчивости, а гены Pl5/Pl8 комплекса – к 6-ой группе сцепления и non-TIR-NBS-LRR группе. В последних источниках сообщается об обнаружении новых генов устойчивости Pl13 и Pl16 у линии культурного подсолнечника HA-R5, который обусловливает резистентность к расам: 100, 300, 310, 330, 700, 710, 730, 731 и 770, но чувствителен к расам 307 и 703 [3; 5].
С помощью стандартного набора линий-дифференциаторов подсолнечника в регионах Северного Кавказа идентифицировано 7 рас патогена [6; 7; 8]. Установлено, что доминирующее положение в большинстве районов занимает раса 330 с преобладанием на отдельных полях рас 710 и 730. Исходя из этого, селекцию подсолнечника на устойчивость к ложной мучнистой росе в Южном регионе, в том числе и в Ростовской области, следует акцентировать на расы 330, 710 и 730.
Целью настоящей работы являлась оценка в лабораторных условиях устойчивости селекционного материала подсолнечника к расам 330 и 710 возбудителя ложной мучнистой росы и генотипирование линий подсолнечника с различной устойчивостью к ЛМР с помощью STS-маркеров трех Pl-локусов.
Материалы и методы. Объектом исследования служили 16 линий подсол- нечника – восстановителей фертильности пыльцы ЦМС PET1 из Донской опытной станции масличных культур им. Л.А. Жданова ВНИИМК (табл. 2). Оценку степени устойчивости растений этих линий к расам 330 и 710 ЛМР проводили по методике, описанной в работе Антоновой с соавторами [9]. Критерием восприимчивости при идентификации гриба являлось наличие конидиального спороношения на семядольных и настоящих листьях, некроз и хлороз; критерием устойчивости – отсутствие на растениях проявления болезни. Устойчивость/восприимчивость оценивали как процентное соотношение пораженных и здоровых проростков. Исследование проводили в 3–5 повторах для 50–100 растений каждой линии в камере искусственного климата (Binder, Германия).
Для молекулярно-генетического анализа геномную ДНК выделяли из листовой ткани проростков согласно [10]. Праймеры для идентификации 9 STS-маркеров трех Pl -локусов – Pl 5 , Pl 6 и Pl 8 ассоциированных с устойчивостью подсолнечника к ЛМР были отобраны из данных литературы [2; 11] (табл. 1).
Таблица 1
Характеристика праймеров, использованных для идентификации STS-маркеров Pl-локусов
|
Праймер |
5′–3′последовательность |
Локус |
|
|
HaP1 |
F: R |
GGTAATGGCTGTTGAATTTATGGAGC : AGCATGATCCGGCTAGAGCCTTCTA |
Pl 6 |
|
HaP2 |
F: R |
GTCTACTACATGGTTTCCGTTTTC : TGCTTCTTCCTTCTATCTCACTC |
Pl 6 |
|
HaP3 |
F: R |
GTTTGTGGATCATCTCTATGCG : TGCTTCTTCCTTCTATCTCACTC |
Pl 6 |
|
Ha-P1 |
F: R |
GCCCAAAATTGAAAGAAAGGTGTG : GGCGAAATTGGTTCCCGTGAGTCG |
Pl 5 , Pl 8 |
|
Ha-P2 |
F: R |
AATCTTGAGTCATTACCCGAGC : CAGCGTCTCTGGTAGATCGTTCACC |
Pl 5 |
|
Ha-P3 |
F: R |
TAGTTAACCATGGCTGAAACCGCTG : TTTGAAAGATAAGTTCGCCTCTCG |
Pl 5 , Pl 8 |
|
Ha-P4 |
F: R |
GCTGTTACTGCCCTCTTCAAAGTC : CCCAACTCGACATATCTTCAAACC |
Pl 8 |
|
Ha-P5 |
F: R |
TAGTTAACCATGGCTGAAACCGCTG : CCCCATATTGACAAAGAGTTGAGG |
Pl 8 |
|
Ha-P6 |
F: R |
TAGTTAACCATGGCTGAAACCGCTG : CGTCTCTGGTAGATCGTTCACCTT |
Pl 8 |
Полимеразную цепную реакцию проводили в 25 мкл реакционной смеси сле- дующего состава: 67 мМтрис – HCl, рН 8,8; 16мМ (NH4)2SO4, 2,5 мМ MgSO4, 0,1 мМ меркаптоэтанола, 0,25 мМ каждого ДНТФ (ДАТФ, ДЦТФ, ДТТФ, ДГТФ), по 20 пМ праймеров; 2,5 ед. Taq-полимеразы, 15 нг выделенной ДНК. Амплификацию проводили в термоциклере PalmCycler (Corbett Research, Австралия).
Термальный режим реакций подбирали для каждой пары праймеров с учетом их нуклеотидного состава. Для большинства проведенных реакций оптимальным оказался терморежим с начальной денатурацией при 95 оС в течение 3 мин., затем 35 циклов при соблюдении температурновременного режима: отжиг при 60 оС в течение 30 сек., элонгация – 2 мин. при 72 оС, денатурация при 95 оС – 30 сек., финальная элонгация – 1 мин. Для остальных режим амплификации был следующим: начальная денатурация – 94 ºС – 3 мин., затем 33 цикла: 94 ºС – 10 сек., 60 ºС – 30 сек. и 72 ºС – 1 мин. 30 сек.; финальная элонгация – 5 мин. при 72 ºС.
Продукты амплификации разделяли в 1 %-ном агарозном геле с бромистым этидием, используя трис-боратный буфер. После окончания электрофореза гели фотодокументировали (GelDoc 2000, BioRad, США). В качестве маркера массы, использовали Gene Ruler 1 Kb DNA Ladder (Fermentas).
Результаты и обсуждение. В лабораторных условиях методом искусственного заражения проростков подсолнечника спорами гриба Plasmopara halstedii проведена оценка устойчивости 16 отцовских линий (Rf-линии) к двум расам ложной мучнистой росы – 330 и 710. Из 16 изученных линий (табл. 2) 5 линий – J-6/1285, J-8/154, J-11/420, J-11/536 и J-7/465 устойчивы как к 330, так и 710 расам ЛМР. Шесть линий – J-5/2884, J-7/108, J-10/256, J-10/186, J-9/508 и J-9/428, напротив, неустойчивы к этим расами. Остальные пять линий – J-5/3452, J-5/2586, J-7/381, J-11/385 и J-11/112 не поражались расой 330, но оказались неустойчивыми к расе 710. Таким образом, в результате лабораторных ис- следований были определены линии подсолнечника, контрастно различающиеся по степени поражения ЛМР. Так как устойчивость к возбудителю ЛМР у подсолнечника контролируется доминантными генами, нами протестированы известные STS-маркеры трех Pl-локусов – Pl5, Pl6 и Pl8 ассоциированных с устойчивостью подсолнечника к ЛМР на линиях демонстрирующих различное проявление признака устойчивости к заболеванию с целью определить наиболее информативные для маркер-вспомогательной селекции. Такие ДНК-маркеры могут быть полезными для быстрой идентификации потенциально устойчивых к этому патогену генотипов в больших выборках, что позволит более эффективно решать проблему устойчивости к ЛМР этой сельскохозяйственной культуры.
Таблица 2
Линии подсолнечника, изученные по степени поражения расами 330 и 710 ложной мучнистой росы
|
Линия |
Степень поражения ложной мучнистой росой, % |
|
|
раса 330 |
раcа 710 |
|
|
J-5/3452 |
0 |
100 |
|
J-5/2884 |
100 |
100 |
|
J-5/2586 |
0 |
91,7 |
|
J-6/1285 |
0 |
0 |
|
J-7/108 |
100 |
100 |
|
J-10/256 |
100 |
100 |
|
J-7/381 |
0 |
100 |
|
J-8/154 |
0 |
0 |
|
J-11/385 |
0 |
100 |
|
J-11/420 |
0 |
0 |
|
J-11/536 |
0 |
0 |
|
J-11/112 |
0 |
100 |
|
J-7/465 |
0 |
0 |
|
J-10/186 |
100 |
100 |
|
J-9/508 |
92 |
100 |
|
J-9/428 |
100 |
100 |
Из 9 изученных STS-маркеров (табл. 1) только два – НаР2 и НаР3 – маркирующие локус Pl6 оказались информативными и позволили из 5, устойчивых к ЛМР линий, маркировать 4 линии: J-6/1285, J-8/154, J-11/420 и J-7/465. При этом в генотипе устойчивых линий определены специфичные ПЦР-фрагменты размером около 1200 п.н. (НаР2) и 1800 п.н. (НаР3), что согласуется с данными представленными в работе [2]. Интересно отметить, что третий из маркеров локуса Pl6 – HaP1, праймеры которого фланкируют участок (около 2000 п.н.), включающий маркерные последовательности НаР2 и НаР3, не позволил идентифицировать устойчивые генотипы. Протестированные STS-маркеры локусов – Pl5 и Pl8 (табл. 1) не позволили определить устойчивые к ЛМР генотипы, так как одинаково представлены у всех исследованных линий. Необходимо отметить, что у подсолнечника болезнь может не проявляться на ранних этапах роста растения [12]. Кроме того показано, что здоровые по внешним признакам растения подсолнечника, выросшие в окружении больных, дают семена, которые являются носителями инфекционного начала возбудителя ЛМР [13]. В этой связи растения линии J-11/536 проявившие устойчивость к ЛМР на раннем этапе роста и не маркированные с помощью STS по локусам устойчивости необходимо исследовать в течение всего периода вегетации, а также протестировать семенной материал этих образцов.
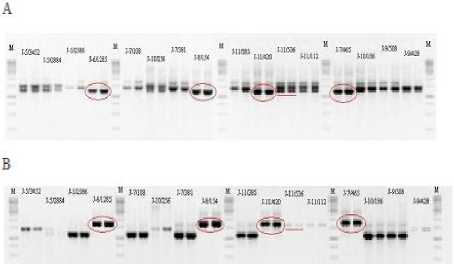
Рисунок – Электрофореграмма продуктов амплификации геномной ДНК линий подсолнечника: А) с праймером НаР2 и В) с праймером НаР3 . Представлены результаты двух независимых ПЦР реакций для каждой линии. Фрагменты уникальные для устойчивых к ЛМР (расы 330 и 710) линий подсолнечника обведены. Чертой отмечен образец, проявивший устойчивость к ЛМР в лабораторных испытаниях, но при этом специфичный ПЦР-фрагмент не идентифицирован.
М – маркер массы (1 Kb).
Заключение. Таким образом, проведена оценка устойчивости Rf -линий подсолнечника селекции Донской опытной станции масличных культур им. Л.А. Жданова ВНИИМК к наиболее распространенным в Ростовской области расам ложной мучнистой росы – 330 и 710. В лабораторных условиях методом искусственного заражения определены линии, контрастно различающиеся по устойчивости к этим расам ЛМР и с помощью 9 STS-маркеров трех Pl -локусов – Pl 5 , Pl 6 и Pl 8 ассоциированных с устойчивостью подсолнечника к ЛМР линии были гено-типированы. Из 9 изученных STS-маркеров только два – НаР2 и НаР3 (локус Pl 6 ) позволили идентифицировать линии продемонстрировавшие устойчивость к ЛМР в условиях искусственного заражения. Изученные ДНК-маркеры НаР2 и НаР3 могут представлять особый интерес в маркер-вспомогательной селекции подсолнечника на устойчивость к заболеванию ЛМР.
Исследование выполнено в рамках государственной темы Министерства образования и науки РФ (регистрационный номер: 4.5642.2011), при финансовой поддержке ФЦП Министерства образования и науки РФ (госконтракт № 16.740.11.0485).


