Гибридный метод ПЭТ/МРТ головного мозга с 18F-ФДГ в диагностике фокальной кортикальной дисплазии у пациентов с фокальной фармакорезистентной эпилепсией
Автор: Ростовцева Т.М., Долгушин М.Б., Дворянчиков А.В., Наделяев Р.В., Каралкина М.А., Джафаров В.М., Рублева Ю.В., Баранова Е.А., Пацап О.И., Бурд С.Г.
Журнал: Клиническая практика @clinpractice
Рубрика: Оригинальные исследования
Статья в выпуске: 4 т.16, 2025 года.
Бесплатный доступ
Обоснование. До 30% пациентов с эпилепсией резистентны к терапии. Одной из ведущих причин фармакорезистентной эпилепсии у взрослых и детей является фокальная кортикальная дисплазия. Полная резекция эпилептогенного очага в 60–70% случаев приводит к полному избавлению от эпилептических приступов, однако выявление и определение его границ с помощью магнитно-резонансной томографии (МРТ) может быть трудной задачей. Совмещённая с МРТ позитронная эмиссионная томография (ПЭТ/МРТ) — новый гибридный метод диагностики, который может применяться при отрицательных и неопределённых результатах МРТ, а также при несоответствии данных МРТ и видеоэлектроэнцефалографии (видео-ЭЭГ-мониторинг). Цель исследования — изучить диагностические возможности гибридного метода ПЭТ/МРТ головного мозга с радиофармпрепаратом фтордезоксиглюкозой (18F-ФДГ) в выявлении фокальной кортикальной дисплазии у пациентов с фокальной фармакорезистентной эпилепсией и проанализировать метаболические паттерны при фокальной кортикальной дисплазии различного типа и локализации. Методы. Ретроспективный анализ данных 23 пациентов включал сопоставление данных ПЭТ/МРТ головного мозга с 18F-ФДГ, МРТ и видео-ЭЭГ-мониторинга, а также анализ паттернов гипометаболизма 18F-ФДГ при фокальных кортикальных дисплазиях различных типов и локализаций. Результаты. Фокальная кортикальная дисплазия выявлена у 13 (56,5%) пациентов с помощью МРТ, у 22 (95,6%) — с помощью ПЭТ/МРТ с 18F-ФДГ; 6 (26,1%) были МР-негативными, в 3 (13%) случаях признаки фокальной кортикальной дисплазии обнаружены при ретроспективном прицельном анализе изображений МРТ в зоне гипометаболизма 18F-ФДГ. Небольшой фокальный участок гипометаболизма 18F-ФДГ в нашем исследовании наблюдался исключительно при локализации эпилептогенного очага в лобной доле, что составило 75% случаев лобного варианта фокальной кортикальной дисплазии. Во всех случаях височной локализации зона распространялась на две и более извилин. На момент публикации статьи отсутствие приступов по классификации J. Engel (Engel I) в послеоперационный период наблюдалось у 11 (84,6%) из 13 прооперированных пациентов, исход класса Engel II зарегистрирован у 1 (4,3%) пациента. Заключение. ПЭТ/МРТ головного мозга с 18F-ФДГ у пациентов с фокальной фармакорезистентной эпилепсией повышает выявление случаев фокальной кортикальной дисплазии на 39% по сравнению с МРТ, в том числе у МР-негативных пациентов и пациентов с небольшими структурными изменениями. Анализ изображений ПЭТ/МРТ у пациентов с подозрением на наличие эпилептогенного очага лобной локализации требует особого внимания.
Фармакорезистентная эпилепсия, фокальная кортикальная дисплазия, ФКД, совмещённая позитронная эмиссионная томография и магнитно-резонансная томография, ПЭТ/МРТ
Короткий адрес: https://sciup.org/143185364
IDR: 143185364 | DOI: 10.17816/clinpract691913
The hybrid brain PET/MRI method with 18F-FDG in the diagnostics of focal cortical dysplasia in patients with focal drug-resistant epilepsy
BACKGROUND: Up to 30% of the patients with epilepsy are resistant to drug therapy. One of the leading causes of drug-resistant epilepsy in adults and children is the focal cortical dysplasia. The complete resection of the epileptogenic focus in 60–70% of the cases results in the complete resolving of epileptic seizures, however, its detection and determining its margins by using magnetic resonance imaging (MRI) could be a difficult task. Positron emission tomography combined with MRI (PET/MRI) is a new hybrid method of diagnostics, which can be used in case of negative and indefinite MRI results, as well as in case of non-compliance of the MRI findings to the data from videoelectroencephalography (video-EEG-monitoring). AIM: To evaluate the diagnostic possibilities of the hybrid brain PET/MRI method with the use of the radiopharmaceutical — Fluorodeoxyglucose (18F-FDG) in detecting the focal cortical dysplasia in patients with focal drug-resistant epilepsy and to analyze the metabolic patterns in cases of focal cortical dysplasia of various type and location. METHODS: The retrospective analysis of data from 23 patients included the comparison of data from the brain PET/MRI with 18F-FDG, from the MRI and from the video-EEG-monitoring, as well as the analysis of 18F-FDG hypometabolism patterns in cases of focal cortical dysplasia of various types and locations. RESULTS: Focal cortical dysplasia was found in 13 (56.5%) patients by means of MRI, in 22 (95.6%) — by means of PET/MRI with 18F-FDG; 6 (26.1%) were MRI-negative, while in 3 (13%) cases the signs of focal cortical dysplasia were found upon the retrospective targeted analysis of MRI images in the 18F-FDG hypometabolism zone. Small focal area of 18F-FDG hypometabolism in our research was found only when the epileptogenic focus was located in the frontal lobe, which was 75% of the cases of the frontal variant of FCD. In all the cases of the temporal location, the zone was spreading to two and more gyri. As of the moment of article publication, the absence of seizures acc. to the classification by J. Engel (Engel I) in the postoperative period was reported for 11 (84.6%) of 13 operated patients, the Engel II class outcome was registered in 1 (4.3%) patient. CONCLUSION: Brain PET/MRI with 18F-FDG in patients with focal drug-resistant epilepsy increases the detection rates of focal cortical dysplasia by 39% comparing to MRI, including the MRI-negative patients and the patients with minor structural changes. The analysis of PET/MRI images in patients with suspected presence of epileptogenic focus of frontal location requires special attention.
Текст научной статьи Гибридный метод ПЭТ/МРТ головного мозга с 18F-ФДГ в диагностике фокальной кортикальной дисплазии у пациентов с фокальной фармакорезистентной эпилепсией
Submitted 03.10.2025 Accepted 06.11.2025 Published online 03.01.2026
ОБОСНОВАНИЕ
Эпилепсия — одно из наиболее распространённых неврологических заболеваний, которым страдает более 50 миллионов человек в мире1. Наиболее частой формой эпилепсии является фокальная [1]. Около 30% пациентов с эпилепсией резистентны к противоэпилептической терапии, наиболее оптимальным методом лечения для пациентов с фармакорезистентной фокальной эпилепсией является хирургический [2]. Фокальная кортикальная дисплазия (ФКД) является одной из ведущих причин фармакорезистентной эпилепсии у взрослых


Список сокращений
КТ — компьютерная томография
МРТ — магнитно-резонансная томография
ПЭТ/МРТ — технология совмещения позитронно-эмиссионной томографии с магнитно-резонансной томографией
ФКД — фокальная кортикальная дисплазия
ЭЭГ — электроэнцефалография
ЭЭГ-ВМ (ЭЭГ-видеомониторирование) — видеоэлектроэнцефалография стерео-ЭЭГ-ВМ (стерео-ЭЭГ-видеомониториро-вание) — стереоэлектроэнцефалография
18F-ФДГ ([18F]Fluorodeoxyglucose, [18F]FDG) — радиофармацевтический лекарственный препарат [18F]фтордезоксиглюкоза
Т1-/Т2-ВИ — Т1-/Т2-взвешенное изображение
T2-FLAIR (T2-Fluid-Attenuated Inversion Recovery) — режим магнитно-резонансной томографии, представляющий собой импульсную последовательность «инверсия–восстановление с подавлением сигнала от свободной жидкости»
и детей и связана с тяжёлыми формами заболевания, требующими специфического подхода к терапии и часто хирургического вмешательства. До 70% случаев мальформаций коры приходится на ФКД, что делает её одним из основных факторов в развитии резистентной эпилепсии [3].
ФКД представляет собой локальное расстройство нормального развития и организации коры головного мозга, возникающее в результате нарушения пролиферации, миграции и дифференцировки нейронов во внутриутробном периоде [4]. Классификация ФКД, предложенная I. Blumcke и соавт. в 2011 году [5], оставалась общепринятой до последнего времени. Различия между подтипами ФКД I типа (аномальная кора с нарушением цитоархитектоники, но без дисморфичных нейронов и баллонных клеток) в данной классификации определяются характером кортикальной дислами-нации (Ia — радиальная, Ib — тангенциальная, Ic — сочетанная); подтипы ФКД II типа (с дисморфич-ными нейронами) — наличием баллонных клеток (присутствие дисморфичных нейронов без баллонных клеток при подтипе IIa и обоих типов клеток — при IIb); ФКД III типа представляет собой сочетание ФКД Ic с другими патологиями (IIIa — с гиппокампальным склерозом, IIIb — с глионейрональными опухолями, IIIc — с сосудистыми мальформациями, IIId — с зонами глиоза различного генеза) [5]. Актуальная классификация ФКД, предложенная в 2022 году Международной лигой по борьбе с эпилепсией (International League Against Epilepsy, ILAE), строится на принципах комплексной диагностики и включает, помимо классических патоморфологи-ческих типов, новые категории, отражающие гистологические, генетические и нейровизуализацион-ные данные, среди которых малая мальформация кортикального развития (mild malformation of cortical development, mMCD), малая мальформация кортикального развития с олигодендроглиальной гиперплазией и лобной эпилепсией (mild malformations of cortical development with oligodendroglial hyperplasia in epilepsy, MOGHE), а также отсутствие ФКД по данным патоморфологического исследования [6].
В ряде исследований при полном хирургическом удалении ФКД длительная ремиссия и отсутствие припадков по классификации Дж. Энгеля (Engel I) достигается в 60–70% случаев [7, 8]. Частичные резекции или неполное удаление очага, напротив, связаны с более низким уровнем контроля припадков (14–22%) и более высоким риском рецидивов [8]. Одним из важных факторов прогноза является также тип ФКД: пациенты с ФКД II типа чаще достигают свободы от припадков (до 75–80%), в то время как у пациентов с ФКД I типа и с mMCD результаты резекции хуже, но всё равно значительные [8, 9].
Алгоритм обследования пациентов с эпилепсией включает, как правило, видеоэлектроэнцефалографию (ЭЭГ-видеомониторирование, ЭЭГ-ВМ) и магнитно-резонансную томографию (МРТ). Типичная МРТ-картина при ФКД характеризуется утолщением коры, размытостью границы серого и белого вещества, повышением сигнала в режиме T2-FLAIR (T2-Fluid-Attenuated Inversion Recovery), наличием трансмантийного признака [линейный участок повышения интенсивности МР-сигнала на Т2-взвешенном изображении (Т2-ВИ) и импульсной последовательности FLAIR от коры к стенке бокового желудочка, характерного для ФКД IIb подтипа], изменением формы извилин [10]. Выявление и точная оценка границ ФКД с помощью МРТ нередко бывают затруднительны, а в ряде случаев — невозможны. Уточнить локализацию и резектабельность эпилептогенной зоны в случаях, когда структурные изменения в веществе мозга не удаётся выявить с помощью МРТ, когда данные МРТ и ЭЭГ не совпадают, а также у пациентов с двусторонним и мультифокальным поражением помогут дополнительные радионуклидные диагностические методики — однофотонная эмиссионная томография и позитронно-эмиссионная томография (ПЭТ) [11]. Новой гибридной методикой, позволяющей последовательно или одномоментно оценить структурные и метаболические изменения головного мозга в рамках одного сканирования, является совмещённая ПЭТ/МРТ.
Цель исследования — изучить диагностические возможности гибридного метода ПЭТ/МРТ головного мозга с радиофармпрепаратом фтордезоксиглюкозой (18F-ФДГ) в выявлении ФКД у пациентов с фокальной фармакорезистентной эпилепсией и проанализировать метаболические паттерны при ФКД различного типа и локализации.
МЕТОДЫ
Дизайн исследования
Проведено ретроспективное одногрупповое когортное исследование. Проанализированы данные исследований ПЭТ/МРТ головного мозга с 18F-ФДГ, выполненных в период с 2023 по 2025 год 23 пациентам (11 мужчин, 12 женщин; возраст от 19 лет до 51 года, средний возраст 31,48 года) с фокальной фармакорезистентной эпилепсией. Сопоставляли количество случаев ФКД, выявленных с помощью МРТ, ПЭТ и совместного анализа ПЭТ/МРТ. Проанализированы паттерны гипометаболизма 18F-ФДГ в зависимости от типа и локализации ФКД.
Критерии соответствия
Критерии включения: пациенты с установленным диагнозом фокальной фармакорезистентной эпилепсии.
Критерии невключения: наличие генерализованной эпилепсии и других форм эпилепсии, за исключением фокальной; наличие фокальной эпилепсии без лекарственной устойчивости; наличие эпилептического синдрома, обусловленного объёмными образованиями головного мозга, артериовенозными мальформациями, инфарктом мозга, черепномозговой травмой, а также другими возможными причинами, за исключением ФКД.
Условия проведения
Лечение пациентов, а также все исследования выполнялись на базе ФГБУ «Федеральный центр мозга и нейротехнологий» Федерального медико-биологического агентства (ФГБУ ФЦМН ФМБА России).
Продолжительность исследования
Набор пациентов производился в 2023–2025 годах, анализ результатов — в 2025 году.
Описание медицинского вмешательства
Все пациенты, включённые в исследование, получали противоэпилептические препараты в режиме политерапии с частичным эффектом или его отсутствием.
Всем пациентам выполнены клинико-неврологическое обследование, продолженное ЭЭГ-ВМ, гибридное сканирование ПЭТ/МРТ головного мозга с 18F-ФДГ; проведён анализ функциональных, структурных и метаболических изменений головного мозга. Во всех случаях выявлена или заподозрена ФКД.
В дальнейшем каждый клинический случай обсуждался на консилиуме с участием эпилептологов, нейрофизиологов, радиологов, рентгенологов и нейрохирургов: производилось сопоставление клинических данных и результатов проведённых исследований с последующим принятием решения о дальнейшей тактике ведения пациента, в частности хирургической резекции эпилептогенного очага, инвазивном ЭЭГ-ВМ, малоинвазивных хирургических вмешательствах, коррекции терапии и наблюдении в динамике. Так, стерео-ЭЭГ-видеомониторирование (стерео-ЭЭГ-ВМ) было выполнено 12 пациентам, хирургическая резекция эпилептогенной зоны — 13 (из них 10 пациентам перед хирургической резекцией выполнено инвазивное ЭЭГ-ВМ).
Методы регистрации исходов
Продолженное ЭЭГ-ВМ проводили на аппаратах «Нейрон-Спектр-4/П» и «Нейрон-Спектр-65» компании «Нейрософт» (Россия) в соответствии с рекомендациями Международной федерации клинической нейрофизиологии (International Federation of Clinical Neurophysiology, IFCN) с использованием 21 электрода с расположением по схеме 10-20 с наложением дополнительных каналов ЭКГ. В ходе ЭЭГ-ВМ исследовали биоэлектрическую активность головного мозга, проводили запись приступов.
Исследования ПЭТ/МРТ проводили с использованием интегрированной ПЭТ/МР-системы SIGNA PET/MR 3Тл (GE Healthcare, США), которая по-
зволяет одновременно проводить как ПЭТ, так и МР-визуализацию головного мозга. Для всех исследований ПЭТ/МРТ использовалась 8-канальная катушка для нейрорадиологических исследований высокого разрешения. Во всех случаях не менее чем за 2 часа до исследования пациенты находились под наблюдением медицинского персонала; в случае возникновения эпилептического приступа исследование переносилось на другой день. Перед проведением ПЭТ/МРТ головного мозга с 18F-ФДГ пациентам проводили предвари- тельную подготовку, стандартную для исследований ПЭТ с 18F-ФДГ [12]: внутривенное введение радиофармацевтического лекарственного препарата на основе 18F-ФДГ в дозировке, назначенной врачом-радиологом, исходя из веса и роста пациента (125–250 МБк, в среднем 180 МБк). После инъекции радиофармпрепарата пациенты в течение 20–30 минут находились в затемнённом помещении под наблюдением медицинского персонала, соблюдая удобное положение лёжа с закрытыми глазами и воздерживаясь от использования мобильных устройств, прослушивания музыки, чтения, активных движений.
Протокол гибридного ПЭТ/МРТ-сканирования был сформирован следующим образом: при сборе данных ПЭТ (в течение 15 минут, размер матрицы 192 x 192) на основании технических возможностей системы и рекомендованного протокола HARNESS-MRI (Harmonized Neuroimaging of Epilepsy Structural Sequences-Magnetic Resonance Imaging) для пациентов с эпилепсией (рекомендации ILAE-2019) выполнены следующие МР-последова-тельности высокого разрешения [13]:
-
• 3D T1-взвешенная последовательность с инверсионным восстановлением (IR-FSPGR) по сагиттальной плоскости: поле зрения 25,6 см; толщина среза 1,2 мм; угол наклона 12; частотное разрешение 256; фазовое разрешение 256; ширина полосы пропускания 31,25 кГц;
-
• 3D T2-взвешенная последовательность (Cube T2) по сагиттальной плоскости: поле зрения 25,6 см; TR (repetition time — время повторения) 2500 мс; TE (echo time — время эха) — максимальное; ETL (echo train length — длина цепочки эхосигналов) 125; частотное разрешение 320; фазовое разрешение 320; ширина полосы пропускания 50 кГц;
-
• 3D T2-FLAIR-взвешенная последовательность (Cube T2-FLAIR) по сагиттальной плоскости: поле зрения 25,6 см; толщина среза 1,2 мм;
TR 6500 мс; TE 90 мс; ETL 140; частотное разрешение 256; фазовое разрешение 256; ширина полосы пропускания 31,25 кГц;
-
• 2D корональная T2-взвешенная последовательность с быстрым спин-эхо (FRFSE-XL): поле зрения 20 см; толщина среза 2,0 мм; межсрезовое расстояние 0,2 мм; TR 4877 мс; TE 120 мс; угол наклона 111; ETL 14; частотное разрешение 288; фазовое разрешение 224; ширина полосы пропускания 19,23 кГц.
Помимо вышеизложенных последовательностей также получена последовательность коррекции затухания (magnetic resonance attenuation correction, MR AC) длительностью 18 секунд, используемая для создания карт коррекции на основе атласа для получения псевдо-КТ, которая включает информацию о непрерывном затухании для головы с использованием атласа одной головы, основанного на КТ-изображениях.
Независимо друг от друга два врача-радиолога и два врача-рентгенолога провели визуальный анализ полученных изображений гибридного исследования. Помимо визуального анализа проводился анализ с использованием рабочей станции Advantage Workstation 4.6 (AWS, GE Healthcare, США) со специальным клиническим программным обеспечением CortexID Suite ver. 1.04-5.
Анализ изображений ПЭТ/МРТ проводился последовательно: в первую очередь производили оценку изображений МРТ и анализировали структурные изменения в веществе головного мозга. В дальнейшем производили качественную и количественную оценку метаболизма 18F-ФДГ в веществе мозга. На основании данных ПЭТ оценивали асимметрию метаболизма 18F-ФДГ в зеркальных участках вещества мозга. Количественный анализ включал измерение стандартных величин накопления (SUVmax, SUVmean) в областях интереса (region of interest, ROI) и в областях скорректированного поглощения (COROA), вычисление индекса асимметрии метаболизма 18F-ФДГ в предполагаемой эпилептогенной зоне в сравнении с контралатеральным участком вещества мозга; объём выбранных ROI составил 400–600 мм3.
На заключительном этапе производили сопоставление структурных изменений, выявленных на МРТ, зон метаболизма, выявленных на ПЭТ, и данных ЭЭГ-ВМ. В случаях несовпадения результатов производили повторный детальный анализ структурных изменений вещества мозга в выявленных зонах гипометаболизма 18F-ФДГ.
Исходы исследования
Основной исход исследования: диагностическая результативность гибридного ПЭТ/МРТ головного мозга с 18F-ФДГ, определяемая как частота выявления ФКД, в исследуемой когорте пациентов с фокальной фармакорезистентной эпилепсией в сравнении со стандартной МРТ.
Дополнительные исходы исследования: анализ паттернов гипометаболизма 18F-ФДГ при различных типах и локализациях ФКД, сопоставление данных ПЭТ/МРТ с результатами ЭЭГ-ВМ и МРТ, а также послеоперационные исходы (Engel) у пациентов, которым была выполнена резекция эпилептогенного очага.
Анализ в подгруппах
Пациенты разделены на подгруппы в зависимости от локализации и типа ФКД, а также от наличия характерных структурных изменений на МРТ. У 12 прооперированных пациентов тип ФКД определяли по данным патоморфологического исследования, в остальных случаях — по данным МРТ. У всех включённых в исследование МР-негативных пациентов тип ФКД определён по данным патомор-фологического исследования.
Методы регистрации исходов
Регистрацию основных и дополнительных исходов исследования проводили по результатам анализа всех ПЭТ/МРТ с участием двух независимых экспертов-радиологов (стаж не менее 5 лет, наличие опыта в нейровизуализации) с применением стандартных протоколов количественной и визуальной оценки очагов гипометаболизма.
Статистический анализ
Статистический анализ результатов проводили с помощью пакета программ SPSS Statistics, версия 23.0 (IBM, США), а также библиотек SciPy и Matplotlib (Python Software Foundation, США). Количественные данные представлены в виде средних значений и стандартных отклонений (M±SD) или медианы с межквартильным размахом в зависимости от характера распределения. Нормальность проверяли с помощью критерия Шапиро–Уилка. Для сравнения независимых групп с нормальным распределением применяли t-тест Стьюдента, при ненормальном — U-критерий Манна–Уитни. Для сравнения связанных выборок использовали парный t-тест или критерий Уилкоксона. Корреляционный анализ проводили с расчётом коэффициента корреляции Пирсона или Спирмена в зависимости от типа данных. Статистическую значимость различий определяли при уровне p <0,05.
РЕЗУЛЬТАТЫ
Объекты (участники) исследования
Проанализированы данные гибридных исследований ПЭТ/МРТ головного мозга с 18F-ФДГ 23 пациентов с ФКД.
Основные результаты исследования
ФКД выявлена у 13 (56,5%) пациентов с помощью МРТ, у 22 (95,6%) — с помощью гибридного исследования ПЭТ/МРТ с 18F-ФДГ, из них 6 (26,1%) пациентов были МР-негативными, в 3 (13%) случаях признаки ФКД обнаружены на изображениях МРТ при повторном прицельном анализе изображений в зоне гипометаболизма 18F-ФДГ (рис. 1). В одном МР-негативном случае зона гипометаболизма 18F-ФДГ выявлена ретроспективно при пересмотре изображений ПЭТ/МРТ после инвазивного ЭЭГ-ВМ.
Из 13 пациентов, которым после ПЭТ/МРТ выполнялся инвазивный ЭЭГ-ВМ, локализация зоны начала приступа полностью совпадала с зоной гипометаболизма 18F-ФДГ в 12 (92,3%) случаях. В одном случае зона начала приступа также выявлена в контралатеральной поясной извилине, в которой отсутствовали признаки структурных и метаболических изменений.
Резекция ФКД выполнена 13 пациентам, период наблюдения после оперативного лечения составил от 4 до 25 месяцев, более 12 месяцев — у 5/13 (38,5%).
Отсутствие приступов (Engel I) в послеоперационном периоде на момент публикации наблюдалось в 11 (84,6%) случаях. Исход класса Engel II зарегистрирован у 1 (7,69%), исход класса Engel III — у 1 (7,69%) МР-негативного пациента: перед резекцией локализация эпилептогенного очага была подтверждена с помощью инвазивного ЭЭГ-ВМ.
Распределение по типам ФКД было следующим: I тип — у 4 (17,4%) пациентов, II тип — у 16 (69,6%), III тип — у 3 (13,0%). Анализ топографической локализации гипометаболических зон показал, что лобная локализация является наиболее частой (43,5% всех случаев), за ней следуют островковая (26,1%) и теменная (17,4%). Оценка характера распространённости метаболических нарушений выявила, что паттерн «несколько извилин» встречается в 39,1% случаев, «фокальный участок» — в 30,4%.
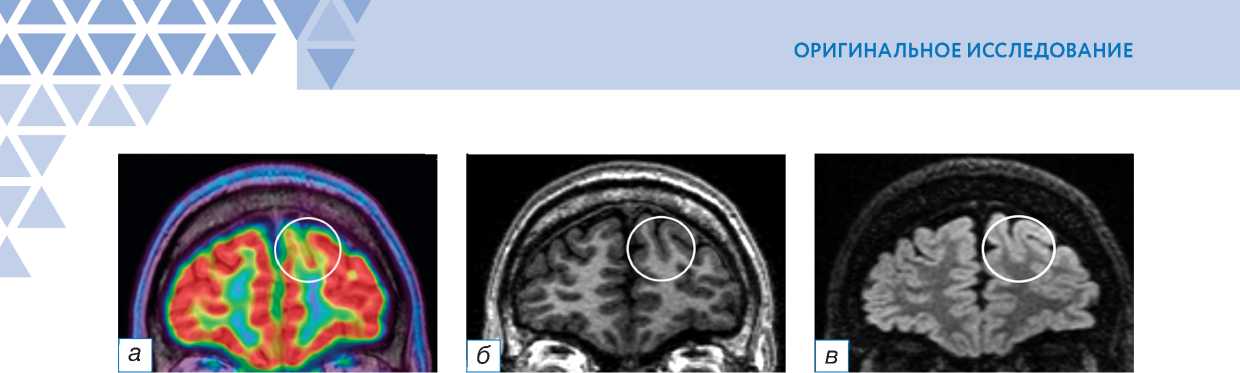
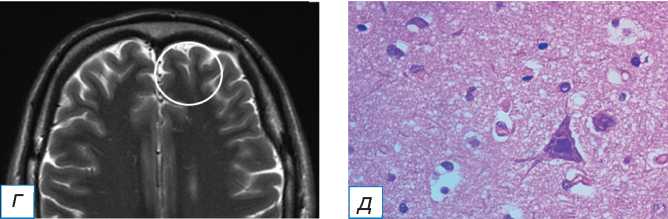
Рис. 1. Совмещённая позитронно-эмиссионная томография с магнитно-резонансной томографией (ПЭТ/МРТ) головного мозга с 18F-ФДГ пациента с фокальной кортикальной дисплазией дна борозды в левой лобной доле: а (совмещённое изображение ПЭТ/МРТ в корональной плоскости) — участок гипометаболизма 18F-ФДГ в области фокальной кортикальной дисплазии (окружность); б (Т1-ВИ в корональной плоскости) — небольшой участок снижения серо-белой демаркации в области дна борозды в левой лобной доле (окружность); в (Т2-FLAIR в коро-нальной плоскости) — небольшой участок повышения интенсивности МР-сигнала и снижения серо-белой демаркации в области дна борозды в левой лобной доле (окружность); г (Т2-ВИ в аксиальной плоскости) — небольшой участок снижения серо-белой демаркации в области дна борозды в левой лобной доле (окружность); д (гистологический препарат, окраска гематоксилином и эозином, х400) — дисморфичные нейроны.
Статистический анализ с использованием критерия хи-квадрат Пирсона не выявил значимой связи между типом ФКД и локализацией зоны гипометаболизма ( p =0,450), а также между типом ФКД и характером распространённости метаболических изменений, что может быть обусловлено относительно небольшим размером выборки и неравномерным распределением по подгруппам.
Выделены следующие паттерны гипометаболизма 18F-ФДГ, наблюдавшиеся при ФКД: небольшой фокальный участок гипометаболизма 18F-ФДГ; зона гипометаболизма 18F-ФДГ, распространяющаяся в пределах одной извилины; зона гипометаболизма 18F-ФДГ, распространяющаяся на две и более извилин. Паттерны гипометаболизма 18F-ФДГ изучены в зависимости от локализации ФКД. Фокальный паттерн гипометаболизма 18F-ФДГ (ограниченный гипометаболизм) практически полностью ассоциирован с лобной локализацией ФКД: такой паттерн выявлен у 75% пациентов с лобной локализацией ФКД и не зарегистрирован при других локализациях ФКД. Паттерн «несколько извилин» преобладает при поражении островковой, теменной, затылочной и височной зон, отражая наиболее распространённый характер гипометаболизма в этих областях. Для островковой и теменной долей преимущественно характерно мультифокальное распределение метаболических изменений, одиночное поражение извилины обнаруживалось крайне редко. При затылочной, теменной и островковой локализациях ФКД зона гипометаболизма 18F-ФДГ чаще вовлекает несколько соседних извилин, что затрудняет чёткую локализацию очага.
Дополнительные результаты исследования
У 2 пациентов с ФКД теменной локализации зона гипометаболизма 18F-ФДГ не совпадала с локализацией структурных изменений на МРТ, но располагалась в соседних участках вещества мозга (рис. 2, 3). При проведении этим пациентам стерео-ЭЭГ-ВМ эпилептиформная активность определялась в зоне выявленных структурных изменений и не регистрировалась в зоне метаболических изменений.
У 3 пациентов с ФКД I и II типов в зоне расположения ФКД помимо зоны гипометаболизма 18F-ФДГ определялись дополнительные зоны гипометаболизма 18F-ФДГ в других участках коры больших полушарий без признаков структурных изменений на МРТ, в 2 случаях по данным стерео-ЭЭГ-ВМ в этих участках определялась эпилепти-
С клиническая?
^практика
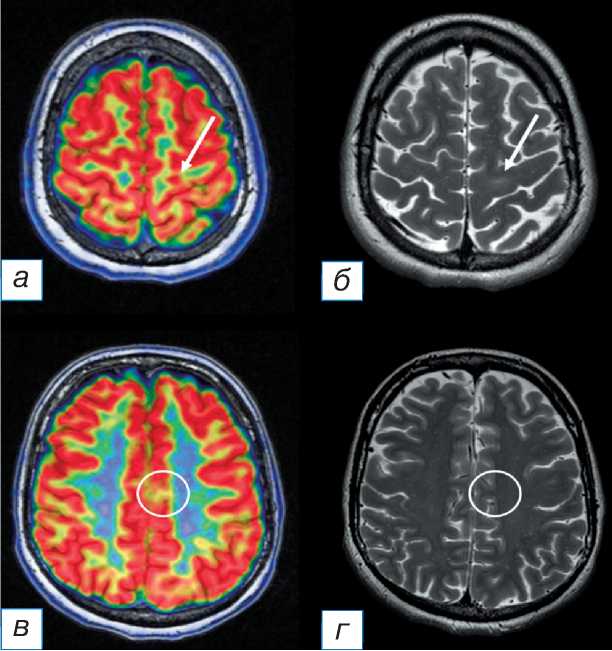
Рис. 2. Совмещённая позитронно-эмиссионная томография с магнитно-резонансной томографией (ПЭТ/МРТ) головного мозга с 18F-ФДГ пациента с фокальной кортикальной дисплазией в левой теменной доле: а (совмещённое изображение ПЭТ-МРТ в аксиальной плоскости) — отсутствие признаков гипометаболизма 18F-ФДГ в области фокальной кортикальной дисплазии (стрелка); б (Т2-ВИ в аксиальной плоскости) — участок повышения интенсивности МР-сигнала и снижения серо-белой демаркации в левой теменной доле (стрелка); в (совмещённое изображение ПЭТ-МРТ в аксиальной плоскости) — зона гипометаболизма 18F-ФДГ в парамедианных отделах левой лобной доли (окружность); г (Т2-ВИ в аксиальной плоскости) — отсутствие патологических структурных изменений в зоне гипометаболизма 18F-ФДГ (окружность).
формная активность, в 1 случае стерео-ЭЭГ-ВМ не выполнялась, после резекции ФКД был достигнут исход класса Engel II.
ОБСУЖДЕНИЕ
ПЭТ с 18F-ФДГ выполняется, как правило, в интериктальную фазу и позволяет выявить зоны гипометаболизма 18F-ФДГ в эпилептогенных очагах. Снижение накопления 18F-ФДГ в потенциальных очагах чувствительно, но неспецифично для эпилепсии: гипометаболизм 18F-ФДГ может наблюдаться и при других патологических состояниях вещества мозга, таких как инфаркт, опухоль, последствия травмы, а локализация зоны гипометаболизма не всегда точно соответствует малому эпилептогенному очагу, поэтому критически важно сопоставление данных ПЭТ с данными КТ или МРТ с целью точной анатомической локализации зоны гипометаболизма 18F-ФДГ, оценки её структуры, границ и взаимоотношения с окружающим веществом мозга [14]. В ряде исследований ПЭТ с 18F-ФДГ демонстрирует значительное преимущество по сравнению с МРТ в выявлении небольших пороков развития (таких как фокальная корковая дисплазия), которые с помощью ПЭТ обнаруживаются в 72–83% случаев, а при МРТ — лишь в 21–39% [15, 16].
Гибридный метод ПЭТ/МРТ обладает рядом преимуществ при обследовании пациентов с фармакорезистентной эпилепсией. В частности, метод лишён недостатков, присущих ПЭТ/КТ, таких как низкая анатомическая детализация мелких структур головного мозга, а также излишняя лучевая нагрузка от
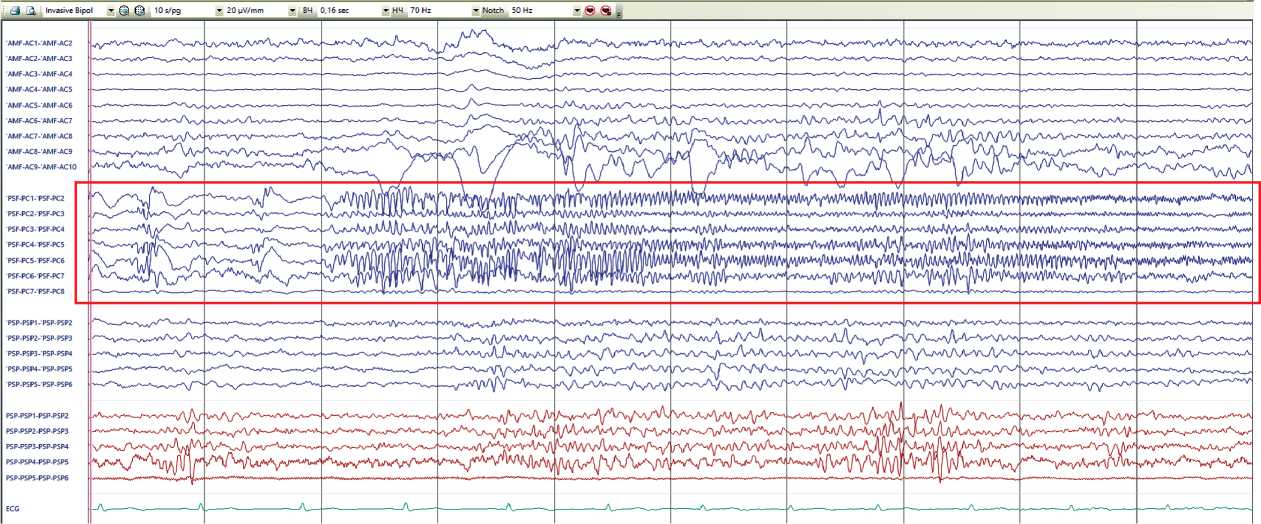
Рис. 3. Данные стереоэлектроэнцефалографии: за время мониторинга в течение 24 часов зарегистрировано 13 фокальных немоторных приступов с переходом в моторные с инициацией слева под электродом ‘PSF-PC’ (задняя верхняя лобная извилина — задняя часть поясной извилины, 8 контактов).

рентгеновской компьютерной томографии [17]. Технология ПЭТ/МРТ особенно удобна для применения в педиатрии благодаря снижению лучевой нагрузки и меньшему времени анестезии [18, 19].
Исследования эффективности гибридной методики ПЭТ/МРТ показали лучшие диагностические результаты и более точную идентификацию фокальных эпилептогенных очагов (в том числе у пациентов с рефрактерной эпилепсией) по сравнению с изолированным использованием ПЭТ или МРТ, а также методом ПЭТ-КТ [20]. В нашем исследовании с помощью ПЭТ/МРТ с 18F-ФДГ удалось увеличить выявляемость ФКД на 39% за счёт МР-негативных случаев, а также за счёт прицельного повторного пересмотра изображений МРТ с учётом метаболических данных. В ретроспективном исследовании K. Guo и соавт. [21] добавление компонента ПЭТ к МРТ позволило увеличить количество пациентов с единственным очагом, подозрительным в отношении эпилептогенной зоны, с 35% до 74%, что в свою очередь являлось сильным прогностическим фактором благоприятного исхода хирургической резекции эпилептогенного очага (Engel I). В большинстве литературных источников отмечается, что размеры зоны гипометаболизма 18F-ФДГ, как правило, превосходят размеры эпилептогенного очага, что следует учитывать при предоперационном планировании и оценке объёма резекции [22–24]. Зона гипометаболизма 18F-ФДГ, вероятно, включает в себя область инициации и распространения возбуждения, кроме того, обширный гипометаболизм 18F-ФДГ может быть связан с распространением эпилептической активности по нейрональным сетям, а также с феноменом пропагации или вовлечением функционально связанных областей [10, 19].
В нашем исследовании небольшой фокальный участок гипометаболизма 18F-ФДГ встречался исключительно при локализации ФКД в лобной доле, что составило 75% случаев лобного варианта ФКД. При ФКД височной локализации во всех случаях зона гипометаболизма 18F-ФДГ была обширной и распространялась на две и более извилин. Схожие данные получены в исследовании X. Wang и соавт. [15], в котором участки гипометаболизма 18F-ФДГ меньшей протяжённости отмечались при ФКД, локализующихся в лобных долях, в сравнении с другими локализациями, а также при II типе ФКД в сравнении с I типом. Таким образом, при подозрении на наличие ФКД лобной локализации анализ изображений требует особого внимания.
В исследовании H. Yokota и соавт. [25] размеры зоны гипометаболизма 18F-ФДГ при височной локализации ФКД также превышали размеры зон гипометаболизма 18F-ФДГ, наблюдавшиеся при ФКД других локализаций.
Часть обнаруженных очагов гипометаболизма 18F-ФДГ не находит подтверждения по данным МРТ, тем не менее хирургическая резекция данной области, проводимая с использованием ЭЭГ-ВМ, в большинстве случаев приводит к улучшению клинической симптоматики вплоть до полного исчезновения приступов. ПЭТ с 18F-ФДГ в ряде случаев может выявить эпилептогенную зону при МР-нега-тивной эпилепсии, кроме того, топическая локализация области гипометаболизма на ПЭТ помогает обнаружить органическую патологию при пересмотре данных МРТ, что особенно характерно для мелких очаговых корковых дисплазий [15].
В нашем исследовании эпилептогенный очаг был выявлен с помощью ПЭТ/МРТ с 18F-ФДГ у 6 (26,1%) пациентов с негативной МРТ-картиной. В исследовании H. Li и соавт. [26] совместная регистрация ПЭТ и МРТ позволила топически локализовать зоны гипометаболизма у 46% МР-негатив-ных пациентов и подтвердить 12% сомнительных результатов МРТ, что повысило частоту выявления фокальных корковых аномалий до 94%. Это связано в том числе с возможностью пересмотра данных МРТ при выявлении каких-либо аномалий метаболизма, что позволяет выявить мелкие структурные изменения, незамеченные или недооценённые ранее. В нашем исследовании при прицельном пересмотре изображений МРТ с учётом метаболических изменений признаки ФКД были обнаружены у 3 (13%) пациентов. Кроме того, ПЭТ/МРТ позволяет выявить больше потенциальных мишеней при планировании размещения электродов для стерео-ЭЭГ-ВМ и повысить тем самым количество выявленных эпилептогенных зон даже при МРТ-негативных формах эпилепсии [27].
В нашем исследовании у 5 пациентов с ФКД I и II типов были выявлены дополнительные участки гипометаболизма 18F-ФДГ в коре больших полушарий, в 2 случаях пациентам выполнялся инвазивный ЭЭГ-ВМ, при котором в этих участках определялась эпилептиформная активность. По данным литературных источников стоит также отметить, что у некоторых пациентов МР-негативный эпилептический очаг визуализируется контралатерально данным ЭЭГ: в таких случаях приоритетными являются данные стерео-ЭЭГ-ВМ [28].
иническая
эактика
В представленном нами исследовании кон-тралатерально расположенных участков гипометаболизма 18F-ФДГ зарегистрировано не было, однако у 2 пациентов локализация структурных и метаболических изменений не совпадала, зоны гипометаболизма 18F-ФДГ располагались в участках мозга, расположенных рядом с ФКД, и, вероятно, представляли собой зону функционального дефицита. По данным инвазивного ЭЭГ-ВМ, эпилептиформная активность у этих пациентов была зарегистрирована в зоне выявленных структурных изменений и не обнаружена в зоне метаболических изменений. Несоответствие между локализацией зоны гипометаболизма 18F-ФДГ по данным ПЭТ, эпилептогенной зоной, выявленной с помощью ЭЭГ, и клинической картиной может являться предиктором неблагоприятного исхода хирургического лечения. В исследовании Z.M. Wang и соавт. [28] сочетанный анализ данных ПЭТ совместно с МРТ в случае согласованности данных этих методик позволил выявить до 89% пациентов с благоприятным исходом хирургического лечения.
По полученным нами данным, исход класса Engel I был достигнут у 84,6% прооперированных пациентов, из них только у 39% период наблюдения составил более 12 месяцев, таким образом, полученные данные являются предварительным результатом.
Ограничения исследования
В исследование ретроспективно включены пациенты, у которых эпилептогенный очаг выявлен с помощью ПЭТ/МРТ, либо пациенты без выявленного очага, диагноз которых установлен с помощью стерео-ЭЭГ-ВМ и хирургической резекции. Несмотря на то, что перед исследованием ПЭТ, а также во время исследования все пациенты находились под наблюдением медицинского персонала, и у них не зарегистрировано клинических проявлений эпилептических приступов, тот факт, что непосредственно перед исследованием пациентам не проводился скальповый ЭЭГ-ВМ, также мог повлиять на результаты исследования в положительную сторону.
ЗАКЛЮЧЕНИЕ
Применение нового гибридного метода ПЭТ/ МРТ головного мозга с 18F-ФДГ в алгоритме предоперационного обследования пациентов с фокальной фармакорезистентной эпилепсией позволяет увеличить выявляемость ФКД (95,6% при ПЭТ/МРТ, 56,5% при МРТ) за счёт МР-негативных пациентов и пациентов с небольшими структурными изменениями в веществе мозга.
Наименьшие участки гипометаболизма 18F-ФДГ наблюдались у пациентов с локализацией ФКД в лобных долях: таким образом, подозрение на наличие ФКД лобной локализации требует наиболее внимательного и подробного анализа изображений ПЭТ/МРТ.
Применение ПЭТ/МРТ позволяет выявить дополнительные потенциально эпилептогенные очаги, что может применяться для уточнения расположения электродов для стерео-ЭЭГ-ВМ, а также для планирования и оценки прогноза хирургической резекции.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Вклад авторов. Т.М. Ростовцева , Р.В. Наделяев — написание статьи; А.В. Дворянчиков , М.А. Каралкина — аналитическая работа; М.Б. Долгушин , С.Г. Бурд — руководство, концепция, обсуждение результатов исследования; В.М. Джафаров — проведение хирургической резекции эпилептогенных очагов; Ю.В. Рублева — лечение пациентов; Е.А. Баранова — проведение скальпового и инвазивного видео-ЭЭГ-мониторинга; О.И. Пацап — проведение патоморфологического исследования. Все авторы одобрили рукопись (версию для публикации), а также согласились нести ответственность за все аспекты работы, гарантируя надлежащее рассмотрение и решение вопросов, связанных с точностью и добросовестностью любой её части.
Этическая экспертиза. Протокол исследования одобрен локальным этическим комитетом ФГБУ ФЦМН ФМБА России (протокол № 12/05-12-22 от 05.12.2022). Все участники исследования добровольно подписали форму информированного согласия до включения в исследование.
Раскрытие интересов. Авторы подтвердили отсутствие конфликта интересов, связанных с публикацией настоящей статьи.
Оригинальность. При проведении исследования и создании настоящей работы авторы не использовали ранее опубликованные сведения (текст, иллюстрации, данные).
Доступ к данным. Редакционная политика в отношении совместного использования данных к настоящей работе неприменима, данные могут быть опубликованы в открытом доступе.
Генеративный искусственный интеллект. При создании настоящей статьи технологии генеративного искусственного интеллекта не использовали.
ADDITIONAL INFORMATION
Author contributions: T.M. Rostovtseva , R.V. Nadelyaev , writing the text of the article; A.V. Dvoryanchikov , M.A. Karalkina , search and analytical work; M.B. Dolgushin , S.G. Burd , conception, discussion of the results of the study; V.M. Dzhafarov , surgical resection of the epileptogenic lesions; Yu.V. Rubleva , treatment of the patients; E.A. Baranova , scalp and stereo video EEG monitoring; O.I. Patsap , pathomorphological study. Thereby, all authors provided approval of the version to be published and agree to be accountable for all aspects of the work in ensuring that questions related to the accuracy or integrity of any part of the work are appropriately investigated and resolved.
Ethics approval: The research protocol was approved by the Ethics Committee at the Federal State Budgetary Institution “Federal
Center of Brain Research and Neurotechnologies” of the Federal Medical Biological Agency (extract from Protocol No. 12/05-12-22 dated 2022 Dec 05). All the study participants voluntarily signed an informed consent form before being included in the research.
Disclosure of interests: The authors declare that they have no competing interests.
Statement of originality: The authors did not use previously published information (text, illustrations, data) while conducting this work.
Data availability statement: The editorial policy regarding data sharing does not apply to this work, data can be published as open access.
Generative AI: Generative AI technologies were not used for this article creation.


