Гигиенические подходы к оценке факторов образа жизни, формирующих риск развития онкологических заболеваний (обзор)
Автор: Чехомов С.Ю., Елисеев Ю.Ю.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Гигиена
Статья в выпуске: 4 т.20, 2024 года.
Бесплатный доступ
Цель: с позиций профилактической медицины уточнить триггерные механизмы основных канцерогенных факторов нездорового образа жизни, участвующих в развитии онкозаболеваемости населения. Методика написания обзора. Проанализированы 46 научных работ, опубликованных в 2013-2023 гг., размещенных в базах данных Web of Science, Scopus, PubMed, CyberLeninka, eLibrary.ru. Электронный поиск проводился с использованием комбинации ключевых слов: «carcinogenic factors of an unhealthy lifestyle», «bad habits», «smoking», «passive smoking», «use of smokeless tobacco products», «alcohol consumption», «artificial sources of ultraviolet radiation», «cancer».
Канцерогенные факторы нездорового образа жизни, табакокурение, употребление алкоголя, искусственные источники ультрафиолетового излучения, онкологическая заболеваемость
Короткий адрес: https://sciup.org/149148654
IDR: 149148654 | УДК: 614.314:616-006 | DOI: 10.15275/ssmj462
Hygienic approaches to the assessment of lifestyle factors involved in the risk of cancer diseases (review)
Objective: from the standpoint of preventive medicine, clarify the trigger mechanisms of the main carcinogenic factors of an unhealthy lifestyle involved in the development of cancer in the population. Methodology for writing a review. 46 scientific papers published in 2013-2023, posted in the databases Web of Science, Scopus, PubMed, CyberLeninka, eLibrary.ru. Electronic search was carried out using a combination of keywords: "carcinogenic factors of an unhealthy lifestyle," "bad habits," "smoking," "passive smoking," "use of smokeless tobacco products," "alcohol consumption," "artificial sources of ultraviolet radiation," "cancer." Conclusion. An analysis of the scientific literature showed that the leading trigger mechanisms for the development of cancer in the population associated with an unhealthy lifestyle include: when drinking alcohol - the toxic effect on the body of the alcoholic beverage metabolite - acetaldehyde; with active, passive smoking -, exposure to highly active volatile N-nitrosoamines and, especially, dimethylnitrosoamine and benzopyrene; when using smoking vapes, vaporous propylene oxide compounds, formaldehyde and acetaldehyde; when using smokeless tobacco products, the presence in them of compounds of non-volatile tobacco-specific nitrosoamines (TSNA), which are indicators of genotoxicity; the use of artificial ultraviolet radiation sources for tanning is accompanied by sequential reactions of the formation of photoproducts consisting of cyclobutane pyrimidine dimers (CPDs), damaging genomic DNA and causing mutations with dysregulation of epidermal metabolism, apoptosis processes and immune mechanisms.
Текст обзорной статьи Гигиенические подходы к оценке факторов образа жизни, формирующих риск развития онкологических заболеваний (обзор)
EDN: PNRRLV
1Введение. Одной из приоритетных задач действующей системы российского здравоохранения, направленной на сохранение здоровья населения, является внедрение и совершенствование мер, обеспечивающих организацию профилактической работы в отношении безопасности для человека канцерогенных факторов среды обитания. Грамотная организация эффективной работы специалистами санитарной службы, и прежде всего сотрудниками Роспотребнадзора в осуществлении государственного контроля за безопасностью для человека канцерогенных факторов образа жизни, должна способствовать обеспечению высокой эффективности профилактической работы в системе отечественного здравоохранения [1, 2]. Действующий на территории Российской Федерации государственный нормативно-правовой акт Санитарные правила и нормы (СанПиН) 1.2.3685–21 «Гигиенические нормативы и требования к обеспечению безопасности и (или) безвредности для человека факторов среды обитания» относит к числу одних из ведущих факторов риска, представляющих опасность для человека, вредные привычки образа жизни человека [3]. Согласно VIII разделу СанПиН 1.2.3685–21 к канцерогенным факторам, участвующим в формировании образа жизни человека, относятся табакокурение, в том числе пассивное; употребление бездымных табачных продуктов (нюхательный и жевательный табак); злоупотребление алкогольными напитками; использование искусственных источников ультрафиолетового излучения для получения загара. Международное агентство по изучению рака (МАИР), входящее в систему Всемирной организацией здравоохранения (ВОЗ), считает проведение работ, направленных на исследования канцерогенных факторов нездорового образа жизни, глобальной проблемой современности. По данным экспертов МАИР ВОЗ, прекращение контактов человека с канцерогенами, основанное на исключении влияние триггеров вредных привычек неправильного образа жизни, приводит к снижению на 70% заболеваемости людей злокачественными новообразованиями (ЗНО) [4, 5] Таким образом, необходимость организации санитарно-гигиенической службой разъяснительной профилактической работы о влиянии канцерогенных триггеров неправильного образа жизни является фактором, направленным на обеспечение безопасности жизнедеятельности населения.
Цель представленного обзора заключалась в уточнении с позиций профилактической медицины триггерных механизмов основных канцерогенных факторов нездорового образа жизни, участвующих в развитии онкозаболеваемости населения.
Методика написания обзора. Проанализировано 109 научных работ, размещенных в базах данных Web of Science, Scopus, PubMed, CyberLeninka, eLibrary.ru. Электронный поиск в базах данных проводился с использованием комбинации ключевых слов: «carcinogenic factors of an unhealthy lifestyle», «bad habits», «smoking», «passive smoking», «use of smokeless tobacco products», «alcohol consumption», «artificial sources of ultraviolet radiation», «cancer», из которых отобраны 46 источников. Поисковый запрос был определен с помощью стратегии интерактивного поиска, основанного на использовании релевантной выборки достоверных данных аналитических исследований. Поиск в электронных базах данных и списках цитирований составил период с 2013 по 2023 г. Критериями включения и исключения в обзор явились данные научных работ, освещающих в качестве канцерогенных факторов неправильного образа жизни только объекты, признанные по данным экспертов МАИР и изданные после 2013 г. Отбор источников осуществлялся в соответствии с критериями PRISMA (Preferred Reporting Items for Systematic reviews and Meta-Analyses) (рисунок).
Результаты. Действующий на территории Российской Федерации современный государственный нормативно-правовой акт — СанПиН 1.2.3685–21 — содержит перечень основных существующих канцерогенных факторов нездорового образа жизни (та-бако-, пассивное курение, употребления бездымных табачных продуктов, алкоголь, искусственные источники ультрафиолетового излучения), представляющих онкологическую опасность для человека.
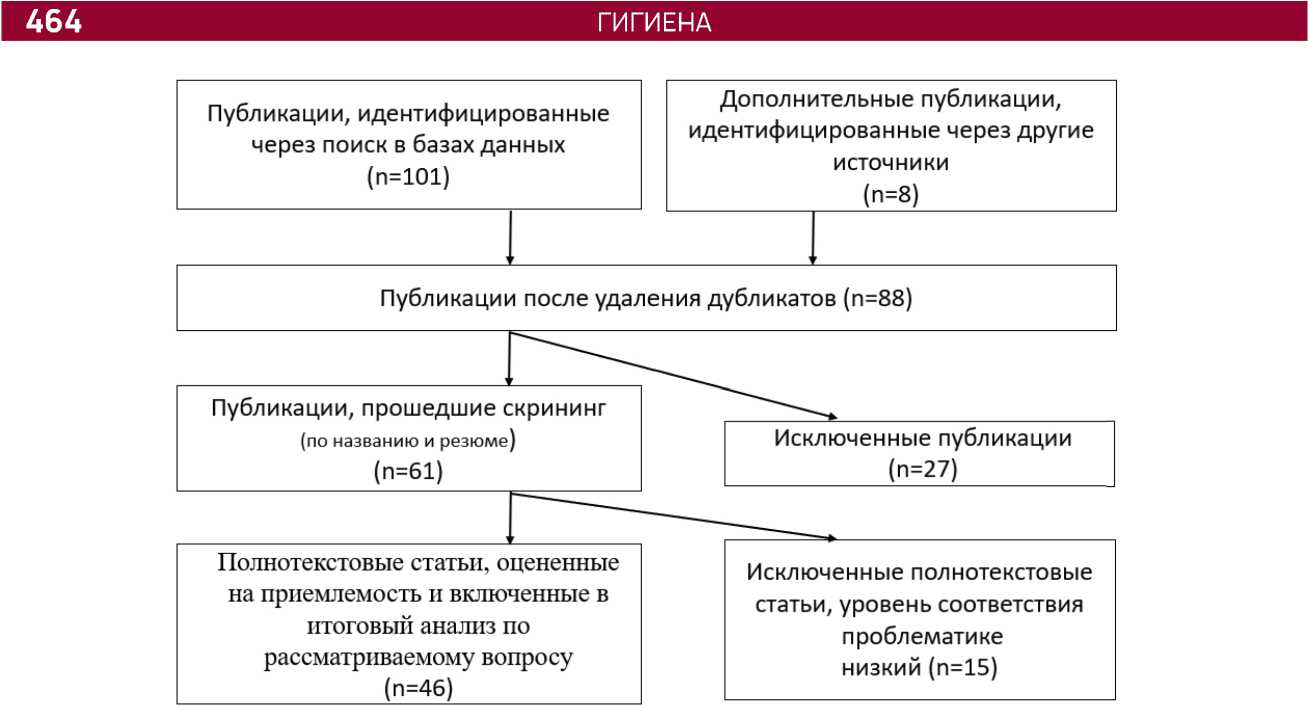
Методология отбора литературных источников
во вторичном выдыхаемом дыме происходит 50-кратное концентрирование вредных веществ, представляющих опасность за счет продуктов метаболизма и токсинов. О крайней степени канцерогенной опасности пассивного курения свидетельствуют результаты, полученные специалистами МАИР о влиянии последнего на повышение риска развития рака легких (на 30%) и почечно-клеточной карциномы (на 13%). В семьях курящих мужчин в сравнении с некурящими на 70% повышается риск развития рака молочной железы (РМЖ) и женских гениталий, на 60% — риск рака легких у женщин и на 12% — риск развития опухоли мозга у детей. Вторичный дым оказывает дополнительное негативное влияние на человека, оседая на коже, волосах, слизистой оболочке глаз, одежде, стенах помещений [6–11].
В настоящее время с учетом накопившихся знаний о негативных последствиях для здоровья населения общепринятого табакокурения отмечается рост уровня альтернативного курения, связанного с использованием различных паровых коктейлей, электронных сигарет, а также бездымных способов курения, таких как нюхательный и жевательный табак. Так, по данным Минздрава России, количество традиционных курильщиков в стране уменьшается, и сегодня не превышает 32,45%, а число лиц, употребляющих электронные сигареты, наоборот, постоянно растет [12, 13]. Использование паровых коктейлей нашло широкое применение в результате распространения ароматизированных специями и усиливающих вкусовые свойства табачных смесей. Культивируется также мнение о безопасности кальянного табака, который сгорает только частично, а образующие в небольшом количестве смолы задерживаются, проходя через водяные трубки. Мнение о безопасном низкотемпературном тлении углей и табака с современных позиций подвергается жесточайшей критике и остается в корне не верным. Последнее объясняется не только образованием монооксида углерода и канцерогенных веществ, но и значительным их поступлением в организм, что связано с длительностью культа процедуры одномоментного курения кальяна. В результате количество канцерогенов и токсических веществ, поступающих в организм человека, оказывается значительно большим, чем при курении сигарет.
Процесс курения мини-кальянов, электронных сигарет — вейпинг — основан на вдыхании курильщиком пара, образующегося при закипании жидкости, состоящей из глицерина, пропиленгликоля (Е1520), ароматических добавок, органических кислот, никотина (не всегда), бензилбензоата, метила, всего примерно 20 компонентов. Несмотря на то, что большинство компонентов состава электронных сигарет безопасны, риск развития рака легкого зависит от состава применяемых в девайсах жидкостей для курения. После нагревания аккумулятора содержащиеся в жидкостях вейпов глицерин и пропиленгликоль переходят в парообразное состояние, распадаясь до оксида пропилена, формальдегида и ацетальдегида, обладающих высоким канцерогенным потенциалом. Определенную онкогенную опасность представляют и частицы тяжелого металла кадмия, входящего в состав электронных сигарет.
Бездымная никотиновая продукция. Нюхательный и жевательный табак как виды бездымных табачных изделий значительной популярностью в Российской Федерации не пользуются. Доля их потребления колеблется от 1 до 4% [14].
Жевательный табак получил свое происхождение от предложенного в качестве альтернативы сигаретам в 1964 г. в Швеции сосательного табака (снюса). В отличие от последнего в составе жевательного табака отсутствуют табачные листья, а присутствуют ароматизаторы, пропиленгликоль, глицерин, целлюлоза и соли. Несмотря на то, что употребление жевательного табака не вредит в виде дыма окружающим, он остается опасным для индивидуального пользователя. По данным национального института онкологии США, в нем содержится приблизительно 28 химических веществ, в том числе канцерогенные нитрозоамины, полициклические ароматические углеводороды, а также присутствующий в табачных удобрениях радиоактивный элемент полоний-210, способствующие развитию рака ротовой полости, пищевода и ПЖ [15]. Представленные в данных МАИР современные результаты изучения употребления жевательного табака убедительно свидетельствуют о его пагубном влиянии: фиксирован рост смертности от онкологических заболеваний полости рта среди лиц, жующих табак, более чем в 5 раз. Помимо того, жевание табака населением Юго-Восточной Азии является одной из основных причин повышенного риска смертности от онкологических заболеваний не только верхних дыхательных путей (ВДП) и желудочно-кишечного тракта (ЖКТ), но женских гениталий, и особенно шейки матки [16–24].
Нюхательный табак (снафф) представляет собой высушенный и перетертый в порошок табак, предназначенный для втягивания в нос. Использование курильщиками нюхательного табака обусловлено легким всасыванием никотина с последующим развитием у потребителя быстрой зависимости. Нюхательный табак может содержать до 28 различных канцерогенных веществ, сильно различающихся в зависимости от типа продукта и способа производства. Вместе с тем в этих бездымных табачных изделиях обязательно присутствуют соединения нелетучих табакоспецифических нитрозоаминов (TSNA), полученных из алкалоидов N-нитрозоаминокислоты. Соединения TSNA идентифицируют как наиболее распространенные и самые канцерогенные вещества в бездымном табаке, являющиеся индикатором генотоксичности. По данным ВОЗ, на них приходится от 76 до 91 % общей нагрузки N-нитрозосоединений, вызывающей повреждения ДНК и в итоге — рак полости рта (лейкоплакию) и онкологических заболеваний ВДП [25, 26].
Алкогольные напитки. Сегодня во всем мировом сообществе обсуждаются вопросы злоупотребления алкогольными напитками. Более того, МАИР отнесло употребление последних к канцерогенным факторам образа жизни. Подобное определение находит объяснение в высокой онкологической заболеваемости и смертности как в мировом, так и европейском масштабе соответственно: 5,1 на 100 тыс. населения и 8,4 на 100 тыс. населения и 4,6% от всех случаев рака в мире и 6,2% — в Европе. При этом в показателях заболеваемости раком, обусловленных потреблением алкоголя, наблюдаются определенные закономерности. Так, в европейских регионах, по данным исследований МАИР, заболеваемость среди пьющих мусульман в 10 раз более низкая, чем среди христиан, соответственно 2 на 100 тыс. населения и 20 на 100 тыс. населения [27]. Смертность в Европе, обусловленная потреблением алкоголя, в 2,2 раза выше среди мужчин, чем среди женщин: 8 и 3,6% соответственно [28-30]. Вместе с этим следует отметить, что, несмотря на отсутствие нижнего порогового значения в шкале риска зависимости «доза — эффект», даже небольшие количества потребления алкоголя могут являться факторами риска развития таких онкозаболеваний, как рак полости рта (26,4%), ротоглотки (30,5%), пищевода (16,9%), а в комбинации с курением — плоскоклеточной карциномы пищевода (80,0%) и всех случаев рака печени (25,2%) [4, 31]. Каждые дополнительные 10 г ежедневного приема чистого алкоголя увеличивают на 7% риск возникновения у женщин РМЖ, а регулярное употребление 50 г чистого спирта на 10-20% стимулируют относительный риск развития рака прямой и толстой кишки пьющего [32]. Среди триггерных механизмов, вызывающих многие виды рака, связанные с регулярным употреблением алкоголя, установлено токсическое действие на организм выпивающего метаболита алкогольного напитка — ацетальдегида [32, 33].
Искусственные источники ультрафиолетового излучения для загара. В настоящее время использование ультрафиолетового (УФ) излучения для получения загара признано МАИР как установленный фактор риска развития онкологических заболеваний. Между тем среди физических факторов, направленных на получение искусственного загара в солярии или для лечения хронических заболеваний кожи, все более широко применяются методы УФ-излучения. Являясь одной из разновидностей электромагнитного излучения, УФ-излучение несет в себе определенное количество радиации, и уже в связи с этим оно может считаться потенциально опасным в отношении способности вызывать рак [36]. Установлено, что УФ-спектр излучения все больше признается не только как элемент, необходимый для нормальной жизнедеятельности или лечебнопрофилактических процедур, но и как фактор риска развития онкопатологии — различных видов кожного рака и меланом, занимающих ведущее место в структуре онкологической заболеваемости населения Земли [37]. Рост ежегодной кожной онкопатологии в масштабах планеты достигает 10,6%. При этом распределение кожной онкологической заболеваемости, обусловленной УФ-излучением, сегодня выглядит следующим образом: 63,6% — базальноклеточная карцинома, 25,8% — сквамозный плоскоклеточный рак и 10,6% — меланомы. В России в структуре общей онкозаболеваемости ЗНО кожи (без меланомы) также занимают лидирующее место, составляя 12,5% [36]. Рядом исследователей также установлено, что при использовании искусственного УФ-излучения риск заболеть меланомой резко повышается (в 4 раза и более) [38].
Регулярно и длительно проводимая, признанная наиболее высокоэффективной в лечении тяжелых форм псориаза, так называемая ПУВА-терапия (psoralen+ultraviolet A), основана на использовании фотосенсибилизаторов с одновременным облучением кожи длинноволновым УФ-излучением в диапазоне 320–400 нм. По наблюдениям ряда медицинских работников [39], данная терапия способствует возникновению у пациентов отдаленных эффектов канцерогенного действия с риском через 15 лет и более заболеть меланомой.
Поскольку рак кожи после искусственного воздействия УФ-излучения возникает не сразу, предполагается появление мутированных генов, остающихся в течение длительного времени в латентном состоянии, хотя в соответствии с законом Гротгу-са — Дрейпера фотохимический эффект воздействия УФ-излучения на организм человека должен быть пропорционален количеству поглощенной энергии. В результате нет ясности в вопросе о дозах, наиболее характерных для мутагенного хронического УФ-излучения, так же как и нет четких сведений связи частоты развития базально- и плоскоклеточного рака кожи от текущих и кумулятивных доз инсоляции, вызывающих УФ-индуцированный канцерогенез [40].
Еще один механизм повреждения ДНК клетки человека под воздействием УФ-лучей (В-диапазона) находит вполне доказанное объяснение в образовании циклобутановых пиримидиновых димеров (CPDs — cyclobutane pyrimidine dimers), 6–4-фотопродуктов, поперечных сшивок ДНК, одиночных разрывов или двойных разрывов нитей ДНК. Известно, что главная роль здесь принадлежит CPDs, которые являются выраженными мутагенами, способствующими появлению до 80% УФ-индуцированных мутаций с весьма высокой устойчивостью к апоптозу и стимулированию иммуносупрессии генов цитокинов [41, 42].
Однако, несмотря на значительный рост онкологической заболеваемости кожи большинство населения, проживающего даже в зоне истощения озонового слоя, а следовательно, под интенсивным воздействием УФ-излучения, остается здоровым [43]. Последнее видимо объясняется механизмами репарации (восстановления) ДНК, с последующей элиминацией мутагенов, сначала из базального слоя эпидермиса, а затем и из шиповатого в ходе эпидермального обмена. Однако даже при полностью завершенном процессе мутагенеза, большая часть онкоантигенов мутировавших клеток гибнут в результате апоптоза, аутофагии или элиминируются механизмами иммунитета [37, 44–46]. В результате с современных позиций патогенез фотоповреждения кожи под воздействием искусственных источников
УФ-излучения, приводящий к последующему канцерогенезу, следует рассматривать как хроническое воспаление с явлениями вторичной иммуносупрессии. Данный процесс характеризуется сложным и многоступенчатым развитием последовательных реакций, включающих:
-
— формирование фотопродуктов;
-
— повреждение геномной ДНК и других клеточных структур;
-
— наличие мутаций с ведущей ролью CPDs;
-
— нарушения регуляции эпидермального обмена, процессов апоптоза и механизмов иммунитета [36].
Санитарно-гигиенические аспекты организации профилактической работы в отношении обеспечения канцерогенной безопасности для человека факторов образа жизни. В настоящее время перечисленные в СанПиН 1.2.3685–21 и представленные в данном обзоре факторы образа жизни населения (табако-, пассивное курение, употребление бездымных табачных продуктов, употребление алкоголя, искусственные источники УФ-излучения) признаны МАИР канцерогенами, ответственными за онкогенез, способствующий развитию ряда ЗНО [6, 8, 11, 15, 22, 34, 39, 46].
Выявленные нами в результате анализа литературы основные механизмы риска развития онкозаболеваемости населения, обусловленные канцерогенными факторами образа жизни населения, а также связанная с ними современная эпидемиологическая обстановка и характеристика обнаруженных при этом форм раковых патологий, представлены в таблице.
Учитывая высокую канцерогенную опасность, обусловленную несоблюдением факторов
Механизмы риска развития онкозаболеваемости населения, обусловленные канцерогенными факторами образа жизни населения
|
Канцерогенные факторы образа жизни по СанПиН 1.2.3685–21 |
Авторы, название статьи, страна, год, ссылка |
Характеристика эпидемиологии, механизмов развития и форм онкозаболеваемости населения, обусловленных факторами образа жизни |
||
|
современная эпидемиологическая характеристика канцерогенного фактора |
механизмы риска развития онкозаболеваний под влиянием канцерогенных факторов образа жизни |
онкозаболевания населения, обусловленные канцерогенными факторами образа жизни |
||
|
Табакокурение Активное |
Левшин В. Ф., Слепчен-ко Н. И. Табако-курение и риск возникновения злокачественных опухолей и других хронических неинфекционных заболеваний. Россия, 2020 [11] |
Ежегодная смертность в мире от рака легких, связанная с табакокурением, составляет 87% от ежегодной онкологической смертности. В России курят 27 млн россиян (32,45% взрослого населения) |
69 доказанных канцерогенов, в том числе высокоактивные летучие N-нитрозоамины, и особенно диметилнитрозоамин и бенз[ a ]пирен |
Раковые заболевания легких, полости рта, гортани, носовых пазух, органов ЖКТ, мочевыделительной системы, женской и мужской половой сферы, миелоидный лейкоз |
|
Пассивное |
Куликов А. В. Пассивное курение и его последствия Россия, 2017 [6] |
Повышает на 30% риска развития рака легких, на 70% — РМЖ и женских гениталий, на 13% — почечноклеточную карциному; на 12% риск рака мозга у детей |
Те же |
РМЖ и женских гениталий, почечно-клеточная карцинома, рак мозга у детей |
|
Кальяны и электронные сигареты |
Немова О. А., Водолагин М. В., Гамбарян М. Г. и др. Анализ факторов, связанных с потреблением электронных сигарет населением в возрасте 18–35 лет. Россия, 2024 [13] |
Курят до 10,8 млн человек. Риск развития рака легкого зависит от состава применяемых в девайсах жидкостей для курения и частиц тяжелого металла кадмия, входящего в состав электронных сигарет |
Те же, а также канцерогенные оксид пропилена, формальдегид и ацетальдегид, находящиеся в парообразном состоянии в курительных жидкостях вейпов. Кадмий (канцероген), находящийся в составе электронных сигарет |
Риск развития рака легкого |
Окончание табл.
|
Канцерогенные факторы образа жизни по СанПиН 1.2.3685–21 |
Авторы, название статьи, страна, год, ссылка |
Характеристика эпидемиологии, механизмов развития и форм онкозаболеваемости населения, обусловленных факторами образа жизни |
||
|
современная эпидемиологическая характеристика канцерогенного фактора |
механизмы риска развития онкозаболеваний под влиянием канцерогенных факторов образа жизни |
онкозаболевания населения, обусловленные канцерогенными факторами образа жизни |
||
|
Бездымные табачные продукты |
Калашников С. В., Шкидюк М. В. Идентификационные признаки некурительной табачной продукции. Россия, 2021 [25] |
Доля потребления бездымных табачных изделий населением России не велика и колеблется от 1 до 4% |
Содержат до 28 канцерогенных веществ различающихся в зависимости от типа продукта и способа производства |
Рак заболеваний ротовой полости (лейкоплакия), ВДП, пищевода, ПЖ |
|
Нюхательный табак |
Салагай О. О., Антонов Н. С., Сахарова Г. М. Анализ структуры и динамики потребления табака и никотинсодержащей продукции в РФ в 2019–2022 гг. Россия, 2022 [14] |
Увеличивает до 76– 91 % общей нагрузки N-нитрозосоединений, вызывающих повреждения ДНК и в итоге рак полости рта (лейкоплакию) и ЗНО ВДП |
Те же, а также присутствуют канцерогенные соединения TSNA, являющиеся индикатором генотоксичности |
Те же |
|
Жевательный табак |
Loomis D, Huang W, Chen G. The International Agency for Research on Cancer (IARC) evaluation of the carcinogenicity of outdoor air pollution: Focus on China. Китай, 2014 [24] |
Основная причина роста смертности от ЗНО (ВДП, ЖКТ и шейки матки) в Юго-Восточной Азии. Пятикратный рост онкологической заболеваемости полости рта среди жующих табак в сравнении с теми, кто никогда его не употреблял |
Те же, а также канцерогенные нитрозами-ны, полициклические ароматические углеводороды, радиоактивный элемент — полоний-210, накапливающиеся в удобрениях и способствующие развитию рака различных отделов ЖКТ курильщиков |
Те же |
|
Алкогольные напитки |
Rumgay H, Shield K, Char-vat H, et al. Global burden of cancer in 2020 attributable to alcohol consumption: a population-based study. США, 2021 [34] |
Из 9 млн случаев смерти от рака в мире, 4,2% обусловлены потреблением алкоголя; в Европе таких причин смерти — 6,1 % (8% у мужчин и 3,6% у женщин) |
Среди триггерных механизмов, доказано токсическое действие ацетальдегида, который является метаболитом алкоголя в организме регулярно пьющего контингента населения |
Большинство смертей, связанных с употреблением алкоголя происходит не из-за острого отравления, а из-за вызванных им хронических заболеваний, в 29% случаев приводящих к раку: ротовой полости, горла, гортани, пищевода, печени, поджелудочной железы, прямой кишки, грудной железы |
|
Искусственные источники УФ-излучения для загара |
Синицын Б. Ф., Каладзе Н. Н., Чинов С. Г. и др. К профилактике повышения риска фотоканцерогенеза при использовании инсоляции и ультрафиолетового излучения в практике лечения и оздоровления. Россия, 2019 [36] |
Ежегодный рост кожной онкопатологии в масштабах планеты составляет 10,6%. Распределение кожной онкозаболеваемости, обусловленной УФ-излучением, выглядит следующим образом: 63,6% — базальноклеточная карцинома, 25,8% — сквамозный плоскоклеточный рак и 10,6% — меланомы. В России в структуре общей онкозаболеваемости ЗНО кожи (без меланомы), лидируют и составляют 12,5% |
Патогенез фотоповреждения кожи под воздействием искусственных источников УФ-излучения, приводящий к канцерогенезу рассматривается как хроническое воспаление с явлениями вторичной иммуносупрессии. Процесс включает последовательные реакций: формирование фотопродуктов, повреждение геномной ДНК и других клеточных структур; мутации с ведущей ролью CPDs; нарушения регуляции эпидермального обмена, процессов апоптоза и механизмов иммунитета |
Меланома, базаль-но- и плоскоклеточная формы рака кожи |
здорового образа жизни, информацию по устранению или уменьшению этой опасности от вредных привычек в соответствии с требованиями настоящего документа необходимо доводить до населения. Основными мероприятиями в этом отношении должны служить знания населения о канцерогенной опасности рассматриваемых факторов, а также исключение возможности контакта человека с вредными факторами в производственной и бытовой сферах.
Заключение. Проведенный анализ научной литературы показал, что к ведущим триггерным механизмам развития онкозаболеваемости населения, связанным с нездоровым образом жизни, относятся следующие:
при употреблении алкоголя — токсическое действие на организм метаболита алкогольного напитка — ацетальдегида;
активном, пассивном табакокурении — воздействие высокоактивных летучих N-нитрозоаминов, и особенно диметилнитрозоамина и бенз[ a ]пирена;
использовании курительных вейпов, находящиеся в парообразном состоянии, — соединения оксида пропилена, формальдегида и ацетальдегида;
пользовании бездымной табачной продукцией — соединения TSNA, являющиеся индикаторами генотоксичности;
применении искусственных источников УФ-излучения для загара — последовательные реакции формирования фотопродуктов, состоящих из CPDs, повреждающих геномные ДНК и вызывающих мутации с нарушениями регуляции эпидермального обмена, процессов апоптоза и механизмов иммунитета.
Финансирование. Исследование не имело спонсорской поддержки.
Вклад авторов. Все авторы внесли эквивалентный вклад в подготовку публикации.


