Гипоксическая проба как метод прогнозирования гемотрансфузионной тактики и характера течения раннего послеоперационного периода в коронарной хирургии
Автор: Мандель Ирина Аркадьевна, Киселев Валерий Олегович, Подоксенов Юрий Кириллович, Свирко Юлия Станиславовна, Шипулин Владимир Митрофанович
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Анестезиология, реаниматология и перфузиология
Статья в выпуске: 2 т.16, 2012 года.
Бесплатный доступ
Рассмотрена тактика гемотрансфузионной терапии при операции коронарного шунтирования в условиях искусственного кровообращения у больных с фракцией выброса левого желудочка выше и ниже 40%. В дооперационном периоде пациентам основной группы проводили гипокси-ческую пробу, на основании которой прогнозировали тактику периоперационной гемотрансфузии. Группу сравнения составили пациенты с традиционным подходом к назначению донорской крови. Проанализированы клинические и лабораторные данные, показатели гемодинамики и кислородного баланса, течение послеоперационного периода. В результате исследования доказана возможность снижения использования аллокрови на 48,8% (p = 0,02). На основании пробы определены критерии для снижения периоперационного триггерного уровня гемоглобина до 70 г/л, в том числе в группе больных с низкой фракцией выброса левого желудочка. Показано, что при нашей тактике определения триггерного уровня гемоглобина снижается продолжительность искусственной вентиляции легких (ИВЛ), частота развития гастроинтестинальных осложнений, полиорганной дисфункции и срок пребывания в отделении реанимации.
Гемотрансфузия, кровесберегающие технологии, низкая фракция выброса левого желудочка, гипоксическая проба, послеоперационные осложнения
Короткий адрес: https://sciup.org/142140477
IDR: 142140477 | УДК: 616-06
Prediction of transfusion therapy tactics for prophylaxis of early postoperative complications in coronary surgery
The study focuses on the tactics of transfusion therapy during coronary artery bypass surgery with cardiopulmonary bypass in patients with left ventricular ejection fraction higher or lower than 40%. To predict the tactics of intraoperative transfusion therapy, hypoxic tests were preoperatively conducted in the main group of patients. A traditional approach to blood transfusion was applied in the control group of patients. The analysis of clinical and laboratory data, hemodynamics and oxygen balance, as well as follow-up data allowed to prove the possibility of decreasing allogenic blood use by 48.8% (p = 0,02). Based on the hypoxic test data, criteria for lowering the intraoperative trigger hemoglobin level down to 70 g/l, including the patients with a low left ventricular ejection fraction. It was shown that our tactics of trigger hemoglobin level calculation allows for reducing artificial lung ventilation time, frequency of gastrointestinal complications, multiple organ failure, as well as duration of stay at ICU.
Текст научной статьи Гипоксическая проба как метод прогнозирования гемотрансфузионной тактики и характера течения раннего послеоперационного периода в коронарной хирургии
Кардиохирургические операции в условиях искусственного кровообращения (ИК) сопровождаются кровопотерей, которая является одним из факторов риска развития осложнений и обусловливает применение аллогемотрансфузий с частотой до 80% [11]. Учитывая спектр осложнений и проблем, связанных с применением донорской крови и ее компонентов, ограничение показаний становится предметом клинических исследований [1, 6, 8]. Кровесберегающие технологии в кардиохирургии предполагают совершенствование методов профилактики периоперационной кровопотери, заготовку аутокрови, реинфузии крови, ультрафильтрацию, применение аппарата «Cell-Saver» и определение безопасных триггерных уровней гемоглобина (Hb) для гемотрансфузии в периоперационном периоде [7, 9, 15].
Показания к переливанию крови и ее препаратов неоднозначны: периоперационная кровопотеря в объеме больше 12–15% ОЦК, снижение концентрации Hb до 70 г/л [9, 10, 13] или до 100 г/л [4, 12–14]. Однако многие факторы индивидуальной толерантности к анемии и компенсаторные воз- можности пациента не учитываются, что может привести к завышению показаний к гемотрансфузии. Цель исследования – разработка и оценка эффективного и безопасного метода прогнозирования толерантности кардиохирургических пациентов к периоперационной анемии и интраоперационной гемодилюции.
МАТЕРИАЛ И МЕТОДЫ
Исследование выполнено в отделении анестезиологии и реанимации НИИ кардиологии г. Томска в 2007–2011 гг. и одобрено этическим комитетом. Всего обследовано 208 больных, перенесших операцию реваскуляризации миокарда в условиях искусственного кровообращения. В основную группу включены 133 пациента с ишемической болезнью сердца (ИБС) в возрасте 56±8 лет III–IV функционального класса по канадской классификации. Пациентов с фракцией выброса левого желудочка (ФВ ЛЖ) <40% было 54 (40,6%).
За 5–7 суток до кардиохирургической операции всем пациентам для выявления пато- логии желудочно-кишечного тракта (ЖКТ) проводили фиброгастродуоденоскопию (ФГДС). За трое суток больным основной группы выполняли общую гипоксическую пробу (ОГП) – сеанс дыхания гипоксической газовой смесью с 14% (ГГС-14), 12% (ГГС-12) или 10% (ГГС-10) содержанием кислорода в течение 40 мин [4]. Гипоксическую газовую смесь готовили с помощью прибора «Гипок-сикатор ГП-М», работающего по принципу мембранного газоразделителя. Пробу начинали с ГГС-14 с 14% содержанием кислорода. При стабильном состоянии больного на этом уровне гипоксии переходили к дыханию смесью с 12%, затем с 10% кислорода. В исходном состоянии и на 10, 20, 30 и 40-й мин гипоксической пробы больным измеряли артериальное давление (АД), частоту сердечных сокращений (ЧСС), частоту дыхания (ЧД), оценивали клинические данные и жалобы больного.
Толерантность к гипоксии (ТГ) определяли по показателям сатурации крови методом пульсоксиметрии (SрО2), сатурации венозной крови прямым методом (SvO2), уровню в крови лактата, рассчитывали индекс экстракции кислорода: O2EI = (SрО2 – SvO2) / SрО2 × 100. Нормой считали SрО2 >85%; SvO2 >60%; O2EI – 22–30%; лактат – менее 2,5 ммоль/л [2]. При значениях показателей SрО2 >85%; SvO2 >60%; O2EI <30% и отсутствии роста уровня лактата на фоне 40 мин дыхания ГГС-10 ТГ считали высокой. Если указанные значения показателей кислородного баланса имели место при ГГС-12, ТГ – средняя. При низкой ТГ нормальные значения показателей кислородного баланса имели место при применении ГГС-14.
На основании результатов пробы определяли показания к инфузии препаратов аллокрови в периопераци- онном периоде и триггерный уровень Hb и гематокрита (Ht). Поскольку эти значения варьируют в различных клинических руководствах от 60–70 [9, 10, 13] до 100 г/л [4, 12–14], мы при выборе тактики гемотрансфузионной терапии руководствовались результатами пробы. Так, у больных с высокой ТГ считали допустимым снижение Ht во время ИК до 21% и снижение Hb <70 г/л в течение операции и раннего послеоперационного периода. При средней ТГ гемотрансфузионную терапию начинали в случае снижения концентрации Hb <80 г/л на любом этапе лечения, а во время ИК при уровне Ht менее 24%. Больным с низкой ТГ назначали препараты аллокрови при снижении Hb <90 г/л и уровне Ht <27% [13, 14].
Группу сравнения составили 75 больных, которые по клинической характеристике значимо не отличались от основной (табл. 1). У 27 (36%) из них до операции ФВ ЛЖ <40%. Всем пациентам этой группы, исходя из данных литературы, показанием для переливания донорской крови во время операции и в раннем послеоперационном периоде выбран триггерный уровень Hb 90 г/л [13, 14].
Больные основной и группы сравнения сопоставимы по объему операции, длительности ИК и окклюзии аорты, характеру и степени выраженности сопутствующей патологии, объему кровопотери. Все пациенты до операции заполняли информированное согласие по утвержденной в клинике форме. Критерии исключения из исследования – послеоперационное кровотечение, продленное ИК, реторакотомия, внутриаортальная балонная контрпульсация.
|
Таблица 1 Клиническая |
Показатель |
Группа |
р |
|
|
основная, n = 133 |
сравнения, n = 75 |
|||
|
характеристика |
Средний возраст, лет |
56±8 |
54±6 |
НД |
|
пациентов |
Мужской пол, % |
84 |
79 |
НД |
|
НД – различие между |
Площадь поверхности тела, м 2 |
1,95±0,14 |
1,94±0,15 |
НД |
|
группами недостоверно |
Функциональный класс по канадской классификации, n (%) |
|||
|
III |
84 (63,2) |
59 (78,7) |
НД |
|
|
IV |
49 (36,8) |
16 (21,3) |
НД |
|
|
Степень артериальной гипертензии, % |
||||
|
II |
28 |
34 |
НД |
|
|
III |
72 |
66 |
НД |
|
|
Класс сердечной недостаточности по NYHA, n (%) |
||||
|
II |
38 (28,6) |
24 (32,0) |
НД |
|
|
III |
95 (71,4) |
51 (68,0) |
НД |
|
|
ЧСС, уд/мин |
74±12 |
75±9 |
НД |
|
|
Инфаркт миокарда в анамнезе, % |
90,1 |
88,0 |
НД |
|
|
ФВ ЛЖ, n (%) |
||||
|
более 40% |
79 (59,4) |
48 (64,0) |
НД |
|
|
менее 40% |
54 (40,6) |
27 (36,0) |
НД |
|
|
Риск операции по шкале EuroSCORE, баллы (%) |
7±5 (2,43–31,79) |
7±5 (2,75–29,31) |
НД |
|
Рис. 1.
Показатели кислородного баланса у пациентов основной группы при проведении ОГП с 10% содержанием кислорода в газовой смеси (n = 87)
S±Sx; SрО2 – сатурация кислорода артериальной крови, %; SvО2 – сатурация кислорода венозной крови, %; O2EI – индекс экстракции кислорода; Lac – лактат, ммоль/л.
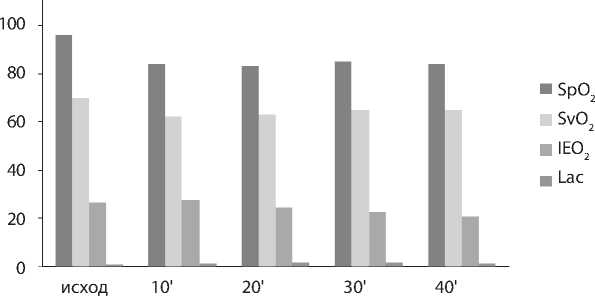
Рис. 2.
Соотношение больных с нормальной ( >40%) и сниженной ( <40%) ФВ ЛЖ в подгруппах основной группы (n = 128) и в группе сравнения (n = 75).
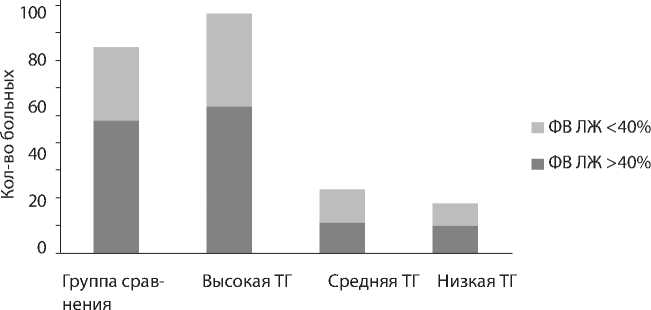
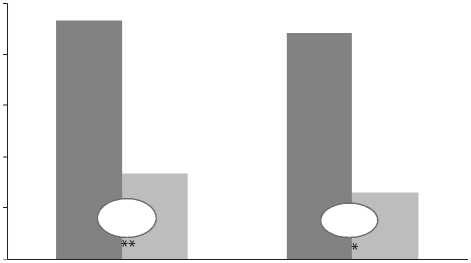
Рис. 3.
Средний объем периоперационных гемотрансфузий (мл) у пациентов с различной дооперационной сократимостью левого желудочка: * p = 0,05;
** p = 0,02.
т 100
S
■ Контрольная группа
■ Основная группа
ФВ ЛЖ >40%
ФВ ЛЖ <40%
Все операции проводили по стандартному анестезиологическому протоколу c использованием фентанила, бензодиазепинов, миорелаксантов [7] в условиях нормотермического ИК с объемной скоростью перфузии не ниже 2,5 л/мин × м2 и уровнем АД 60–80 мм рт. ст. Кардиоплегию осуществляли кустодиолом (20 мл/кг). Всем пациентам проводили ультрафильтрацию во время искусственного кровообращения.
Параметры центральной гемодинамики определяли методом термодилюции с использованием катетера Сван – Ганца у пациентов с ФВ ЛЖ менее 40% и с помощью чреспищеводного ультразвукового исследования у остальных пациентов. Исследовали газовый состав крови на приборе «Stat Profile 5» («Nova Bi o med i c a l», США), показатели кислотно-основного равновесия артериальной и венозной крови, уровни Hb и Ht, индексы п отребле ния и доставки кислорода, сатурацию крови (SрО2 и SvО2),
Таблица 2
Характеристика интра-и послеоперационного периодов у пациентов в основной (n = 128) и группе сравнения (n = 75) НД – различия показателей не достоверны
|
Показатель |
Группа сравнения |
ТГ в основной группе |
p |
||
|
высокая |
средняя |
низкая |
|||
|
Исходный Hb, г/л |
145±23 |
139±15 |
141±18 |
142±21 |
НД |
|
Исходный Ht, % |
38±3 |
37±2 |
36±3 |
39±4 |
НД |
|
Длительность ИК, мин |
86,3±7,6 |
73,4±7,2 |
78,9±10,3 |
75,3±7,6 |
НД |
|
Ишемия миокарда, мин |
52,1±9,3 |
44,90±8,44 |
49,7±6,9 |
47,1±6,3 |
НД |
|
Объем кровопотери, мл |
|||||
|
интраоперационной |
778±186 |
766±98 |
745±62 |
803±67 |
НД |
|
послеоперационной (за 12 ч) |
134±50 |
122±53 |
125±75 |
130±84 |
НД |
|
Объем интраоперационных и послеоперационных гемотрансфузий, мл/чел |
227±54 |
74±25* |
123±37 |
111±28 |
* 0,02 относительно группы сравнения |
ФВ ЛЖ, n
Таблица 3
Характеристика послеоперационного периода исследуемых групп больных
* p = 0,05 между основной и группой сравнения
|
Показатели |
группа сравнения |
группа высо |
кой ТГ |
|
|
>40%, 48 |
<40%, 27 |
>40%, 53 |
<40%, 34 |
|
|
Инотропная поддержка, ч |
12±3 |
29±9 |
14±4 |
47±15* |
|
ИВЛ, ч |
9±2 |
11±3 |
8±3 |
9±3 |
|
Медиастенит, n |
1 |
– |
– |
– |
|
Пневмония, n |
2 |
1 |
– |
1 |
|
Нагноение п/о раны, n |
1 |
2 |
2 |
– |
|
Гастроинтестинальные осложнения, n (%) |
2 (4,2) |
1 (3,7) |
1 (1,9) |
– |
|
Респираторные осложнения, n (%) |
1 (2,1) |
1 (3,7) |
– |
1 (2,9) |
|
Ренальная дисфункция, n (%) |
1 (2,1) |
2 (7,4) |
1 (1,9) |
1 (2,9) |
|
Неврологические осложнения, n (%) |
1 (2,1) |
– |
– |
– |
|
Пребывание в ОАР, дней |
4±1 |
4±1 |
3±1 |
4±1 |
|
Летальность, % |
4,2 |
3,7 |
3,8 |
2,9 |
индекс экстракции кислорода (O2EI), артериовенозную разницу по кислороду, уровень лактата крови, а также общий белок и альбумин на уже перечисленных этапах.
Объем кровопотери рассчитывали гравиметрическим методом, измеряли объем крови в аспирационных и дренажных резервуарах. Определяли частоту развития периоперационной анемии, инфекционных осложнений (медиастинита, пневмонии, нагноения послеоперационной раны). Характеристика интраоперационного периода представлена в табл. 2.
Статистическую обработку результатов выполняли с применением системы статистического анализа Statistica 6.0. Сравнение двух групп проводили с помощью t-критерия Стьюдента. Результаты представляли как среднее и среднеквадратичное отклонение (X±Sx ). Статистически значимыми считали различия при р <0,05.
РЕЗУЛЬТАТЫ
Непереносимость ОГП выявлена у 5 больных (3,8%), которых исключили из дальнейшего исследования.
Индивидуальную непереносимость ОГП констатиро- вали на основании увеличения клинических признаков: ЧСС более чем на 30 в мин, прироста АД более чем на 30 мм рт. ст., ЧД более чем на 10 в мин. Применение метода считали противопоказанным, если на первых минутах дыхания ГГС-14 наступали отмеченные изменения. Указанные симптомы были преходящими и ни в одном случае не привели к осложнениям.
Успешно пробу перенесли 128 (96,2%) пациентов основной группы, высокая ТГ выявлена у 53 пациентов (39,8%) с ФВ ЛЖ >40% и у 34 (25,6%) с ФВ ЛЖ <40%. Интегральные показатели кислородного баланса, наблюдаемые нами при дыхании ГГС-10, представлены на рис. 1. Статистически значимо снижалась лишь SрO2 до 83,0±4,2 (р = 0,02) на 13,55%, минимальная SvO2 за время проведения пробы составила 62,0±4,1 (р = 0,02), уровень лактата не поднимался выше 1,70±0,58 мМ/л (р = 0,02), O2EI находился в пределах нормы (24,50±5,21). Средняя ТГ отмечена у 23 больных (17,3%), из них ФВ ЛЖ <40% у 11 человек. Низкую ТГ наблюдали у 18 больных (13,5%), ФВ ЛЖ <40% у 9 человек (рис. 2).
В течение основного этапа операции показатели кислородтранспортной функции крови у больных основной группы закономерно изменялись и возвращались к нормальным значениям в постперфузионном периоде, что свидетельствовало об адекватном уровне Hb и Ht у каждого больного. У пациентов основной группы, имевших высокую ТГ, гемотрансфузии проводили в 14,9% случаев, из них 6 пациентам (6,9%) переливали донорскую кровь во время операции, 4 (4,6%) – в послеоперационном периоде, троим (3,4%) – как во время, так и после операции. В группе со средней ТГ – 30,4% случаев, из них 4 пациентам (17,4%) переливание донорской крови было во время операции, одному (4,3%) – в послеоперационном периоде, двоим (8,7%) – как во время, так и после операции. При низкой ТГ – в 44,5%, из них 4 пациентам (22,2%) переливали донорскую кровь во время операции, троим (16,7%) – в послеоперационном периоде, одному (5,6%) – как во время, так и после операции.
Поскольку 87 пациентов (65,4%) основной группы обладали высокой ТГ, потребность в аллокрови в этой группе в целом была ниже на 49,1% (р = 0,02). Объем кровопотери во время операции и в раннем послеоперационном периоде не имел значимого различия в исследуемых группах (табл. 2). Объем периоперационных гемотрансфузий у больных с ФВ ЛЖ >40% статистически значимо различался и был на 35,6% ниже в основной группе (p = 0,02; рис. 3). У пациентов с высокой ТГ и ФВ ЛЖ <40% объем периоперационных гемотрансфузий также на 33,4% меньше, чем в группе сравнения (p = 0,05). Свежезамороженную плазму у наших больных не использовали, так как не было показаний: синдрома диссеминированного внутрисосудистого свертывания, массивной кровопотери, дефицита плазменных факторов свертывания.
Частота ранних послеоперационных инфекционных осложнений в основной группе: 4,7% (6 больных), из них 2,3% (трое) – в группе с высокой ТГ; 0,8% (один) – со средней; 1,6% (двое) – с низкой. Инфекционные осложнения в группе больных с выбором тактики гемотрансфузии, основанной на результатах гипоксической пробы, встречались на 4,6% реже, чем в группе сравнения (табл. 3). В группе сравнения гемотрансфузионную терапию назначали более чем половине – 48 больным (64%). Частота послеоперационных инфекционных осложнений в группе сравнения – 9,3% (n = 7; р >0,05).
В раннем послеоперационном периоде больные с высокой ТГ, но исходно сниженной ФВ ЛЖ требовали более длительного проведения инотропной поддержки (47±15 ч), чем пациенты группы сравнения (29±9 ч; р = 0,05). Другие показатели, такие как продолжительность ИВЛ, частота развития гастроинтестинальных осложнений, респираторные и неврологические осложнения, ренальная и полиорганная дисфункции, показатель 30-дневной летальности, сроки пребывания в отделении реанимации и стационаре, статистически не различались.
По данным ФГДС, из 128 кардиохирургических пациентов основной группы, включенных в настоящее исследо- вание, патология ЖКТ обнаружена у 68 (53,1%). Этим пациентам интраоперационно назначали «Лосек». В группе сравнения патология ЖКТ определена у 43 больных (57,3%). В раннем послеоперационном периоде исследование ЖКТ включало клиническую оценку дисфункции и ФГДС по показаниям. Клинически значимые осложнения выявлены у троих больных (4%) группы сравнения и в одном случае (1,1%) в группе высокой ТГ (р >0,05).
ОБСУЖДЕНИЕ
В обзоре тактики гемотрансфузионной терапии у критических больных P.C. Hébert и др. (2000) п р едс т авили б оль шие различия в триггерном уровне Hb, диапазон которого составлял от 50 до 120 г/л, а также показали, что 40% врачей придерживались уровня Hb в 100 г/л. На решение о трансфузии влияли: возраст, диагноз, лекарственная терапия, кровопотеря, гипоксемия, шок, лак-татацидоз и тяжесть заболевания по шкале APACHE II, определяемая при поступлении [13, 14]. В исследовании проанализирована предложенная нами тактика выбора безопасного триггерного уровня Нb и Ht в пери-операционном периоде у кардиохирургических пациентов с ишемической болезнью сердца. В ходе гипоксической пробы выявлена группа больных, имеющих высокую ТГ, которым переливание крови проводили на 49,1% реже (р = 0,02), чем в группе сравнения, где гемотрансфузию назначали при триггерном уровне Hb 90 г/л.
Известно, что наиболее безопасными критериями определения ТГ являются значения O2EI выше 30% и отсутствие роста концентрации лактата в крови выше 2,5 М/л [4]. Этим критериям соответствовало большинство пациентов основной группы (65,4%) при проведении гипоксической пробы. Определенная в ходе пробы высокая ТГ дала основания снизить триггерный уровень Hb до 70 г/л. По нашему мнению, предлагаемый подход к определению показаний к гемотрансфузии позволил проводить рациональную гемотрансфузионную терапию и снизить частоту «рутинного» назначения аллокрови благодаря дифференцированной оценке адаптационного резерва и кислородного баланса у кардиохирургических больных [3, 4].
Нам представлялось особенно важным оценить возможность «рестриктивной» тактики гемотрансфузионной терапии у больных с исходно низкой фракцией выброса левого желудочка. Традиционно принято считать, что такие пациенты после операции нуждаются в более высоком уровне Hb дл я п оддержания адекватной газотранспортной функции крови [5]. Нами обследованы 34 пациента (25,6% из группы с высокой ТГ) с ФВ ЛЖ <40%, у которых мы безопасно сократили объем гемотрансфузий, что не привело к увеличению частоты ранних послеоперационных осложнений (рис. 3; табл. 3).
Снижение триггерного уровня Hb у пациентов основной группы с ФВ ЛЖ <40% могло быть одной из причин увеличения продолжительности периода инотропной терапии до 47±15 ч (р = 0,02). Однако, в целом, это не повлияло на продолжительность ИВЛ, частоту развития гастроинтестинальных, респираторных, ренальных осложнений, характеризующих симптомокомплекс синдрома малого сердечного выброса. Последние данные A.H.M. Straten и его коллег (2010) о том, что гемотрансфузия является фактором риска синдрома низкого сердечного выброса после аортокоронарного шунтирования, согласуются с нашими клиническими результатами и показывают, что «рестриктивная» тактика назначения алло-крови у пациентов со сниженной ФВ ЛЖ оправдана [14].
Меньшая частота ранних послеоперационных инфекционных осложнений у больных основной группы, составивших 4,7%, по сравнению с 9,3% в контрольной (р = 0,05), может быть обусловлена иммуносупрессивным воздействием аллогемотрансфузий [8], поскольку антибиотикопрофилактика в группах была стандартной. Таким образом, предлагаемая нами тактика прогнозирования толерантности к периоперационной анемии и интраоперационной гемодилюции методом проведения гипоксической пробы у пациентов с ИБС перед кардиохирургической операцией в условиях ИК позволяет проводить индивидуальную гемотрансфузионную терапию, эффективна и безопасна.
ВЫВОДЫ
-
1. Метод дооперационной оценки ТГ в хирургии ИБС безопасен и снижает частоту периоперационных гемотрансфузий в группе пациентов с высокой ТГ на 48,9%.
-
2. Дооперационная высокая ТГ в хирургии ИБС позволяет достоверно снизить периоперационный триггерный уровень Hb до 70 г/л.
-
3. Толерантность к гипоксии, выявленная при проведении гипоксической пробы, и дооперационный показатель ФВ ЛЖ у пациентов с ИБС не имеют статистически значимой зависимости.
-
4. Снижение триггерного уровня гемоглобина до 70 г/л на основании дооперационной оценки ТГ в коронарной хирургии не увеличивает продолжительность ИВЛ, частоту развития гастроинтестинальных осложнений, полиорганной дисфункции и срок пребывания в отделении реанимации.
Список литературы Гипоксическая проба как метод прогнозирования гемотрансфузионной тактики и характера течения раннего послеоперационного периода в коронарной хирургии
- Зильбер А.П. Клинико-физиологические основы кровопотери и гемотрансфузии//Бескровная хирургия -итоги и перспективы развития. М., 2002. С. 22-34.
- Ищук В.А.//Украинский кардиологический журнал. 2011. http://www.ukrcardio.org/journal.php/article/608.
- Караськов А.М., Ломиворотов В.В., Сидельников С.Г. и др.//Патология кровообращения и кардиохирургия. 2001. № 1. С. 48-53.
- Караш Ю.М., Стрелков Р.Б., Чижов А.Я. Нормобарическая гипоксия в лечении, профилактике и реабилитации. М., 1988.
- Ломиворотов В.В., Бобошко В.А., Чернявский А.М. и др.//Патология кровообращения и кардиохирургия. 2011. № 2. С. 49-54.
- Слепушкин В.Д., Доев Д.П., Аддаев Д.А. Бескровная хирургия (новые направления в хирургии, анестезиологии, трансфузиологии)/Под ред. Ю.В. Таричко. М., 2003. С. 23-25.
- Справочник по анестезиологии и реаниматологии/Под ред. А.А. Бунятяна. М., 2005.
- Таричко Ю.В., Стефанов С.А., Кириленко А.С. и др.//Вестник РУДН. 2004. № 1 (25). С. 58-61.
- Шипулин В.М., Подоксенов Ю.К., Свирко Ю.С. Кровесбережение в кардиохирургии. Томск, 2010.
- Bloody easy 3: blood transfusions, blood alternatives and transfusion reations: a guide to transfusion medicine/Ed. J.L. Callum, Y. Lin, P.H. Pinkerton et al. Canada: Ontario Regional Blood Coordinating Network. 2011. 152 р.
- Emmert M.Y., Salzberg S.P., Theusinger O.M. et al.//Interactive Cardiovasc. Thorac. Surg. 2011. V. 12 (2). Р. 183-188.
- Hébert P.C., Szick Sh.//JCOM. 2000. V. 7, № 9. Р. 29-40.
- Practice Guidelines for Blood Transfusion: A Compilation from Recent Peer-Reviewed Literature/Ed. R. Cable, B. Carlson, L. Chambers. Am. National Red Cross. 2007. 60 р.
- Straten A.H., Bekker M.W., Hamad M.A. et al.//Interactive Cardiovasc. Thorac. Surg. 2010. V. 10. Р. 37-42.
- Ferraris V.A., Brown J.R., Despotis GJ. et al.//Ann. Thorac. Surg. 2011. V. 91. Р. 944-982.


