Гипоплазия дуги аорты
Автор: Синельников Юрий Семенович, Кшановская Марина Сергеевна, Горбатых Артем Викторович, Иванцов Сергей Михайлович, Прохорова Дарья Станиславовна
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Обзоры
Статья в выпуске: 3 т.17, 2013 года.
Бесплатный доступ
Агрессивный подход к устранению коарктации аорты с сопутствующей гипоплазией дуги аорты при ранней коррекции порока привел к существенному улучшению отдаленных результатов хирургической коррекции, снизив количество случаев рекоарктации аорты и персистенции артериальной гипертензии. В настоящее время существует ряд методик, позволяющих определить степень гипоплазии дуги аорты, что позволяет планировать объем вмешательства на дуге аорты у пациентов педиатрической группы. Обзор посвящен анализу современных методик определения гипоплазии дуги аорты и результатов хирургического лечения данной патологии.
Гипоплазия дуги аорты, коарктация аорты, aortic сoarctation
Короткий адрес: https://sciup.org/142140560
IDR: 142140560 | УДК: 616.132.14
Hypoplasia of the aortic arch
An aggressive surgical approach to early repair of aortic coarctation and concomitant arch hypoplasia results in considerable improvement of the long-term outcomes of surgical treatment by reducing the number of aortic re-coarctation and arterial hypertension persistence events. At present, there exist some methods of determining the degree of aortic arch hypoplasia, which allow for arch reconstruction planning. Our review focuses on the analysis of modern methods of determination of the aortic arch hypoplasia and the outcomes of surgical treatment of this disease.
Текст обзорной статьи Гипоплазия дуги аорты
Агрессивный подход к устранению коарктации аорты с сопутствующей гипоплазией дуги аорты при ранней коррекции порока привел к существенному улучшению отдаленных результатов хирургической коррекции, снизив количество случаев рекоарктации аорты и персистенции артериальной гипертензии. В настоящее время существует ряд методик, позволяющих определить степень гипоплазии дуги аорты, что позволяет планировать объем вмешательства на дуге аорты у пациентов педиатрической группы. Обзор посвящен анализу современных методик определения гипоплазии дуги аорты и результатов хирургического лечения данной патологии. Ключевые слова: гипоплазия дуги аорты; коарктация аорты.
Поступила в редколлегию 4 июня 2013 г.
М.С. Кшановская,
А.В. Горбатых,
С.М. Иванцов,
Д.С. Прохорова, 2013
Коарктация аорты относится к группе часто встречаемых заболеваний. Среди новорожденных с врожденными пороками сердца частота может достигать 20% [2]. Впервые коарктация аорты была описана в 1760 г. Morgagni, а более точное описание этого порока в 1791 г. дал Paris, он же предложил и термин «коарктация» (от франц. «coarctare» – суживать, сдавливать). Первый прижизненный диагноз коарктации аорты установил Legrand в 1835 г. Детальное описание анатомии порока сделал в 1866 г. Barie на основании патологоанатомических исследований 86 случаев. Первые успешные операции выполнены в 1945 г. в США и Швеции Crafoord и Nylin. Резекция коарктации у младенца была осуществлена W. Mustard и др. в 1953 г. Методика заключалась в создании прямого циркулярного анастомоза.
В России первая операция по устранению коарктации аорты была выполнена в ННИИПК Е.Н. Мешалкиным в 1955 г. Возможность успешного хирургического лечения коарктации аорты стала очевидной, однако отдаленные результаты были неудовлетворительными вследствие высокой частоты рецидива порока. Дальнейший путь развития хирургии в этой области сводился к разработке и усовершенствованию новых технологий анастомозирования. В последние несколько десятков лет широко обсуждается роль гипоплазии дуги аорты как одного из факторов риска развития отдаленных осложнений хирургического лечения коарктации аорты. У детей сегментарное сужение аорты нередко сочетается с гипопла- зией перешейка или дуги аорты. Сочетание коарктации аорты с гипоплазией дуги аорты у новорожденных является частой находкой, ее распространенность достигает 70%, что связано с повышенным риском рекоарктаций [15]. Впервые четкое определение гипоплазии дуги было предложено Moulaert в 1976 г., которое было основано на измерении внешнего диаметра образцов при вскрытии. В соответствии с анатомией дуга аорты делится на три сегмента: проксимальный и дистальный сегменты поперечной части дуги и перешеек аорты (рис. 1).
Согласно исследованиям Moulaert и коллег, поперечная часть дуги считается гипоп-лазированной, когда ее внешний диаметр составляет 60% или менее от восходящей аорты. Для дистального отдела дуги и перешейка аорты эти цифры составили 50% или менее и 40% или менее.
Также они выявили патогенетическую связь между сопутствующей патологией, включающей в себя лево-правый сброс, и развитием патологии дуги аорты [18].
Морфология гипоплазированной дуги Имеются сообщения, что гипоплазиро-ванный сегмент содержит меньше эластина, чем сопоставимые сегменты нормальной дуги аорты. Функциональное значение этого наблюдения являлось гипотетическим, в частности потому что оно не было соотнесено с другими потенциальными показателями роста, такими как наличие или отсутствие гладкомышечных клеток, плот- ность коллагена и соотношение этих элементов по сравнению с другими сегментами аорты [4].
В своих исследованиях M. Machii и коллеги установили, что, несмотря на то что гипоплазированный сегмент имеет абсолютно меньшее количество пластин эластина, чем нормальная дуга, относительное к диаметру содержание пластин эластина превышает значения этого показателя для нормально развитой дуги аорты [14]. Эта парадоксальная ситуация, по мнению авторов, специфична для тубулярной гипоплазии дуги аорты. Кроме того, было определено содержание α-актин-положительных клеток в медии, так как этот показатель потенциально важен, поскольку в аорте плода с увеличением гестационного возраста содержание гладкомышечных α-актин клеток увеличивается, а гладкомышечных β-актин клеток уменьшается. Фенотипические характеристики этих клеток гладкой мускулатуры важны, потому что синтетическими являются те клетки, которые способны к пролиферации и производству компонентов внеклеточного матрикса, за счет чего происходит процесс роста. Таким образом, относительно высокое содержание пластин эластина и уменьшение α-актин-позитивных клеток указывают на снижение потенциала роста. При сравнении плотности коллагена отмечено значительно большее содержание коллагена в гипоплазиро-ванном сегменте в сравнении с нативной аортой. В восходящей аорте также определяется более высокая плотность коллагена, чем в норме. Эти морфологические изменения оказывают негативное влияние на растяжимость аорты.
Патологическая физиология
У пациентов с коарктацией аорты большой круг кровообращения частично разъединен на два бассейна (верхний и нижний) с разными значениями артериального давления. Нарушения гемодинамики при этой патологии обусловлены тремя главными факторами: артериальной гипертензией верхней половины тела, относительным снижением давления в артериях нижней половины тела, разницей давления (градиентом) в верхнем и нижнем артериальных бассейнах. При успешной коррекции коарктации аорты, но не диагностированной гипоплазии дуги все эти факторы сохраняются в относительной степени.
Самый простой, с физиологической точки зрения, случай наблюдается при легкой или умеренной обструкции. В результате этого возникает проксимальная системная гипертензия, левожелудочковая гипертрофия без левожелудочковой недостаточности и градиент давления на верхних и нижних конечностях.
По мере развития коллатеральных сосудов градиент давления может уменьшаться или даже исчезнуть. Такая физиологическая обстановка хорошо переносится пациентами, может оставаться асимпто-матичной в течение многих лет, до тех пор пока не возникают осложнения, связанные с левожелудочковой гипертрофией, дегенеративными изменениями аорты или хронической системной гипертензией.
Ограниченная пропускная способность аорты на уровне стеноза создает патологический градиент систолического давления между верхним и нижним артериальными бассейнами. Вследствие этого возникает некоторая задержка крови в верхней компрессионной камере, а все ее составляющие, включая восходящую аорту и брахиоцефальные сосуды, компенсаторно расширяются. Практически все артериальные сосуды верхней половины тела находятся в состоянии постоянной гипертензии, а некоторые из них, в частности межреберные, несут кровь в обратном направлении. В связи с тем что градиент давления существует не только в период систолы, но и в период диастолы, кровь из проксимальной части аорты в дистальную перетекает непрерывно. Поскольку в аорте на месте сужения остается рестриктивное отверстие, скорость крови в этом участке повышена. В широком посткоарктационном отделе струя создает турбулентные потоки, травмирующие стенку сосуда и способные привести к развитию аневризм аорты.
В результате гипертензии возникают аневризмы в сосудах виллизиевого круга, повреждается барроре-цепторный аппарат. Гемодинамическая обструкция выводного тракта левого желудочка ведет к его гипертрофии и застойной недостаточности кровообращения. Важная гемодинамическая особенность кровотока в дистальной аорте – его демпфированный (сглаженный) характер, отсутствие систолических и диастолических колебаний. Это неестественное свойство кровотока нарушает механизмы функционирования микрососудистого русла и является главной причиной его компенсаторной и патологической перестройки.
Систолическое давление в желудочке повышается в соответствии с уровнем артериальной гипертензии, сердечный выброс обеспечивается компенсаторной гипертрофией миокарда. Сердечная недостаточность развивается не всегда, поскольку высокое диастолическое давление в восходящей аорте обеспечивает хорошее коронарное кровообращение. С возрастом мощность миокарда левого желудочка уменьшается, что приводит к его дилатации. Диастолическое давление в полости левого желудочка повышается, вследствие чего давление в левом предсердии и легочных венах также растет. Митрализа-ция порока в некоторых случаях может достигать картины функционального митрального стеноза или относительной недостаточности левого АV-клапана [1, 6].
Диагностика гипоплазии дуги
Диагностика гипоплазии дуги весьма важна у новорожденных и детей раннего возраста. При пренатальном скрининге заподозрить порок практически невозможно. В большинстве наблюдений диагностика основывается на данных двухмерной ЭхоКГ с цветовой допплерографией и МРТ исследования. По данным ЭхоКГ визуализируются все сегменты аорты, обязательно измеряют размеры всех сегментов дуги аорты. По данным допплерографии отмечается ускоренный турбулентный кровоток, снижение импульсной волны давления в нисходящей аорте.
prox
Рис. 1.
Сегмент поперечной части дуги: prox. TA – проксимальный; dist. TA – дистальный, ist. – перешеек аорты.
Рис. 2.
МСКТ ангиография аорты с контрастированием, виден гипоплази-рованный дистальный сегмент дуги аорты.
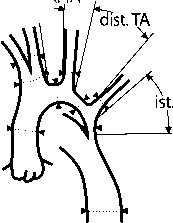
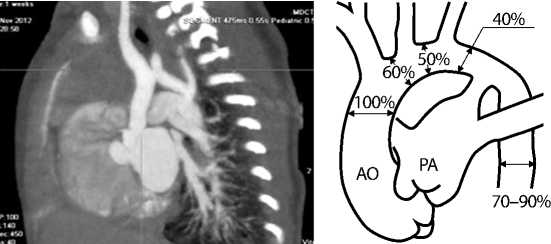
Рис. 3.
Правило, предложенное Moulaert.
Наличие антеградного кровотока в диастолу подтверждает гемодинамическую значимость обструкции аорты [25, 26]. Ультразвуковая локация позволяет получить изображения коарктации аорты с гипоплазией дуги и смежных структур, но иногда это оказывается невозможным в связи с экранированием сужения легочной тканью. Стандартным и наиболее достоверным методом для оценки анатомии дуги аорты является МРТ и МСКТ исследование (рис. 2). Благодаря данному методу возможно идентифицировать локализацию и длину сужения, состояние ветвей аортальной дуги, постстенотическую дилатацию, а после операции – обнаружить рестеноз и аневризму.
Методики определения гипоплазии дуги аорты
Метод хирургического лечения коарктации с гипоплазией дуги определяется степенью гипоплазии и анатомией дуги аорты. Впервые для определения гипоплазии дуги было предложено правило Moulaert и др. (1976), которое гласит, что диаметр проксимальной дуги должен быть больше чем 60%, диаметр дистальной дуги больше чем 50% и диаметр перешейка больше чем 40% от диаметра восходящей аорты (рис. 3). А при длине данных сегментов дуги аорты 5 мм и более принято говорить о тубулярной гипоплазии дуги аорты. Например, согласно данным критериям, тубулярная гипоплазия перешейка аорты присутствует, когда этот сегмент больше чем на 5 мм, а внешний диаметр составляет 40% или меньше, чем диаметр восходящей аорты [18]. Этого правила до настоящего времени придерживаются многие клиники и активно применяют его.
Второе правило, также активно применяемое многими клиниками, сформулировали Mee и его коллеги. Оно определяет наличие гипоплазии дуги аорты, требующей коррекции [13]. Реконструкция дуги показана, если диаметр поперечной части дуги (мм), измеренной на ЭхоКГ, в численном выражении меньше массы тела пациента (кг) плюс 1. Например, если у младенца массой 3 кг диаметр дуги аорты менее 4 мм (т. е. 3+1), дугу следует счи- тать гипоплазированной и ему показано хирургическое расширение дуги аорты каким-либо известным способом. Sakurai и др. [9] расширили это правило, сравнив размер безымянной артерии и поперечной дуги и предположив, что гипоплазия имеется, если диаметр поперечной дуги меньше, чем размер безымянной артерии (мм).
Morrow и др. [16] для измерения степени гипоплазии дуги аорты предложили использовать индекс дуги аорты. Данный параметр был разработан на основании морфометрического анализа магистральных сосудов способом двумерной эхокардиографии у 14 новорожденных с изолированной коарктацией и 14 здоровых новорожденных в возрасте менее 1 месяца. У пациентов с коарктацией поперечная дуга и перешеек были значительно меньше, чем в контрольной группе (р≤0,001). Кроме того, диаметр клапана легочной артерии и ее ствол были значительно больше у новорожденных с коарктацией, чем в группе здоровых новорожденных. Эти измерения были стандартизированы с помощью сравнительного коэффициента (индекса дуги аорты), который рассчитывался как диаметр поперечной дуги, деленный на диаметр восходящей аорты (ARCH INDEX = TA/AA). Этот показатель в контрольной группе составлял 0,76, у новорожденных с коарктацией – 0,54. Таким образом, о гипоплазии дуги аорты можно говорить в случаях, когда индекс дуги менее 0,5.
В последнее время наиболее популярно и, вероятно, наиболее точно измерение диаметра дуги и расчет отношения конкретного (определенного) сегмента дуги аорты относительно нормальных размеров, то есть определение отклонения от среднего значения возрастной нормы (Z). Дуга считается гипоплазированной при отклонении от стандартного значения – 2Z и более. Важно отметить, что стандартное отклонение может меняться в зависимости от размеров тела [7]. Для большинства измерений рекомендовано проводить расчет Z-scores относительно площади поверхности тела, а не роста или веса
|
Таблица 1 |
Автор |
Возраст |
Год |
Пациенты |
Летальность |
Рекоарктация |
||
|
Результаты резекции |
Wood et al. [28] |
<12 мес. |
2004 |
181 |
1 |
4 (2,2%) |
||
|
с расширенным |
Wright et al. [29] |
≤12 мес. |
2005 |
83 |
2 (2%) |
4 (%) |
||
|
анастомозом «конец |
Thomson et al. [27] |
<12 мес. |
2005 |
191 |
9 (5%) |
7 (4,2%) |
||
|
в конец» |
Burch et al. [5] |
<6 мес. |
2009 |
177 |
1 |
17 (9,6%) |
||
|
Kaushal et al. [13] |
<1 мес. |
2009 |
201 |
4 (2%) |
8 (4%) |
|||
|
Mc Guinness et al. [17] |
<3 мес. |
2010 |
192 |
2% |
4% |
|||
|
Таблица 2 |
Период наблю- |
|||||||
|
Результаты пластики |
Автор |
Возраст Год |
Пациенты дения, лет |
Летальность |
Рекоарктация |
|||
|
лоскутом подключичной |
Jahangiri et al. [10] |
<3 мес. 2000 |
185 |
24 |
6 (3%) |
11 (6%) |
||
|
артерии |
Kanter et al. [11] |
<3 мес. 2001 |
46 |
10 |
0 |
5 (11%) |
||
|
Pandey et al. [20] |
<1 мес. 2006 |
399 |
24 |
24,8 % |
13,6% |
|||
|
Barreiro et al. [3] |
<1 мес. 2007 |
119 |
20 |
5 (4%) |
12 (11%) |
|||
|
Таблица 3 |
Автор |
Возраст Год |
Период наблю- |
Торакотомия |
Срединная |
|||
|
Соотношение коррекции |
дения, лет |
Пациенты |
стернотомия |
|||||
|
гипоплазии дуги |
Elgamal et al. [9] |
<1 мес. 2002 |
5 |
65 |
0 |
65 (100%) |
||
|
аорты из срединной |
Kaushal et al. [12] |
<1 мес. 2009 |
16 |
201 |
157 (78%) |
44 (22%) |
||
|
стернотомии |
Sakurai et al. [23] |
<1 мес. 2012 |
20 |
288 |
237 (82%) |
51 (18%) |
||
|
Rakhra et al. [22] |
<1 мес. 2012 |
20 |
305 |
231 (76%) |
74 (24%) |
|||
в отдельности. Важно знать, что для маленьких пациентов нулевое значение может находиться в пределах двух стандартных отклонений от среднего значения. Например, полное отсутствие движения при тканевом Допплере в некоторых позициях в одной возрастной группе может давать Z-scores >–2 [8]. Petterson, проводя антропометрические измерения в большой группе детей (782 пациента), предложил специально для инфантов и детей раннего возраста таблицы расчета Z-scores для 21 отдельной сердечной структуры [21].
Современные возможности диагностики, анестезиологического, медикаментозного обеспечения, внедрение новых технологий перфузионного сопровождения обеспечили качественно новый подход в лечении пациентов с коарктацией аорты в сочетании с гипоплазией дуги. Во-первых, это ранняя (в период новорожденности) коррекция порока с агрессивным подходом к устранению гипоплазии дуги аорты, в том числе в условиях искусственного кровообращения из срединного стернотомного доступа с применением регионарной перфузии головного мозга; во-вторых, появилась возможность выхаживать пациентов с низкой массой тела, что в совокупности привело к существенному улучшению отдаленных результатов хирургической коррекции, снизилось количество случаев рекоарктации и персистенции артериальной гипертензии. При выборе метода коррекции у новорожденных и детей раннего возраста в последнее время отдается предпочтение технике расширенного анастомоза «конец в конец» или же пластике лоскутом подключичной артерии, у пациен- тов с умеренной коарктацией аорты с гипоплазией дуги методом выбора является баллонная ангиопластика.
Отдаленные результаты большинства клиник демонстрируют низкий процент рекоарктаций. Клиники, в которых предпочтительным методом хирургического лечения является выполнение «extended» анастомоза, сообщают о достаточно низком проценте рекоарктации в отдаленном периоде (табл. 1). Так, например, Kaushal и др. сообщают о 201 прооперированном за 16-летний период пациенте и выполнении резекции с расширенным анастомозом «конец в конец», 157 (78%) коррекция выполнялась из боковой торакотомии и 44 (22%) – из срединной стернотомии. Критерием для определения гипоплазии дуги аорты была формула, предложенная Mee и его сотрудниками: масса тела пациента (кг) плюс 1. Средний период наблюдения составил 5,0±4,3 года. В раннем послеоперационном периоде в течение 3 суток троим пациентам в связи с рекоарктацией была выполнена реверсивная пластика лоскутом подключичной артерии. Повторное вмешательство в связи с рекоарктацией в отдаленном периоде потребовалось восьми пациентам (4%) [13].
Несмотря на большее количество сторонников данной техники, некоторые центры для устранения гипоплазии дуги рекомендуют исключительно метод пластики лоскутом подключичной артерии, демонстрирующий хорошие результаты (табл. 2).
В исследуемой группе Johns Hopkins Medical Institutions, Baltimore [3] выявлена 4% летальность и 11% (12/114)
рекоарктации у пациентов с изолированной реверсивной пластикой. K.R. Kanter с коллегами [11] в группе пациентов с реверсивной пластикой лоскутом подключичной артерии отмечают нулевую 30-дневную летальность и 5 (11%) случаев рекоарктации. Для определения гипоплазии дуги применялись правила Moulaert [18] и Karl [12] с соавторами. Такая техника позволяет устранить гипоплазиро-ванный длинный сегмент дистальной части дуги аорты без использования искусственного кровообращения.
Совершенствование искусственного кровообращения и появление регионарной перфузии головного мозга определили новую эру в хирургии новорожденных. Появилась возможность устранения гипоплазии проксимальной и поперечной частей дуги аорты с одномоментной коррекцией сопутствующей патологии, в том числе и у детей с низкой массой тела. Последние наблюдения разных клиник отмечают более радикальный подход в лечении гипоплазии дуги аорты и устранение доступом из срединной стернотомии в условиях искусственного кровообращения (табл. 3).
Sakurai и соавторы [23], проводя анализ за 20-летний период и разделив свое исследование на два десятилетия, выявили, что в период между 1991–2000 гг. из срединного доступа было прооперировано 6%, а в период между 2001–2010 гг. – 36%. При этом в данной группе отмечался более низкий процент рекоарктаций (4%) в сравнении с группой, в которой коррекция порока выполнялась из боковой торакотомии: 16% в течение 1991–2000 гг. и 5% в период 2001–2010 гг. Таким образом, они определили, что коррекция коарктации с гипоплазией дуги доступом из срединной стернотомии значительно снижает риск рекоарктации, и считают это приемлемым даже у пациентов с пограничными размерами дуги. Для определения степени гипоплазии дуги авторы применяли предложенную ими формулу, сравнивая размер безымянной артерии и поперечной дуги, или же формулу, предложенную Mee и коллегами [13].
Группа ученых из Royal Children’s Hospital, Melbourne [22] в своем долгосрочном наблюдении также выявили, что техника «конец в бок», выполненная из срединного доступа, может быть предложена большинству пациентов с гипоплазией дуги аорты, так как процент рекоарктаций в данной группе был меньше, чем в группе, где коррекция порока выполнялась из боковой торакотомии методом расширенного анастомоза (свобода от рекоарктаций 92 против 61% за 10-летний период, p<0,001). Для определения степени гипоплазии дуги авторы использовали расчеты от среднего отклонения (Z-scores). Таким образом, анализируя результаты различных клиник, можно сделать вывод о том, что вопрос об «идеальной» технике хирургического лечения у детей гипоплазии дуги аорты остается открытым. Вероятно, при выборе метода хирургического лечения в каждом случае не должно быть шаблона и необходимо руководствоваться конкретной анатомо-гемодинамической ситуацией, учитывая все возможные варианты и предусматривая их последствия. В техническом выполнении выбранного способа лучше придерживаться проверенных стандартов, так как в условиях ограниченного времени безопасного пережатия аорты творческие поиски могут стать серьезной проблемой на пути надежности.
Список литературы Гипоплазия дуги аорты
- Дыкуха С.Е. и др.//Клин. хирургия. 1997. № 7. С. 77-78.
- Матчин Ю.Г., Козлов С.Г., Лякишев А.А. и др.//Кардиология. 1991. № 12. C. 105-106.
- Barreiro C.J., Ellison T.A., Williams J.A. et al.//Eur. J. Cardiothorac. Surg. 2007. V. 31. P. 649-653.
- Becker A.E.//Int. J. Cardiol. 1988. V. 20. P. 247-255.
- Burch P. et al.//J. Thorac. Cardiovasc. Surg. 2009. V. 138. P. 547-552.
- Castaneda A.R., Jonas R.A. et al.//Cardiac. Surgery Neonate Infant. 1994. V. 21. P. 337-339.
- Chubb H. et al.//Ann. Pediatric Cardiology. 2012. V. 5. P. 179-184.
- Eidem B.W., McMahon C.J., Cohen R.R. et al.//J. Am. Soc. Echocardiogr. 2004. V. 17. P. 212-221.
- Elgamal M.A. et al.//Ann. Thorac. Surg. 2002. V. 73. P. 1267-1273.
- Jahangiri M., Shinebourne E.A., Zurakowski D. et al.//J. Thorac. Cardiovasc. Surg. 2000. V. 120. P. 224-229.
- Kanter K.R. et al.//Ann. Thorac. Surg. 2001. V. 71. P. 1530-1536.
- Karl T.R., Sano B., Brawn W., Mee R.B.//J. Thorac. Cardiovasc. Surg. 1992. V. 104. P. 688-695.
- Kaushal S. et al.//Ann. Thorac. Surg. 2009. V. 88. P. 1932-1938.
- Machii M., Becket A.E.//Ann. Thorac. Surg. 1997. V. 64. P. 516-520.
- Mc Elhinney D.B., Yang S.G., Hogarty A.N. et al.//J. Thorac. Cardiovasc. Surg. 2001. V. 122. P. 883-890.
- Morrow W.R., Huhta J.C., Murphy D.J.Jr.//J. Am. Coll. Cardiol. 1986. V. 8. P. 616-620.
- Mc Guinness J.G., Elhassan Y., Lee S.Y. et al.//Ann. Thoracic. Surg, 2010. V. 90. P. 2023-2027.
- Moulaert A.J., Bruins C.C., Oppenheimer-Dekker A.//Circulation. 1976. V. 53. P. 1011-1015.
- Nielsen J.C., Powell A.J., Gauvreau K. et al.//Circulation. 2005. V. 111. P. 622-628.
- Pandey R., Jackson M., Ajab S. et al.//Ann. Thorac. Surg. 2006. V. 81. P. 1420-1428.
- Pettersen M.D., Du W., Skeens M.E.//J. Am. Soc. Echocardiogr. 2008. V. 21 (8). P. 922-934.
- Rakhra S.S., Lee M., Iyengar A.J. et al.//Interact. Cardio Vasc. Thorac. Surg. 2012. V. 1. P. 301.
- Sakurai T., Stickley J., Stumper O. et al.//Interact. Cardio Vasc. Thorac. Surg. 2012. V. 15 (5). P. 865-870.
- Sluysmans T., Colan S.D.//J. Appl. Physiol. 2005. V. 99. P. 445-457.
- Shaddy R.E. et al.//Circulation. 1986. V. 73. P. 82.
- Simpson I.A., Sahn D.J. et al.//Circulation. 1988. V. 77. P. 736.
- Thomson J.D., Mulpur A. et al.//Heart. 2006. V. 92. P. 90-94.
- Wood A.E., Javadpour H., Duff D. et al.//Ann. Thorac. Surg. 2004. V. 77. P. 1353-1357.
- Wright G.E., Nowak C.A., Goldberg C.S. et al.//Ann. Thorac. Surg. 2005. V. 80. P. 1453-1459.


