Гистологические проявления остеоартроза запястья в зависимости от давности и тяжести заболевания
Автор: Щудло Н.А., Ступина Т.А., Куттыгул К.Ш.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 4 т.31, 2025 года.
Бесплатный доступ
Введение. Возможности медицинской визуализации изменений суставного хряща и субхондральной кости при остеоартрозе запястья ограничены, гистологическим исследованиям посвящены единичные публикации. Цель работы — определение взаимосвязей гистологических оценок остеоартроза запястья с давностью и стадией SLAC / SNAC синдрома. Материал и методы. Исследован операционный материал 12 пациентов, которым выполнены резекция проксимального ряда костей запястья либо удаление ладьевидной кости с межзапястным артродезом. У девяти пациентов давность заболевания — менее четырёх лет, у трёх — от 10 до 22 лет. Стадия I SLAC / SNAC синдрома выявлена у двух пациентов, стадия II — у шести, стадия III — у четырёх. Изменения хряща оценены по международной шкале OARSI, распространённость некроза субхондральной кости определена полуколичественно (от 0 до 3 баллов) в 3–10 полях зрения микроскопа от каждого пациента. Результаты. При давности заболевания менее четырех лет (n = 9) оценка OARSI варьировала от 1–2 до 5, при давности от 10 до 22 лет — от 3–4 до 4–5. Оценка остеонекроза в сравниваемых подгруппах составила 3 (2÷3)(0–3) и 3 (2÷3)(2–3), p = 0,11. При SLAC / SNAC стадии I вариативность оценок OARSI — от 1–2 до 4, при стадии II — от 2 до 4–5, при стадии III — от 3–4 до 5. Оценка остеонекроза в сравниваемых подгруппах была 2 (1÷2)(1–3), 3 (2÷3)(1–3) и 3 (2÷3)(0-3) (P1-2 = 0,03; P2-3 = 0,62; P1-3 = 0,02). Обсуждение. SLAC / SNAC синдром может иметь два типа течения, — прогрессирующий и стагнирующий. При втором типе заболевание долго протекает бессимптомно. Независимо от причины SLAC / SNAC синдрома у всех пациентов остеоартроз запястья сопровождается необратимым остеонекрозом субхондральной кости и костного мозга, что, вероятно, отражает степень острых либо хронических повреждений питающих кость сосудов. Заключение. При общей тенденции бóльших дегенеративных изменений суставного хряща при большей стадии SLAC / SNAC синдрома их гистологическая оценка межиндивидуально варьирует на каждой стадии. Остеонекроз субхондральной кости более распространён при SLAC / SNAC стадий II–III, чем стадии I.
SLAC / SNAC синдром, остеоартроз запястья, хрящ, субхондральная кость, гистология
Короткий адрес: https://sciup.org/142245420
IDR: 142245420 | УДК: 616.727.4-007.248-076:612.086 | DOI: 10.18019/1028-4427-2025-31-4-444-451
Histological manifestations of wrist osteoarthritis and their dependence on the duration and severity of the disease
Introduction The possibilities of medical visualization of changes in the articular cartilage and subchondral bone in wrist osteoarthritis are limited. There are few studies devoted to its histological manifestations. The purpose f the work was to determine the relationships between histological features of wrist osteoarthritis and the duration and stage of SLAC / SNAC syndrome. Material and methods The surgical material of 12 patients who underwent resection of the proximal row of wrist bones or removal of the scaphoid bone and intercarpal arthrodesis was studied. In nine patients, the duration of the disease was shorter than four years and in three it was from 10 to 22 years. Stage I SLAC / SNAC syndrome was detected in two patients, stage II — in six, stage III — in four. Cartilage changes were assessed using the international OARSI scale, the prevalence of subchondral bone necrosis was determined semi-quantitatively (from 0 to 3 points) in 3–10 fields of microscopic views of the from each patient. Results The OARSI score varied from 1–2 to 5 points if the duration of the disease was shorter than four years and from 3–4 to 4–5 points if it continued from 10 to 22 years. The osteonecrosis score in the compared subgroups was 3 (2÷3)(0–3) and 3 (2÷3)(2–3), p = 0.11. In SLAC / SNAC stage I, the OARSI score variability ranges from 1–2 to 4, in stage II — from 2 to 4–5, in stage III — from 3–4 to 5. The osteonecrosis score in the compared subgroups was 2 (1÷2)(1–3), 3 (2÷3)(1–3), and 3 (2÷3)(0–3) (P1-2 = 0.03; P2-3 = 0.62; P1-3 = 0.02). Discussion The SLAC / SNAC syndrome can be of two types, progressive and stagnant. In the second type, the disease is asymptomatic for a long time. Regardless of the cause of SLAC / SNAC syndrome, all patients with wrist osteoarthritis experience irreversible osteonecrosis of the subchondral bone and bone marrow, which probably reflects the degree of acute or chronic damage to the vessels that feed the bone. Conclusion With a general tendency for greater degenerative changes in the articular cartilage at a higher stage of SLAC / SNAC syndrome, their histological manifestations vary between individuals at each stage. Osteonecrosis of the subchondral bone is more common in SLAC / SNAC stages II–III than in stage I.
Текст научной статьи Гистологические проявления остеоартроза запястья в зависимости от давности и тяжести заболевания
Запястье состоит из восьми небольших костей и множества сочленений между ними, которые легко травмируются, и является компонентом одного из самых сложных суставов человеческого тела, — лучезапястного, обеспечивающего разнонаправленные движения кисти относительно предплечья [1].
Наиболее частые повреждения, которые приводят к посттравматическому остеоартрозу запястья, — разрывы ладьевидно-полулунной связки либо несращения переломов ладьевидной кости с последующим развитием прогрессирующего коллапса запястья, соответственно SLAC и SNAC синдромов ( англ .: scapholunate advanced collapse & scaphoid nonunion advanced collapse) [2]. Как свидетельствуют обзоры литературы, повреждения ладьевидно-полулунной связки нередко сочетаются с переломами лучевой или ладьевидной костей либо другими травмами запястья [3]. Повреждения ладьевидно-полулунной связки могут возникать вторично при кристаллических артропатиях [4]. Наряду с травмами нелеченые идиопатические аваскулярные остеонекрозы полулунной и ладьевидной костей (болезнь Кинбека и болезнь Прайзера) также могут привести к прогрессирующему коллапсу и остеоартрозу запястья [5].
Общий фактор развития SLAC и SNAC синдромов — нестабильность ладьевидной кости. Поэтому они проявляются схожей и предсказуемой последовательностью дегенеративных изменений суставов запястья [6–10], значимых клинически, так как вызывают боли при нагрузках и в покое, уменьшение объёма движений и силы кистевого схвата. Диагноз и прогрессирование заболевания уточняют рентгенологически, методами компьютерной и магнитно-резонансной томографии [6, 11], а также при артроскопии [12].
Гистологическим характеристикам остеоартроза запястья посвящены единичные исследования, в которых установлены значимые корреляционные связи деструктивно-дистрофических изменений псевдоартрозной поверхности ладьевидной кости с давностью травмы, гипертрофии ворсинок синовиального слоя капсулы кистевого сустава с выраженностью контрактуры, остеонекрозов в ладьевидной кости с интенсивностью боли [13]. В последние годы боль при остеоартрозе ассоциируется с повреждениями костного мозга субхондральной кости [14]. Это даёт основание для продолжения исследований гистологических характеристик остеоартроза запястья, что необходимо для понимания патогенеза заболевания и разработки тактики лечения.
Цель работы — определение взаимосвязей гистологических оценок остеоартроза запястья с давностью и стадией SLAC / SNAC синдрома.
МАТЕРИАЛЫ И МЕТОДЫ
Исследован операционный материал от 12 пациентов (10 мужчин и две женщины), прооперированных в 2023–2024 гг. по поводу остеоартроза запястья. Пациентам выполнены резекция проксимального ряда костей запястья либо четырёхсторонний артродез.
Возраст пациентов на момент операции варьировал от 20 до 65 лет (41,50 ± 15,88), возраст в момент травмы или появления первых симптомов заболевания — от 17 до 64 лет (35,86 ± 17,04).
Травмы в анамнезе были у 10 (83 %) пациентов: у восьми — низкоэнергетическая (падение c высоты роста с упором на кисть), у двух — высокоэнергетическая (ДТП у одного и удар мячом в спорте у другого), два пациента травму отрицали. Давность с момента травмы либо появления болевого синдрома в случае отрицания травмы варьировала от восьми месяцев до 22 лет (5,64 ± 7,6).
У четырёх (33 %) пациентов диагносцирован SLAC синдром, у остальных восьми — SNAC синдром. По данным лучевых медов исследования, остеоартроз первой стадии по классификациям Vender et al., Watson and Ballet [7, 15] выявлен у двух пациентов, второй — у шести и третьей — у четырёх. На основании рентгенометрических показателей у 10 (83 %) пациентов выявлена деформация DISI (нестабильность вставочного интеркалярного сегмента).
Исследование проведено в соответствии с этическими стандартами Хельсинской декларации 2013 г. и одобрено этическим Комитетом учреждения (протокол от 07.10.2022 № 2 (72)).
Операционный материал (удалённые полулунная и/или ладьевидная кость либо фрагменты последней) подвергали фиксации в растворе 10 % нейтрального формалина. После декальцинации в смеси растворов муравьиной и соляной кислот материал осуществляли гистологическую проводку в аппарате для вакуумной проводки тканей HISTOSAFETM INFILTRATM (ООО «ЭргоПродакшн», Россия).
Гистологические микропрепараты (парафиновые срезы изготовлены на микротоме НМ 450 Thermo Scientific (США) и окрашены гематокислином и эозином либо трёхцветным методом Массона). Для получения цифровых изображений микропрепаратов использовали микроскоп AxioScope.A1 в комплекте с камерой AxioCam ICc 5 и ПО Zenblue (CarlZeissMicroImagingGmbH, Германия). Изменения суставного хряща оценены по международной шкале OARSI [16] слепым методом.
Распространённость некроза субхондральной кости определена полуколичественно (от 0 до 3 баллов) в 3–10 полях зрения от каждого пациента (всего 78 полей) при инструментальном увеличении 400×: 0 баллов — нет признаков некроза; 1 — охвачены признаками гибели остеоцитов до трети площади поля зрения; 2 — до двух третей площади поля зрения; 3 — до трёх третей (100 %) поля зрения (демонстрируют некротические изменения).
Для статистической обработки количественных данных использовали приложение к программе Excel Attestat, версия 9.3.1 (разработчик И.П. Гайдышев, сертификат о регистрации в Роспатенте № 2002611109). Учитывая малую численность сравниваемых подгрупп пациентов, гипотезы о различиях проверяли с помощью непараметрического критерия Манна – Уитни.
РЕЗУЛЬТАТЫ
У большинства пациентов ( n = 9) давность заболевания не превышала четырех лет, а у трех составляла от 10 до 22 лет (табл. 1). При давности заболевания менее 4 лет ( n = 9) оценка суставного хряща по шкале OARSI варьировала от 1–2 до 5, при давности от 10 до 22 лет — от 3–4 до 4–5. При SLAC / SNAC стадии I вариативность оценок OARSI от 1–2 до 4, при SLAC / SNAC стадии II — от 2 до 4–5, при SLAC / SNAC стадии III — от 3–4 до 5. У всех пациентов выявлен распространённый некроз субхондральной кости, который занимал от 56,67 % до 100 % тестовой площади.
Таблица 1
Основные характеристики пациентов и операционного материала
|
№ |
Возраст, лет |
Давность травмы, лет |
Рентгенологическая стадия SLAC / SNAC |
Оценка суставного хряща по OARSI |
Остеонекроз субхондральной кости (% тестовой площади) |
|
1. |
48 |
2,33 |
SNAC II |
4 |
100,00 |
|
2. |
23 |
2 |
SLAC II Некроз полулунной кости |
4–5 |
75,00 |
|
3. |
41 |
20 |
SNAC II |
4 |
93,33 |
|
4. |
61 |
1,5 |
SLAC III |
4–5 |
93,33 |
|
5. |
41 |
10 |
SNAC III |
3–4 |
86,67 |
|
6. |
51 |
22 |
SNAC III |
4–5 |
100,00 |
|
7. |
20 |
2,25 |
SNAC I |
1–2 |
56,67 |
|
8. |
31 |
0,75 |
SLAC II |
2–3 |
76,67 |
|
9. |
36 |
1,17 |
SNAC II |
2 |
89,00 |
|
10. |
21 |
3,6 |
SNAC I Асептический некроз дистального полюса ладьевидной кости |
4 |
77,67 |
|
11. |
60 |
1,42 |
SLAC II |
2 |
100,00 |
|
12. |
65 |
0,67 |
SLAC III |
5 |
70,83 |
Наименьшая степень повреждений суставного хряща (степень 1–2) была у одного пациента (рис. 1). Суставная поверхность не разволокнена, в поверхностной зоне определяли деструктивно измененные хондроциты, пустые клеточные лакуны. Базофильная линия не определялась, местами отсутствовала субхондральная костная пластинка, отмечены участки проникновения костно-мозгового паннуса (рис. 1, а). В субхондральной зоне нарушена целостность трабекулярной сети, выражен остеолизис, встречались костные трабекулы с мелкими интерстициальными остеонекрозами (рис. 1, б), отмечены признаки репаративного остеогенеза, — остеобласты на поверхности костных трабекул (рис. 1, в). В межтрабекулярных промежутках преобладали жировой костный мозг, большие скопления сладжи-рованных эритроцитов и эритроциты вне сосудов (рис. 1, в).
Повреждения хряща степени 3 по OARSI определены также у одного пациента (рис. 2). Суставной хрящ присутствовал на всем протяжении, поверхностная зона разволокнена, выражено отслоение мелких фрагментов хряща, встречались участки с синовиальным паннусом (рис. 2, а). Толщина кальцифицированного хряща увеличена и составляла 1/2–2/3 от некальцифицированного хряща. В субхондральной зоне нарушена целостность трабекулярной сети, трабекулы — с мелкими интерстициальными остеонекрозами (рис. 2, б), отмечены признаки репаративного остеогенеза (рис. 2, в). Фиброз костного мозга, в сосудах — сладжированные эритроциты.
Повреждения хряща 3–4 степени по OARSI выявлены у четырех пациентов (двое с давностью заболевания менее четырёх лет и двое — из группы с давностью от 10 до 22 лет). На всем протяжении выражено отслоение поверхностной и промежуточной зон хряща, так что на большом протяжении суставная поверхность представлена глубокой зоной (рис. 3, а). Выявлены участки замещения глубокой зоны хряща костной тканью и новообразование базофильного раздела (рис. 3, б). Выраженный некроз субхондральной кости сопровождался гладкой резорбцией, расслоением основного вещества трабекул по линиям склеивания. Признаки репаративного остеогенеза не выражены. Встречались однокамерные и двухкамерные кисты (рис. 3, в).
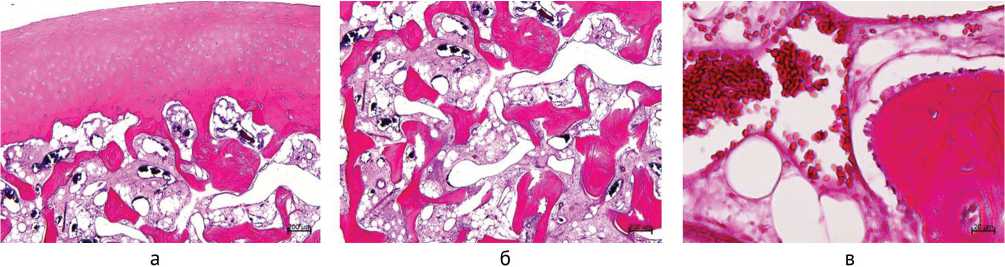
Рис. 1. Фото микропрепаратов пациента Л. 20 лет (SNAC I, давность 2,3 года, OARSI 1–2): а — общий вид суставного хряща; б — субхондральная зона; в — сладжированные эритроциты, остеобласты на поверхности костной трабекулы. Окраска гематоксилином и эозином. Увеличение ×40 (а, б), ×400 (в)
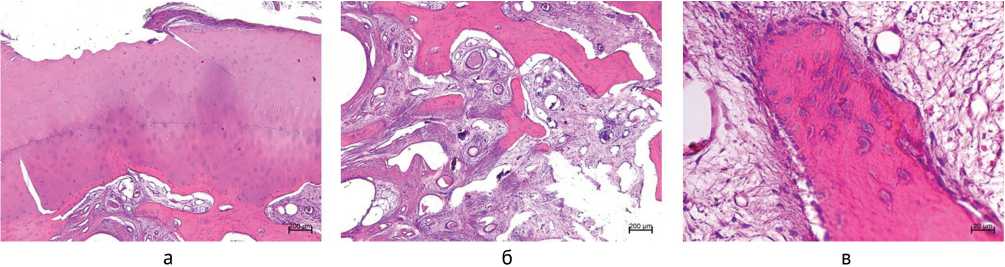
Рис. 2. Микрофото препаратов пациента П. 31 года (SLAC II, давность 0,75 года, OARSI 3): а — очаг разволокнения поверхностной зоны, синовиальный паннус; б — трабекулы с интерстициальными остеонекрозами, фиброз костного мозга; в — новообразованная трабекула поверхность, которой выстлана активными остеобластами. Окраска гематоксилином и эозином. Увеличение ×40 (а, б), ×400 (в)
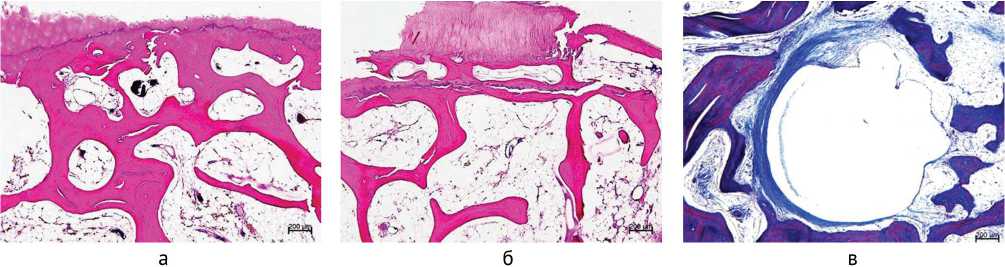
Рис. 3. Микрофото препаратов пациентки И., 48 лет, (SNAC II, давность 2,33 года, OARSI 3–4): а — суставная поверхность представлена разволокненной глубокой зоной хряща; б — продвижение процесса костеобразования по направлению к суставной поверхности, новообразование базофильного раздела; в — субхондральная зона, киста с толстой фиброзной капсулой. Окраска гематоксилином и эозином (а, б) и трихромным методом по Массону (в). Увеличение ×40
Степень повреждения хряща 4–5 выявлена также у четырёх пациентов (трое с давностью заболевания до четырёх лет, один — с давностью от 10 до 22 лет ). Суставной хрящ местами разволокнен, местами покрыт синовиальным паннусом, в очагах разволокнения гигантские изогенные группы хондроцитов (рис. 4, а). Выявлены участи замещения глубокой и промежуточной зон со стороны субхондральной зоны костномозговым паннусом, новообразование субхондральной костной пластинки сверху покрытой соединительной тканью (рис. 4, б). На большом протяжении – тонкий слой фиброзной ткани. Выраженный остеонекроз субхондральной кости, разрежение костных трабекул, признаки остеокла-стической резорбции, кисты. Признаки репаративного остеогенеза слабо выражены.
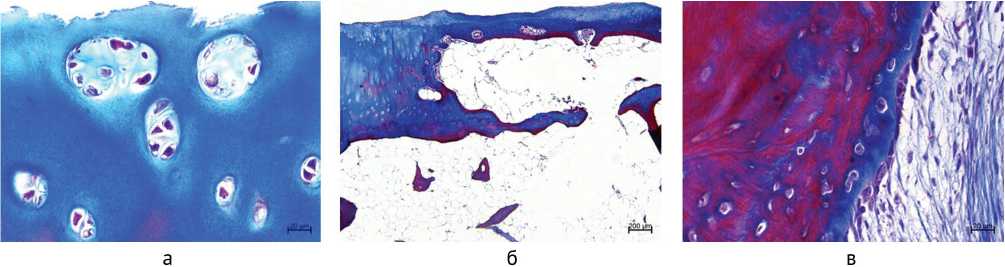
Рис. 4. Микрофото препаратов пациентки Д., 61 года, (SLAC III, давность 1,5 года, OARSI 4–5: а — многочленные изогенные группы клеток, б — замещение суставного хряща костно-мозговым паннусом, новообразование базофильного раздела, в — активные остеобласты на поверхности субхондральной костной пластинки, фиброз костного мозга. Окраска трихромным методом по Массону. Увеличение ×400 (а, в), ×40 (в)
Степень повреждения суставного хряща 5 выявлена у одного пациента с давностью заболевания менее года (рис. 5), который отрицал травму. Суставная поверхность представлена оголенной костной тканью, так как суставной хрящ отсутствовал (рис. 5, а). Выраженный остеонекроз, остеолизис, расслоение основного вещества костных трабекул (рис. 5, б). В межтрабекулярных промежутках некротический детрит. Отмечены очаги репаративного остеогенеза, новообразованные трабекулы и протяжённые участки фиброзного замещения костного мозга (рис. 5, в).
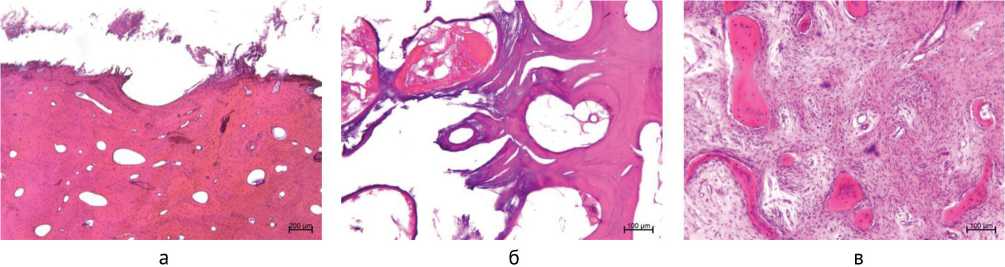
Рис. 5. Микрофото препаратов пациента К., 65 лет, (SLAC III, давность 0,67 года, OARSI 5): а — суставная поверхность представлена субхондральной костью, б — остеолизис, расслоение основного вещества костных трабекул, в – очаги репаративного остеогенеза. Окраска гематоксилином и эозином. Увеличение ×40 (а), ×100 (б, в)
Оценка остеонекроза в баллах варьировала от 0 до 3 у пациентов с давностью до четырёх лет и от 2 до 3 — при давности от 10 до 22 лет, отличия статистически незначимы (табл. 2). Медиана оценки остеонекроза меньше при SLAC / SNAC стадии I по сравнению со стадиями II и III на уровне значимости 0,05 (табл. 3).
Таблица 2
Оценка остеонекроза в баллах зависимости от давности заболевания
|
Давность SLAC / SNAC синдрома |
Оценка остеонекроза в баллах Me (Q1÷Q3) (min–max) |
p |
|
Менее 4 лет ( n = 9) |
3 (2÷3) (0–3) |
0,11 |
|
От 10 до 22 лет ( n = 3) |
3 (2÷3) (2–3) |
Таблица 3
Оценка остеонекроза в зависимости от стадии остеоартроза
|
Стадия остеоартроза |
Оценка остеонекроза в баллах Me (Q1÷Q3) (min–max) |
p |
|
SLAC / SNAC I ( n = 2) |
2 (1÷2) (1–3) |
P 1–2 = 0,03* |
|
SLAC / SNAC II ( n = 6) |
3 (2÷3) (1–3) |
P 2–3 = 0,62 |
|
SLAC / SNAC III ( n = 4) |
3 (2÷3) (0–3) |
P 1–3 = 0,02* |
Примечание : * — p < 0,05 по критерию Манна – Уитни.
ОБСУЖДЕНИЕ
В выполненном исследовании впервые проведена оценка повреждений суставного хряща по международной шкале OARSI и полуколичественная оценка распространённости некроза субхондральной кости при остеоартрозе запястья, вызванном развитием SLAC / SNAC синдромов.
Гиалиновый хрящ костей запястья в несколько раз тоньше, чем хрящ крупных суставов, однако он не является нагружаемым [17]. Поэтому развитию остеоартроза запястья в большинстве случаев предшествует острая травма, в том числе в исследованной нами группе пациентов. Хроническая травматизация запястья при ручном труде не рассматривается как доказанный фактор остеоартроза запястья [18], однако повторяющиеся микротравмы запястья у элитных спортсменов считается значимым этиологическим фактором [19]. Другие авторы описали расширение ладьевидно-полулунного промежутка нетравматической этиологии, которое с возрастом вызывает прогрессирующую нестабильность и остеоартроз запястья [20]. Однако некоторые пациенты могут не помнить эпизода полученной травмы.
Как показало выполненное исследование, независимо от анамнеза в большинстве случаев дегенерация хряща суставных поверхностей костей запястья происходила в сроки менее четырёх лет, а у некоторых — меньше года. При этом некроз субхондральной кости выявляется у всех пациентов и является необратимым, поскольку ни в одном случае он не был отнесён к классу 1, при котором ишемические события не нарушают непрерывности костных трабекул, несмотря на гибель остеоцитов [21]. Нарушение непрерывности, лизис и разрежение костных трабекул были выражены во всех исследованных случаях, что отражает сущность и последствия коллапса запястья. В межтрабекулярных пространствах располагался преимущественно жировой костный мозг, у большинства пациентов выявлены участки его фиброзного замещения и кистозного перерождения.
Полученные данные дают возможность предположить ограниченные возможности органосохраняющих и хондропластических операций при остеоартрозе запястья. Как свидетельствуют данные мировой литературы, радиочастотная хондропластика при артроскопии запястья создаёт высокий риск для выживания хондроцитов [22]. Для купирования хронической посттравматической боли в запястье давно рекомендован способ стимуляции костного мозга, — артроскопический дриллинг, но распространения в клинической практике методика не получила [23]. У одного пациента после безуспешного консервативного лечения остеоартроза запястья применяли ювенильные хрящевые аллографты [24], остеохондральные ауто- и аллотрансплантаты для лечения хрящевых дефектов запястья использовали в небольших группах из двух и трёх пациентов [25, 26], трансплантаты рёберного хряща в качестве спейсера — при лечении пациентов с болезнью Кинбека [27, 28]. Информация об эффективности перечисленных методов на сегодняшний день явно недостаточна.
Золотым стандартом хирургического лечения SLAC / SNAC синдрома на сегодняшний день остаются «спасительные» операции (резекция проксимального ряда костей запястья и четырёхсторонний артродез), которые позволяют купировать болевой синдром и сохранить приемлемые функциональные возможности кисти [29, 30], однако остаётся нерешённой проблема оптимального лечения молодых пациентов с начальными проявлениями остеоартроза запястья.
Для разработки технологий лечения представляется перспективным дальнейшее изучение клиникопатоморфологических вариантов течения остеоартроза запястья в зависимости от механизма травмы, видов активности, пола и возраста пациентов. Полученные данные указывают на то, что SLAC / SNAC синдром может иметь два типа течения, — прогрессирующий и стагнирующий, при втором типе заболевание долго протекает бессимптомно. Независимо от причины SLAC / SNAC синдрома (разрыв ладьевидно-полулунной связки, перелом ладьевидной кости или идиопатический некроз ладьевидной или полулунной костей) у всех пациентов остеоартроз запястья сопровождается необратимым остеонекрозом субхондральной кости и костного мозга, что, вероятно, отражает степень острых либо хронических повреждений питающих кость сосудов.
ЗАКЛЮЧЕНИЕ
При общей тенденции бóльших дегенеративных изменений суставного хряща при бОльшей стадии SLAC / SNAC синдрома их гистологическая оценка межиндивидуально варьирует на каждой стадии. Остеонекроз субхондральной кости более распространён при SLAC / SNAC синдроме стадий II–III, чем стадии I.


