Глубокая артерия бедра - надежда хирурга, спасение больного
Автор: Султанян Т.Л., Малхасян А.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Бариатрическая хирургия
Статья в выпуске: 1 (79), 2022 года.
Бесплатный доступ
Введение. Одной из самых сложных проблем облитерирующих заболеваний брюшной аорты и артерий н/к является варианты множественных и диффузных изменений сосудов. Целью исследования явилось стремление к улучшению результатов хирургического лечения больных с облитерирующим атеросклерозом путем обоснованного использования глубокой бедренной артерии.Материалы и методы исследования. В настоящей работе представлен опыт хирургического лечения в отделении сосудистой хирургии университетской клиники Институт хирургии Микаелян'' в период с 2008 по 2020гг. Реваскуляризация с применением пластики ГБА у 121 больного (118мужчин и 3 женщины).Результаты лечения. При шунтирующих операциях на аорто-подвздошно-бедренном сегменте применение ГБА в качестве единственного воспринимающего коллектора в 87,19 % случаев позволяет достичь улучшения клинического статуса в ближайшем послеоперационном периоде (в 92,6 % при ГПИД
Глубокая бедренная артерия, эндартерэктомия, шунтирование, реваскуляризация
Короткий адрес: https://sciup.org/142234536
IDR: 142234536 | УДК: 616.13-004.6-007.271-031.59-02-089
Te deep artery of the thigh is the surgeon's hope, the patient's salvation
Introduction. One of the most difcult problems of obliterating diseases of the abdominal aorta and arteries n/a is the variants of multiple and di use vascular changes. Te aim of the study was to improve the results of surgical treatment of patients with obliterating atherosclerosis by reasonable use of the deep femoral artery.Materials and methods of research. Tis paper presents the experience of surgical treatment of 121 patients with the use of HBA plastic surgery (118 men and 3 women) who underwent revascularization in the Department of Vascular Surgery of the University clinic Mikaelian Institute of Surgery" in the period from 2008 to 2020.Results. In bypass operations on the aorto-iliac-femoral segment, the use of HBA as the only receptive collector in 87.19% of cases makes it possible to achieve an improvement in the clinical status in the immediate postoperative period (in 92.6% with GPID
Текст научной статьи Глубокая артерия бедра - надежда хирурга, спасение больного
Одной из самых сложных проблем облитерирующих заболеваний брюшной аорты и артерий н/к являются варианты множественных и диффузных изменений сосудов, которые, как правило, приводят к хронической ишемии, угрожающей потерей конечности. Ведущую роль в лечении этих больных играет хирургическая реваскуляризация. При этом, в виду разнообразия поражений, каждый пациент нуждается в индивидуальном подходе [9].
С другой стороны, на наш взгляд, необходимым является выделение узловых зон, коррекция которых обеспечит достижение достаточного объема кровообращения. Чрезвычайно важным является то обстоятельство, что зачастую эти больные имеют клиническое проявление системного поражения артериального русла атеросклерозом (ИБС, ИБМ, поражение висцеральных ветвей) [10]. Сопутствующие заболевания, и особенно сахарный диабет, в свою очередь снижают резервные возможности организма [5].
Таким образом, актуальным является также поиск путей снижения объема инвазивности при сохранении достаточности необходимой реваскуляризации [1, 2, 3, 4].
Не секрет, что глубокая артерия бедра является своеобразном резервным коллектором, способным сохранить определенный кровоток (через коллатеральное кровообращение) при блокировании патологическим процессом подвздошного и бедренного сегментов [6, 12, 13]. Попытки хирургического увеличения объема кровотока в этой системе всегда были в поле зрения ангиохирургов, с 1961г., когда были выполнены первые реконструкции ГБА, разработаны и предложены различные варианты профундолластики [14, 11]. Процесс сдерживался рядом обстоятельств: необходимость расширений эндартерэктомии в ряде случаев, малым диаметром ГБА; неоцененность возможности постепенного развития коллатералей; неизученность целесообразности выполнения процедуры при язвенно-некротических поражения тканей конечностей и т.п. [12, 8]. Для определения функциональных возможности коллатеральной системы и прогнозирования результатов реваскуляризации через систему ГБА еще 1980г. был предложен глубоко-бедренно-подколенный индекс давления (ГПИД).
Он вычисляется по формуле: ГПИД=(АДВК–АДНК)/ АДВК, где
АД – систолическое артериальное давление.
ВК – регионарное систолическое давление на артериях выше колена.
НК – регионарное систолическое давление в артериях ниже колена.
design of the article, selection of literature.
Значение ГЛИД выше 0,4 указывает на возрастания резистентности системы окольного кровообращения и слабые функциональные резервы ГБА [8].
По мнению ряда авторов, существует четкая коррелляция между значением ГПИД и результатами реваскуляризации через систему ГБА: при значениях выше 0,4 рассчитывать на успех не приходится. Другие исследователи полагают, что результаты включения в кровоток ГБА находятся в прямой зависимости от состояния подколенной артерии и артерий голени. Нам представляется, что возвращение к обсуждению этих вопросов (с учетом открывающихся новых возможностей) может показаться интересными.
Целью исследования явилось стремление к улучшению результатов хирургического лечения больных с облитерирующим атеросклерозом путем обоснованного использования глубокой бедренной артерии в качестве воспринимающего коллектора в реваскуляризации нижних конечностей.
Для этого были поставлены следующие задачи:
-
1) провести анализ результатов шунтирующих операций на аорто-подзвдошно-бедренном сегменте, при которых ГБА применялась как единственный воспринимающий коллектор.
-
2) оценить эффективность реваскуляризации в зависимости от состояния ГПИД ближайшие и отдельные сроки.
-
3) оценить компенсаторные и резервные возможности коллатеральной системы ГБА при высоком регионарном сопротивлении.
Особенностью атеросклеротического поражения артериального русла является развивающееся коллатеральное кровообращение через межсистемные артериальные анастомозы, располагающиеся дистальнее окклюзирующего процесса. Так, при поражении ПБА, ветви ГБА широко анастомозируют с проксимальными ветвями ПкА.
Dunlop GR назвал этот окольный путь, естественным бедренно-подколенным шунтом!
Материалы и методы исследования
В настоящей работе представлен опыт хирургическое лечение 121 больного с применением пластики ГБA (118мужчин и 3 женщины), которым была проведена реваскуляризация в отделении сосудистой хирургии университетской клиники Институт хирургии Микаелян›› в период с 2008 по 2020 гг. Путем включения в кровоток ГБА реваскуляризированы 164 конечностей (в 43 случаях двухсторонних диффузных поражений ПБА были реваскуляризированы обе н/к одномоментно). Больные распределены на 2 группы: I (контрольная) (n-81) (49,39 %) – ГПИД < 0,4, II (основная) (n-83; (50,61 %) – ГПИД > 0,4 (табл. 1).
Таблица 1
Распределение больных в группах по возрастным категориям
Table 1
Distribution of patients in groups by age categories
|
Возраст/ Age |
Контрольная группа/ Control group (n=63) |
Основная группа/ Main group (n=58) |
p |
||
|
N |
% |
N |
% |
||
|
25-44 (молодой возраст/ young age) |
3 |
4.76 |
2 |
3.45 |
p > 0.2 |
|
45-59 (средний возраст/ middle age) |
24 |
38.1 |
21 |
36.21 |
|
|
60-74 (пожилой возраст) |
30 |
47.62 |
27 |
46.55 |
|
|
75-89 (старческий возраст/ old age) |
6 |
9.52 |
8 |
13.79 |
|
Сопутствующие заболевания представлены в таблице 2.
Таблица 2
Сопутствующие заболевания у больных контрольной и основной групп
Table 2
Concomitant diseases in patients of the control and main groups
|
Сопутствующие заболевания/ Concomitant diseases |
Контрольная группа/ Control group (n=63) |
Основная группа/ Main group (n=58) |
P |
||
|
N |
% |
N |
% |
P > 0.2 |
|
|
Ишемическая болезнь сердца/ Ischemic heart disease |
21 |
33,33 |
24 |
41,37 |
|
|
Постинфарктный кардиосклероз/ Post-infarction cardiosclerosis |
5 |
7,94 |
7 |
12,07 |
|
|
Артериальная гипертензия/ Arterial hypertension |
17 |
26,98 |
11 |
18,97 |
|
|
Сахарный диабет/Diabetes mellitus |
5 |
7,94 |
3 |
5,17 |
|
|
Хроническая цереброваскулярная недостаточность/ Chronic cerebrovascular insufficiency |
2 |
3,17 |
1 |
1,72 |
|
|
Язвенная болезнь желудка и 12-ти перстной кишки/ Peptic ulcer of the stomach and 12 duodenum |
3 |
4,76 |
2 |
3,45 |
|
Распределение по стадиям ишемии представлены в таблице 3.
Таблица 3
Распределение наблюдений по группам в зависимости от стадии ишемии
Table 3
Distribution of observations by groups depending on the stage of ischemia
|
Стадия ишемии/ Stage of schemia |
Контрольная группа/ Control group (n=81) |
Основная группа / Main group (n=83) |
p |
||
|
N |
% |
N |
% |
||
|
II б |
35 |
43.21 |
17 |
20.48 |
0.05>p>0.02 |
|
III-(ХКИНК ) |
28 |
34.57 |
37 |
45.58 |
|
|
IV-(ХКИНК) |
18 |
22.22 |
29 |
34.94 |
|
* ХКИНК – chronic critical ischemia of the lower extremities
Использование ГБА при различных видах шунтирования отмечено в таблице 4.
B 52 наблюдениях во время операции просвет ГБА был проходим, в 112 возникла необходимость профундопластики, при этом в 44 из них (26,8 %) произведена расширенная открытая и/или эверсионная эндартерэктомия из ветвей II и III порядка. Распределение исследуемых конечностей в зависимости от вмешательств на ГБА представлены в таблице 5.
Таким образом:
-
1) в обеих группах основной контингент составляли пациенты трудоспособного возраста (45–65), что придавало особую актуальность задаче о максимальном предотвращении ампутаций.
-
2) достоверно различалось количество пациентов с хронической ишемией, угрожающей потерей конечности (p<0,05).
-
3) разница основных параметров в обеих группах не имела достоверной характер, следовательно, полученные результаты можно связывать только с исходной величиной ГПИД и со стадией ишемии.
Барагамян Г.С. сопоставляя показатели функционального состояния ГПИД и степень ишемии, установил статистически высокую зависимость между этими показателями, что свидетельствует о том, что состояние ГПИД играет важную роль в степени циркуляторных нарушений при поражениях бедренно-подколенно-берцового сегмента.
Необходимо отметить, что все расчеты исходили из количества реваскуляризированных конечностей (164), а не из числа больных.
Таблица 4
Количество использованных ГБА во время различных видах шунтирования
Table 4
The number of deep femoral artery used during various types of bypass surgery
|
Название операции/ Name of the operation |
Контрольная группа/ Control group (n=81) |
Основная группа/ Main group (n=83) |
||
|
N |
% |
N |
% |
|
|
Бифуркационное аорто-глубокобедренное шунтирование/ Bifurcation aorto-hip bypass surgery |
46 |
56,79 |
37 |
44,58 |
|
Одностороннее аорто- глубокобедренное шунтирование/ Unilateral aorto-hip bypass surgery |
3 |
3,7 |
2 |
2,41 |
|
Одностороннее подвздошно-глубокобедренное шунтирование/ Unilateral ilio-hip bypass surgery |
9 |
11,11 |
12 |
14,46 |
|
Бедренно-глубокобедренное перекрестное (в том числе и аутовенозное) шунтирование/ Femoral-deep-femoral cross (including autovenous) bypass surgery |
23 |
28.39 |
32 |
38.55 |
|
p |
p > 0.2 |
|||
Таблица 5
Распределение исследуемых конечностей в зависимости от вмешательства на ГБА
Table 5
Distribution of the examined limbs depending on the intervention of deep femoral artery
|
Объем реконструкции ГБА/ Volume of reconstruction deep femoral artery |
Контрольная группа/ Control group (n=81) |
Основная группа/ Main group (n=83) |
||
|
N |
% |
N |
% |
|
|
Без реконструкции (просвет ГБА изначально проходим)/ Without reconstruction (we initially pass the gap of the deep femoral artery) |
30 |
37,04 |
22 |
26,51 |
|
Произведены эндартерэктомии из устья и/или проксимальной части ГБА/ Endarterectomy was performed from the mouth and/or proximal part of the deep femoral artery |
31 |
38,27 |
37 |
44,58 |
|
Выполнялись расширенные открытые и/или эверсионные эндартерэктомии из ГБА до ветвей II и III порядка/ Extended open and/or inversion endarterectomy was performed from deep femoral artery to branches II and III of the order |
20 |
24,69 |
24 |
28,91 |
|
p |
p > 0,2 |
|||
При обследовании пациентов помимо общеклинических методов применялись ультразвуковая допплерография, дуплексное сканирование, контрастная спиральная КТ ангиография и прямая ангиография в операционной.
Средние величины ЛПИ и ГПИД в контрольной и основной группах представлены в таблице 6.
Таблица 6
Средние величины ЛПИ и ГПИД в контрольной и основной группах до операции
Table 6
Average values of ABI and deep femoral –popliteal index in the control and main groups before surgery
|
Показатель регионарной гемодинамики/Indicator of regional hemodynamics |
Контрольная группа/Control group deep femoral-popliteal index (n=81) < 0,4 |
Основная группа/ Main group (n=83) deep femoral-opliteal index ≥ 0,4 |
p |
|
Средняя величина ЛПИ/ Average value of ABI |
0,34 ± 0,082 |
0,29 ± 0,061 |
p = 0,053 |
|
Среднее значение ГПИД/ Average value of deep femoral-popliteal index |
0,31 ± 0,033 |
0,48 ± 0,045 |
p < 0,001 |
Оценка достоверности средних величин ЛПИ в группах в зависимости от состояния ГБА приведена в таблице 7.
Таблица 7
Оценка достоверности различия средних величин ЛПИ в группах в зависимости от состояния ГБА
Table 7
Assessment of the reliability of the difference in the average values of ABI in groups depending on the state of the deep femoral artery
|
Состояние ГБА/State of the deep femoral artery |
Контрольная группа / Control group (n=81) |
Основная группа/Main group (n=83) |
Достоверность различия между группами/ Reliability of the difference between groups (p) |
|
Среднее значение ЛПИ/ Average ABI value |
Среднее значение ЛПИ/ Average ABI value |
||
|
Просвет ГБА изначально был проходим/ The clearance of the deep femoral artery was initially passable |
0,43 ± 0,023 |
0,38 ± 0,021 |
p < 0,05 |
|
ГБА локальный (проксимальный) стеноз более 50%/Deep femoral artery local (proximal) stenosis more than 50% |
0,33 ± 0,032 |
0,26 ± 0,029 |
p < 0,05 |
|
ГБА стеноз выше 50% и окклюзия (протяженное поражение)/Deep femoral artery local stenosis above 50% and occlusion (extended lesion) |
0,23 ± 0,026 |
0,19 ± 0,034 |
p > 0,05 |
Статистическая обработка полученных результатов. Объем выборки рассчитывался по формуле:
N=2(Pi μ1–σ μ2 ) (где σ=0.1; α=0.017; β=0.1)
и составил по 21в каждой группе.
Полученные данные подвергнуты статистической обработке с использованием общепринятых показателей: среднее значение выборки (М), стандартное отклонение (sd). Сравнение параметрических данных осуществлялось с помощью t-теста Стьюдента (при нормальном распределении признака). Также использовались тесты непараметрических статистик (при от- личном от нормального распределения признака) (критерия U Манна-Уитнии при n<50; распределение Колмоговора-Смир-ного λ при n>50) и при p<0,05 различия считались статистически значимыми. Изучение сопряженной вариабельности показателей выборки проводилось с использованием корреляционного анализа Пирсона (линейная корреляция(r)) и Спирмена (нелинейная корреляция). Значимость корреляции также оценивалась по общепризнанным критериям (при p<0,05 фиксировалась зависимость между признаками). Анализ отдаленной проходимости зоны реконструкции, выживаемости и уровня сохранения конечностей осуществлялся с помощью метода Каплана-Мейера.
Коротко о вариантах выполнения и технических аспектах профундопластики. Поскольку значительная часть исследуемых пациентов были пожилого возраста и имели множество сопутствующих заболеваний, мы часто применяли экстраанатомическое шунтирование (перекрестное бедренное-бедрен-ное) – 55 (45,45 %).
В нашей практике встречались случаи с односторонними поражениями аорто-подвздошно-бедренных зон, которые сочетались с двусторонней окклюзией ПБА и гемодинамически значимыми изменениями ОБА реципиентной зоны у пациентов с высоким операционным риском.
В подобной ситуации возникла необходимость реконструкции и донорской зоны при перекрестном шунтировании для профилактики синдрома обкрадывания. Одним из возможных вариантов решения этой проблемы является выполнение профундопластики зоны наложения проксимального анастомоза.
Прежде всего, если была такая возможность, выполнялась профундопластика по Waible (аутоартериальная профундо-пластика клювовидным лоскутом из начального отдела ПБА с наложением проксимального анастомоза перекрестного шунта конец в бок с ОБА под тупым (рис. 1) или острым (рис. 2) углом (3 наблюдения).
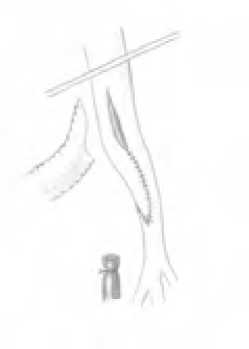
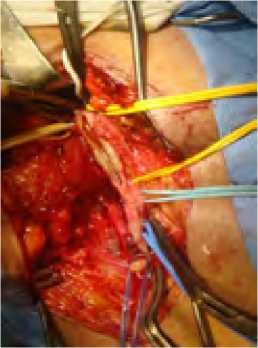
Рис. 1. Накладывание проксимального анастомоза по типу конец-в-бок
Fig. 1. Imposition of proximal anastomosis by end-to-side type
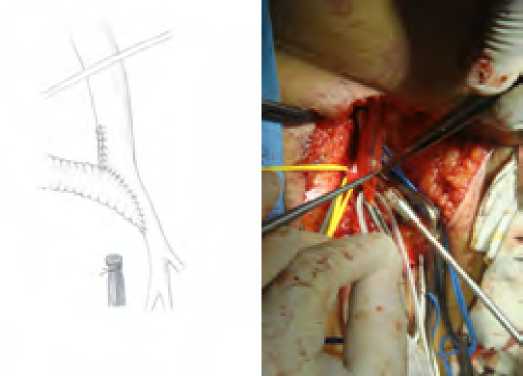
Рис. 2. Проксимальный анастомоз под острым углом
Fig. 2. Proximal anastomosis at an acute angle
Если не было возможности аутоартериальной профундопластики, последнюю выполняли синтетической заплатой (рис. 3) – 2 пациента.
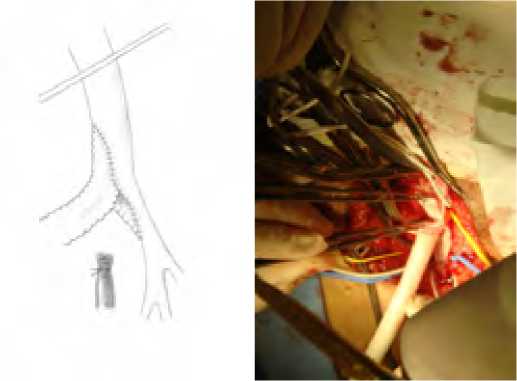
Рис. 3. Проксимальный анастомоз под тупым углом
Fig. 3. Proximal anastomosis at an obtuse angle
В наших наблюдениях на стороне реципиентной зоны всегда удавалось включить в кровоток ГБА в результате открытых либо эверсионных эндартерэктомий или продолженного выделения ГБА до ее ветвей с протяженными эндартерэктомиями из ветвей ГБА II и III порядка.
При устьевых поражениях (рис. 4) выполняли открытую эндартерэктомию из продольного разреза на ГБА и формировали дистальный анастомоз по типу конец протеза в бок ГБА (рис. 5) – 29 пациентов.
При коротком стволе ГБА (<1см) (рис. 6) эндартерэктомия проводилась из разреза на ОБА с переходом на ГБА. При этом в 23 наблюдениях анастомоз выполняли по типу конец в бок (рис. 7), а в 6 случаях возникновения необходимости формирования площадки из задне -латеральной стенки ОБА и короткого ствола ГБА для формирования анастомоза конец в конец (рис. 8)
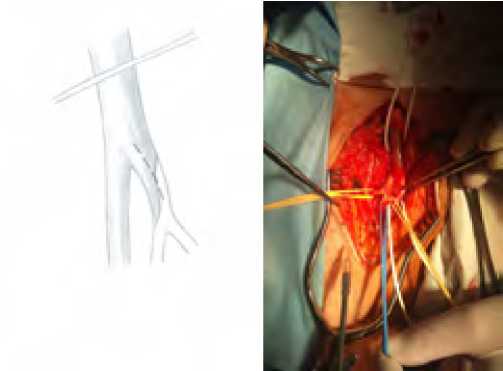
Рис. 4. Вариант проксимального поражения ГБА
Fig. 4. Variant of proximal deep femoral artery lesion
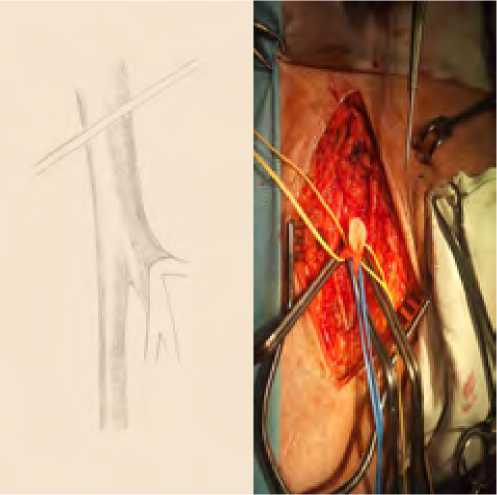
Рис. 6. Короткий ствол глубокой бедренной артерии
Fig. 6. The short trunk of the deep femoral artery
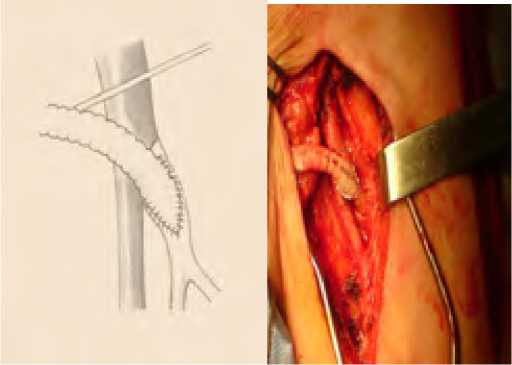
Рис. 5. Формирование дистального анастомоза по типу конец-в-бок
Fig. 5. Formation of distal anastomosis by end-to-side type
Рис. 7. Открытая эндартерэктомия из артериотомического отверстия на ОБА с переходом на ГБА
Fig. 7. Open endarterectomy from the arteriotomy opening on common femoral artery with the transition to deep femoral artery
В тех случаях, когда ГБА имела несколько функционирующих ветвей, которые нами оценивались, как пригодные для реваскуляризации и при условии их отхождения на близких расстояниях друг от друга (рис. 9), выполнялись открытые и/или эверсионные эндартерэктомии из расширенного продольного артериотомического отверстия и формировались площадки для анастомозирования конец в конец (рис. 10) – 21 наблюдение.
При формировании дистального анастомоза протез вырезается таким образом, чтобы длина вырезанного клювовидного его конца соответствовала сформированной площадке.
При анатомическом варианте, когда после 1-ого разветвления ГБА продолжается в виде ствола на 3–4 см до 2-ой бифуркации (рис. 11), после протяженной эндартерэктомии в 5 случаях возникла необходимость дополнительной пластики ГБА.
Последнюю можно осуществить с помощью длинной синтетической заплаты, что снижает качество конструкции или можно прошить непрерывным боковым швом, если позволяет диаметр ГБА. При малом диаметре сосуда нами осуществлялась следующая реконструкция: резецируется стволовая часть ГБА (рис. 12), мобилизуется проксимальная ветвь на площадке и смещается в дистальном направлении. Таким образом, вшива- ется дистальный край проксимальной ветки с проксимальным краем дистальной части ГБА и формируется новая площадка для анастомоза (рис. 13).
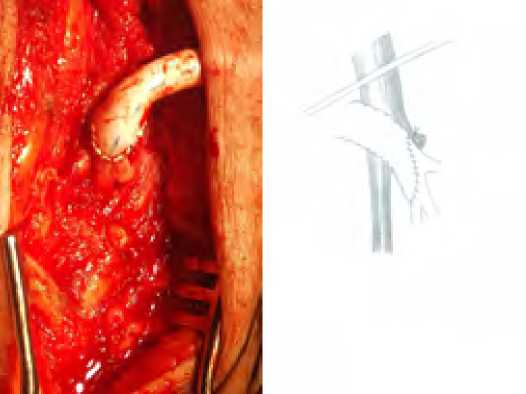
Рис. 8. Дистальный анастомоз по типу конец-в-конец
Fig. 8. Distal end-to-end anastomosis
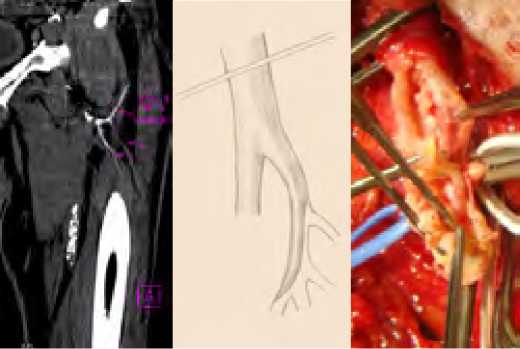
Рис. 9. Функционирующие ветви ГБА отходят на близких расстояниях
Fig. 9. Functioning branches of the deep femoral artery depart at close distances
Такая тактика неприемлема, если ветви ГБА отходят на протяжении и близких расстояниях друг от друга (рис. 14).
В подобной ситуации после открытой протяженной эндартерэктомии мы частично прошивали артерию непрерывным боковым швом (4 случая,) формируя следующим этапом дистальной анастомоз с протезом (рис. 15, 16).
При восстановлении кровообращении в нижней конечности очевидно желание хирурга по возможности включить в кровоток и бассейн ПБА, и бассейн ГБА.
Ниже приводим ряд вариантов выполнения данной задачи.
Подготовка зоны дистального анастомоза может быть осуществлена путем эндартерэктомии при первичной реконструктивной операции, но в определенных случаях (повторные вмешательства, рубцовый процесс вокруг сосуда и характер поражения внутри его и т.п.) эндартерэктомия технически не возможна (рис. 17).
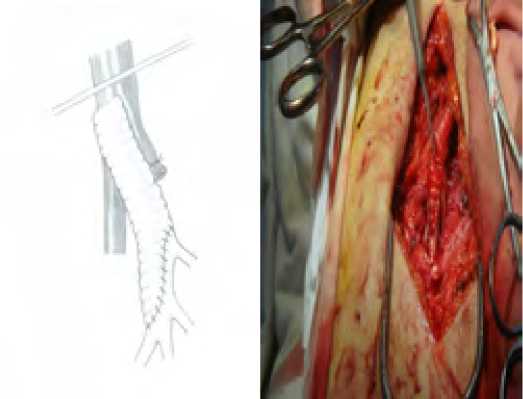
Рис. 10. Дистальный анастомоз с клювовидным концом протеза соответственной длины Fig. 10. Distal anastomosis with the beak-shaped end of the prosthesis of the corresponding length
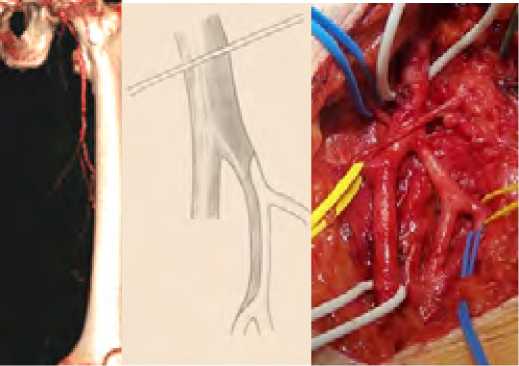
Рис. 11. КТ-ангиограмма, схема и интраоперационная картина (слева на права) описанного варианта разветвления ГБА Fig. 11. CT angiogram, diagram and intraoperative picture (from left to right) of the described variant of the deep femoral artery branching
В подобной ситуации наиболее приемлема резекция начальных пораженных отделов ПБА и ГБА, после чего встает вопрос о способе формирования реципиентной зоны и воссоздания новой бифуркации (рис. 18, 19)
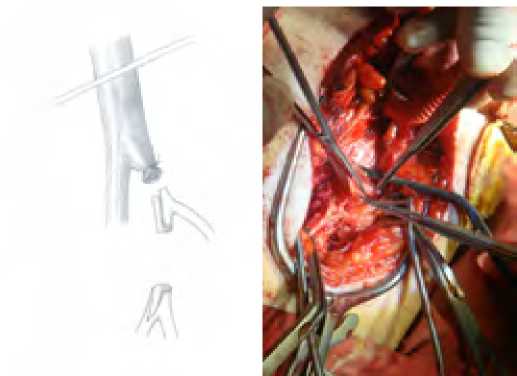
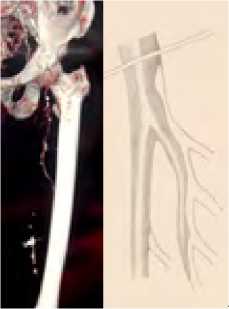
Рис. 14. а -МСКТ-ангиограмма и схема вида поражения, б-открытая эндартерэктомия на протяжении 15 см
Fig. 14. a-MSCT-angiogram and diagram of the type of lesion, b-open endarterectomy for 15 cm
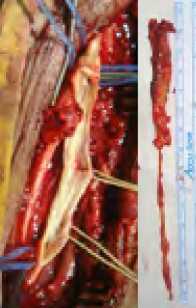
б
Рис. 12. Резекция пораженной стволовой части глубокой бедренной артерии
Fig. 12. Resection of the affected stem part of the deep femoral artery
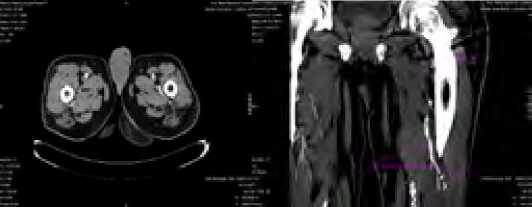
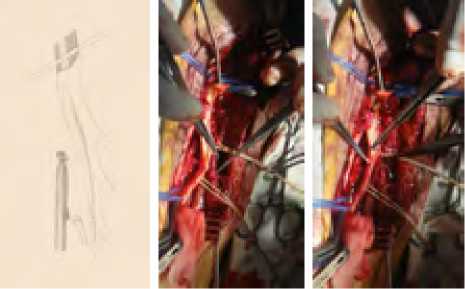
Рис. 15. Боковое пришивание артерии непрерывным обвивным швом полипропиленовой нитью 6.0
Fig. 15. Lateral suturing of the artery with a continuous wound suture with a polypropylene thread 6.0
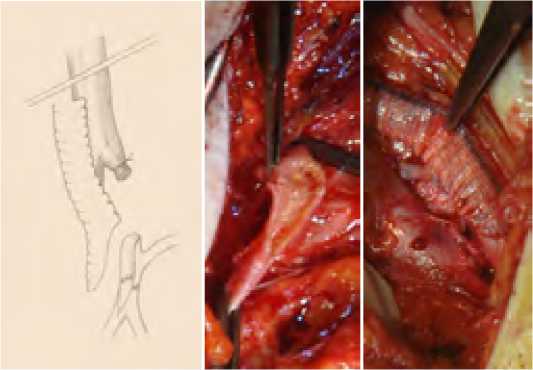
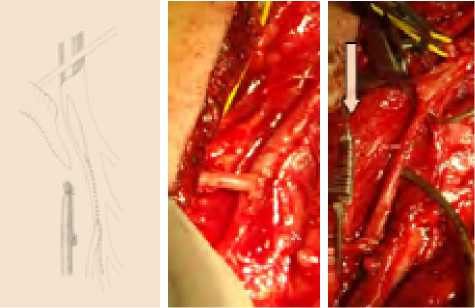
Рис. 16. Имплантация функционирующей ветви поверхностной бедренной артерии по типу конец-в-бок
Fig. 16. Implantation of a functioning branch of the superficial femoral artery by the end-to-side type
б
Рис. 13. а -КТ-ангиограмма пациента, б-схема и этапы формирования новой площадки для анастомозирования Fig. 13. a-CT angiogram of the patient, b-scheme and stages of formation of a new site for anastomosis
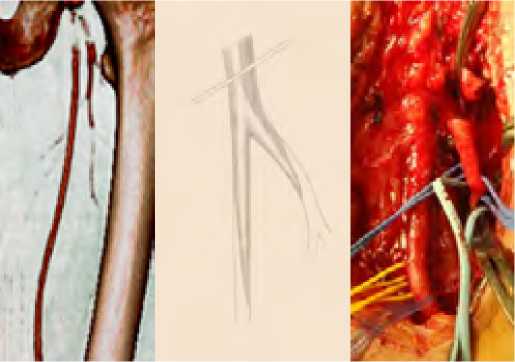
Рис. 17. МСКТ - ангиографическая картина поражения начальных отделов ПБА и ГБА, схема поражения, рубцовый процесс вокруг сосуда (слева на права) Fig. 17. MSCT - angiographic picture of the lesion of the initial parts of superficial and deep femoral arteries, lesion diagram, scarring process around the vessel (left to right)
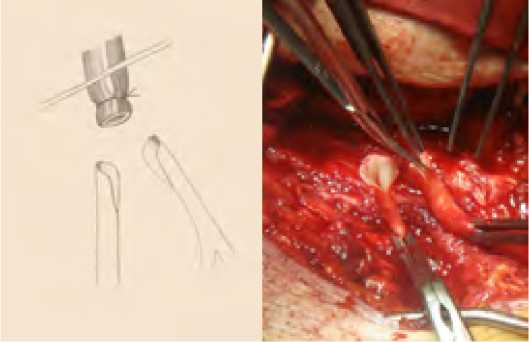
Рис. 18. Резекция начальных пораженных отделов ПБА и ГБА
Fig. 18. Resection of the initial affected parts of superficial and deep femoral artery
Вариант позволяет увеличить диаметр воспринимающего сосуда и привести его в относительное соответствие с диаметром используемого синтетического протеза.
Если ГБА имела несколько ветвей (нет возможности достаточной ее мобилизации) во избежание перекрута артерий вокруг своих собственных осей, сшивались только задние стенки сосудов и на сформированной площадке выполняли дистальный анастомоз конец в конец, вырезав конец протеза соответствующей формы (рис. 20, 21).
Таким образом передняя стенка аллопротеза служила заплатой для обоих сосудов.
В некоторых случаях (не соответствие с диаметром протеза, ограничение возможности мобилизации) возможно форми- рование бифуркации сопоставлением медиальной стенки ГБА с латеральной стенкой ПБА, а дистальный конец протеза выкраивали W-образно (протез с развилкой в виде «лепестков») (рис. 22, 23).
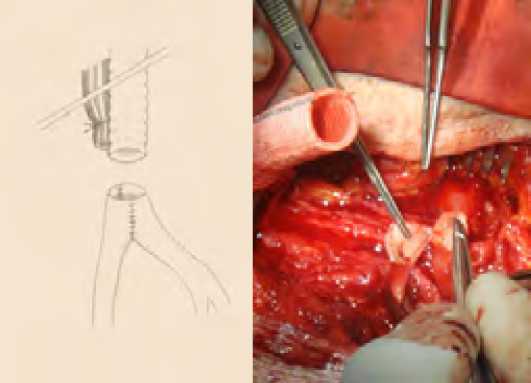
Рис. 19. Формирование новой бифуркации
Fig. 19. Formation of a new bifurcation
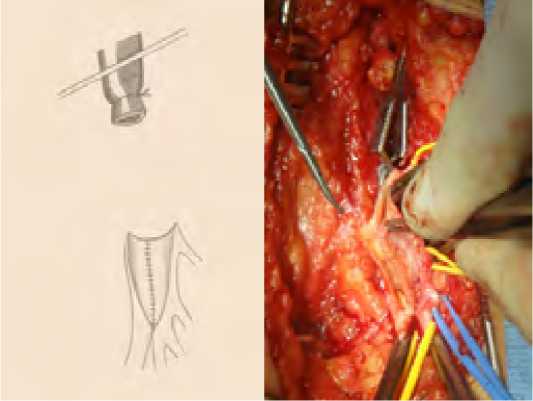
Рис. 20. Сопостовление задних стенок артерий без перекрута
Fig. 20. Comparison of the posterior walls of the arteries without torsion
Однако формирование новой бифуркации возможно лишь при осуществлении резекции ПБА и ГБА примерно на одном уровне.
Когда пересечение ПБА и ГБА осуществляется на разных уровнях (ПБА обычно более дистально рис. 24), реципиентная зона может формироваться выполнением анастомоза конец протеза в конец ПБА (в одном наблюдении конец протеза анастомозировался с проксимальной частью ПКА (рис. 25), а ГБА имплантировалась в шунт (рис. 26).
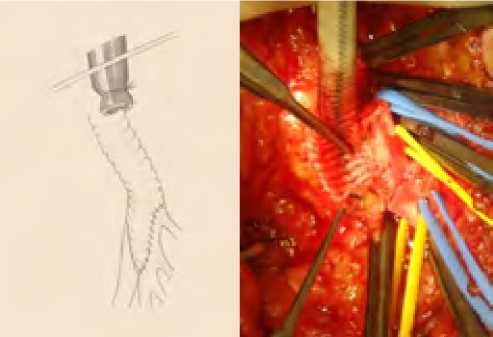
Рис. 21. Дистальный анастомоз выполняется с одномоментной пластикой
Fig. 21. Distal anastomosis is performed with simultaneous plastic surgery
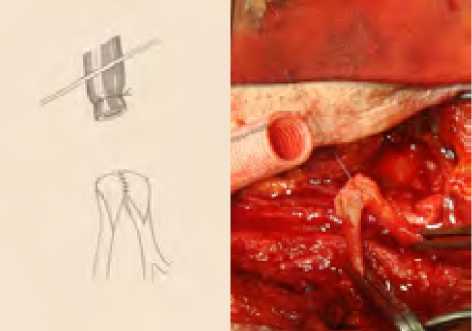
Рис. 22. Техника формирования бифуркации бок-о-бок
Fig. 22. Technique of side-by-side bifurcation formation
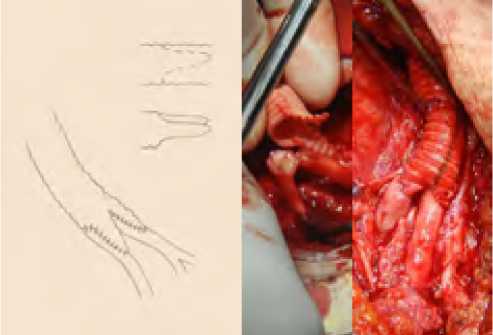
Рис. 23. W-образное выкраивание дистального конца протеза, двойная пластика одним этапом
Fig. 23. W-shaped cutting out of the distal end of the prosthesis, double plastic surgery in one step
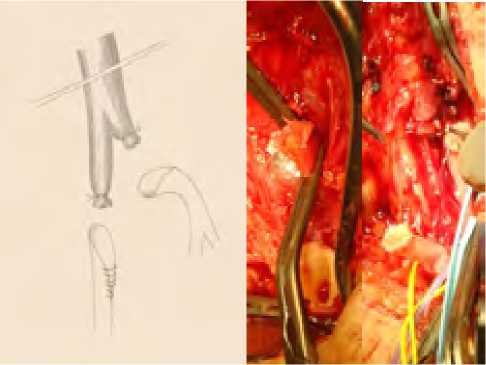
Рис. 24. Пересечение ПБА и ГБА на разных уровнях
Fig. 24. Intersection of superficial and deep femoral artery at different levels
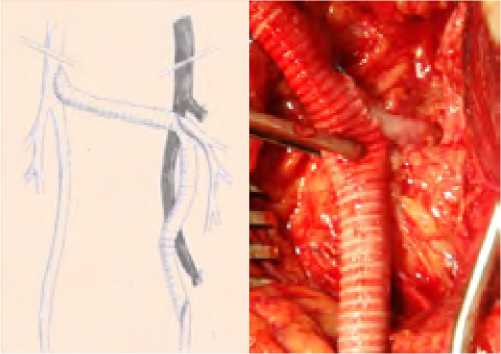
Рис. 25. Дистальный анастомоз с подколенной артерий, реконструкция двух этажей включая в кровоток систему ГБА Fig. 25. Distal anastomosis with popliteal arteries, reconstruction of two floors including the deep femoral artery system in the bloodstream
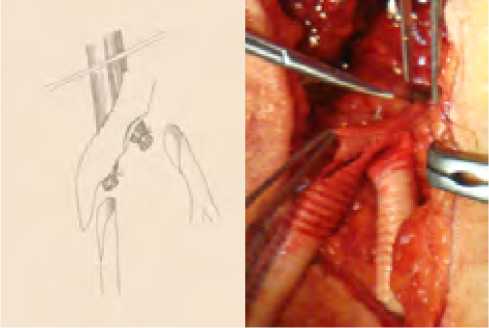
Рис. 26. Имплантация ГБА в шунт
Fig. 26. Implantation of the deep femoral artery into the shunt
Очевидно, в этом случае анастомоз конец в конец осуществляется между разнокалиберными сосудами, что с гемодинамической точки зрения не оптимально. Кроме того, оба дистальных анастомоза создаются между артерией и протезом, что так же, в свою очередь, снижает качество конструкции.
Нами предложен способ формирования реципиентной зоны, позволяющей обойти вышеотмеченные недостатки. Выделяли ГБА на протяжении 4–5см (обычно до ее бифуркации), что давало возможность выполнить анастомоз между ПБА и ГБА конец в конец (медиальная полуокружность ГБА сопоставляется с латеральной полуокружностью ПБА, диаметр сосудов практически совпадает) (рис. 27).
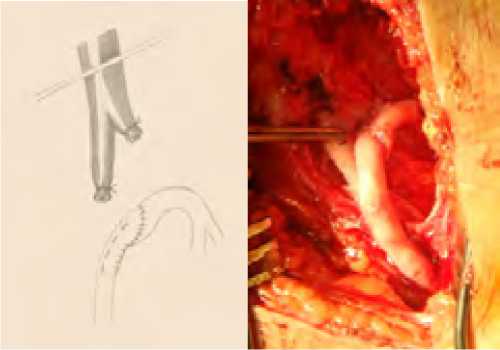
Рис. 27. Формирование новой «сосудистой дуги»
Fig. 27. Formation of a new “vascular arch”
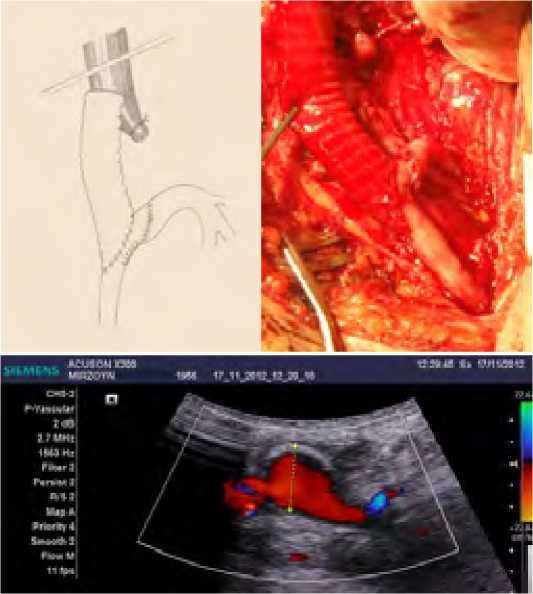
Рис. 28. а – дистальный анастомоз по типу конец в бок, б – ультразвуковая (ДС) картина формированной конструкции Fig. 28. a – distal anastomosis of the end-to-side type, b – ultrasound (DS) picture of the formed structure
Фактически формируется не новая бифуркация, а своеобразная сосудистая дуга. В наших случаях выполнялись открытые и эвирсионные эндартерэктомии из ПБА и ГБА, а «избытки» продольных артериотомических отверстий ушивались непрерывным боковым швом.
Подобное формирование реципиентной зоны давало возможность выполнить дистальный анастомоз по типу конец аллопротеза в бок «сосудистой дуги» несколько дистальнее артериального анастомоза конец в конец (рис. 28).
Тоже самое можно выполнить в случаях, когда ГБА резецируется более дистально (становясь иммобильной в связи с разветвленностью); при этом следует мобилизовать ПБА и наложить анастомоз с ГБА и следовать вышеописанной методике.
Предлагаемая конструкция значительно более удобна и гемодинамически целесообразна при перекрестном бедренно-бедренном шунтировании, так как позволяет сместить по отношению друг к другу во фронтальной плоскости донорский и реципиентный анастомозы, что сохраняет оптимальный антеградный характер кровотока (как это бывает при подвздошно-бедренном перекрестном шунтировании).
Таким образом, предлагаемый способ формирования реципиентной зоны дает возможность добиться максимальной гемодинамической оптимизации и улучшает качество конструкции.
Важно подчеркнуть, что результаты реконструкций, включающих в кровоток ПБА, исключены из исследования, оценивающего возможности ГБА, как единственного коллектора кровообращения нижней конечности.
Результаты
Результаты реваскуляризирующих операций обобщались нами на основании рекомендуемых стандартов оценки лечения пациентов с хронической ишемией н/конечностей.
Ближайшие результаты оценены у всех 121 больных.
Интраоперационных осложнений не наблюдали.
Основными критериями явились ЛПИ, объективные и субъективные показатели изменения клинического статуса.
Поскольку у всех пациентов кровоснабжение восстанавливалось коллатеральными путями в ближайшем послеоперационном периоде значительного улучшения (+3балла) не наблюдалось.
Таблица 8
Степень изменения клинического статуса в непосредственном послеоперационном периоде в контрольной и основной группах
Table 8
The degree of change in the clinical status in the immediate postoperative period in the control and main groups
|
Ближайшие послеоперационные изменения/ Immediate postoperative changes |
Контрольная группа/ Control group (n=81) |
Основная группа/Main group (n=83) |
||
|
N |
% |
N |
% |
|
|
Значительное улучшение/ Significant improvement +3 |
- |
- |
- |
- |
|
Умеренное улучшение/Moderate improvement +2 |
71 |
87,65 |
53 |
63,86 |
|
Минимальное улучшение/ Minimum improvement +1 |
4 |
4,94 |
15 |
18,07 |
|
Без изменений/No changes 0 |
2 |
2,47 |
6 |
7,23 |
|
Незначительное ухудшение/ Slight deterioration -1 |
- |
- |
1 |
1,21 |
|
Умеренное ухудшение/ Moderate deterioration -2 |
1 |
1,23 |
3 |
3,61 |
|
Значительное ухудшение/ Significant deterioration -3 |
3 |
3,71 |
5 |
6,02 |
|
p |
p < 0,02 |
|||
Таким образом, наибольшее влияние на исход реконструкций в ближайшем послеоперационном периоде оказало состояние глубоко-бедренно-подколенной коллатеральной сети. В этом аспекте ГПИД достаточно чувствительный показатель для прогнозирования результатов реконструкции ГБА.
При низком сопротивлении приток крови (контрольная группа) после устранения гемодинамически значимых препятствий в ГБА происходит ощутимое улучшение кровоснабжения конечности.
В I группe (ГБИД<0,4) наступало более выраженное клиническое улучшение (p<0,02), чем в группе с ГПИД>0,4 (основная группа), где наблюдалось ухудшение состояния (–1, –2, –3 по Rutherford) в 10,84 %.
Прогрессирования ишемии во всех (13–17,93 %) случаях в обеих группах приводило к необходимости ампутаций на разных уровнях.
Послеоперационная смертность составила 9 % (11больных): от ИМ7 (5,8 %), от ОНМК-1 (0,8 %), от тромбоза мезентериальных сосудов –1 (0,8 %); от других причин – 2 (1,6 %).
После операций на аорто-подвздошно-бедренном сегменте (66 больных) летальный исход наступил в 9 (13,6 %) наблюдениях; при в неополостных операциях (55 больных) – в 2(3,6 %).
В ближайшем и раннем (до 30 дней) послеоперационном периоде различные осложнения развились у 24 (19,8 %) пациентов.
Тромбоз зоны реконструкции наблюдался в двух (1,2 %) случаях в основной группе.
Таблица 9
Осложнения в ближайшем и раннем послеоперационном периоде по группам
Table 9
Complications in the immediate and early postoperative period by groups
|
Вид осложнения/Type of complication / |
Контрольная группа/Con-trol group |
Основная Группа/ Main Group |
Общее количество (%) (из числа операций)/ Total number (%) (from the number of operations) |
||
|
N |
% |
N |
% |
||
|
Тромбоз зоны реконструкции/Throm-bosis of the reconstruction zone |
- |
- |
2 |
2,41 |
2 (4,96) |
|
Лимфоррея и нагноение ран/Lymphorrhea and suppuration of wounds |
7 |
8,64 |
5 |
6,02 |
12 (9,92) |
|
Краевой некроз раны, нагноение раны/Marginal necrosis of the wound, suppuration of the wound |
2 |
2,47 |
5 |
6,02 |
7 (5,78) |
|
Желудочно-кишечное кровотечение/ Gastrointestinal bleeding |
2 |
2,47 |
1 |
1,2 |
3 (2,48) |
|
Кровотечение из зоны реконструкции/ Bleeding from the reconstruction area |
- |
- |
- |
- |
- |
|
Всего/Total (p > 0.05) |
11 |
13,58 |
13 |
15,66 |
24 (19,83) |
Первый тромбоз развился на вторые сутки после протяженной (10 см) эндартерэктомии из ГБА (ГПИД=0,56), второй диагностирован спустя 5 дней после подвздошно - глубокобедренного шунтирования (ГПИД =0,62).
Из таблицы следует, что между группами с точки зрения послеоперационных осложнений, различия статистически недостоверны (p>0,05).
Можно только предположить, что возникновению местных осложнений сосудистого характера кроме хирургической травматизации стенок артерии также способствовали неблагоприятное воспринимающее русло и высокое периферическое сопротивление.
В таблице 10 показаны количество и уровень ампутации в ближайшем послеоперационном периоде по группам.
Таблица 10
Количество (%) и уровень ампутаций в исследуемых группах
Table 10
The number (%) and level of amputations in the study groups
|
Уровень ампутации/ Amputation rate |
Контрольная груп-па/Control group |
p |
Основная группа/ MainGroup |
Всего/ Total |
||
|
N |
% |
N |
% |
|||
|
На уровне голени/ At shin level |
1 |
1,23 |
p < 0,05 |
3 |
3,61 |
4 (2,44%) |
|
На уровне бедра (высокие ампутации)/ At hip level (high amputations) |
3 |
3,7 |
p < 0,05 |
6 |
7,23 |
9 (5,49%) |
Как видно из этих данных достоверно высокие (p<0,005) проценты ампутаций наблюдаются в основной группе.
Все пациенты, у которых выполнены ампутации в ближайшем послеоперационном периоде, имели исходную критическую ишемию (46 в контрольной и 66 в основной группах – см. таблицу 3). Учитывая, что проценты наблюдений с критической ишемией в группах достоверно различались (p<0,05), было решено в каждой группе рассчитать проценты ампутации (табл. 11) из количества случаев, когда имела место изначально хроническая критическая ишемия.
Различие показателей оказалось статистически недостоверно (p>0,1), то есть при ХКИНК в результате операций изменение клинического статуса мало зависит от исходного состояния ГПИД.
Средние величины ЛПИ после хирургического вмешательства в группах достоверно различаются (табл. 12).
По данным таблицы можно предположить, что послеоперационный пророст ЛПИ во многом зависит не только от величины ГПИД, но и от степени имеющегося поражения ГБА и его устранения.
Корреляционная зависимость средней силы между величиной ГПИД и приростом ЛПИ в результате операции показана на рисунке 29.
Таблица 11
Процентное соотношение ампутаций по группам, рассчитанное из количества случаев, когда имелась исходная критическая ишемия
|
Уровень ампутации/ Amputation rate |
Контрольная груп-па/Control group |
p |
Основная группа/ MainGroup |
Всего/ Total |
||
|
N |
% |
N |
% |
|||
|
На уровне голе-ни/At shin level |
1 |
2,17 |
p > 0,1 |
3 |
4,54 |
4 (3,57%) |
|
На уровне бедра (высокие ампутации)/ At hip level (high amputations) |
3 |
6,52 |
p > 0,1 |
6 |
9,09 |
9 (8,04%) |
|
Число наблюдений с ХКИНК/ Number of observations with chronic critical ischemia of the lower extremities |
46 |
100 |
- |
66 |
100 |
112(100%) |
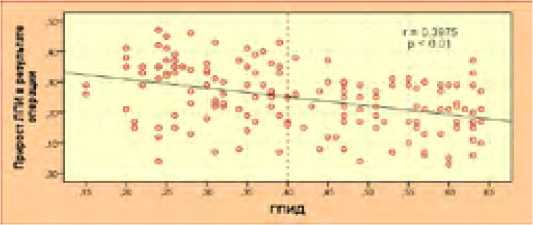
Рис. 29. Линейная корреляция по Пирсону между значением ГПИД и приростом ЛПИ
Fig. 29. Pearson linear correlation between the value of deep femoral-popliteal index and the increase in ABI
Исследование зависимости между приростом ЛПИ и протяженностью поражения ГБА (рис. 30) установило достоверную корреляционную связь средней силы (рис. 30).
Резюме ближайшего послеоперационного периода:
-
1) ГПИД является одним из наиболее важных прогностических критериев при решении вопроса о реваскуляризации конечности через систему ГБА, но у больных с ХКИК результаты операции и изменение клинического статуса мало зависит от величины ГПИД.
-
2) Установлена достоверная корреляционная связь (p<0,001) между приростом ЛПИ и протяжностью поражения ГБА (r=0,344), то есть послеоперационный прирост ЛПИ во многом зависит
от степени имеющегося поражения ГБА и его устранения (чем больше поражена ГБА, тем более высокий прирост ЛПИ ожидается после ее реконструкции).

Рис. 30. Корреляционный диалог прироста ЛПИ в группах и объема хирургического вмешательства на ГБА
Fig. 30. Correlation dialogue of the increase in ABI in groups and the volume of surgical intervention on deep femoral artery
Отдаленные результаты.
Кумулятивная выживаемость в течение первых 2,5 лет после операций в группах мало отличается (p >0,1), а после этого различие становится статистически достоверным (p < 0,05) (рис. 31).
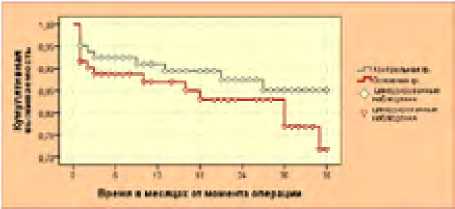
Рис. 31. Кумулятивная выживаемость пациентов в контрольной и основной группах. (Kaplan-Meier)
Fig. 31. Cumulative survival of patients in the control and main groups. (Kaplan-Meier)
Таблица 12
Динамика ЛПИ в группах в зависимости от вмешательства на ГБА
Table 12
Dynamics of IBI in groups depending on the intervention on deep femoral artery
|
Вмешательства на ГБА/Interventions on deep femoral artery |
ЛПИ до операций в среднем/IBI before operations on average |
ЛПИ после операций в среднем/ IBI after operations on average |
Прирост ЛПИ в среднем/The increase in IBI on average |
|||
|
Контр.гр./ Control group |
Основ.гр./ MainGroup |
Контр. гр./ Control group |
Основ.гр./ MainGroup |
Контр.гр./ Control group |
Основ.гр./ MainGroup |
|
|
Просвет ГБА изначально был проходим/ The clearance of the deep femoral artery was initially passable |
0,43 ± 0,02 |
0,38±0,02 |
0,62 ±0,07 |
0,53 ±0,05 |
0,19±0,03 |
0,15±0,04 |
|
p > 0,05 |
0,1 < p > 0,05 |
p > 0,05 |
||||
|
Произведены эндартерэктомии из устья и/ или проксимальной части ГБ/ Endarterectomy was performed from the mouth and/or proximal part of deep femoral artery |
0,33±0,03 |
0,26±0,03 |
0,51 ±0,08 |
0,45 ±0,09 |
0,18±0,05 |
0,19±0,07 |
|
p < 0,05 |
p < 0,05 |
p > 0,05 |
||||
|
Выполнялись расширенные открытые и/или эверсионные эндартерэктомии из ГБА до ветвей II и III порядка/ Extended open and/or eversion endarterectomies were performed from the deep femoral artery to the branches of the II and III order |
0,23±0,03 |
0,19±0,03 |
0,59 ±0,05 |
0,43 ±0,06 |
0,33±0,04 |
0,24±0,03 |
|
p > 0,05 |
p < 0,05 |
p < 0,01 |
||||
Через 3 года кумулятивная выживаемость составила 85,1 % и 71,7 % в контрольной и основной группах соответственно. Это можно объяснить тем, что пациенты с ХКИНК, имеющие сопутствующую ИБС в основной группе, превосходят число таковых в контрольной группе, что естественно может повлиять на выживаемость в трехлетнем диапазоне.
Через 3 года кумулятивная выживаемость составила 85,1 % и 71,7 % в контрольной и основной группах соответственно. Это можно объяснить тем, что пациенты с ХКИНК, имеющие сопутствующую ИБС в основной группе, превосходят число таковых в контрольной группе, что естественно может повлиять на выживаемость в трехлетнем диапазоне.
На рисунке 32 представлены уровни сохраненных конечностей в обеих группах в отдаленные сроки исследования (рис. 32)
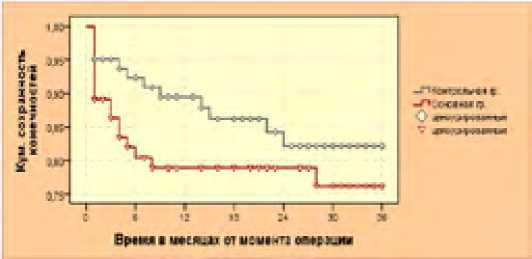
Рис. 32. Кумулятивная сохранность конечностей в течение 3 лет, в контрольной группе и в основной (Kaplan-Meier) Fig. 32. Cumulative limb preservation for 3 years, in the control group and in the main group (Kaplan-Meier)
Кумулятивная сохранность конечностей в течение 30 дней после операций составила 95,1 % (стандартная ошибка кумулятивной сохранности 2,4 %) и 89,2 % (ст. ошибка 3,4%) в контрольной и в основной группах соответственно. Кумулятивный уровень сохранности в контрольной группе через 12, 24 и 36 месяцев составил 89,5% (ст. ошибка 3,5 %), 82,2 % (ст. ошибка 4,8 %) и 82,2 %, а в основной группе соответственно 79,0 % (ст. ошибка 4,7 %), 79,0 % и 76,3 % (ст. ошибка 5,3 %) (рис. 32). Анализируя соотношение полученных процентов, становится ясно, что основная часть потерь конечностей в основной группе происходит до 1 года после операций, а в контрольной группе – в течение 2 лет. Важно акцентировать тот факт, что после 2 лет различие между этими показателями становится недостоверным (p > 0,05).
Кумулятивная сохранность конечностей в течение всего периода исследования в зависимости от исходной степени ишемии представлена на рисунке 33.
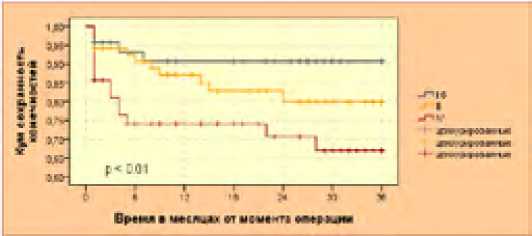
Рис. 33. Кривые кумулятивной сохранности Каплана-Мейера в зависимости от стадии ишемии Fig. 33. Kaplan-Meyer cumulative preservation curves depending on the stage of ischemia
Очевидно, что в течение всего срока наблюдения уровни кумулятивной сохранности конечностей в зависимости от стадии ишемии достоверно различаются (p<0,01). После 6 месяцев кумулятивная сохранность конечностей составляет 95,7 ± 2,9 %, 94,1 ± 2,9 % и 85,7 ± 5,0 % соответственно при II-б, III и IV стадиях ишемии по Фонтейну-Покровскому, после года – 90,7 ± 4,5 %, 85,1 ± 4,6 % и 74,1 ± 6,5 %, а через 3 года – 90,7 ± 4,5 %, 79,9 ± 5,6 % и 67,0 ± 7,6 % соответственно. Основная часть послеоперационных ампутаций относится к IV степени ишемии (ХКИНК) и это свидетельствует о том, что с точки зрения сохранности конечностей большую роль играют язвенно-некротические поражения нижних конечностей.
В течение 3 лет мы обращали особое внимание также на уровень выполненных ампутаций и не нашли достоверной разницы между процентами ампутаций на уровне голени и бедра (p > 0,1).
Для установления причин отдаленных послеоперационных тромбозов мы также рассчитали кумулятивную проходимость зон реконструкций ГБА в зависимости от объема вмешательства на ГБА в общем числе наблюдений (рис. 34). С этой точки зрения достоверные различия также не наблюдались (p > 0,05). Через год кумулятивная проходимость в группе наблюдений со свободным просветом ГБА (n = 52), составила 91,9±4,6 %, а спустя 3 года после операций – 87,1±6,4 %. В тех наблюдениях, где проводились локальные проксимальные эндартерэктомии (n=68), кумулятивная проходимость зон вмешательств в те же сроки исследования (1 и 3 лет) равнялась 90,5±4,1 % и 87,9±4,7 % соответственно. В третьей категории наблюдений, где проводились расширенные вмешательства на ГБА при ее протяженном поражении (n=44), эти значения равнялись 95,0±3,5 % и 91,7±4,6 % (рис. 34).
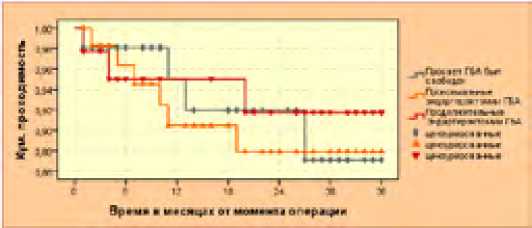
Рис. 34. Кумулятивная проходимость зон формирования дистального анастомоза в зависимости от объема вмешательства на ГБА ( Kaplan-Meier) Fig. 34. Cumulative patency of distal anastomosis formation zones depending on the volume of intervention on deep femoral artery (Kaplan-Meier)
Результаты исследования показали, что степень поражения ГБА и ее устранение, а также состояние ГПИК не обусловливают развития тромбозов в реципиентной зоне.
Мы изучили влияние исходного состояния ГБА на риск развития тромбозов в зоне реконструкции в контрольной и в основной группе по отдельности. Кривые кумулятивной проходимости реципиентных зон в контрольной группе с точки зрения исходной степени поражения ГБА, представлены на рисунке 35.
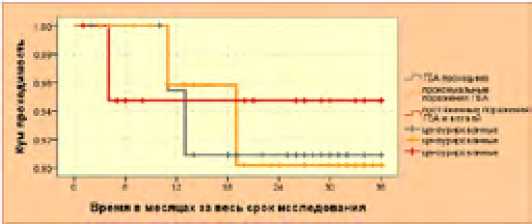
Рис. 35. Кумулятивная проходимость зон реконструкции ГБА в контрольной группе в зависимости от изначальной степени ее поражения (Kaplan-Meier) Fig. 35. Cumulative patency of the deep femoral artery reconstruction zone in the control group, depending on the initial degree of its lesion (Kaplan-Meier)
Метод Каплана-Мейера показал, что кумулятивная проходимость в контрольной группе не зависит от объема вмешательства на ГБА (p>0,05) в течение всего периода исследования (до 3 лет). При ГПИД <0,4, после расширенных вмешательств на ГБА во время шунтирующих операций на аорто-подвздошно-бедренном сегменте кумулятивная проходимость реципиентных зон составляет 94,7 ± 5,1 %. Аналогичное исследование в основной группе наблюдений представлено на рисунке 36.
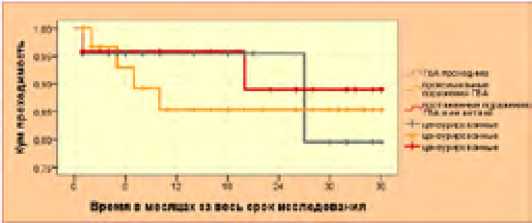
Рис. 36. Кривые кумулятивной проходимости Каплана-Мейера дистальных анастомозов в зависимости от исходного статуса поражения ГБА в основной группе
Fig. 36. Kaplan-Meyer cumulative patency curves of distal anastomoses depending on the initial status of deep femoral artery lesion in the main group
Изучая основную группу (ГПИД ≥ 0,4) в отдельности, стало ясно, что после ограниченных вмешательств на ГБА (n=37) тромбозы наблюдаются в течение года, а после первого года до 3 лет уровень кумулятивной проходимости составляет 85,4 ± 6,8 % и достоверно различается (p< 0,05) от соответственных величин «параллельных» кривых. В случаях невовлеченной в процесс ГБА (n=22) и при протяженных ее поражениях (n =24), кумулятивная проходимость в течение 1,5 лет остается в пределах 95 % (95,5±4,4 % и 95,8±4,1 % соответственно). После двух лет между этими значениями разница становится достоверной (p<0,05) (79,5±8,5 % и 89,0±7,6 % соответственно).
Таким образом, применение эндартерэктомии из ГБА и ее ветвей (продолжительные эндартерэктомии) даже при высоком регионарном сопротивлении (ГПИД ≥ 0,4) дает удовлетворительные результаты и не сопровождается достоверным повышением частоты ближайших и отдаленных послеоперационных тромбозов.
Нам удалось также зарегистрировать динамику прироста среднего значения ЛПИ у 83 пациентов в обеих группах (54 и 43 наблюдения в контрольной и в основной группе соответственно) в течение 1 года (рис. 37).
В контрольной группе (n = 54) достоверный прирост среднего значения ЛПИ (p<0,002) наблюдается только непосредственно после операции.
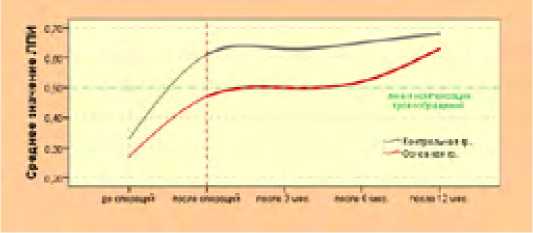
Рис. 37. Динамика среднего значения ЛПИ в отдаленные сроки исследования
Fig. 37. Dynamics of the average value of ABI in the long-term study
В контрольной группе (n=54) достоверный прирост среднего значения ЛПИ (p<0,002) наблюдается только непосредственно после операции.За год ЛПИ в среднем достоверно увеличивался на 0,07±0,02 (p < 0,05) и составлял 0,68 ± 0,06. Этот факт потверждает гипотезу разивающейся коллатеральной системы ГБА после ее реваскуляризации при ГПИД <0,4 (ЛПИ в среднем увеличивался на 11,47 % за год). В основной группе (n=43) в исходе опера-ций также наблюдался достоверный прирост ЛПИ (p < 0,01), но в этой группе в течение года после операций ЛПИ в среднем возрастал на 34,04 % (p < 0,02) и составлял 0,63 ± 0,08 (прирост ЛПИ в среднем за год равен 0,16 ± 0,03). Заслуживают внимания темпы увеличивания ЛПИ в течение года в основной группе (рис. 37).
Исследование показало, что в основной группе особенно большие темпы развития коллатеральной системы ГБА наблюдаются в периоде от 6 месяцев до 1 года. За первые полгода прирост ЛПИ составил 10,64 % (0,05 ± 0,01) (p > 0,05), за второе полугодие – 21,15 % (0,11 ± 0,03) (p < 0,05). Таким образом, коллатеральная сеть ГБА при ГПИД ≥ 0,4 начинает развиваться спустя 6 месяцев после реконструктивной операции. После года различие средних значений ЛПИ в группах становится статистически недостоверным (p > 0,05).
На рисунке 38 показана линейная корреляционная диаграмма между ГПИД и приростом ЛПИ за год после операции. Коэффицент корреляции находится в диапазоне независимости (r = 0,065).
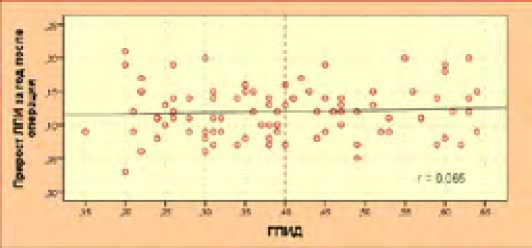
Рис. 38. Корреляция Пирсона между ГПИД и приростом ЛПИ за год
Fig. 38. Pearson correlation between deep femoral-popliteal index and ABI growth over the year
Следовательно, полученную достоверную разницу среднегодовых приростов ЛПИ в группах можно обосновать уже имеющейся достоверной разницей средних значений ЛПИ непосредственно после операций, то есть, предполагается, что системе ГБА свойственен весьма определенный резерв компенсаторных возможностей, в связи с чем мы и выявили корреляционную зависимость между приростом ЛПИ за год и послеоперационным значением ЛПИ (рис. 39).
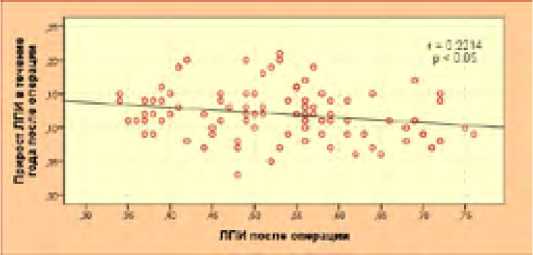
Рис. 39. Параметрическая корреляционная зависимость послеоперационной величины ЛПИ и роста ЛПИ за год после операции Fig. 39. Parametric correlation of the postoperative value of ABI and the growth of ABI for the year after surgery
Таким образом, выявлена значимая корреляция (p<0,05) между послеоперационным значением ЛПИ и приростом ЛПИ за год после операции (рис. 39). Это свидетельствует о том, что в течение года выраженная разница в ЛПИ в ближайшем послеоперационном периоде в основной группе нивелируется за счет включения и развития коллатеральной сети (бездействующей в условиях отсутствия магистрального снабжения). А в контрольной группе коллатеральная сеть изначально достаточно адекватно функционирует, чем и можно объяснить менее выраженный дальнейший прирост. В обоих случаях кровоснабжение осуществляется коллатеральной системой ГБА, возможности которой обусловливают компенсацию кровообращения конечности. Следовательно, при относительно низких значениях ЛПИ, полученных после реваскуляризации, можно ожидать весьма значительный его прирост в течение года после хирургического вмешательства и – наоборот.
Ранее мы показали достоверную связь между объемом поражения ГБА и его устранением с непосредственным приростом ЛПИ (рис. 30). Для выявления особенностей улучшения кровоснабжения н/к (в частности, динамики ЛПИ), мы изучили данные 97 наблюдений в зависимости от объема вмешательства на ГБА (рис. 40). В доступной нам научной литературе мы не встретили такой классификации атеросклеротических поражений артерий нижних конечностей, которая включала бы в критерии степень поражения ГБА. В связи с чем мы условно подразделили все наблюдения на группы А, В и С в зависимости только от степени поражения ГБА (нужно отметить, что хирургическая реконструкция и пластика ГБА строго соответствовала степени ее поражения):
А – изначально просвет ГБА был свободен;
В – локальные, проксимальные поражения (гемодинамически значимые стенозы и окклюзии);
С – стенозы и окклюзии ГБА протяженностью больше 3 см, с вовлечением ветвей II и III порядка.
В результате анализа в группе «В» выявлена статистически достоверная (p < 0,05) значимая линейная корреляция (r = 226) между величиной ГПИД и приростом ЛПИ за год. Получена слабая обратная корреляционная зависимость (r = – 0,170) в условной группе наблюдений «А», а в группе «С» получена линейная корреляция слабой силы (r = 0,182).
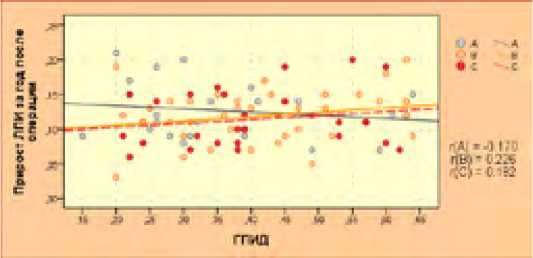
Рис. 40. Корреляционные взаимоотношения между годовым послеоперационным приростом ЛПИ и исходной степени поражения ГБА Fig. 40. Correlation relationship between the annual postoperative increase in ABI and the initial degree of deep femoral artery lesion
Вышеописанные взаимосвязи свидетельствуют о том, что при низких значениях ГПИД после хирургической реваскуляризации интактной ГБА, в течение года наблюдается относительно низкий прирост ЛПИ и наоборот. В то же время ЛПИ достоверно увеличивается в течение года после устранения препятствия в ГБА различной локализации и протяженности при относительно низких значениях ГПИД.
Мы наблюдали также за темпами изменения ЛПИ в течение года после включения ГБА в кровоток в качестве единственного воспринимающего русла (рис. 41).
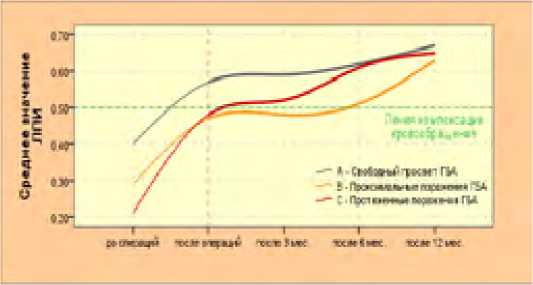
Рис. 41. Динамика ЛПИ в зависимости от объема хирургического вмешательства на ГБА
Fig. 41. Dynamics of ABI depending on the volume of surgical intervention on deep femoral artery
В течение года средние величины ЛПИ достоверно увеличивались (p< 0,05) во всех случаях (рис. 41). В группе наблюдений с изначально свободным просветом ГБА (группа «А») прирост ЛПИ за год составил 0,10 ± 0,04 (17,54 %), в группе «B» (проксимальные поражения ГБА) – 0,16 ± 0,03 (34,04 %) и в группе «С» (ГБА поражена на протяжении) – 0,17 ± 0,04 (35,42 %). После года разница между средними значениями ЛПИ в группах А, В и С становится статистически недостоверной (p>0,1). Мы обратили внимание на темпы увеличения ЛПИ и выявили достоверный прирост за второе полугодие в группе «В» (0,12 ± 0,02 (p < 0,02), от 3 до 6 месяцев в группе «С» (0,09 ± 0,03 (p < 0,05)). Таким образом, коллатеральная сеть ГБА после ее реваскуляризации во всех случаях развивается и темпы ее развития во многом зависят от исходной степени поражения ГБА и ее оперативного устранения. То есть, если после устранения протяженных поражений ГБА и включения в кровоток ее бассейна, кровообращение нижней конечности не компенсируется, то в отдаленные сроки после операции (от 3 до 6 месяцев) за счет развития коллатералей системы ГБА можно получить удовлетворительный результат (рис. 40).
Заключение
-
1. Основная часть случаев потери конечностей происходит при ХКИНК в основной группе до 1 года после операций, а в контрольной группе – в течение 2 лет. После 2 лет различие между этими показателями становится статистически недостоверным (p > 0.05) благодаря работе развивающейся коллатеральной сети ГБА и, как следствие, уменьшения частоты отдаленных ампутаций в основной группе.
-
2. Применение эндартерэктомии из ГБА и ее ветвей (продолженные эндартерэктомии), даже при высоком регионарном сопротивлении (ГПИД ≥ 0,4), целесообразно и не сопровождается достоверным повышением частоты ближайших и отдаленных послеоперационных тромбозов.
-
3. Описанные увеличения ЛПИ обусловлены развитием коллатеральной сети н/к в результате восстановления магистрального кровотока в ГБА. В основной группе (ГПИД ≥ 0,4) достоверное увеличиение ЛПИ наблюдается спустя 6 месяцев после реконструктивной реваскуляризации. После года различие средних значений ЛПИ в группах становится статистически недостоверным (p > 0,05).
-
4. Выявлена значимая корреляция (r=0,221) между послеоперационным значением ЛПИ и приростом ЛПИ за год после операции (p < 0,05). Это свидетельствует о том, что система ГБА имеет определенный потенциал резервных возможностей, способный обеспечивать жизнеспособность конечности. Следовательно, при относительно низких значениях ЛПИ, полученных после реваскуляризации, можно ожидать более высокий его прирост в течение года после хирургического вмешательства и наоборот.
-
5. Коллатеральная сеть ГБА после ее реваскуляризации развивается во всех случаях, и темпы ее развития во многом зависят от исходной степени поражения ГБА и, соответственно, объема вмешательства. При этом, в течение года после устранения препятствий в ГБА различной локализации и протяженности ожидается более высокий прирост ЛПИ при относительно низких значениях ГПИД. Примечательно, что после выполнения объемных вмешательств на ГБА такой прирост наблюдается примерно через 3 месяца.
Выводы
-
1. При шунтирующих операциях на аорто-подвздошно-бедренном сегменте применение ГБА в качестве единственного воспринимающего коллектора в 87,19 % случаев позволяет достичь улучшения клинического статуса в ближайшем послеоперационном периоде (в 92,6 % при ГПИД<0,4; в 81,9 % при ГПИД ≥ 0,4 (p < 0,02).
-
2. Эффективность реваскуляризаций у больных с ХКИНК практически не зависит от исходного функционального состояния ГПКС (у больных с ХКИНК улучшение клинического статуса наблюдается в 91,30 % при ГПИД < 0,4; в 86,36 % при ГПИД ≥ 0,4 (p > 0,1)). Основная часть случаев потери конечностей при ХКИНК происходит во II группе до 1 года после операций, а в I группе – в течение 2 лет; после 2 лет различие между этими показателями становится статистически недостоверным.
-
3. Применение расширенных эндартерэктомий из ГБА и ее ветвей при высоком регионарном сопротивлении (ГПИД ≥ 0,4) обосновано и не сопровождается достоверным повышением частоты послеоперационных тромбозов (p > 0.05).
-
4. Резервный потенциал бассейна ГБА, проявляющийся в динамике послеоперационного периода, позволяет компенсировать кровообращение в течение года после операции и сохранять жизнеспособность конечности.
Список литературы Глубокая артерия бедра - надежда хирурга, спасение больного
- Асланов А.Д., Мизаушев Б.А., Логвина О.Е., Таукенова Л.И., Исхак Л.Н. Хроническая критическая ишемия нижних конечностей на фоне атеросклероза. Методические рекомендации. Нальчик, 2010. 24 с.
- Белов Ю.В., Сандриков В.А., Косенков А.Н. Назаров А.Б., Степаненко А.Б., Минкина С.М., Баймагамбетов А.К. Хирургическое лечение больных с хронической критической ишемией нижних конечностей атеросклеротической этиологии. Хирургия, 1997. № 2. С. 45–51.
- Гаибов А.Д., Каримзаде Б.Д., Эсаналиев У.А. Выбор метода лечения при множественных поражениях периферических сосудов. Кардиология и сердечно-сосудистая хирургия, 2011. том 4. № 4. С. 40–42.
- Захарова Г.Н., Лосев Р.З., Гаврилов В.А. Реконструктивные операции при окклюзионных поражениях аорты и артерий нижних конечностей. Хирургия, 1997. № 11. С. 28–34.
- Калинин Л.Е., Сучков Л.А., Климентова Е.А., Шанаев И.Н. Клиническая анатомия глубоких сосудов бедра области бедренного треугольника. Ангиология и сосудистая хирургия, 1921. T. 27. № 1. С. 17–23.
- Российский Консенсус. Диагностика и лечение пациентов с критической ишемии нижних конечностей. Москва, 2002. 40 с.
- Русин B.I., Корсак В.В., Русин В.В., Горленко Ф.В., Добош В. М. Глибока артерiя стегна як джерело притоку для дистальних реконструкцiй. Сучаснi Медичнi Технологii, 2019. № 2. С. 35–38.
- Adam D.J., Beard J.D., Cleveland T. et al. Bypass versus angioplasty in severe ischemia of the leg (BASIL): multicentre randomized controlled trial. Am.J.Surg., 2005, № 366, pр. 1925–1934.
- Gaibov A.D., Sultanov D.D., Baratov A.K.et al. Surgical tactics for multiple and diffuse lesions of lower limb arteries. Kardiolserdečno-sosudhir, 2010, № 3, p. 44.
- Gyurkovics E., Nagy Z., Jámbor G., Kaliszky P. The role of the V-Y plastics in vascular reconstructions directed to the deep femoral artery. Magy. Seb., 2001, № 54(6), pр. 379–382.
- Krzyasztof A. Tomashevski et al. Varitions in the origin of the deep femoral artery: A meta-analysis. Clin. Anatomy, 2017, Vol.30, № 1, pр. 106–113
- Kwon J.H., Shin Ji H. Hypoplastic superficial femoral artery combined with connection of the deep femoral artery to the popliteal artery. Radiology Case Reports, 2018, Vol. 13, № 1, pр. 39–42.
- J. Veith et al. Unusual surgical exposures to avoid scarred or infected standard access routes to the common femoral, deep femoral, and popliteal arteries. Vascular and Endovascular Techniques. Journal of Vascular Surgery, 2016, Vol. 64, № 4, pр. 1160–1168.
- Steven M., Nassef T. Treatment of chronic lower limb ischemia. Vascular and Endovascular Surgery, 2006, 3rd ed., pр. 35–68.


