Характеристика изменений ультраструктуры нейронов коры головного мозга крыс с частичной церебральной ишемией
Автор: Бонь Елизавета Игоревна, Максимович Наталия Евгеньевна, Зиматкин Сергей Михайлович, Островская Оксана Борисовна, Смирнов Виталий Юрьевич, Носович Мирослав Алексеевич, Храповицкая Ксения Александровна
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Биологические науки
Статья в выпуске: 1, 2023 года.
Бесплатный доступ
Ультраструктурные характеристики органелл нейронов являются значимыми показателями степени повреждения головного мозга при ишемическом воздействии, что обусловливает потребность в исследовании изменений ультраструктуры нейронов головного мозга. Цель. Изучить характер нарушений нейронов головного мозга при его частичной ишемии на ультраструктурном уровне на экспериментальной модели. Материалы и методы. В группу исследования вошли 12 самцов крыс массой 260±20 г, контрольную группу составили 6 ложно оперированных крыс аналогичного пола и веса. Частичную ишемию головного мозга (ЧИГМ) моделировали путем перевязки общей сонной артерии справа. Взятие материала осуществляли через 1 ч после операции. Результаты. При исследовании установлено, что размеры и форма митохондрий нейронов теменной коры и гиппокампа крыс с ЧИГМ не имели отличий по сравнению с контрольной группой (р>0,05), за исключением меньшего количества крист на единицу площади в митохондриях нейронов теменной коры (на 18 %, р
Нейроны, теменная кора, гиппокамп, ишемия
Короткий адрес: https://sciup.org/14127218
IDR: 14127218 | УДК: 616.831.31-005.4-092.913:618.33 | DOI: 10.34014/2227-1848-2023-1-137-144
Changes in the cerebral cortex neuron ultrastructure in rats with partial cerebral ischemia
The ultrastructural characteristics of neuronal organelles are significant indicators of brain damage under ischemic exposure, which necessitates the study of changes in the ultrastructure of brain neurons. The aim of the study was to examine the disorders of brain neurons under its partial ischemia at the ultra-structural level using an experimental model. Materials and Methods. The experimental group included 12 male rats weighing 260±20 g, the control group consisted of 6 falsely operated male rats of the same weight. Partial cerebral ischemia (PCI) was modeled by right common carotid artery ligation. The material was taken 1 hour after the operation. Results. The study showed that the size and shape of the mitochondria of neurons of the parietal cortex and the hippocampus in PCI rats did not differ from those of the control group (p>0.05), except for a smaller number of cristae per unit area in the mitochondria of parietal cortex neurons (by 18 %, p
Текст научной статьи Характеристика изменений ультраструктуры нейронов коры головного мозга крыс с частичной церебральной ишемией
Введение. При ишемии головного мозга (ИГМ) развивается цепь патогенетических нарушений в его структурах, к которым относится энергодефицит, что приводит к формированию клеточной патологии из-за изменений гомеоcтаза, активности ферментов, целостности мембран и работы энергетических насосов. В условиях ИГМ нарушаются преимущественно механизмы синаптической передачи, что способствует нарушению ауторегуляции местного кровотока, развитию спазма сосудов, усилению агрегации тромбоцитов и развитию внутрисосудистого стаза, усугубляя гипоксию и усиливая энергодефицит. Помимо этого, наблюдаются изменения в работе ферментов, в т.ч. натрий-калиевой АТФазы, что в свою очередь приводит к дисбалансу ионов и отеку головного мозга [1–4].
Ультраструктурные характеристики органелл нейронов являются значимыми показателями cтепени повреждения головного мозга при ишемическом воздействии, что обусловливает потребность в исследовании изменений ультраструктуры нейронов головного мозга.
Согласно имеющимся данным, при ИГМ в цитоплазме нейронов наблюдается набухание митохондрий и разрушение их крист, расширение цистерн эндоплазматической cети и комплекса Гольджи, увеличение количества свободных рибосом, образующих обширные скопления в цитоплазме. Увеличивается общее количество лизосом, а также их размеры.
Однако отсутствуют данные о степени выраженности данных нарушений в зависимости от вида ишемического повреждения и степени его тяжести [5–12].
В наших предыдущих гистологических исследованиях в модели частичной ишемии установлено увеличение количества гиперх-ромных нейронов. Обнаружен неврологический дефицит при использовании теста «открытое поле» [3].
В связи с этим представляет интерес электронно-микроскопическое исследование нейронов при частичной ишемии для изучения ультраструктурных основ выявленных изменений.
Цель исследования. Изучить характер нарушений нейронов головного мозга на уль-траструктурном уровне при частичной ишемии головного мозга на экспериментальной модели.
Материалы и методы. Эксперименты выполнены на 12 самцах беспородных белых крыс массой 260±20 г с соблюдением требований Директивы Европейского парламента и Совета Европейского союза о защите животных, использующихся для научных целей (№ 2010/63/EU от 22.09.2010).
В исследованиях использовалась модель частичной ишемии головного мозга (ЧИГМ). Моделирование ЧИГМ осуществлялось путем перевязки общей сонной артерии справа в условиях внутривенного тиопенталового наркоза (40–50 мг/кг). Взятие материала проводилось через 1 ч после операции [3].
Контрольную группу составили 6 ложно оперированных крыс аналогичного пола и веса.
Электронно-микроскопические исследования выполнялись в теменной коре и гиппокампе головного мозга крыс.
Сразу после декапитации и быстрого извлечения головного мозга лезвием вырезались участки теменной коры и гиппокампа и помещались в 1 % осмиевый фиксатор на буфере Миллонига (рН=7,4) на 2 ч при 4 °С. Далее срезы промывались в смеси буфера Милло-нига (20 мл) и сахарозы (900 мг), обезвоживались в спиртах возрастающей концентрации, смеси спирта и ацетона, чистом ацетоне; проводились через смесь смол (аралдит М + арал-дит Н + дибутилфталат + ДМР-30) и ацетона и заключались в смесь смол.
Полутонкие срезы (толщиной около 350 нм) изготавливались на ультрамикротоме МТ-7000 (RMC, США), окрашивались метиленовым синим, из них вырезались лезвием необходимые для изучения участки внутреннего пирамидного слоя теменной коры и пирамидного слоя поля СА1 гиппокампа. Полученные препараты изучались под электронным микроскопом JEM-1011 (JEOL, Япония), фотографировались цифровой камерой Olympus MegaView III (Olympus Soft Imaging Solutions, Германия).
Морфометрия ультраструктур проводилась с помощью программы для обработки изображения Image Warp (Bit Flow, США), для чего обводились курсором на мониторе компьютера митохондрии, комплекс Гольджи, гранулярная эндоплазматическая сеть, рибосомы и лизосомы. Измерялось количество на единицу площади, размеры и форма органелл, количество связанных с эндоплазматической сетью субъединиц рибосом.
Для предотвращения систематической ошибки измерений образцы головного мозга животных контрольной и опытной групп изучались в одинаковых условиях.
В результате исследований были получены количественные непрерывные данные. Так как в эксперименте использовались малые выборки, которые имели ненормальное распределение, анализ проводился методами непараметрической статистики с помощью лицензионной компьютерной программы Sta-tistica 10.0 для Windows (StatSoft. Inc., США). Данные представлены в виде Me (LQ; UQ), где Me – медиана, LQ – значение нижнего квартиля; UQ – значение верхнего квартиля. Различия между группами считались достоверными при р<0,05 (тест Крускела – Уоллиса с поправкой Бонферрони).
Результаты и обсуждение. При электронно-микроскопическом исследовании установлено, что размеры и форма митохондрий нейронов теменной коры и гиппокампа у крыс опытной и контрольной групп не различаются (р>0,05), за исключением количества крист на единицу площади в митохондриях нейронов теменной коры, которое у крыс опытной группы меньше на 18 % (р<0,05) (табл. 1).
Таблица 1
Table 1
Показатели ультрамикроскопической морфометрии органелл нейронов теменной коры и гиппокампа крыс с частичной церебральной ишемией
Parameters of ultramicroscopic morphometry of neuron organelles in parietal cortex and hippocampus of rats with partial cerebral ischemia
|
Показатель Parameter |
Теменная кора Parietal cortex |
Гиппокамп Hippocampus |
|||
|
Контроль Control |
ЧИГМ PCI |
Контроль Control |
ЧИГМ PCI |
||
|
"О Г О s s о о и S S |
Количество на единицу площади Quantity per unit area |
1,8 (1,7; 2,2) |
1,9 (1,6; 2,3) |
2,1 (1,7; 2,2) |
2,2 (1,6; 2,4) |
|
Площадь, мкм2 Area, µm2 |
0,26 (0,17; 0,37) |
0,27 (0,18; 0,33) |
0,21 (0,17; 0,26) |
0,22 (0,18; 0,25) |
|
|
Форм-фактор, ед. Form factor, unit |
0,63 (0,61; 0,72) |
0,69 (0,60; 0,75) |
0,71 (0,60; 0,75)* |
0,76 (0,66; 0,78) |
|
|
Фактор элонгации, ед. Elongation factor, units |
3,8 (3,5; 4,1) |
3,7 (3,5; 4,1) |
2,1 (1,9; 2,5) |
2,0 (1,9; 2,2) |
|
|
Количество крист на единицу площади митохондрии Number of cristae per unit area of mitochondria |
76 (71; 82) |
62 (58; 67)* |
62 (59; 72) |
68 (60; 78) |
|
|
Длина крист, мкм Cristae length, µm |
12 (10; 15) |
10 (9; 12) |
13 (12; 18) |
13 (10; 15) |
|
|
о О о Ан |
Количество на единицу площади, из них: Number of ribosomes per unit area, including |
20,9 (19,3; 22,7) |
22,3 (19,1; 24,2) |
20,0 (18,1; 22,8) |
21,6 (18,8; 23,9) |
|
свободных free ribosomes, µm2 |
4,7 (4,1; 5,8) |
12,5 (11,2; 13,0) |
6,0 (4,8; 7,3) |
12,8 (11,4; 13,4) |
|
|
связанных fixed ribosomes, µm2 |
16,2 (15,2; 16,9) |
9,8 (7,9; 11,2) |
14,0 (13,3; 15,5) |
8,8 (7,4; 10,5) |
|
|
Коэффициент отношения связанных и свободных рибосом Ratio of fixed and free ribosomes |
3,4 |
0,8* |
2,3 |
0,7* |
|
|
S 8 © © и Ч J |
Количество на единицу площади Number per unit area |
0,4 (0,3; 0,5) |
0,4 (0,3; 0,6) |
0,5 (0,4; 0,6) |
0,5 (0,4; 0,6) |
|
Площадь, мкм2 Area, µm2 |
0,02 (0,01; 0,03) |
0,02 (0,01; 0,03) |
0,03 (0,02; 0,04) |
0,02 (0,01; 0,02) |
|
Примечание. * – статистически значимые различия по сравнению с контролем (р<0,05).
Note. * – the differences are statistically significant compared to control (p<0.05).
Размеры и форма комплекса Гольджи и лизосом в опытной и контрольной группах также не различались. Однако в цитоплазме нейронов теменной коры и гиппокампа крыс с ЧИГМ отмечалось увеличение количества субъединиц рибосом – на 58 % и 54 % соответственно (р<0,05), что свидетельствует о распаде цистерн гранулярной эндоплазматической сети при ЧИГМ.
Коэффициент отношения связанных и свободных рибосом у крыс контрольной группы уменьшился от 3,4 до 0,8 в теменной коре (р<0,05) и от 2,33 до 0,7 в гиппокампе (р<0,05).
Согласно данным литературы, при ишемии головного мозга происходит ряд типовых нарушений ультраструктуры нейронов, которые проявляются набуханием митохондрий и
деструкцией цистерн эндоплазматической сети и комплекса Гольджи [1, 2, 7]. При ЧИГМ подобные нарушения заключаются в преобладании свободных рибосом и деструкции крист в теменной коре (как более чувствительной к недостатку кислорода).
Размеры и форма митохондрий у крыс с ЧИГМ и крыс контрольной группы не различались, за исключением количества крист на единицу площади митохондрий нейронов теменной коры, которое у крыс опытной группы было меньше (рис. 1).
Однако в цитоплазме нейронов теменной коры и гиппокампа крыс с ЧИГМ отмечалось большее количество свободных рибосом (рис. 2).
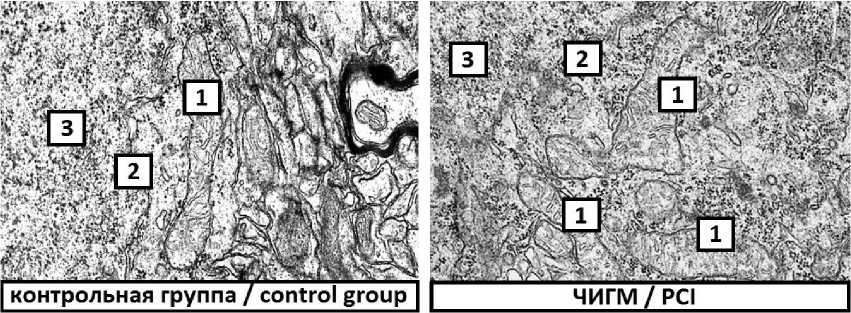
Рис. 1. Митохондрии нейронов теменной коры мозга крыс:
1 – митохондрии, 2 – ядерная оболочка, 3 – ядро. Электронограмма, ×50 000
Fig. 1. Mitochondria of rat parietal cortex neurons.
1 – mitochondria, 2 – nuclear envelope, 3 – nucleus. Electronogram, ×50 000
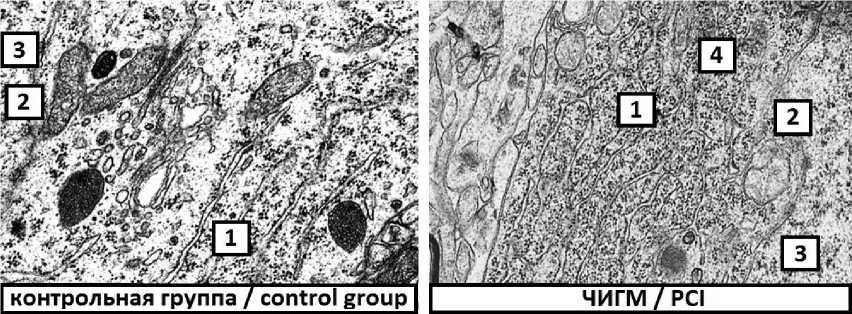
Рис. 2. Гранулярная эндоплазматическая сеть нейронов теменной коры мозга крыс: 1 – гранулярная эндоплазматическая сеть, 2 – ядерная оболочка, 3 – ядро, 4 – свободные рибосомы. Электронограмма, ×50 000
Fig. 2 . Granular endoplasmic reticulum of neurons in the parietal cortex of rat brain. 1 – granular endoplasmic reticulum, 2 – nuclear envelope, 3 – nucleus, 4 – free ribosomes. Electronogram, ×50 000
Среднее количество и размеры лизосом, а также комплексов Гольджи в опытной группе
не отличались от таковых в группе контроля (рис. 3).
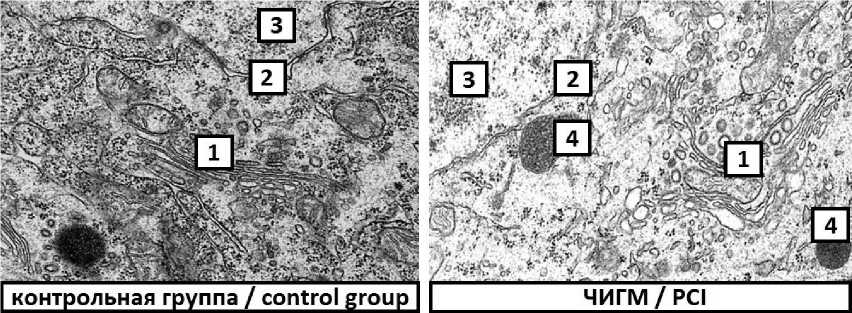
Рис. 3. Комплекс Гольджи нейронов теменной коры мозга крыс: 1 – комплекс Гольджи,
2 – ядерная оболочка, 3 – ядро, 4 – лизосомы. Электронограмма, ×50 000
Fig. 3. Golgi complex of neurons in the parietal cortex of rat brain. 1 – Golgi complex, 2 – nuclear envelope, 3 – nucleus, 4 – lysosomes. Electronogram, ×50 000
Заключение. Таким образом, ультраструктура нейронов при частичной ишемии головного мозга в целом аналогична таковой в контрольной группе, что может быть обусловлено компенсацией кровотока по вилли-зиевому кругу. Однако имеющее место уменьшение количества крист на единицу площади
митохондрий нейронов в теменной коре указывает на возникновение энергодефицита в данной области головного мозга как более чувствительной к недостатку кислорода, что может быть основой для прежде выявленных гистологических и неврологических изменений.
Список литературы Характеристика изменений ультраструктуры нейронов коры головного мозга крыс с частичной церебральной ишемией
- Snider B.J., Gottron F.J., Choi D. W. Apoptosis and necrosis in cerebrovascular disease. Ann N Y Acad Sci. 1999; 893: 243-253.
- Chopp M., Li Y. Apoptosis in focal cerebral ischemia. J. Acta Neurochir Suppl (Wien). 1996; 66: 21-26.
- Максимович Н.Е., Бонь Е.И., Зиматкин С.М. Головной мозг крысы и его реакция на ишемию: монография. Гродно: ГрГМУ; 2020. 240.
- Бонь Е.И., Зиматкин С.М. Темные нейроны мозга. Морфология. 2017; 6: 81-86.
- Syed Suhail Andrabi, Suhel Parvez, Heena Tabassum. Ischemic stroke and mitochondria: mechanisms and targets. Protoplasm. 2020; 257: 335-343.
- Mimi Wu, Xiaoping Gu, Zhengliang Ma. Mitochondrial quality control in cerebral ischemia-reperfusion injury. Mol Neurobiol. 2021; 58 (10): 5253-5271.
- Dirnagl U., Iadecola C., Moskowitz M.A. Pathobiology of ischaemic stroke: an integrated view. Trends Neurosci. 1999; 22: 391-397.
- Семченко В.В. Постаноксическая энцефалопатия. Омск; 1999. 448.
- Colbourne F., Sutherland G.R., Auer R.N. Electron microscopic evidence against apoptosis as the mechanism of neuronal death in global ischemia. J. Neurosci. 1999; 19: 4200-4210.
- Бутин А.А. Закономерности изменений сосудисто-капиллярной сети коры большого мозга в ответ на острую церебральную ишемию. Омский научный вестник. 2004; 26: 46-57.
- Nina J. Solenski, Charles G. diPierro, Patricia A. Trimmer, Aij-Li Kwan, Gregory A. Helms. Ultrastructural changes of neuronal mitochondria after transient and permanent cerebral ischemia. Stroke. 2002; 33: 816-824.
- Zhi H., Niya N., Qiongxiu Zh., SeyedEsmaeilKh. Mitochondria as a therapeutic target for ischemic stroke. Free Radic Biol Med. 2020; 146: 45-58.


