Характеристика токсигенности энтеробактерий, выделенных при желудочно-кишечных болезнях сельскохозяйственных животных
Автор: Ленченко Е.М., Мансурова Е.А., Моторыгин А.В.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Ветеринарная микробиология, ветеринария
Статья в выпуске: 2 т.49, 2014 года.
Бесплатный доступ
Как известно, у бактерий семейства Enterobacteriaceae, которые занимают существенное место в этиологии неонатальных заболеваний сельскохозяйственных животных, в большинстве случаев отсутствует корреляция между серологической группой и токсигенностью. В связи с этим при диагностике целесообразно либо выявлять бактериальные адгезины, либо непосредственно подтверждать присутствие токсинов на различных лабораторных моделях, что, как правило, достаточно сложно и занимает много времени. Мы оценили токсигенность и вирулентность у патогенных и условно-патогенных энтеробактерий, выделенных при желудочно-кишечных болезнях молодняка сельскохозяйственных животных (1-5-суточные телята голштинской и черно-пестрой пород), и у референтных штаммов с использованием различных тестов на лабораторных животных (беспородные белые мыши, морские свинки линии Self, кролики породы Chinchilla и перепела Coturnix comuni). Доминирующая часть эпизоотических энтеробактерий, выделенных нами от телят (64 из 86 изолятов), идентифицировалась как Escherichia coli. Из изолятов E. coli 34 не серотипировались по О-антигену. При этом 35,0 % таких изолятов оказались патогенными и 65,0 % - непатогенными в тесте на белых мышах при внутрибрюшинном заражении бактериальной суспензией. В то же время токсигенность была выявлена у 53,9 % изученных изолятов и референтных штаммов энтеробактерий родов Salmonella (2 изолята), Klebsiella (2 изолята), Kluyvera (1 изолят), Yersinia (3 изолята), Escherichia (13 изолятов). Умеренно токсигенными и слаботоксигенными свойствами характеризовались соответственно 15,4 и 38,5 % изолятов, нетоксигенными - 46,1 %. Гистохимическими методами выявлены структурные изменения в тканях и органах лабораторных животных при экспериментальном моделировании токсемии, вызываемой энтеробактериями. При экспериментальной токсемии, обусловленной токсинами E. coli и Y. pseudotuberculosis, динамика патологических процессов характеризовалась развитием гидропической дистрофии эпителиоцитов ворсинок в тонком отделе кишечника, а также общей реакции сосудов микроциркуляторного русла в слизистой оболочки желудка, тонкого и толстого отделов кишечника животных.
Энтеробактерии, желудочно-кишечные заболевания, сельскохозяйственные животные, лабораторные модели, токсемия
Короткий адрес: https://sciup.org/142133501
IDR: 142133501 | УДК: 636:619:
Characterization of toxigenic enterobacteriaceae from farm animals with gastrointestinal diseases
In most Enterobacteriaceae family bacteria, being the main etiological agents of the diseases in young farm animals, there is no strict correlation between a serological group and toxic activity. Thus, when diagnosing the diseases, a direct identification of the bacterial adhesins or the toxin detection with the laboratory animals are conducted, and of these two procedures the animal test is usually long and difficult. We evaluated toxins and virulence in the pathogenic and opportunistic bacteria isolated from 1-5 days Holstein and Black Mottled calves with the diarrhea syndrome, and in the reference strains using different tests with the laboratory animals (white mice, the Self line guinea pigs, Chinchilla rabbits, and quail Coturnix comuni ). Most of the samples (64 of 86 isolates) were identified as Escherichia coli. In 34 E. coli isolates the O-antigen was not detected. In the test on white mice, infected intraperitoneally with a bacterial suspension, 35.0 % and 65.0 % of the bacteria were identified as pathogenic and nonpathogenic, respectively. Nevertheless, the toxins were detected in 53.9 % of the studied isolates and reference strains of Salmonella (2 strains), Klebsiella (2 strains), Kluyvera (a strain), Yersinia (3 straines), Escherichia (13 strains) genera. Moderate and low toxic properties were identified in 15.4 % and 38.5 % of these isolates, respectively, and in 46.1 % no toxigenic activity was found. By the histochemical methods, the histomorphological changes in tissues and organs of the laboratory animals were revealed under the experimental toxicoinfection caused by Enterobacteriaceae. At experimental toxemia, induced by E. coli and Y. pseudotuberculosis strains, a hydropic dystrophy of the villus epithelium cells developed in the small intestine, and a generalized microvascular reaction occurred in the gastric mucosa and in the mucosa of small and large intestines.
Текст научной статьи Характеристика токсигенности энтеробактерий, выделенных при желудочно-кишечных болезнях сельскохозяйственных животных
Целью работы была оценка токсигенности энтеробактерий, доминирующих при желудочно-кишечных болезнях молодняка сельскохозяйственных животных, с использованием различных лабораторных тестов, а также регистрации гематологических и гистохимических изменений, наблюдаемых при инфицировании лабораторных животных.
Методика . Исследовали изоляты энтеробактерий, выделенные из патологического материала, смывов из носовой полости и из фекалий телят голштинской и черно-пестрой пород в возрасте от 1 до 5 сут ( n = 70) из хозяйств Кораблинского района Рязанской области. Видовую принадлежность изолятов идентифицировали с использованием дифференциально-диагностических питательных сред: ВСА, Эндо («HiMedia Laboratories Pvt. Ltd.», Индия), Rambach agar, XLT-4 agar, Cromocult Coliform agar («Merck KGaA», Германия). Биохимические свойства микроорганизмов изучали с использованием сред Гисса и множественной тест-системы «Пластина биохимическая, дифференцирующая энтеробактерии» («ПБДЭ», НПО «Диагностические системы», г. Нижний Новгород, Россия) и API («BioM e rieux S.A.S.», Франция). Для серотипирования E . coli по О-ан-тигену применяли диагностические сыворотки (ФГУП «Армавирская биофабрика», Россия) в соответствии с рекомендациями («Наставления по применению агглютинирующих О-коли сывороток». М., 1998). В качестве референтных использовали паспортизированные штаммы Escherichia coli О2 № 388, E . coli О78:К80 № 320, E . coli О138:К81 № 723, Klebsiella pneumonia № 356, Salmonella typhimurium № 5715, Yersinia pseudotuberculosis I № 290, Y. enterocolitica (S- и R-формы) № 383 (получены из коллекции «Центр качества и стандартизации лекарственных средств для животных и кормов» — ВГНКИ, г. Москва).
Патогенные и токсигенные свойства энтеробактерий изучали общепринятыми методами на лабораторных животных — беспородных белых мышах (живая масса 14-16 г), морских свинках (линия Self, живая масса 200-300 г), кроликах (порода Chinchilla, живая масса 2,5 кг) и перепелах Coturnix comuni (6, 7).
При оценке патогенности изолятов заражали беспородных белых мышей внутрибрюшинно взвесью микроорганизмов (по 0,5 см3; плотность бактериальной суспензии — 1 млрд кл/см3) ( n = 60). Для наблюдения за местными изменениями в слизистых оболочках с применением ке-ратоконъюнктивальной пробы морским свинкам ( n = 6) в конъюнктивальную полость вводили взвесь изучаемых микроорганизмов (1*109-1х1010 клеток) (8). При исследовании токсигенных свойств штаммы предварительно выращивали в жидкой среде Хоттингера в течение 24 ч при 37 ° С ( Y. pseudotuberculosis и Y. enterocolitica — при 28 ° С), культуры (S-формы) осветляли центрифугированием (6000 об/мин в течение 30 мин) и супернатант использовали в плантарном тесте и тесте расширения кишечника. В плантарном тесте осветленную культуральную жидкость вводили беспородным белым мышам ( n = 3) в область плантарной поверхности лапы (в контроле стерильный бульон Хоттингера инъецировали в другую лапу в том же количестве). В тесте расширения кишечника белым беспородным мышам-сосункам 2-3-суточного возраста per rectum вводили надосадочную жидкость в объеме 0,2 мл и рассчитывали коэффициент расширения тонкого кишечника (отношение массы тонкого кишечника с содержимым к остальной массе тела).
С целью исследования клинико-гематологических показателей морским свинкам (n = 6) и кроликам (n = 6) внутрибрюшинно в дозе 5*109 клеток вводили 18-часовую бактериальную культуру; в аналогичных контрольных группах животным инъецировали стерильный раствор NaCl (0,9 %). При изучении клинико-гематологических изменений у 10-суточных перепелов Coturnix comuni (n = 12) птицу интраназально заражали 18часовой культурой Е. coli 1111 (О149:К91:К88) в дозе 5*109 бактериальных клеток. Клинико-гематологические показатели изучали на морских свин- ках при внутрибрюшинном заражении референтным штаммом Y. pseudotuberculosis I и изолятом Е. coli 0115.
Для оценки динамики гибели белых мышей использовали внутрибрюшинное заражение культурой микроорганизмов (500 млн кл/см3) и интрагастральное введение 0,5 см3 токсина, полученного после осветления жидкой культуры. Из животных по принципу аналогов сформировали 6 групп (по 10 гол. в каждой): особям из I и II группы вводили соответственно культуру микроорганизмов и токсин E. coli 08 (выделен из фекалий 3-суточного теленка с клиническими признаками диареи; из III и IV — соответственно культуру микроорганизмов и токсин K. pneumoniae (референтный штамм № 356); из V групп — внутрибрюшинно ассоциацию (по 250 млн кл/см3) культур микроорганизмов E. coli O8 и K . pneumoniae ; из VI группы (контроль) — внутрибрюшинно и интрагастрально стерильный раствор NaCl (0,9 %). Рассчитывали летальность (отношение числа погибших от болезни к числу заболевших) и смертность (отношение числа погибших от болезни к общей численности контролируемой популяции).
Патологоанатомические исследования проводили общепринятыми методами, при гистохимических исследованиях патологический материал от животных и птицы фиксировали 10,0 % формалином и заключали в парафин, срезы окрашивали гематоксилином и эозином, по Ван Гизону, по Крантцу и по Лейшману.
В экспериментах использовали анализаторы крови фирмы « Mindray» (Китай); микроскоп модели H604 Trinocular («Unico, Inc.», США) с цифровой фотокамерой Canon Power Shot A 640 (США), цифровую окулярную видеокамеру МА 88 («Hight Technology Inc.», США).
Полученные данные обрабатывали методом вариационной статистики в соответствии с методическим руководством с применением программы Statgraphics Plus v. 5.0 (9).
Результаты . Использование питательных сред Rambach agar, XLT-4 agar, Cromocult Coliform agar при проведении бактериологических исследований позволило идентифицировать и дифференцировать колонии таксономически сходных видов энтеробактерий. Результаты идентификации с применением сред Гисса согласовывались с результатами тест-систем, но последние позволяли сократить сроки и снизить затратность процедуры. Из патологического материала, смывов из носовой полости и фекалий телят, а также смывов, полученных в репродукторных помещениях животноводческих объектов, выделили 86 культур микроорганизмов, принадлежащих к семейству Enterobacteriaceae , из которых 64 культуры идентифицировались как E . coli, 10 — как Proteus mirabilis, 9 — Klebsiella pneumoniae , 3 — Salmonella typhimurium , то есть среди них доминировали эшерихии.
При серологической идентификации с использованием О-коли сывороток из 139 эпизоотических штаммов E . coli к группе 08 отнесли 20 штаммов, к 0141 — 27, 0138 — 18, 09 — 11, 0139 — 9 и к 0157 — 3. К нетипируемым причислили 34 изолята E . coli. По данным литературы, се-ротипирование E . coli по 0-антигену затруднено из-за узкого спектра и невысокой чувствительности существующих наборов 0-коли сывороток, в частности по 0-серогруппе не удалось типировать 49,0 % изолятов E . colt , выделенных от птицы, и 22,0 % изолятов E . coli от пушных зверей (10, 11).
При идентификации микроорганизмов, не типируемых по 0-антигену, в соответствии с общепринятыми методами определяли патогенные свойства при внутрибрюшинном заражении белых мышей. Из исследо- ванных нами штаммов энтеробактерий 35,0 % оказались патогенными и 65,0 % — непатогенными. Известно, что парентеральное введение иер-синий мышевидным грызунам из-за естественной восприимчивости последних не дает объективных сведений о наличии факторов патогенности у указанных микроорганизмов и их способности вызвать инфекционный процесс (8). Поэтому для изучения патогенных свойств референтных штаммов Y. enterocolitica 09 № 383 и Y. pseudotuberculosis № 290 мы апробировали кератоконъюнктивальную пробу. Для сравнения в качестве тест-штамма использовали изолят E. coli 08, выделенный из фекалий 2-суточного теленка с клиническими признаками диареи. На морских свинках в течение 1 нед при ежедневном осмотре после введения в конъюнктивальную полость взвеси микроорганизмов (штамм E. coli 08, референтные штаммы Y. enterocolitica 09 № 383 и Y. pseudotuberculosis № 290), регистрируя выраженность признаков конъюнктивита (сужение глазной щели, гиперемия конъюнктивы, отек век, наличие и характер отделяемого) и состояния роговицы, установили следующие различия. Штамм E. coli 08 вызывал прогрессирующий конъюнктивит и кератит, характеризующийся склеиванием изъязвленных век, обильным гнойным или гнойно-творожистым экссудатом, сильное помутнение роговицы. В случае референтного штамма Y. enterocolitica 09 (S-форма) № 383 отмечался выраженный и прогрессирующий к 5-7-м сут конъюнктивит при незначительном непрогрессирующем помутнении роговицы, в то время как в варианте с референтными штаммами Y. enterocolitica (R-форма) № 383 и Y. pseudotuberculosis № 290 наблюдали незначительно выраженный конъюнктивит через 2-3 сут после заражения, отсутствие или слабую выраженность кератита через 2-3 сут без прогрессирования или даже с исчезновением помутнения роговицы через 5-7 сут. В целом было установлено, что кератоконъюнктивальная проба может считаться чувствительным и легко воспроизводимым в практических условиях тестом для оценки патогенности иерсиний.
В плантарном тесте на продукцию токсина средняя разность массы лапок у мышей в опыте и контроле через 24 ч колебалась от 6,66 ± 4,41 до 48,33+3,54 мг. У 42,8 % изолятов энтеробактерий получили критерий достоверности td > 9,9, что соответствовало достоверности различий Р < 0,01; у 52,4 % изолятов — td > 4,3, что соответствовало достоверности различий Р < 0,05. Из 21 изученной культуры референтных и эпизоотических штаммов энтеробактерий, в том числе эшерихий, не типируемых набором 0-коли сывороток, 42,9 % были умеренно токсигенными, 28,5 % — слаботоксигенными и 33,3 % — нетоксигенными (табл. 1).
1. Результаты оценки токсигенности эпизоотических и референтных штаммов энтеробактерий в плантарном тесте на белых лабораторных мышах
|
Вид микроорганизма, № штамма (источник выделения) |
Токсигенность |
||
|
масса лапки, мг |
средняя разность массы, мг ( M ± m ) |
t d |
|
|
опыт контроль |
|||
|
Salmonella typhimurium № 5715 (референтный штамм) 205 160 215 165 45,00±2,64 12,4 205 165 S . typhimurium (смывы, полученные в репродукторных по- 185 165 мещениях) 185 160 23,33±6,43 8,3 200 175 Klebsiella pneumoniae № 356 (референтный штамм) 190 155 195 150 38,33±4,32 7,2 190 145 |
|||
Ïðîäîëæåíèå òàáëèöû 1
Гистохимические изменения в тканях плантарной поверхности лап при введении токсина Y. pseudotuberculosis характеризовались деструкцией ороговевшего слоя эпидермиса кожи и общей сосудистой реакцией, отеком и гиперемией соединительной ткани дермы. В сосочковом слое дермы между волокнами рыхлой волокнистой соединительной ткани располагались гомогенные массы экссудата бледно-красного цвета. Гемоциркуляторные изменения проявлялись в виде полнокровия артериол, венул, капилляров, в просвете сосудов микроциркуляторного русла отмечалась агрегация эритроцитов и нити фибрина, что свидетельствовало о процессе тромбообразования, вдоль эндотелия сосудов наблюдалась так называемая пограничная локализация лейкоцитов. В сосочковом слое дермы между волокнами рыхлой волокнистой соединительной ткани находились гомогенные массы экссудата бледно-красного цвета, наблюдалась инфильтрация лейкоцитами (рис. 1, а, б).
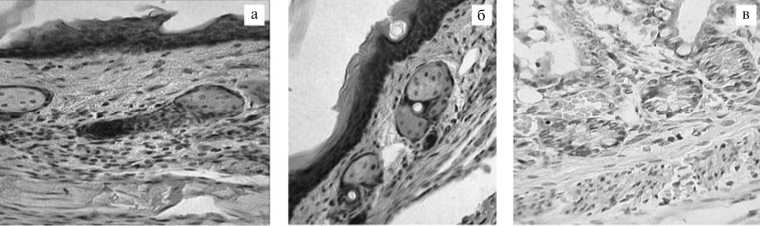
Рис. 1. Морфология тканей у лабораторных мышей после введения бактериальной взвеси референтного штамма Yersinia pseudotuberculosis внутрикожно (плантарный тест) и его токсина per rectum (осветленная культуральная жидкость, тест расширения кишечника): а — деструкция ороговевшего слоя эпидермиса плантарной поверхности лап, б — инфильтрация лейкоцитами сосочкового слоя дермы плантарной поверхности лап; в — гидропическая дистрофия энтеро-цитов кишечника . Окрашивание гематоксилином и эозином, увеличение *250.
В тесте расширения кишечника с использованием надосадочной жидкости Y. pseudotuberculosis средние значения коэффициента для тонкого кишечника находились в пределах от 0,070±0,009 до 0,116±0,005. Из общего числа изученных штаммов 27,7 % характеризовались как токси-генные, 18,1 % — как слаботоксигенные и 54,5 % — как нетоксигенные. Гистохимические изменения при введении токсина энтеробактерий проявлялись в гидропической дистрофии энтероцитов за счет накопления жидкости в цитоплазме клеток, деструктивно-некротических изменениях, во всех оболочках тонкого и толстого отдела кишечника наблюдались сосудистые нарушения и инфильтративные явления (см. рис. 1, в).
В целом результаты теста расширения кишечника и плантарного теста имели высокую степень корреляции ( r = 0,96). Вместе с тем недостатком теста расширения кишечника на мышах-сосунках следует считать б о льшую чувствительность и гибель животных при транспортировке и содержании, возможность выбраковки при травме кишечника при введении материала. Оценка токсигенности энтеробактерий в плантарном тесте онкометрическим методом с использованием плетизмо-метра позволяет наблюдать развитие экспериментально вызванной реакции у животных за счет изменения объема вытесняемой жидкости из водной камеры до и через определенный промежуток времени после введения токсина (12).
Оценка динамики гибели белых мышей при внутрибрюшинном заражении и интрагастральном введении токсина изолята E. coli О8 и референтного штамма K. pneumoniae № 356 показала, что летальность и смертность составили 100 % независимо от способа поступления исследуемого материала в организм. При внутрибрюшинном заражении изоля-том E. coli О8, выделенным из фекалий 3-суточного теленка с клиническими признаками диареи (I группа), гибель 6 мышей наступила через 24 ч, 4 — через 48 ч, тогда как при интрагастральном введении токсина E. coli О8 (II группа) гибель 8 особей регистрировали через 12 ч, 2 — через 24 ч. При внутрибрюшинном заражении культурой микроорганизмов референтным штаммом K. pneumoniae № 356 (III группа) гибель 2 мышей зафиксировали через 24 ч, 8 — через 48 ч, тогда как при интрагастраль- ном введении токсина K. pneumoniae № 356 (IV группа) смерть 4 мышей наступила через 12 ч, 6 — через 24 ч. При внутрибрюшинном заражении ассоциацией эшерихий и клебсиелл (V группа) 3 особи погибли через 6 ч, 7 — через 12 ч. В целом при введении токсина животные погибали быстрее, чем при заражении культурой микроорганизмов (рис. 2).
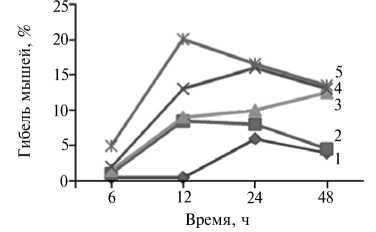
Рис. 2. Динамика гибели лабораторных мышей при внутрибрюшинном заражении культурой энтеробактерий или интрагастральном введении их токсинов: 1 и 2 — I и II группы, соответственно культура и токсин изолята Escherichia coli 08 (выделен из фекалий 3-суточного теленка с клиническими признаками диареи); 3 и 4 — III и IV группы, соответственно культура и токсин Klebsiella pneumoniae (референтный штамм № 356); 5 — V группа, введение внутрибрюшинно ассоциации E. coli O8 и K . pneumoniae ; 6 — VI группа
(контроль), введение внутрибрюшинно и интрагастрально стерильного раствора NaCl (0,9 %) .
Учитывая данные литературы о восприимчивости лабораторных животных к энтеробактериям (13), клинико-гематологические показатели при внутрибрюшинном заражении референтным штаммом Y. pseudotuberculosis исследовали на морских свинках, изолятом Е. coli 0115 — на кроликах. Клинические признаки болезни у морских свинок отмечали на 2-е сут после заражения в виде потери аппетита и отказа от корма, конъ- юнктивита, повышения температуры тела до 40 °C, прогрессирующей диареи, через 5 сут у животных наблюдались судороги и паралич конечностей. У кроликов клинические признаки болезни регистрировали через 5 сут после заражения Е. coli 0115 (отсутствие аппетита, жажда, цианоз слизистых оболочек, прогрессирующая диарея). Гематологические и биохимические показатели крови и сыворотки крови у животных при заражении Y. pseudotuberculosis и E. coli 0115 характеризовались снижением содержания гемоглобина, альбумина и глюкозы, повышением гематокрита, числа лейкоцитов, количества билирубина, аланинаминотрансферазы (АлАТ), аспартатаминотрансферазы (АсАТ) и лактатдегидрогеназы (ЛДГ), креатинина, а-амилазы (табл. 2).
2. Изменение гематологических и биохимических показателей при заражении морских свинок референтным штаммом Yersinia pseudotuberculosis и кроликов изолятом Escherichia coli 0115 ( M ± m )
Р < 0,001.
После интраназального заражения 10-суточных перепелов Coturnix comuni ( n = 12) референтным штаммом Е. coli 1111 (О149:К91:К88) клинические признаки болезни наблюдали через 3 сут в виде прогрессирующей депрессии, жажды, отсутствия аппетита, цианоза слизистых оболочек, в последующие 4-5 сут развивались признаки диареи. Патологоанатомические изменения, обусловленные подострой септикотоксемией, характеризовались геморрагическим энтеритом, серозно-фибринозным перигепатитом, атрофией фабрициевой бурсы, серозно-фибринозным аэро-саккулитом, серозно-фибринозным перитонитом.
При прогрессирующей диарее на 3-5-е сут после заражения цыплят наблюдались нарушения водно-электролитного баланса. Так, показатели по Na + (ммоль/л) составили в опыте 128,11±0,32, в контроле — 154,21±0,33; по К + (ммоль/л) — соответственно 33,81±0,23 и 3,97±0,13; по Cl - (ммоль/л) — 102,66±0,31 и 101,16±0,42. В первую очередь при потерях ионов натрия развивались компенсаторные изменения кислотно-щелочного состояния, при тяжелой дегидратации — гиперкалиемия. Такие нарушения относятся к тяжелым патоморфологическим синдромам, особенно при средней и тяжелой степени дегидратации, и будучи нераспознанными и неустраненными, во многом определяют выраженность клинических признаков, течение и исход заболевания. Ранее мы сообщали, что при доминировании токсигенных энтеробактерий в микробиоценозах кишечника поросят гематологические показатели характеризовались повышением показателя гематокрита, фагоцитарной активности и общей окислительно-восстановительной способности лейкоцитов крови (14). Наши результаты изучения изменений, происходящих при патологических процессах, в целом согласуются с данными других исследователей: например, установлено, что токсины энтеробактерий, адсорбируясь на эпителиальных клетках ворсинок тонкого кишечника, стимулируют адени-латциклазу, поэтому увеличивается концентрация аденозинмонофосфата, усиливающего гиперсекрецию воды и хлоридов в просвет кишечника и угнетающего резорбцию натрия. Как следствие, просвет кишки переполняется жидкостью, активируется перистальтика кишечника и развивается диарея (15, 16).
Таким образом, при идентификации энтеробактерий, не типируе-мых по О-антигену, общепринятая схема бактериологического исследования завершается биологической пробой. Восприимчивость лабораторных моделей зависит от вирулентности возбудителя, дозы, метода введения, чувствительности к термолабильным и термостабильным токсинам. Так, при внутрибрюшинном введении белым беспородным мышам бактериальной взвеси результаты воспроизведения болезни на лабораторных и 102
естественно восприимчивых животных не коррелируют (16). Установлено, что энтеротоксигенные (ЕТЕС) штаммы E . coli продуцируют два типа энтеротоксинов — термолабильный (ТЛЭ) и термостабильный (ТСЭ), различающиеся по структуре, молекулярной массе, иммуногенности, механизмам действия. В настоящее время для оценки ТЛЭ применяют тест отека лап у белых мышей, кожную пробу на кроликах, реакции агрегации тромбоцитов, в случае ТСЭ — инокуляцию 15-суточных куриных эмбрионов и анальную пробу на 15-суточных мышатах-сосунах (5, 16). Однако вследствие того, что оценка токсического эффекта на лабораторных моделях сопряжена с определенными трудностями, перспективными для этих целей признаны тест-системы, основанные на методе обратной пассивной латексной агглютинации, методы иммунодиффузии, позволяющие быстро определить наличие термостабильного и термолабильного токсинов.


